Pese a que el primer estudio sobre la eficacia de metotrexato en el tratamiento de la psoriasis se remonta a 1958, hasta no hace mucho ha sido escasa la evidencia científica disponible sobre su uso en esta indicación.
Disponemos de nuevos datos acerca de la farmacocinética y el mecanismo de acción del metotrexato, así como de nuevas presentaciones por vía subcutánea que mejoran la biodisponibilidad, la eficacia y la conveniencia de la administración de este fármaco. La reciente publicación de ensayos clínicos comparativos con diversos biológicos permite considerar al metotrexato como el estándar terapéutico dentro de los tratamientos sistémicos clásicos de la psoriasis, con un cociente coste-eficacia incremental favorable al metotrexato subcutáneo si se compara con ciclosporina, adalimumab o infliximab.
Although the first study on the efficacy of methotrexate in the treatment of psoriasis was reported in 1958, scientific evidence for this indication has been scant until quite recently. We now have new data on the pharmacokinetics and mechanism of action of methotrexate and new subcutaneous formulations that have improved the bioavailability, efficacy, and ease of administration of the drug. The results of recent clinical trials comparing methotrexate with several biologic agents have shown it to be the first-line therapy among the classic systemic treatments for psoriasis. Moreover, the incremental cost-effectiveness ratio for subcutaneous methotrexate has been shown to be superior to that of ciclosporin, adalimumab, and infliximab.
El metotrexato (ácido 4-amino-N10-metilpteroil glutámico) es un análogo de la aminopterina (ácido 4-amino-pteroil glutámico), un antagonista del ácido fólico introducido en 1948 para el tratamiento de la leucemia aguda pediátrica, al que sustituyó por su perfil de toxicidad más favorable. El primer estudio sobre la eficacia de este tratamiento en la psoriasis se remonta a 19581, y en 1972 se publicaron las primeras directrices sobre su empleo en Dermatología2, pero hasta no hace mucho ha sido escasa la evidencia científica disponible sobre su uso en el tratamiento de la psoriasis.
Los nuevos datos de los que disponemos en cuanto a la eficacia del metotrexato en la psoriasis, que permiten considerarlo como el estándar terapéutico dentro de los tratamientos sistémicos clásicos, y la disponibilidad de presentaciones por vía subcutánea, que mejoran la biodisponibilidad y la conveniencia de la administración de metotrexato, justifican esta revisión.
FarmacocinéticaEl metotrexato se puede administrar por vía oral, subcutánea, intramuscular o intravenosa; para el tratamiento de la psoriasis, a la dosis habitual de 7,5 hasta 25mg/semana, casi siempre se emplea la vía oral o subcutánea. La biodisponibilidad del metotrexato por vía oral a dosis bajas es alta (un 70%)3, aunque variable entre individuos; a dosis superiores a unos 15mg/semana disminuye hasta un 30%, ya que la absorción del metotrexato por el tracto gastrointestinal viene determinada por un transportador saturable, el reduced folate carrier 1 (transportador de folato reducido [RFC])3. Por este motivo, y por su mayor tolerabilidad gastrointestinal, se tiende a preferir la vía parenteral en estos casos4, aunque la administración oral en dosis separadas puede mejorar la biodisponibilidad5. La absorción oral de metotrexato, que se produce fundamentalmente en el yeyuno proximal, no se ve reducida por la ingesta de alimentos, pero sí en el contexto de malabsorción o enfermedad inflamatoria intestinal. La biodisponibilidad del metotrexato administrado por vía parenteral es similar, independientemente de la vía.
Tras la absorción un 10% del metotrexato es objeto de conversión hepática en un metabolito parcialmente inactivo, el 7-hidroximetotrexato, lo que reduce las concentraciones plasmáticas de metotrexato. La capacidad de catabolización de metotrexato a 7-hidroximetotrexato a través de la aldehído oxidasa es muy variable (las diferencias interindividuales relativas van de 1 a 14), con una distribución bimodal entre la población. Los catabolizadores rápidos tienen una menor respuesta terapéutica a metotrexato; por otra parte, el ácido fólico (a diferencia del folínico) inhibe esta catabolización, y podría contribuir a aumentar los niveles de metotrexato en los catabolizadores rápidos6. El 7-hidroximetotrexato compite por la captación celular del metotrexato a través de RFC, que también internalizan los folatos reducidos y el ácido fólico, aunque con baja afinidad. Las alteraciones cuantitativas o cualitativas de los RFC, al igual que los niveles elevados de folato exógeno compitiendo por el receptor, pueden determinar una resistencia mediada por transporte a la acción terapéutica del metotrexato. Recientemente se ha descrito un polimorfismo del gen del RCF1 que predice la respuesta terapéutica al metotrexato en pacientes japoneses con artritis reumatoide7, lo que ilustra el potencial futuro de los estudios farmacogenéticos con vistas a mejorar los resultados del tratamiento.
El metotrexato, al igual que el 7-hidroximetotrexato, es objeto de metabolización intracelular a mono y poliglutamatos, que son los principales responsables de la inhibición de diversas enzimas, por lo que sus niveles intracelulares se correlacionan con la actividad terapéutica del metotrexato (que en realidad es un profármaco)5. La vía de administración determina en parte tanto la biodisponibilidad como la conjugación intracelular del metotrexato: la sustitución de la vía oral de administración por la vía parenteral determina un incremento de un 37% en la concentración de poliglutamatos de cadena muy larga y una disminución del 31% en la actividad de la enfermedad en pacientes con artritis reumatoide8. Los poliglutamatos se liberan lentamente del interior de la célula por la acción de transportadores de eflujo activos, lo que puede contribuir a prolongar la eliminación del fármaco y determina diferencias farmacogenéticas9: aunque la variabilidad genética en cuanto a las enzimas que intervienen en el metabolismo del metotrexato no se ha demostrado por el momento que tenga relevancia clínica en la psoriasis10, existen diferencias en cuanto a la eficacia y al riesgo de toxicidad asociadas con la variabilidad genética en los transportadores de eflujo de poliglutamatos11.
Por lo que respecta a la distribución, un 35-50% del metotrexato circulante se une a la albúmina (frente a un 91-95% del 7-OH metotrexato), y alcanza sus máximas concentraciones en el riñón, el hígado, la vesícula biliar, el bazo, la piel y los hematíes; la concentración en estos últimos puede reflejar la posible toxicidad hematológica y la acumulación hepática del fármaco. El metotrexato tiende a acumularse en el compartimiento extravascular, por lo que debe extremarse la precaución cuando se administra a pacientes con derrame pleural, ascitis o edema masivo, por el riesgo de toxicidad al reabsorberse el fluido extravascular.
En cuanto al aclaramiento del metotrexato, el 65-80% del fármaco se excreta por los riñones sin metabolizar (en su mayor parte en las primeras 12 horas después de la administración) y un 20-35% es objeto de secreción biliar y se metaboliza o transfiere a otros compartimentos. La filtración glomerular es la principal responsable de la excreción renal, siendo menos importantes la secreción y reabsorción tubulares; por lo que respecta a la secreción biliar adquiere importancia en pacientes con insuficiencia renal, en los que disminuye el aclaramiento del fármaco y aumenta el riesgo de toxicidad. La hemodiálisis y la diálisis peritoneal determinan disminuciones limitadas y transitorias en las concentraciones séricas del fármaco, debido a su baja-media unión a proteínas y su elevada distribución tisular.
La semivida terminal del metotrexato en suero es aproximadamente de 7-10 h, pero puede prolongarse hasta 26 h en algunos pacientes; las concentraciones intraeritrocitarias permanecen estables durante 9 días, mientras que las séricas se vuelven indetectables al cabo de 52 h12. Aunque se puede establecer el aclaramiento individual de metotrexato con solo 2 determinaciones (a los 30 y 120 minutos después de la administración), ello no resulta útil para definir el régimen terapéutico óptimo en la artritis reumatoide13. La lista de interacciones medicamentosas del metotrexato es amplia, pero no se han descrito diferencias en las concentraciones séricas de metotrexato entre grupos de pacientes tratados o no con diversos antiinflamatorios no esteroideos;14 en cualquier caso, es muy importante recordar que se debe disminuir la dosis de metotrexato en los ancianos (>65 años) y en pacientes con insuficiencia renal15.
Mecanismos de acción del metotrexatoSe han propuesto diversos mecanismos de acción, entre los que destaca por su trascendencia en el tratamiento de enfermedades inflamatorias la promoción de la liberación de adenosina con la consiguiente supresión de la inflamación3.
El metotrexato inhibe la proliferación de las células neoplásicas impidiendo la síntesis de novo de purinas y pirimidinas como consecuencia de la inhibición irreversible de la dihidrofolato reductasa, responsable de la producción de tetrahidrofolato; aunque la administración de dosis elevadas de ácido fólico o folínico puede revertir este efecto, no es este el mecanismo que justifica la administración de suplementos de folato para prevenir la toxicidad del metotrexato en el tratamiento de enfermedades inflamatorias, como la artritis reumatoide o la psoriasis, sin que disminuya de forma significativa la eficacia del tratamiento16.
Probablemente en estas enfermedades el mecanismo de acción más importante del metotrexato tenga que ver con la actividad antiinflamatoria de la adenosina a través de receptores específicos, recientemente descrita17. El metotrexato, tanto en modelos animales de inflamación como en pacientes con artritis reumatoide, induce la liberación extracelular de adenosina, que actúa como agente antiinflamatorio a través de receptores específicos, en concreto los de tipo A218, que también intervienen en la patogenia de la fibrosis hepática19.
El metotrexato, especialmente en forma de poliglutamato (la forma en que se acumula en el interior de las células) inhibe la aminoimidazol carboxamida ribonucleótido (AICAR) transformilasa20. En consecuencia se produce una acumulación intracelular de AICAR, que inhibe competitivamente la adenosín monofosfato desaminasa; el aumento de este sustrato determina su liberación al exterior de la célula y su conversión en adenosina por acción de la ecto-5’-nucleotidasa (CD73)21,22. La adenosina tiene una semivida muy corta (segundos) en sangre periférica y fluidos corporales, por lo que es extremadamente difícil determinar sus niveles; la mayoría de los estudios publicados se basan en el bloqueo de sus efectos biológicos mediante inhibidores de su metabolismo o sus receptores23,24, o en el empleo de modelos experimentales en ratones carentes de CD7321 y en otras cepas de ratones25.
La cafeína, un antagonista poco selectivo de los receptores de adenosina, bloquea sus efectos antiinflamatorios in vitro y en modelos animales de artritis26, por lo que es posible que la ingesta de café y otras bebidas con cafeína pudiera interferir con la actividad terapéutica (¿y tóxica?) del metotrexato. Esta hipótesis se ve apoyada por algunos estudios27, aunque no se ha confirmado en un estudio retrospectivo de pacientes con artritis reumatoide28, ni se ha observado ninguna relación entre la dosis de mantenimiento y el consumo de café en pacientes con psoriasis o artritis psoriásica29.
Aunque la acción antiproliferativa del metotrexato explica la estomatitis, anemia, leucopenia y alopecia, la liberación de adenosina puede contribuir a explicar otros efectos adversos del metotrexato: la acción sobre sus receptores A1 y A2B estimula la esteatosis hepática30, mientras que la unión a sus receptores A2A interviene en el desarrollo de fibrosis31 y cirrosis hepática29. Algunos pacientes refieren una marcada astenia el día que toman metotrexato, que podría estar relacionada con la liberación de adenosina en el sistema nervioso central32 y podría mejorar con la administración de aminofilina33.
Otro posible mecanismo de acción del metotrexato podría basarse en su acción inhibitoria sobre la proliferación de los linfocitos T estimulada por antígeno, tanto in vitro como en pacientes tratados con el fármaco34, o en la inducción de apoptosis en linfocitos T activados33, posiblemente también mediada por receptores de adenosina35.
La acción del metotrexato en la psoriasis podría venir asimismo determinada por la supresión de la activación de los linfocitos T (a través de mecanismos dependientes de folato) y la expresión alterada de moléculas de adhesión; la adenosina también estaría implicada en este mecanismo36.
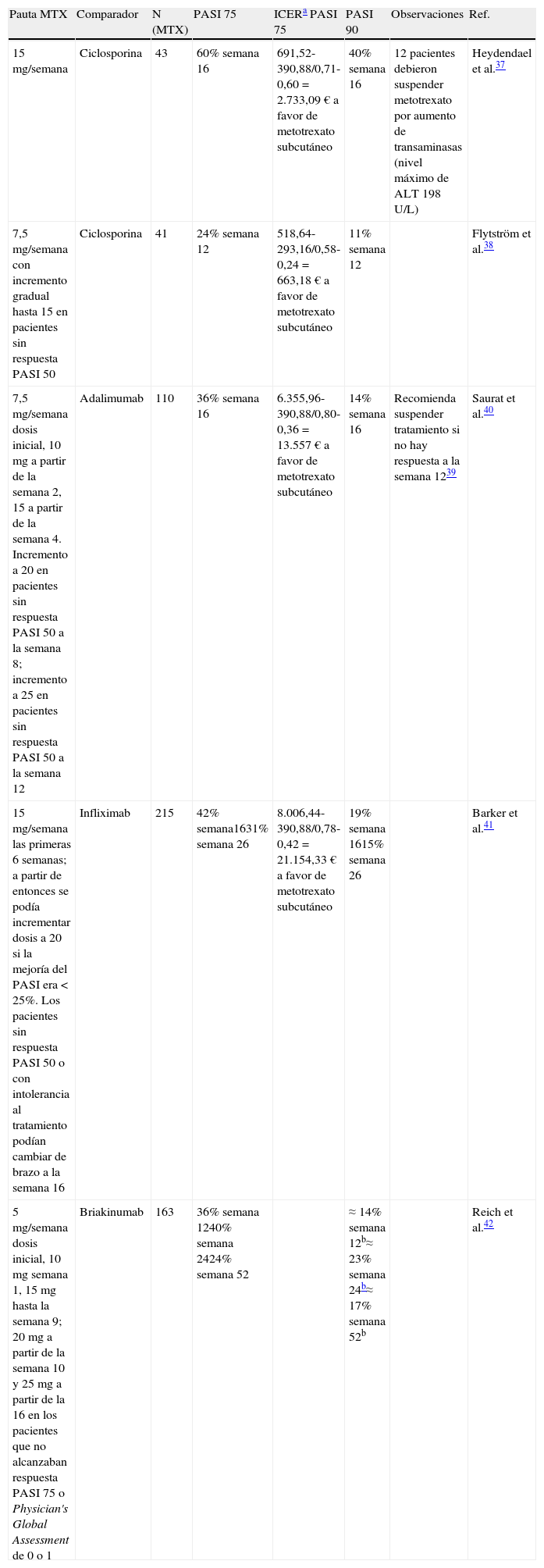
Eficacia en la psoriasisEn los últimos años se han publicado ensayos clínicos que han permitido evaluar la eficacia del metotrexato en el tratamiento de la psoriasis, comparándolo con otras opciones. En la tabla 1 se muestra un resumen de los datos disponibles37–42.
Resumen de los ensayos clínicos comparativos de metotrexato en psoriasis
| Pauta MTX | Comparador | N (MTX) | PASI 75 | ICERa PASI 75 | PASI 90 | Observaciones | Ref. |
| 15 mg/semana | Ciclosporina | 43 | 60% semana 16 | 691,52-390,88/0,71-0,60=2.733,09€ a favor de metotrexato subcutáneo | 40% semana 16 | 12 pacientes debieron suspender metotrexato por aumento de transaminasas (nivel máximo de ALT 198 U/L) | Heydendael et al.37 |
| 7,5 mg/semana con incremento gradual hasta 15 en pacientes sin respuesta PASI 50 | Ciclosporina | 41 | 24% semana 12 | 518,64-293,16/0,58-0,24=663,18€ a favor de metotrexato subcutáneo | 11% semana 12 | Flytström et al.38 | |
| 7,5 mg/semana dosis inicial, 10mg a partir de la semana 2, 15 a partir de la semana 4. Incremento a 20 en pacientes sin respuesta PASI 50 a la semana 8; incremento a 25 en pacientes sin respuesta PASI 50 a la semana 12 | Adalimumab | 110 | 36% semana 16 | 6.355,96-390,88/0,80-0,36=13.557€ a favor de metotrexato subcutáneo | 14% semana 16 | Recomienda suspender tratamiento si no hay respuesta a la semana 1239 | Saurat et al.40 |
| 15 mg/semana las primeras 6 semanas; a partir de entonces se podía incrementar dosis a 20 si la mejoría del PASI era <25%. Los pacientes sin respuesta PASI 50 o con intolerancia al tratamiento podían cambiar de brazo a la semana 16 | Infliximab | 215 | 42% semana1631% semana 26 | 8.006,44-390,88/0,78-0,42=21.154,33€ a favor de metotrexato subcutáneo | 19% semana 1615% semana 26 | Barker et al.41 | |
| 5 mg/semana dosis inicial, 10mg semana 1, 15mg hasta la semana 9; 20mg a partir de la semana 10 y 25mg a partir de la 16 en los pacientes que no alcanzaban respuesta PASI 75 o Physician's Global Assessment de 0 o 1 | Briakinumab | 163 | 36% semana 1240% semana 2424% semana 52 | ≈14% semana 12b≈23% semana 24b≈17% semana 52b | Reich et al.42 |
MTX: metotrexato; PASI: Psoriasis Area and Severity Index; PASI 50: mejoría del Psoriasis Area and Severity Index superior o igual al 50% con respecto al valor basal; PASI 75: mejoría del Psoriasis Area and Severity Index superior o igual al 75% con respecto al valor basal; PASI 90: mejoría del Psoriasis Area and Severity Index superior o igual al 90% con respecto al valor basal.
ICER: cociente de coste-efectividad incremental (coste alternativo-coste metotrexato subcutáneo)/(eficacia alternativo-eficacia metotrexato subcutáneo). Precio de venta al público, octubre 2012: Metoject®: 19,36€/semana (7,5mg); 24,43€/semana (15mg) se toma la dosis máxima por aproximación; Sandimmun Neoral® suspensión 100mg/ml, 128,62€/50ml; se toma la dosis inicial de 3mg/kg/d por aproximación, para un paciente de 80kg: 43,22€/semana; Remicade® (80kg, 4 viales 100mg (615,88€) × 3,25 dosis (16 semanas)=8.006,44€; Humira®: 1.127,57€/2 × 9,5 dosis (16 semanas)=5.355,96€.
Empleando diversas pautas pueden conseguirse tasas de respuesta PASI 75 de hasta un 40% a la semana 24, si bien en la mayoría de los casos la respuesta a la semana 12 permite determinar la conveniencia de continuar o no el tratamiento38.
Por otra parte, se dispone de experiencia sobre el empleo de metotrexato en combinación con diversos tratamientos biológicos para el tratamiento de la psoriasis moderada a grave, permitiendo en muchos casos mejorar la respuesta del paciente o la adherencia al tratamiento; los posibles mecanismos incluyen una disminución del aclaramiento de diversos biológicos o una disminución en la producción de anticuerpos contra los mismos43.
Recientemente se han publicado los resultados de un ensayo clínico44 (incluyendo a 239 pacientes por brazo) que comparaba la administración de etanercept a la dosis habitual (50mg 2 veces por semana durante 12 semanas, seguidos de 50mg semanales durante 12 semanas) asociado a metotrexato (7,5mg semanales las 2 primeras, 10 las 2 siguientes hasta un máximo de 15 hasta la semana 24). Los resultados de este estudio indican la superioridad del tratamiento combinado, con respuestas PASI 75 de 70% frente a 54% a la semana 12 y de 77% frente a 60% a la semana 24; las correspondientes tasas de respuesta PASI 90 fueron de 34% frente a 23% y de 54% frente a 34%, respectivamente.
Patrón de uso y vías de administraciónEn los últimos años se han producido algunos cambios en el patrón de uso del metotrexato, tanto por parte de los reumatólogos como de los dermatólogos. Una reciente revisión concluye que la biodisponibilidad del metotrexato por vía oral disminuye a dosis superiores a 17,5mg45, lo que hace preferible la vía parenteral. Se ha publicado un ensayo clínico en el que se compara la eficacia y seguridad del metotrexato por vía oral y subcutánea en pacientes con artritis reumatoide46. A las 48 semanas alcanzaron el objetivo terapéutico American College of Rheumatology 20 (ACR 20) el 78% de los pacientes tratados por vía subcutánea, frente al 70% de los que recibieron metotrexato oral; por lo que se refiere a la incidencia de efectos adversos también se observó una diferencia (66% frente a 62%), aunque en este caso no fue estadísticamente significativa. En los pacientes que no respondían a la dosis de 15mg por vía oral, un 30% consiguió alcanzar la respuesta ACR 20 cuando se cambió la vía de administración. Este estudio representa la primera prueba formal de la mayor eficacia del metotrexato por vía subcutánea47, y cabe esperar que los resultados puedan extrapolarse al tratamiento de la psoriasis, aunque todavía no existe evidencia científica al respecto. La principal ventaja de la administración subcutánea es la mayor biodisponibilidad; se ha demostrado que cuando se pasa de la vía oral a la administración subcutánea de metotrexato (manteniendo la dosis) el aumento de efectividad en la artritis reumatoide se acompaña de un incremento en los niveles de poliglutamato intraeritrocitario, aunque pueden ser necesarios 6 meses hasta alcanzar el nuevo estado de equilibrio48.
Basándose en esta respuesta superior en el tratamiento de la artritis reumatoide se ha efectuado un análisis farmacoeconómico en España que indica que los costes adicionales del tratamiento con metotrexato por vía subcutánea se verían compensados por su mejora en efectividad49. En la tabla 1 se incluye un análisis de coste-efectividad incremental (sin análisis de sensibilidad o intervalos de confianza, por razones de espacio), que muestra el predominio del metotrexato subcutáneo sobre diversas alternativas terapéuticas (ciclosporina, adalimumab, infliximab) en el tratamiento de la psoriasis moderada a grave, a partir de los datos de los ensayos clínicos comparativos publicados.
En el tratamiento de la psoriasis la mayoría de dermatólogos (97%) y reumatólogos (80%) en Canadá inician el tratamiento por vía oral, pero eventualmente pasan a prescribirlo por vía parenteral un menor porcentaje de dermatólogos (49% frente a 96%) y la preferencia por la vía subcutánea también es menor entre los dermatólogos (63% frente a 98%)50.
Teniendo en cuenta que la utilidad de la dosis de prueba está siendo cuestionada (es una práctica frecuente iniciar el tratamiento con dosis de 10 a 15mg, con una adecuada selección de los pacientes)51, las ventajas en cuanto a eficacia45 y tolerabilidad gastrointestinal52 de la vía subcutánea en pacientes con artritis reumatoide probablemente puedan extrapolarse a los pacientes con psoriasis, y parece razonable suponer que se ampliará el uso del metotrexato por vía subcutánea en el ámbito dermatológico. A ello contribuirá sin duda la mayor familiarización de los pacientes dermatológicos con el empleo de inyecciones subcutáneas y la introducción de formulaciones con una mayor concentración de metotrexato (50mg/ml) en jeringas precargadas, que proporciona una mayor tolerabilidad y conveniencia53 y es preferida a la presentación con 10mg/ml por la mayoría de los pacientes tratados con dosis de 20mg semanales54. Por otra parte, las presentaciones monodosis permiten eliminar el impacto medioambiental y la exposición del personal sanitario, derivado de la manipulación y eventual desecho del contenido no aprovechado del vial o las jeringas55, lo que representa una ventaja adicional.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl autor ha recibido honorarios de Gebro Pharma y Pfizer como conferenciante y/o asesor y/o investigador en ensayos clínicos, así como de Marge Medica Books por la coordinación y coautoría de: Metotrexato y psoriasis. Barcelona: Marge Medica Books; 2012, patrocinado por Gebro Pharma.