Revisar la bibliografía sobre instrumentos específicos de medida de los resultados percibidos por los pacientes (patient reported outcomes, PRO) validados y utilizados en población española con psoriasis, valorar sus propiedades psicométricas y describir los resultados de su aplicación práctica.
Materiales y métodosRevisión sistemática de la literatura científica en bases de datos internacionales (PubMed/Medline) y nacionales (Medes, Ibecs) referente a estudios que validen o implementen instrumentos específicos de valoración de PRO en población española con psoriasis. Se completó la búsqueda en bases de datos específicas de instrumentos para medir PRO (BiblioPRO, PROQOLID). Se incluyeron los estudios publicados en inglés o español hasta el 01/09/2017. Adicionalmente, se revisaron las listas de referencias bibliográficas de las publicaciones clave identificadas. La valoración de la calidad metodológica de los cuestionarios se efectuó con base en sus propiedades psicométricas (constructo, adaptación transcultural, fiabilidad, validez, factibilidad y sensibilidad al cambio).
ResultadosSe seleccionaron 18 publicaciones. Seis artículos describieron la validación al español de 5 instrumentos de PRO: 4 cuestionarios de calidad de vida relacionada con la salud (CVRS) específicos de psoriasis/enfermedades dermatológicas y un cuestionario específico de satisfacción con el tratamiento. La valoración psicométrica muestra variabilidad en los criterios alcanzados por cada instrumento; el cuestionario de CVRS PSO-LIFE resultó el más completo. Los 12 artículos restantes correspondían a estudios observacionales que empleaban los instrumentos validados. Su utilización muestra un elevado impacto de la psoriasis en la CVRS, especialmente en pacientes jóvenes, de género femenino y con enfermedad grave.
ConclusionesSe han identificado 5instrumentos específicos validados en España para valorar los PRO en pacientes con psoriasis. Dada la variedad de sus propiedades psicométricas, resulta esencial conocer las fortalezas y debilidades de cada uno para seleccionar el instrumento apropiado para cada situación. El empleo de estos cuestionarios pone de manifiesto el elevado impacto de la enfermedad en la CVRS de los pacientes. La evaluación de los PRO en el paciente con psoriasis complementa los resultados clínicos tradicionales y puede contribuir a un manejo más óptimo de la enfermedad.
To review the literature on validated tools for measuring patient-reported outcomes (PROs) in psoriasis in Spain. To evaluate the psychometric properties of the tools and describe the results of their practical application.
Material and methodsSystematic review of studies validating or using instruments for assessing PROs in Spanish patients with psoriasis. Literature searches were performed in international (PubMed/Medline) and Spanish (Medes, Ibecs) databases. We also searched databases of instruments for measuring PROs (BiblioPRO, PROQOLID). The review included studies published in English or Spanish up to January 9, 2017. We also checked the reference lists of the key publications identified. The quality of the questionnaires was evaluated based on their psychometric properties (construct, transcultural adaptation, reliability, validity, feasibility, and sensitivity to change).
ResultsEighteen publications were included. Six articles described the validation of Spanish versions of 5 PROs tools: 4 health-related quality of life (HRQoL) questionnaires specific to psoriasis and dermatologic diseases and 1 questionnaire specific to satisfaction with treatment. Our assessment of the HRQoL tools’ psychometric properties showed that the PSO-LIFE questionnaire received the highest scores, although specific properties varied from instrument to instrument. The 12 remaining articles were observational studies that used the validated instruments. In use, these tools detected the high impact of psoriasis on HRQoL, especially in young female patients with severe disease.
ConclusionsWe identified 5 specific instruments validated in Spain for scoring PROs in patients with psoriasis. The tools’ psychometric properties vary, and it is essential to understand their strengths and weaknesses when selecting the right one for each situation. In use, these questionnaires are able to detect the high impact of psoriasis on patients’ HRQoL. PROs provide useful information to complement routine clinical findings in psoriasis and may contribute to improving disease management.
La psoriasis es una enfermedad inflamatoria crónica de la piel1 que puede alterar la calidad de vida de los pacientes de forma sustancial2 y que afecta tanto el bienestar físico como el psicológico1.
Para valorar la gravedad de la enfermedad y la eficacia del tratamiento se suelen utilizar medidas clínicas, como Psoriasis Area and Severity Index (PASI), Body-Surface Area (BSA) o Physician Global Assessment (PGA). Sin embargo, estas medidas no captan la perspectiva del paciente con respecto al impacto de los síntomas en la vida diaria1, por lo que es necesario incorporar resultados percibidos por el paciente (patient-reported outcomes, PRO). Actualmente, existen varios instrumentos para medir los PRO en psoriasis, sin criterios homogéneos sobre cuándo utilizar cada uno.
La calidad de vida relacionada con la salud (CVRS) es el PRO que ha recibido mayor interés en las últimas décadas, con un amplio abanico de cuestionarios genéricos (aplicables a distintas poblaciones), así como específicos, desarrollados para solventar la falta de sensibilidad de los cuestionarios genéricos3. La evaluación de otros PRO, como la satisfacción o las expectativas del paciente, se ha convertido en un aspecto de creciente interés. Sin embargo, en el campo de la psoriasis, este tipo de estudios y los cuestionarios específicos de valoración son escasos4.
Antes de utilizar un nuevo instrumento de medida de PRO, es imprescindible acreditar sus propiedades de medición3. Además, es importante tener en cuenta que la utilización de un instrumento en un contexto cultural diferente al original requiere un proceso sistemático y estandarizado de adaptación transcultural con posterior validación para el país de destino.
El objetivo de este trabajo es revisar la bibliografía sobre los instrumentos de medida de PRO específicos, validados y utilizados en población española con psoriasis, valorar sus propiedades psicométricas y describir los resultados de su aplicación práctica.
MétodosSe realizó una revisión sistemática de la literatura científica sobre estudios que validaran o utilizaran instrumentos específicos de valoración de PRO en población española con psoriasis. Se consultaron bases de datos españolas (Medes, Ibecs) e internacionales (PubMed/Medline) hasta el 1 de septiembre de 2017. La búsqueda se desarrolló según las recomendaciones descritas en el Manual Cochrane de Revisiones Sistemáticas de Intervenciones (Tabla suplementaria 1). Adicionalmente, se realizó una búsqueda en bases de datos específicas de instrumentos para medir PRO (BiblioPRO, PROQOLID). Finalmente, se revisaron las referencias bibliográficas de las publicaciones clave identificadas.
La selección de las publicaciones para su inclusión en el estudio se basó en los siguientes criterios: 1) el artículo hacía referencia al proceso de validación o a la utilización de un instrumento de PRO validado en población con enfermedades dermatológicas en general (incluyendo pacientes con psoriasis) o psoriasis en particular y 2) al menos el 50% de la población de estudio era española.
La selección de los artículos y la valoración de las propiedades psicométricas de los cuestionarios se llevó a cabo por 2revisores independientes. Las discrepancias de selección o de valoración fueron consultadas a un tercer investigador y resueltas por consenso.
La calidad metodológica de los cuestionarios de validación identificados se evaluó con base en sus propiedades psicométricas, siguiendo las recomendaciones de la FDA5, EMPRO6 y Medical Outcomes Trust7. Con el objetivo de proponer una evaluación precisa pero a la vez ágil para la práctica, el número de propiedades evaluadas se limitó a las 6 más relevantes: modelo conceptual y medición (3 ítems), adaptación transcultural (3 ítems), fiabilidad (2 ítems), validez (4 ítems), factibilidad (4 ítems) y sensibilidad al cambio (2 ítems) (Tabla suplementaria 2). Los revisores expresaron su grado de acuerdo con el cumplimiento y adecuación de cada ítem según una escala de 4puntos: totalmente de acuerdo (+++), bastante de acuerdo (++), un poco de acuerdo (+), sin evidencia o nada de acuerdo (Ø). La puntuación total asignada a cada instrumento se obtuvo a partir de la suma de las puntuaciones parciales de cada atributo (+=1 punto) y se transformó en una escala de 0 a 100: una puntuación más alta significa un instrumento con mejores propiedades psicométricas.
El nivel de evidencia de cada estudio se estableció con base en los niveles de evidencia Oxford Centre for Evidence-Based Medicine8.
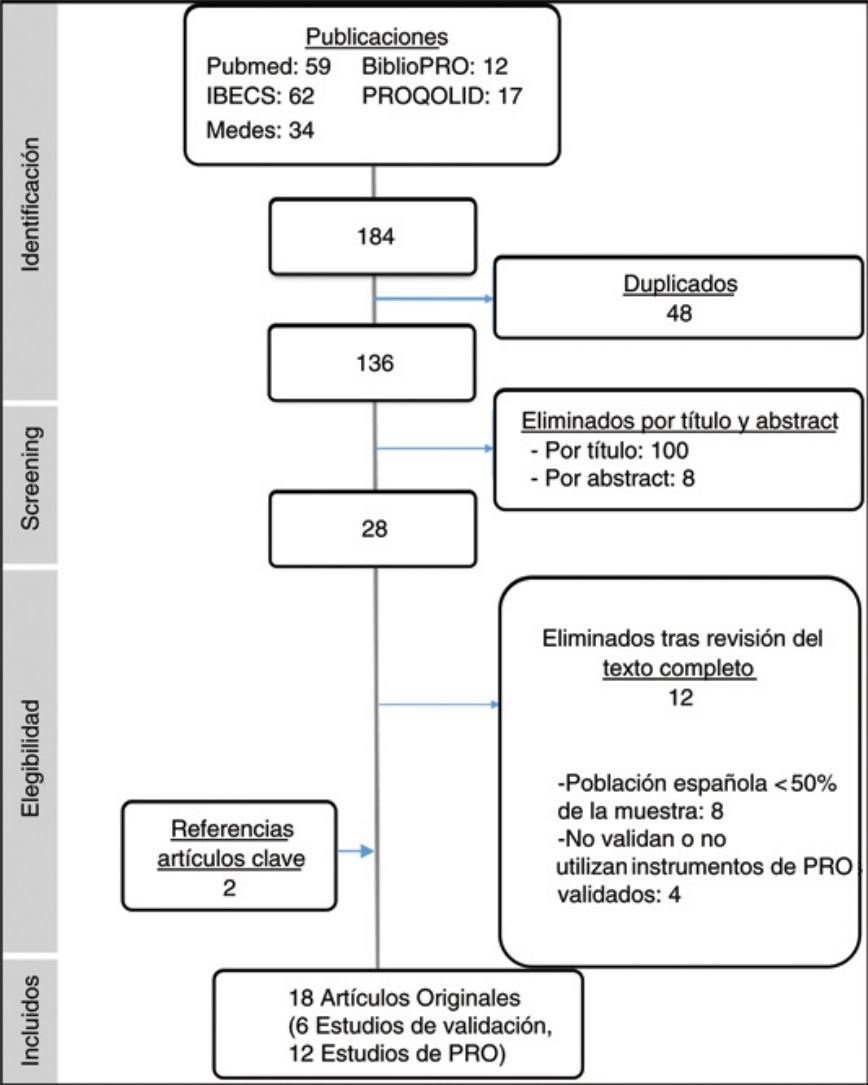
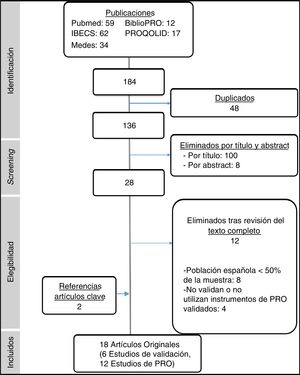
ResultadosSe identificaron 184 artículos y se consideraron 16 publicaciones relevantes para el objetivo del estudio. Adicionalmente, se recopilaron otras 2publicaciones a partir de las referencias de los artículos clave identificados (fig. 1). Seis publicaciones correspondían a estudios de validación al español de instrumentos de medida de PRO (tabla 1) y las 12restantes a estudios observacionales que habían empleado estos cuestionarios en población española (tabla 2). Los 12 artículos excluidos tras aplicar los criterios de selección se incluyen en la tabla suplementaria 3.
Descripción de los estudios de validación de instrumentos de PRO realizados en España
| Instrumento, autor (año), diseño y nivel de evidencia | Características de la muestra empleada | Variables analizadas relacionadas con la CVRS | Resultados | Conclusiones generales | |
|---|---|---|---|---|---|
| Instrumentos específicos para medir la CVRS en psoriasis | |||||
| PSO-LIFEDauden et al.19, 2012Observacional prospectivo y multicéntrico2C | - 304 pacientes con psoriasis activa o estable; y 56 pacientes con urticaria o dermatitis atópica (grupo control).- Edad media pacientes con psoriasis: 45,3 (14,5) años; grupo control: 38,8 (14) años; p <0,01.- Género (masculino). Pacientes con psoriasis: 56,3%; grupo control: 51,8% | CVRS: PSO-LIFE, DLQI, PDIClínicas: PASI | Modelo conceptual | - Descripción clara del concepto que se mide- Revisión de la literatura para establecer la relación entre la psoriasis y la CVRS percibida por el paciente- Identificación de dominios y selección de ítems relacionados con la CVRS en psoriasis a través de un grupo focal de expertos y entrevistas a pacientes- Análisis preliminar con pacientes | Los resultados apoyan la fiabilidad, validez y capacidad de respuesta del cuestionario PSO-LIFE en la población para la que fue diseñado |
| Adaptación transcultural | - Desarrollo de novo en población española con psoriasis | ||||
| Fiabilidad | - Buena consistencia interna (α de Cronbach=0,95)- Grado de reproducibilidad elevado (CCI=0,98) | ||||
| Validez | Contenido- Alta tasa de respuestas- Puntuación de ítems por un panel de expertos- Análisis factorial preliminar con pacientesConstructo- Análisis factorial: cuestionario unidimensionalCriterioConvergente- Diferencias puntuación PSO-LIFE entre pacientes con psoriasis y controles: p <0,03; entre psoriasis activa-inactiva: p <0,01; localización lesiones: p <0,01; enfermedad leve frente a moderada: p <0,01; psoriasis inactiva frente a grupo control: p >0,05- Correlación entre PASI y PSO-LIFE moderada (r=−0,43; p <0,01)- Correlación entre PSO-LIFE y DLQI y PDI de moderada a alta (entre −0,4 y −0,8)Longitudinal- Correlación en cambios de puntuación PASI y PSO-LIFE entre visita inicial-final a los 3 meses (r=−0,4; p <0,01).- Correlación en cambios de puntuación PSO-LIFE y DLQI y PDI de moderada a alta (r=−0,69 y r=−0,67, respectivamente | ||||
| Factibilidad | - Efecto suelo: 0%, efecto techo: 3,2%- Bajo % de ítems no respondidos: 5% | ||||
| Sensibilidad a los cambios | - Tamaño del efecto medio: 0,5, 0,73 en los pacientes con psoriasis activa y 0,29 en los pacientes con psoriasis inactiva- La MDCI a los 3 meses fue de aproximadamente 6,5 puntos. Se calculó utilizando los resultados de los pacientes que reportaron un estado de salud «levemente mejor» a los 3 meses | ||||
| PDIVanaclocha et al.3, 2005Estudio observacional, prospectivo y multicéntrico2C | -294 pacientes con psoriasis moderada o grave- Edad media: 43,1 años- Género (masculino): 58% | CVRS: PDI y EQ-5D (sistema descriptivo y escala visual analógica, EVA), percepción subjetiva de paciente e investigador sobre la gravedad de la psoriasisClínicas: PASI | Modelo conceptual | - Descripción clara del concepto que se mide- Descripción de dominios y número de ítems por dominio | La versión española del PDI presenta buenas cualidades psicométricas de fiabilidad, validez, factibilidad y sensibilidad a los cambios |
| Adaptación transcultural | - Método de traducción-retrotraducción20 | ||||
| Fiabilidad | - Buena consistencia interna (α de Cronbach=0,89) | ||||
| Validez | CriterioConvergente- Mayor puntuación en PDI en pacientes más graves (mayor puntuación PASI), r=0,33; p <0,01- Correlación entre PASI y PDI (r=0,33) y EVA (r=−0,41); p <0,01- Correlación PDI y EQ-5D, p <0,05- Correlación entre mayor gravedad de la psoriasis percibida por el médico y el paciente con mayor impacto en CVRS (mayor puntuación PDI), p <0,001Longitudinal- Cambios puntuación PDI entre visita inicial-final a los 6 meses correlacionaron con los cambios en PASI y EVA (r=0,39 y –0,51; p <0,001) | ||||
| Factibilidad | - El 87,1% contestó el cuestionario completo. El 98,6% contestó> 80% de las preguntas | ||||
| Sensibilidad a los cambios | - Tamaño del efecto adecuado: 0,95 | ||||
| Instrumentos específicos para medir la CVRS en enfermedades dermatológicas | |||||
| DLQIBadia et al.21, 1999Estudio observacional2C | N=237 pacientes con eccema (48%) y psoriasis (52%), población general (n=100) 143 pacientes con tratamiento de novo y 94 con enfermedad estableEdad media: eccema 40,3 años; psoriasis 38,7 años; población general 45,4 añosGénero (masculino): eccema 42,1%; psoriasis 51,2%; población general 32,3% | Patología: severidad clínica (valorada en escala de 4 puntos: ausente, leve, moderado, severo)Herramienta: DLQI y NHP | Adaptación transcultural22 | - Método de traducción-retrotraducción y prueba piloto- Consenso con los traductores y el autor original | La versión española de DLQI presenta un efecto suelo sustancial y una falta de sensibilidad al cambio en la mayoría de las dimensionesLos dominios de Reacciones emocionales y Movilidad del cuestionario genérico NHP respondieron mejor que algunos dominios DLQI. Probablemente sea aconsejable incluir instrumentos genéricos junto con el DLQI |
| Fiabilidad | - Buena consistencia interna (α de Cronbach=0,83)- Buen grado de reproducibilidad (CCI=0,88) | ||||
| Validez | Contenido- Proporción de respuestas no relevantes: 5% (pacientes)Constructo- Comparación de puntuaciones de pacientes con enfermedades dermatológicas y de la población general: puntuaciones de los pacientes significativamente más altas (4,3 vs. 0,27; p <0,001)CriterioConvergente- Correlaciones DLQI, las medidas de gravedad clínica y las puntuaciones de dominio en el cuestionario NHP. Las correlaciones fueron muy débiles, aunque significativas (p <0,001), variación: 0,12-0,32 en los dominios del NHP y 0,26 con las medidas clínicas | ||||
| Factibilidad | - Efecto suelo fue muy elevado para la mayoría de las dimensiones: aceptable (7%) en «percepciones»; alta (53-80%) en el resto de dimensiones.- Solo el 2% de los pacientes no respondieron uno o más ítems- Los pacientes tardaron una media de 7,6min (DE: 4,8 min) en completar el cuestionario autoadministrado | ||||
| Sensibilidad a los cambios | - Tamaño del efecto para el total de pacientes de novo: 0,70. Tamaño del efecto grande (0,82) para pacientes con eccema y moderado (0,58) para pacientes con psoriasis. Sin embargo, el tamaño del efecto resultó pequeño en la mayoría de las dimensiones (rango 0,03-0,35) y solo grande en la dimensión de síntomas y percepciones (1,0) | ||||
| Skindex-29Jones-Caballero et al.23, 2000: traducción, adaptación y validación preliminarEstudio observacional2C | N=103 personas con y sin enfermedades dermatológicas (psoriasis o dermatitis eccematosa, n=41)Edad media: 40 (16) añosGénero (masculino): 31% | Herramienta: Skindex-29 | Modelo conceptual | -Descripción clara del concepto que se mide- Descripción de dimensiones y número de ítems por dimensión- Traducción y adaptación cultural-Selección de ítems: participación de pacientes | Los resultados preliminares sugieren que la versión española de Skindex-29 es equivalente semánticamente, fiable y válida. Para confirmar la equivalencia de la versión española se necesitan la reproducibilidad y sensibilidad del instrumento |
| Adaptación transcultural | -Método de traducción-retrotraducción y estudio piloto-Testeo de la adaptación española con un grupo piloto de personas con y sin enfermedades dermatológicas para valorar la comprensibilidad | ||||
| Fiabilidad | - Buen grado de consistencia interna (α de Cronbach> 0,7)24 | ||||
| Validez | Contenido-Valoración de la relevancia del contenido con pacientes (n=58)-Evaluación de ítems en términos de claridad, comprensión, relevancia y redundanciaConstructo-Puntuaciones de pacientes con enfermedades dermatológicas significativamente más altas que la población general (p <0,01)- Puntuaciones de pacientes con dermatosis inflamatorias significativamente más altas que los pacientes con lesiones cutáneas aisladas (p <0,01)CriterioConvergente-Las puntuaciones entre la versión española y americana no fueron significativamente diferentes, a excepción de la escala emocional (menor en versión española, p <0,05) | ||||
| Skindex-29En 2002, Jones-Caballero et al.25, 2002: validaciónEstudio observacional prospectivo2C | N=318 pacientes dermatológicos (10% pacientes con psoriasis)Edad media: 36 (15) añosGénero (masculino): 35% | Herramienta: Skindex-29 | Fiabilidad | -Buen grado de consistencia interna (α de Cronbach> 0,84)-Buen grado de reproducibilidad (CCI> 0,7) | La versión española de Skindex-29 es en general un instrumento válido, fiable y sensible para medir los efectos de la afectación cutánea en la CVRS de pacientes españoles. La validación no incluyó comparaciones con otros cuestionarios de CVRS ni con variables clínicas. La escala funcional presenta un efecto suelo importante |
| Validez | Constructo-Puntuaciones de pacientes con enfermedades dermatológicas significativamente más altas que la población general (p <0,005)- Puntuaciones de pacientes con dermatosis inflamatorias significativamente más altas que los pacientes con lesiones cutáneas aisladas (p <0,005) | ||||
| Factibilidad | - Efecto techo y suelo adecuados. Solo la escala funcional presentó valores de efecto suelo> 20% (28%). En cuanto al efecto techo, < 1% de los pacientes alcanzan valores altos en sus puntuaciones de empeoramiento- Bajo % de no respuesta: el 7,5% de los individuos dejaron más de un 10% de ítems en blanco; falta de respuesta en cada ítem entre 0-1,9%- Tiempo de cumplimentación: 5 min | ||||
| Sensibilidad a los cambios | - Tamaño del efecto global (n=40): 0,76 | ||||
| Instrumentos específicos para medir la satisfacción con el tratamiento en psoriasis | |||||
| CESTEPRibera et al.4, 2011Estudio observacional prospectivo2C | N=423 pacientes con psoriasis moderada o grave- Edad media: 45,9 (13,9) años- Género (masculino): 61,9% | Patología:Índice PASI,Satisfacción con el tratamiento: CESTEP (cumplimentación del cuestionario en la visita basal y a los 3, 6, 9 y 12 meses de seguimiento) y valoración global de la satisfacción con el tratamiento mediante una escala EVA (0-100)Adherencia: Test Morisky-Green | Modelo conceptual | - Descripción clara del concepto que se mide- Identificación de dominios y selección de ítems relacionados con la satisfacción con el tratamiento en psoriasis a través de la revisión de la literatura y la colaboración de expertos y pacientes | CESTEP ha mostrado ser factible, válido y fiable en la población para la que fue diseñado |
| Adaptación transcultural | - Desarrollo de novo en población española con psoriasis | ||||
| Fiabilidad | - Alta consistencia interna (α de Cronbach=0,92)- Reproducibilidad adecuada (CCI=0,89) | ||||
| Validez | Constructo- Análisis factorial: una única dimensión explica el 54,6% de la varianza explicada por todos los ítems del cuestionarioCriterioConvergente- Correlación CESTEP en la visita basal fue baja con PASI (r=0,145; p=0,003) y alta con EVA (r=−0,806; p=0,001). La misma tendencia se observó durante el seguimiento, con coeficientes de correlación entre 0,38 y 0,33 para PASI y −0,75 y −0,81 para EVA | ||||
| Factibilidad | - Bajo porcentaje global de respuestas en blanco (1,2%) | ||||
| Sensibilidad a los cambios | - Tamaño del efecto global: 1,21 a los 3 meses, 1,07 a los 6 meses, 0,86 a los 9 meses, 0,92 a los 12 meses | ||||
Descripción de los estudios observacionales de CVRS realizados en España
| Autor (año), diseño y nivel de evidencia | Objetivo | Características de la muestra empleada | Variables analizadas relacionadas con la CVRS | Resultados CVRS | Conclusiones generales |
|---|---|---|---|---|---|
| López-Estebaranz et al. (2016)15Transversal2C | Analizar cómo las comorbilidades y la CVRS se ven afectadas por la historia familiar y la edad del paciente con Ps | N=1.022 pacientesTipo de Ps: 100% Ps moderada-grave (PASI> 10 o BSA> 10% o DLQI> 10)Género: 60,3% varonesEdad: 11,4% (18-30 años), 71,7% (31-60 años), 16,9% (> 60)Historia familiar: 46,8% | Patología: PASI, BSAHistoria familiarHerramienta: DLQI | DLQI18-30 años: 5,1 (DE: 5,3)31-60 años: 5,7 (DE: 6,5)> 60 años: 3,8 (DE: 5,1)Correlación directa DLQI con PASI (r=0,628, p <0,001) y BSA (r=0,609, p <0,001), mientras que n.° de comorbilidades no alcanzó significación estadística (r=0,016, p=0,621)La historia familiar de Ps afecta a la CVRS del paciente (OR=1,6; IC 95%: 1,2-2,3; p=0,002), independientemente de la gravedad de la enfermedad (puntuación PASI: OR=1,1, IC 95%: 1,1-1,2; p=0,000). La puntuación PGA impacta en la CVRS (p <0,05)Puntuación DLQI varió significativamente según la edad (5,1± 5,3 para el grupo de 18-30 años, 5,7±6,5 para el grupo de 31-60 años y 3,8±5,1 para el grupo de> 60 años; p=0,001) | La presencia de historia familiar de Ps afecta negativamente a la CVRS del paciente independientemente de la gravedad de la enfermedadLos pacientes más jóvenes tienen una CVRS más deteriorada que los pacientes con mayor edad |
| Martínez-Garcia et al. (2014)9Transversal2C | Analizar la influencia de la Ps en los niveles de ansiedad, depresión y CVRS de la gente que convive con los pacientes con Ps | PACIENTE N=34Tipo de Ps: Ps grave del cuero cabelludo (55%); Ps vulgaris con PASI> 5 (30%); Ps genital (15%)Género: 50% varonesEdad media: 43 años (19-82)Duración enfermedad: 15,6 añosCOHABITANTE N=49Género: 40,8% varonesEdad media: 40 años | Variables paciente: PASIVariables cohabitante: género, edad, estado civil, relación con el paciente, nivel educativo, situación laboral, nivel de ansiedad y depresiónHerramienta CVRS: DLQI y FDLQI | DLQI: 12 (1-28)FDLQI: 8,82 (0-30)Los pacientes con afectación genital presentan mayor impacto en su trabajo o vida académica (puntuación promedio ítem 7 del DLQI, 2 vs. 0,86; p=0,020) y en su vida sexual (puntuación promedio ítem 9 del DLQI, 1,8 vs. 0,52; p=0,008) Los pacientes con afectación del cuero cabelludo presentan más malestar o inhibición social (ítem 2, 2,33 vs. 1,53; p=0,03) y problemas por el tratamiento (ítem 10, 1,60 vs. 0,63; p=0,023)Asociación fuerte FDLQI con DLQI (r=0,554; p <0,001) y PASI de los pacientes (r=0,305; p=0, 033)BSA ≥ 10% se asoció a mayor puntuación FDLQI (11,42 vs. 6,32; p=0,013). Los cohabitantes de pacientes con afectación del cuero cabelludo (11,8 vs. 6,76; p=0,015) o genital (15,40 vs. 8,07; p=0,031) presentaron mayor puntuación FDLQI que los cohabitantes de pacientes con Ps en otras áreas | Se observa una fuerte asociación entre la CVRS del cohabitante (FDLQI) y la CVRS del paciente (DLQI), independientemente de las características del cohabitante |
| Molina-Leyva et al. (2014)16Prospectivo comparativo2C | Explorar la prevalencia de personalidad tipo D en pacientes con Ps moderada-grave y analizar su relación con las comorbilidades físicas y psicológicas y el impacto en la CVRS | N=80 pacientes del HU GranadaTipo de Ps: 100% Ps moderada-graveGénero: 50% varonesEdad media: 43,4 años (DE: 12,7)Duración enfermedad: 9 años (rango 3-27)Tratamientos: AB (48,7%), SC (33,7%), T (17,5%)Se compara con una muestra control de igual edad y sexo | Sociodemográficas: edad, sexoPatologíaComorbilidades: ansiedad/depresión, IMC, hipertensión, dislipemia, diabetes mellitusOtros: personalidad tipo D, fumarHerramienta CVRS: SF-36 y PDI | SF-36 (Pso vs. control):salud general: 53,0 vs. 48,4; función física: 84,6 vs. 97,4; rol físico: 74,7 vs. 90,0; salud mental: 61,0 vs 72,0; vitalidad,: 55,1 vs. 64,2; dolor: 65,3 vs. 79,2; función social: 79,3 vs. 87,0; (p ≤ 0,01). rol emocional: 80,8 vs. 82,1 (p=0,8)PDI:Actividades diarias: 21,2; trabajo/estudios: 13,3; relaciones: 12,2; ocio: 13,0; Tratamiento: 6,6Según PDI, los pacientes con Ps y personalidad tipo D sufren mayor impacto de la enfermedad en el trabajo (p=0,02) y en su vida personal (p=0,01), y una peor percepción sobre su tratamiento (p=0,02)Los pacientes con Ps tienen 2,1 veces más riesgo de desarrollar una personalidad tipo DLos pacientes con Ps y personalidad tipo D tienen 3,2 veces más riesgo de padecer ansiedad que los individuos con personalidad tipo D sin Ps | Los pacientes con Ps tienen una peor CVRS que los controlesLa personalidad tipo D se asocia a un deterioro general, sexual y de la CVRS |
| Fernández-Torres et al. (2014)17Transversal2C | Establecer la relación entre las características de la Ps (gravedad, artropatía, tratamiento) y las comorbilidades, y la CVRS del paciente. Identificar los factores que tienen mayor impacto en la CVRS | N=395 pacientes del HU A CoruñaTipo de Ps: en placaGénero: 59,7% varonesEdad media: 50,79 años (DE: 15,10)Duración enfermedad: 19,53 años (DE: 13,43)Tratamientos: AB (16,7%), SC (30,1%), T (51,4%) | Sociodemográficas: edad, sexoPatología: duración Ps, PASIComorbilidades: artropatíaTratamiento: biológico vs. sistémico convencional; biológico vs. tópicoHerramienta CVRS: DLQI | DLQI=4,17 (DE: 4,51)Variables asociadas con peor CVRS fueron la edad joven, el sexo femenino, la menor duración de la Ps y mayor puntuación BSA y PASI; p=0,000. Los pacientes con mayor duración de la Ps y más tiempo de tratamiento experimentan menor deterioro de la CVRS: OR=0,96 (IC 95%: 0,94-0,99; p=0,004). Un mayor índice de comorbilidad se asoció con mejor CVRS (p=0,005)Peor CVRS en pacientes con tratamiento sistémico tópico y convencional que en aquellos con biológicos (puntuación 4,36±4,71, 4,59±4,57 y 2,91±3,53, respectivamente, p=0,012). La presencia de PsA no se asoció con la CVRS (p=0,890)En el análisis multivariante, las variables asociadas con el deterioro de la CVRS fueron el sexo femenino (p=0,002), menor duración de la Ps (p=0,004), y tipo de tratamiento (p=0,053) | El análisis multivariante muestra el sexo (mujer), una mayor duración de la enfermedad, el tratamiento tópico como los principales determinantes de una peor CVRSLa gravedad de la enfermedad (PASI, BSA) no se asoció con la CVRS |
| Sánchez-Carazo et al. (2014)12Transversal2C | Determinar la asociación entre la CVRS y las comorbilidades en los pacientes con Ps moderada-grave | N=1.022 pacientesTipo de Ps: 89,1% en placas; 61% moderada, 39% grave; 37,3% enfermedad activaGénero: 60,3% varonesEdad media: 46,3 años (DE: 13,8)Duración enfermedad: 20 años (rango: 11,4-29,8),Tratamientos: AB (62,8%), SC (42,6%), F (19,0%), T (62,8%) | Sociodemográficas: géneroPatología: PASI, BSAComorbilidades: dislipidemias, PsA, hipertensión, obesidad, ansiedad, tuberculosis, alteración sueño, depresión, diabetes mellitus, enfermedad cardiovascularHerramienta CVRS: SF-36 y DLQI | SF-36PCS (total): 49,7PCS: PA=48,5 vs. No PA=50,4 (p <0,001)MCS: 46,2MCS: PA=43,2 vs. No PA=48,0 (p <0,001)Menor PCS (peor CVRS) en pacientes con Ps y PsA, presión arterial alta, diabetes mellitus, alteraciones del sueño u obesidad (p <0,05). Menor MCS en mujeres y afectados por depresión o ansiedad (p <0,05)Correlación negativa entre gravedad de la Ps y PCS (PASI, r=−0,160, p=0,0; BSA, r=−0,173, p=0,0) y MCS (PASI, r=−0,227, p=0,0; BSA, r=−0,214, p=0,0)DLQITotal: 5,2PA=9,3 vs. No PA=3,0 (p <0,001)Pacientes con Ps y ansiedad tuvieron peor CVRS según DLQI (p <0,05)Correlación positiva entre DLQI y PASI (r=0,628, p=0,0) y BSA (r=0,609, p=0,0) | Independientemente del sexo, los pacientes con comorbilidades graves como PsA, hipertensión u obesidad presentan una CVRS más deteriorada, principalmente en el componente físicoLas mujeres presentan una mayor afectación del componente mental de la CVRS que los hombres |
| Daudén et al. (2013a)2Prospectivo2C | Valorar el impacto de la Ps en la CVRS mediante diferentes cuestionarios de evaluación | N=304 pacientesTipo Ps: 100% Ps en placa. 60% Ps activa (PA) y 40% estable (PsE)Género: 56,3% varonesEdad media: 45,3 años (DE: 14,5)Duración enfermedad: 18,3 años (DE: 12,2),Tratamientos: AB (38,2%), SC (51%), T (44,1%) | Patología: actividad y localización de la enfermedadHerramienta CVRS: DLQI y PDI | DLQIPA=7,03 (V1) vs. 3,5 (Vf); PsE=2,59 (V1) vs. 2,06 (Vf)PDIPA=8,25 (V1) vs. 4,2 (Vf); PsE=3,61 (V1) vs. 5,52 (Vf)PSO-LIFEPA=57,4 (V1) vs. 72,2 (Vf); PsE=76,4 (V1) vs. 82,3 (Vf)Según PSO-LIFE, puntuaciones diferentes según la localización de las lesiones: zonas visibles (cabeza o extremidades superiores) (63, DE: 22) mayor afectación que zonas no visibles (tronco y extremidades inferiores) (74,8, DE: 23,9) y que pacientes sin lesiones en la visita basal (78,5, DE: 21,6); p <0,01)Correlación moderada PSO-LIFE y PASI: r=−0,4; correlación DLQI y PDI con PASI: r=0,5 y 0,4, respectivamenteMayor tamaño del efecto para PSO-LIFE que para los otros cuestionarios de CVRS | Los pacientes con PA presentan peor CVRSLas diferencias entre pacientes con PA y PsE obtenidas en los cuestionarios fueron mayores en PSO-LIFE, con mayor capacidad discriminatoriaMejoría en la CVRS entre V1 y Vf, asociada a la mejora en la enfermedad gracias al tratamiento. Mayor sensibilidad al cambio del cuestionario PSO-LIFE, respecto al restoLa localización de las lesiones y PASI correlacionaron de forma significativa con las puntuaciones de PSO-LIFE |
| Daudén et al. (2013b)13Prospectivo2C | Determinar la CVRS del paciente con Ps moderada a grave | N=1.217 pacientesTipo Ps: moderada-grave (PASI ≥ 10, PGA ≥ 5, BSA ≥ 10%)Género: 60,8% varonesEdad media: 45,11 años (DE: 13,92)Tratamientos: AB (36,1%), SC (27,6%), T (53,6%), F 14,1%, otros (17,5%) | Sociodemográficas: sexo, edad, peso, fumador, nivel educacional y situación laboralPatología: edad al inicio, numero exacerbaciones, PASI, comorbilidades, tratamiento, área afectadaHerramienta CVRS: SF-36, EQ-5D, DLQI y PDI | SF-36PCS V1=49,43 (DE: 8,83) vs. V2=50,81 (DE: 8,34)MCS V1=45,35 (DE: 11,96) vs. V2=48,07Dimensiones con mejor puntuación en V1: funcionamiento físico (83,67 [21,44]), rol emocional (81,33 [23,63]) y el rol físico (78,02 [25,97]); dimensiones con mayor mejoría entre V1 y V2: funcionamiento social (de 76,14 [25,82] a 83,80 [22,09]), función física (de 78,02 [25,97] a 83,58 [22,48]) y dolor corporal (de 67,08 [29,35] a 73,56 [27,96]); p <0,001EQ-5D (EVA)V1=64,41 (DE: 18,0) vs. V2=72,44 (DE: 17,88)Dimensiones EQ-5D con menor puntuación en V1: dolor (1,57 [0,58]) y ansiedad/depresión (1,42 [0,56]); dimensiones con mayor mejoría entre V1 y V2: dolor (1,48 [0,60]) y ansiedad/depresión (1,35 [0,55])DLQIV1=8,97 (DE: 7,28) vs. V2=4,76 (DE: 5,72); (p <0,001)PDIV1=9,24 (DE: 8,76) vs. V2=4,88 (6,66); (p <0,001)PASI (b=0,405; p <0,001) y género (b=0,075; p=0,048) son los factores que determinan la CRVS | La gravedad de la enfermedad es el principal factor asociado con la CVRS en pacientes con PsEn todos los casos se observa una mejoría de la CVRS entre V1 y V2 |
| Fernández-Torres et al. (2012)10Prospectivo2C | Comparar las características clínicas, prevalencia de comorbilidades y CVRS del paciente con Ps mayor de 65 años y los pacientes jóvenes | N=371 pacientesTipo de Ps: 76% Ps en placasGénero: 58,8% varonesEdad media: 50 años (DE: 14,5); 18,9%> 65 añosDuración enfermedad: 19,3 años (DE: 13,22)Tratamientos: AB (18,0%), SC (32,1%), T (47,9%), SC+AB (2%) | Sociodemográficas: edadTratamientoHerramienta CVRS: DLQI | DLQI<65 años=5,49 (DE: 6,0) vs.> 65 años=3,89 (DE: 5,03); (p=0,012).Los pacientes en tratamiento con SC y AB presentaban mejor CVRS (p=0,012) | Los pacientes < 65 años presentan peor CVRS que los pacientes> 65 añosEn ambos grupos, el picor y la vergüenza eran las quejas más frecuentesLa CVRS se veía afectada por el tipo de tratamiento |
| Hernánz et al. (2012)14Transversal2C | Describir las características clínicas y el perfil terapéutico de los pacientes con Ps moderada a grave en el ámbito español, evaluando su impacto en la CVRS de los pacientes | N=442 pacientesTipo de Ps: 76.2% Ps moderada, 23,8% Ps graveGénero: 62,2% varonesEdad media: 46,7 años (DE: 13,9)Duración enfermedad: 13,1 años (DE: 11,0)Tratamientos: AB (57,5%), SC (32,6%), F (11,0%), T (27,2%), otros (10,3%) | Sociodemográficas: edadPatología: PASI, duración Ps, gravedad y localización de la enfermedadComorbilidades: patología psiquiátricaHerramienta CVRS: DLQI | DLQITotal población=6,7 (DE: 6,6) vs. Ps grave=9,2 (DE: 7,8) y Ps moderada=5,9 (DE: 6,0); p <0,001)Ps grave implica peor puntuación en todas las dimensiones del DLQI (p <0,01, relaciones personales; p <0,001, resto de dimensiones)El 60% de los pacientes con Ps grave tiene CVRS mala o insatisfactoria, vs. 39,8% con Ps moderada (p> 0,001)Pacientes con mejor CVRS tienen mayor edad (48,0±13,9 vs. 44,9±13,8 años, respectivamente; p <0,05), independientemente de la gravedad de la Ps, y mayor tiempo desde el diagnóstico de la enfermedad (14,1±11,8 11,8±9,7 años, respectivamente; p <0,05) vs. los de peor CVRSPeor CVRS se asoció con mayor afectación del cuero cabelludo (74,1 vs. 48,5%; p <0,001), ungueal (48,7 vs. 34,0%) (p <0,001), zonas genitales (24,9 vs. 11,9%; p <0,001) y flexuras (25,9 vs. 14,9%; p <0,01), y mayor prevalencia de enfermedad psiquiátrica (15,7 vs. 4,5%; p <0,001)Factores asociados con la CVRS: edad del paciente es un factor protector (OR: 0,973; IC 95%: 0,957-0,989); afectación del cuero cabelludo (OR: 2,260; IC 95%: 1,401-3,645), enfermedad psiquiátrica (OR: 5,105; IC 95%: 2,177-11,972) y PASI (OR: 1,067; IC 95%: 1,037-1,098) se asociaron con peor CVRS | El 60% de los pacientes con Ps grave reportaba una CVRS mala o insatisfactoria, en comparación con solo el 39,8% de aquellos pacientes con Ps moderada (p> 0,001)La edad es un factor protector de la CVRS, mientras que la afectación del cuero cabelludo, genital, ungueal y flexuras, así como la enfermedad psiquiátrica y el incremento del PASI se asocian con un aumento en el riesgo de tener una peor CVRS |
| Fernández-Peñas et al. (2011)18Prospectivo2C | Comparar las características de los distintos instrumentos de CVRS en pacientes con distinto grado de gravedad de Ps | N=379Tipo Ps: 40% grave (PASI≥12), 32% moderado (PASI 7-12), 24% leve (PASI> 7), 4% PASI desconocido | Herramienta CVRS: SF-36, DLQI, PDI y Skindex-29 | Skindex-29 (379 pacientes); DLQI (144 pacientes); PDI (133 pacientes); SF-36 (100 pacientes)DLQI, PDI y Skindex-29 no detectan diferencias en la CVRS en función del sexo o edad. El SF-36 muestra una mejor CVRS en mujeres que en hombres y la dimensión «dolor corporal» se correlaciona con la edadSkindex-29 muestra una correlación débil-moderada (escala síntomas r <0,35) pero significativa (p <0,01) con PASI, al igual que PDI (r=0,19, p <0,05)Efecto suelo importante en la mayoría de las subescalas del DLQI (5 de 6): actividades diarias (29%), ocio (36%), relaciones personales (51%), trabajo y escuela (50%) y tratamiento (31%); así como para PDI (4 de 5) y SF-36 (5 de 8). El efecto de suelo o techo pequeño (< 5%) para las escalas de Skindex-29 | La mayoría de las subescalas de PDI, DLQI y SF-36 tienen un efecto suelo sustancial, lo que indica que su sensibilidad al cambio de moderado a grave sería bajaSkindex-29 presenta mejor sensibilidad a la gravedad clínica y efecto suelo mínimoSkindex-29 tiene una fuerte correlación con los otros 3 instrumentos |
| Melero et al. (2011)26 Retrospectivo/transversal5 | Conocer las variables sociodemográficas, la localización y el tipo de Ps, el tiempo de evaluación, comorbilidades, la pertenencia a asociaciones, la relación con el médico y los conocimientos sobre Ps | N=200 pacientesTipo dePs: 78% moderada-leve, 53% en placas, 37,5% enfermedad activa (brote)Género: 48% varonesEdad media: 46,21 añosDuración de la enfermedad: el 60,5% llevaban más de 10 años diagnosticadosTratamientos: no especificado | No analiza los factores que determinan la CVRSHerramienta CVRS: SF-36 y Skindex-29 | SF-36Skindex-29(no reporta los datos)El 84% de los participantes refirió empeoramiento de la enfermedad con el estrés, el 49,5% de ellos indicó que había sufrido un trastorno emocional en el último año | Los resultados muestran la importancia de los factores emocionales en la sintomatología de la Ps |
| Ferrándiz-Foraster (2007)11Transversal2C | Conocer la repercusión de la Ps moderada-grave en la CVRS evaluada por medio de PDI | N=3.320 pacientes (90% españoles, 10% portugueses)Tipo de Ps: 100% moderada-grave; 80% en placasGénero: 57% varonesEdad media: 46,74 años (IC 95%: 46,19-29)Duración enfermedad: 18 años (IC 95%: 17,44-18,46)Tratamiento: AB, SC | Sociodemográficas: edad, sexo, antecedentes personales y familiares, n.° de cigarrillosPatología: PASI, BSA, gravedad global, pruritoCostes directos: visitas dermatólogo, días de bajaCostes indirectos: días de baja en el último añoDisposición a pagar por verse libre de lesionesTratamiento recibido en últimos 2 añosComorbilidades: PsAHerramienta CVRS: PDI | PDI=8,93 (IC 95%: 7,83-9,21), que representa 19,9% de discapacidadEfecto suelo entre 8,3 y 64,5%; efecto techo 0-3%Correlación débil entre PDI con PASI (r=0,275; p <0,001) y con BSA (r=0,258; p <0,001)Peor CVRS en mujeres (p <0,001) y pacientes más jóvenes (≤30 años) (p <0,05)Factores asociados con la CVRS (p <0,05): sexo femenino, n.° de cigarrillos, PASI, tratamiento sistémico en los últimos 2 años,PsA, el gasto mensual debido a Ps, lesiones en la cabeza, prurito, n.° de visitas al dermatólogo en el último año, días de baja en el último año y meses de vida y % de sueldo dispuesto a dar por estar libre de lesiones | Discapacidad global de la muestra < 20%. La correlación entre PDI y la gravedad de la enfermedad (PASI y BSA) era débil, aunque significativa. A mayor afectación de la Ps, mayor impacto en la CVRS. PDI no parece ser el instrumento idóneo para determinar la CVRS en estos pacientes |
Nivel de evidencia: 2C: Outcomes research, estudios ecológicos; 5: Opinión de expertos sin valoración crítica explícita, o basados en la fisiología, bench research o first principles. AB: agente biológico; CVRS: calidad de vida relacionada con la salud; DLQI: Dermatology Life Quality Index (0: mín; 30: máx impacto); EQ-5D: (0: peor; 100: mejor CVRS); F: fototerapia; FDLQI: Family Dermatology Life Quality Index (0: mín; 30: máx impacto); IC: intervalo de confianza; MCS: puntuación del componente mental; OR: odds ratio; PA: psoriasis activa; PCS: puntuación del componente físico; PDI: Psoriasis Disability Index (0: mín; 45: máx impacto); Ps: psoriasis; PsA: artritis psoriásica; PSO-LIFE: (0: máx; 100: mín impacto); SC: sistémico convencional; SF-36: (0: peor; 100: mejor CVRS); T: tópico; V1: visita 1; V2: visita 2; Vf: visita final.
De los 6artículos que reportaban el proceso de validación al español (tabla 1), 5se referían a cuestionarios de CVRS (2 de ellos hacían referencia a la validación del mismo cuestionario) y uno reportaba la validación de un cuestionario de satisfacción con el tratamiento. De los 4cuestionarios de CVRS identificados, 2eran específicos de enfermedades dermatológicas y 2eran cuestionarios específicos de psoriasis desarrollados o validados en España. En la tabla 3 se resumen estos instrumentos, sus características y disponibilidad y en la tabla 4 se presenta la valoración de sus propiedades psicométricas.
Instrumentos específicos validados o utilizados en pacientes con psoriasis en España
| PRO | Enfermedad | Instrumento | País | Características generales | Disponibilidad/acceso versión español |
|---|---|---|---|---|---|
| CVRS | Psoriasis | PSO-LIFE19 | España | -Único cuestionario específico realizado en España para evaluar la CVRS en psoriasis- Consta de 20 ítems valorados en una escala de 5 puntos, los cuales miden diversos aspectos de CVRS relevantes para individuos con psoriasis, incluyendo: síntomas, impacto sobre el bienestar emocional, relaciones, actividades y ocio- La puntuación total oscila entre 20 y 100 (a mayor puntuación, mejor CVRS)- Con el fin de simplificar su interpretación y validar el cuestionario PSO-LIFE, la puntuación se transformó en una escala de 0 a 100 (una puntuación más alta indica mejor CVRS) | No disponible. Solicitar a los autores27 |
| PDI3 | Reino Unido | - Consta de 15 ítems, valorados en una escala de 0 a 3, distribuidos en 5 dimensiones: actividades diarias (5 ítems), trabajo/estudios (3 ítems), relaciones personales (2 ítems), ocio (4 ítems) y tratamiento (1 ítem), referidos a las 4 semanas previas- La puntuación total oscila entre 0 y 45 (a mayor puntuación, mayor impacto en la CVRS)3,19- Interpretación de la puntuación: 0=ninguna discapacidad, 1-4=discapacidad leve, 5-9=moderada, 10-18=elevada, y 19-45=discapacidad muy elevada28 | http://sites.cardiff.ac.uk/dermatology/quality-of-life/psoriasis-disability-index-pdi/pdi-different-language-versions/ | ||
| Enfermedades dermatológicas | DLQI21 | Reino Unido | - Constituido por 10 ítems, valorados en una escala de 4 puntos: síntomas, actividades diarias, ocio, trabajo/estudio, relaciones personales y efectos del tratamiento- La puntuación oscila entre 0 (impacto mínimo en la CVRS) y 30 (impacto máximo en la CVRS)19- Interpretación de la puntuación (impacto de la psoriasis en la vida del paciente): 0-1=ningún efecto en absoluto, 2-5=efecto pequeño; 6-10=efecto moderado (puntuaciones de 6 a 10), 11-20=efecto muy grande y 21-30=efecto extremadamente grande17- Tiempo medio de cumplimentación: 2 minutos29 | http://sites.cardiff.ac.uk/dermatology/files/2014/07/DLQI-Spanish.pdf | |
| Skindex-2923,25 | EE. UU. | - Se centra en 3 dimensiones: funcional (12 ítems), emocional (10 ítems) y sintomática (7 ítems). Cada ítem se valora en una escala de 4 puntos- La puntuación de cada dimensión se obtiene transformando la suma de las respuestas en una escala lineal de 100, variando desde 0 (ausencia de impacto en la CVRS) hasta 100 (máximo impacto en la CVRS)- Interpretación de la puntuación: afectación leve de la CVRS (punto de corte: 25 puntos), moderada (punto de corte: 32) y grave (punto de corte: 44 puntos). Como regla general, se redondean los puntos de corte para deterioro leve, moderado y grave a las puntuaciones de 20, 30 y 40, respectivamente, tanto para la puntación global como para los diferentes dominios, exceptuando los síntomas (leve=39, moderado=42 y severo=52)30El estudio llevado a cabo por Nijsten et al.31 estableció una categorización de puntuaciones diferente, la cual puede establecerse como afectación muy leve (puntuación <5), leve (6-17), moderada (puntuación 18-36) y grave (puntuación>37) | Solicitud vía e-mail27 | ||
| Satisfacción | Específico | CESTEP4 | España | - Constituido por 12 ítems, valorados con una escala de 0 (muy satisfecho) y 5 (muy insatisfecho)- Puntuación total entre 0 (máximo valor posible de satisfacción) y 48 puntos (máximo valor posible de insatisfacción) | No disponible. Solicitar a los autores27 |
CESTEP: Cuestionario Español de Satisfacción de Tratamiento en Psoriasis; CVRS: Calidad de Vida relacionada con la Salud; DLQI: Dermatology Life Quality Index; PDI: Psoriasis Disability Index; PSO-LIFE: Psoriasis Quality of Life.
Valoración de las propiedades psicométricas de los instrumentos de medición de PRO específicos de psoriasis/enfermedades dermatológicas validados en España
| CVRS | Satisfacción | ||||
|---|---|---|---|---|---|
| Específicos | Específico | ||||
| AtributoaCuestionario | PSO-LIFE | PDI | DLQI | Skindex-29 | CESTEP |
| Modelo conceptual y de medición | |||||
| Descripción del concepto que se mide | + | +++ | +++22 | +++ | +++ |
| Obtención y combinación de ítems | ++ | + | ++22 | ++23 | ++ |
| Implicación de pacientes en la elaboración | +++ | Ø | +++ | ++23 | ++ |
| Adaptación transcultural | |||||
| Equivalencia lingüística | +++b | + | +++22 | +++23 | +++b |
| Equivalencia conceptual | +++ | Ø | ++22 | +++23 | +++ |
| Diferencias entre original y versiones adaptadas | +++ | Ø | Ø | ++23 | +++ |
| Fiabilidad | |||||
| Consistencia interna (α de Cronbach) | +++ | ++ | + | +++ | +++ |
| Test-retest (CCI) | +++ | Ø | ++ | +++ | ++ |
| Validez | |||||
| Validez del contenido | +++ | Ø | ++ | ++23 | +++ |
| Validez del constructo | |||||
| Análisis factorial | ++ | Ø | Ø | Ø | ++ |
| Método de grupos conocidos/extremos | + | Ø | + | + | Ø |
| Validez de criterio | ++ | ++ | + | Ø | ++ |
| Factibilidad | |||||
| Viabilidad | |||||
| Efecto techo y suelo | +++ | +18 | + | ++ | Ø |
| % de no respuesta | +++ | ++ | +++ | +++ | +++ |
| Simplicidad | |||||
| Modo de administración | ++ | ++ | ++ | ++ | ++ |
| Tiempo de cumplimentación | Ø | Ø | ++ | Ø | Ø |
| Sensibilidad a los cambios | |||||
| Prueba del tamaño del efecto | ++ | +++ | ++ | ++ | +++ |
| Mínima diferencia clínicamente importante (MDCI) | +++ | Ø | Ø | Ø | Ø |
| Puntuación global (sobre 100) | 78 | 31 | 56 | 61 | 67 |
Se han identificado 12 estudios observacionales realizados en España que evalúan la CVRS en población con psoriasis (pueden incluir pacientes con otras enfermedades dermatológicas), mediante alguno de los cuestionarios identificados (tabla 2). Estos estudios medían la CVRS percibida por los pacientes mediante cuestionarios específicos y 5de ellos complementaban la información con cuestionarios genéricos. El cuestionario DLQI fue utilizado en el 69,2% de los estudios identificados, PDI y SF-36 en el 38,5%, Skindex-29 en el 15,4% y PSO-LIFE y EQ-5D en el 7,7%. Un estudio valoraba además la CVRS de las personas que convivían con los pacientes mediante un instrumento específico para enfermedades dermatológicas (Family Dermatology Life Quality Index, FDLQI)9.
Los resultados de estos estudios evidencian el impacto negativo de la psoriasis en la CVRS de los pacientes y en sus familiares (tabla 2).
Determinantes de la calidad de vida relacionada con la salud en pacientes con psoriasisCaracterísticas sociodemográficas del pacienteEl estudio del impacto de las características sociodemográficas del paciente en su CVRS muestra un mayor deterioro de la CVRS en mujeres10-13, pacientes jóvenes10,14,15, con historia familiar de psoriasis15, personalidad tipo D (con estrés negativo)16, pacientes con artritis psoriásica11,12, otras comorbilidades, principalmente psiquiátricas12,14 y en pacientes que consumen tabaco o alcohol11,17 (tabla 5). Adicionalmente, se establece una fuerte asociación (r=0,554; p<0,001) entre la CVRS del cohabitante (FDLQI) y la del paciente (DLQI), independientemente de las características del cohabitante9.
Factores determinantes de la CVRS del paciente con psoriasis
| Características sociodemográficas del paciente | Características de la enfermedad | Tratamiento | |||||||||||||
| Género (mujer) | Edad (jóvenes) | PsA | Comorbilidades (mayor) | Historia familiar | Personalidad Tipo D | Tabaco o alcohol | PASI (mayor) | BSA (mayor) | PGA (mayor) | Duración (mayor) | Afectación cuero cabelludo | Afectación genital | AB | SC | |
| López-Estebaranz et al., 201615 | - | x | - | - | - | - | |||||||||
| Molina-Leyva et al., 201416 | - | ||||||||||||||
| Fernández-Torres et al., 201417 | - | - | x | + | - | - | - | + | +^ | ||||||
| Sánchez-Carazo et al., 201412 | - | - | - | - | - | ||||||||||
| Martínez-García et al., 20149 | - | - | - | - | |||||||||||
| Daudén et al., 2013b13 | - | - | |||||||||||||
| Fernández-Torres et al., 201210 | - | +¿ | +¿ | ||||||||||||
| Hernánz et al., 201214 | - | - | - | - | - | ||||||||||
| Ferrándiz-Foraster et al., 200711 | - | - | - | - | - | -* | |||||||||
AB: agente biológico; PsA: artritis psoriásica; SC: sistémico convencional; X sin impacto en la CVRS;
Símbolos no alfabetizables: -: impacto negativo en la CVRS; +: impacto positivo en la CVRS; *: en comparación con fármacos biológicos; ^: en comparación con fármacos tópicos o sistémicos convencionales; ¿: en comparación con fármacos tópicos.
Las características propias de la enfermedad, como su gravedad, extensión y tiempo de evolución, entre otras, pueden afectar a la CVRS del paciente. Las variables clínicas que presentan mayor asociación con la CVRS en España son la gravedad de la enfermedad evaluada mediante el PASI9,11-15,17 y, en menor medida, mediante el BSA12,15 (tabla 5). Dauden et al.13 muestran que los principales factores relacionados con la CVRS son la gravedad medida por PASI (p <0,001) y el género (p=0,048). Ferrándiz-Foraster et al.11 detectan correlaciones débiles, aunque significativas (p <0,001), entre PDI y las variables de gravedad (PASI y BSA). En el estudio de Hernanz et al.14, el mayor predictor de CVRS es la comorbilidad psiquiátrica, con una OR=5,105, mientras que la puntuación PASI es un predictor más débil, con una OR=1,067. Fernandez-Peñas et al. encuentran una correlación débil-moderada entre PASI y Skindex-29 (r <0,35) y solo significativa en alguna dimensión, mientras que para DLQI no es significativa (r=0,13), y para PDI es débil pero significativa (r=0,19)18. Finalmente, Dauden et al.19 hallan una correlación moderada para PSO-LIFE y PASI (r=−0,4; p <0,01) (tabla 1); mientras que López-Estebaranz et al.15 hallan una correlación importante entre DLQI y PASI (r=0,628; p <0,001), así como una asociación entre la puntuación PGA y el efecto en la CVRS del paciente, valorada por DLQI (p <0,05) (tabla 2).
La localización de las lesiones también es un factor determinante de la CVRS. Daudén et al. establecen una asociación entre mayor afectación de zonas visibles y peor CVRS, según el cuestionario PSO-LIFE, frente a las zonas no tan visibles (p <0,01)2. Hernanz et al. encuentran que una peor CVRS, valorada con el cuestionario DLQI, se asocia de forma significativa con mayor afectación en cuero cabelludo (74,1 vs. 48,5%; p <0,001), ungueal (48,7 vs. 34,0%; p <0,001), genital (24,9 vs. 11,9%; p <0,001) y de flexuras (25,9 vs. 14,9%; p<0,01)14. Martínez-García et al. establecen también que los pacientes con psoriasis genital presentan mayor impacto en su actividad laboral o académica (p=0,020) y su vida sexual (p=0,008)9. Asimismo, el impacto de la psoriasis en la CVRS de los cohabitantes de pacientes con afectación del cuero cabelludo (11,8 vs. 6,76; p=0,015) o genital (15,40 vs. 8,07; p=0,031), medida con el cuestionario FDLQI, fue mayor que en los cohabitantes de pacientes con psoriasis en otras áreas9 (tabla 2).
Con relación a la actividad de la enfermedad, los trabajos muestran peor CVRS en pacientes con enfermedad activa, en comparación con aquellos con enfermedad estabilizada2,12. Otros factores clínicos, como la duración de la enfermedad17, tienen un impacto positivo en la percepción de la salud por parte del paciente. Los pacientes con mayor duración de la psoriasis y con más tiempo de tratamiento experimentan un menor deterioro de la CVRS (OR=0,96; IC del 95%: 0,94-0,99; p=0,004)17.
Tratamiento que recibe el pacienteTres estudios determinan el impacto del tratamiento en la CVRS del paciente. Uno de ellos reporta mejor CVRS en pacientes que reciben fármacos biológicos o terapias sistémicas convencionales frente a tratamientos tópicos10. El segundo muestra mejor CVRS en pacientes con biológicos que en aquellos con tratamiento tópico o sistémico convencional17. Finalmente, el último estudio señala que el tratamiento sistémico es una variable predictiva de una peor CVRS, en comparación con los pacientes que reciben fármacos biológicos11.
DiscusiónLa medición de los PRO, principalmente la CVRS, adquiere cada vez más relevancia en la evaluación de la salud de la población y de la efectividad de las intervenciones sanitarias. En psoriasis, los instrumentos de medida de la CVRS se han desarrollado para intentar conocer de forma objetiva cómo afecta la enfermedad a la vida del paciente desde un punto de vista holístico.
La medición de la CVRS en la práctica clínica requiere de cuestionarios que puedan administrarse de manera rápida y sencilla y, a la vez, permitan obtener resultados fiables y válidos. La generación de novo de un cuestionario es un proceso laborioso, que consume mucho tiempo y recursos. La adaptación transcultural tampoco es un proceso sencillo, pero permite obtener instrumentos utilizables en estudios interculturales.
Actualmente existen varios cuestionarios adaptados y validados al español para pacientes con psoriasis, específicos de enfermedades dermatológicas (DLQI21 y Skindex-2925) o específicos de psoriasis (PDI3). Asimismo, existe un cuestionario específico de psoriasis desarrollado y validado en España: PSO-LIFE19. Estos cuestionarios valoran aspectos de la vida cotidiana claramente afectados por la enfermedad, por lo que sus resultados son fundamentales para el manejo clínico de la psoriasis13. Sin embargo, los cuestionarios validados presentan ciertas limitaciones como parte de su proceso de adaptación, y algunos cuentan además con la dificultad de que no cubren áreas de la vida significativas para la población española, dado que han sido desarrollados en otros entornos culturales19.
El cuestionario DLQI21 es el más utilizado por su brevedad y simplicidad32. No obstante, presenta un efecto suelo importante (que dificulta la detección de empeoramientos en la CVRS percibida), no capta completamente el estado emocional ni la salud mental, y puede no ser suficientemente sensible para detectar pequeñas disfunciones32. Por su parte, Skindex-2925 posee en general buenas propiedades de medición, pero presenta un efecto suelo considerable. El cuestionario PDI se centra en gran medida en síntomas y discapacidad, y su empleo en población española ha evidenciado posibles problemas culturalmente específicos13. El cuestionario PSO-LIFE19 es el único desarrollado específicamente para la población española. La escala es unidimensional (proporciona un valor único), lo que facilita la puntuación e interpretación. Ha demostrado fiabilidad, validez y sensibilidad19, por lo que podría resultar el instrumento más apropiado para valorar la CVRS de los pacientes con psoriasis.
En un estudio observacional desarrollado en España se compararon las características de los instrumentos de CVRS (Skindex-29, DLQI, PDI y SF-36) en 379 pacientes con psoriasis. El SF-36 no resultó un instrumento sensible para medir el efecto de la psoriasis en la CVRS y presentó, al igual que DLQI y PDI, un efecto suelo sustancial. PDI y DLQI mostraron correlación con la gravedad clínica en las subescalas de «tratamiento», que miden el impacto de los tratamientos, pero no el efecto de la gravedad sobre la CVRS. Solo Skindex-29 mostró mejor sensibilidad a la gravedad clínica, con un mínimo efecto suelo18.
En general, se recomienda agregar un cuestionario genérico en la valoración de la CVRS de pacientes con psoriasis32. Los cuestionarios SF-3633, EQ-5D34 y NHP35 han sido validados en España, en población con diferentes enfermedades, y aplicados posteriormente a pacientes con psoriasis en diversos estudios. Sin embargo, todos ellos adolecen de resultar poco sensibles a los cambios clínicos asociados a la psoriasis.
Un hallazgo notable de esta revisión es la correlación débil-moderada encontrada entre las medidas de CVRS y la gravedad clínica medida por PASI, utilizada como una medida de resultado casi universal en psoriasis. Además, existe gran variación en los resultados entre estudios, con una correlación que oscila entre r=0,10 (dimensión emocional) y r=0,35 (dimensión síntomas, p <0,01)18 para Skindex-29; para DLQI entre r=0,1318 y r=0,628 (p <0,001)15; para PDI entre r=0,19 (p <0,05)18 y r=0,33 (p <0,01)3; y finalmente es de r=−0,4 para PSO-LIFE2. Estos resultados son, en general, superiores a los reportados en estudios previos, que obtuvieron valores de correlación entre PASI y las medidas de CVRS entre 0,1 y 0,336. Sin embargo, todos ellos evidencian la importancia de valorar tanto la gravedad clínica como el impacto de la enfermedad percibido por el paciente con psoriasis. Dado que estas medidas valoran diferentes constructos, se deben presentar como puntuaciones independientes, pero complementarias. Esta relación entre el control de la enfermedad y la CVRS del paciente se ha descrito también en otras enfermedades, como por ejemplo en asma37,38 o en enfermedad pulmonar obstructiva crónica38. Así, el impacto de estas enfermedades en el paciente no se explica únicamente con medidas objetivas, como la función pulmonar, por lo que es necesaria su complementación con datos de CVRS37.
ConclusiónLa presente revisión pone de manifiesto que el empleo de instrumentos de PRO en la práctica clínica está escasamente generalizado en al ámbito sanitario español, a pesar del impacto negativo de la psoriasis en la CVRS de los pacientes descrito en diversas publicaciones. Posibles motivos podrían ser el tiempo real requerido para su cumplimentación, así como las posibles dificultades para obtenerlos. No obstante, esta revisión enfatiza que la evaluación de las percepciones del paciente con psoriasis sobre su estado de salud y la determinación de los factores que influyen en estas percepciones puede contribuir a un manejo más óptimo de la enfermedad, y que constituye una medida útil y complementaria a las medidas de resultado tradicionales.
FinanciaciónEl presente trabajo ha sido financiado por Lilly España.
Conflicto de interesesIsabel Belinchón ha colaborado previamente como consultora con Pfizer-Wyeth, Janssen Pharmaceuticals Inc, MSD, Almirall SA, Lilly y Leo-Pharma. Luis Lizán y Clara Gabás-Rivera trabajan para una entidad de investigación independiente, y han recibido honorarios por su contribución al desarrollo del proyecto y la redacción del manuscrito. Tatiana Dilla, Teresa Huete y Silvia Díaz trabajan para Lilly España, promotor del estudio. Los autores afirman que los resultados de la investigación descritos en este manuscrito, así como su interpretación, son resultado de la libre expresión de opiniones y que no existen conflictos para obtener o divulgar tales resultados. Los autores no reportan otros conflictos de interés.