La hidradenitis supurativa (HS) es una enfermedad inflamatoria crónica de la piel que influencia negativamente la calidad de vida. En la actualidad no existen escalas en español que la evalúen. El objetivo del presente estudio fue desarrollar y validar un cuestionario específico para evaluar la calidad de vida en pacientes con HS.
Material y métodosSe desarrolló un estudio multicéntrico en España entre 2016 y 2017 para elaborar un cuestionario. Para ello se consideró tanto el marco conceptual como el conocimiento de la situación del paciente mediante la revisión de la bibliografía, reuniones de profesionales de diferentes áreas y entrevistas con pacientes. El cuestionario resultante se pasó a un grupo de 30 pacientes con 30 ± 10 días de intervalo entre uno y otro.
ResultadosEl análisis de fiabilidad muestra una buena consistencia interna y reproductibilidad con puntuación alfa de Cronbach de 0,920 (test) y 0,917 (retest) y coeficiente de correlación intraclase con DLQI y Skindex-29 de 0,698 IC 95% (0,456-0,844) y 0,900 IC 95% (0,801-0,951) respectivamente. Se establecieron puntos de corte para su uso y se comprobó que el instrumento es sensible al cambio.
ConclusionesEl cuestionario HSQoL-24 es la primera prueba autoadministrada específica para evaluar la calidad de vida en HS en español. Sencillo de usar y puntuar por los profesionales. Este estudio demuestra que el instrumento es fiable, válido y sensible al cambio, pendiente de realizar estudio confirmatorio con una muestra mayor con 100 pacientes con HS.
Hidradenitis suppurativa (HS) is a chronic inflammatory disease of the skin with a negative impact on quality of life. Up to now, there are no disease specific instruments in Spanish to assess quality of life in HS. The objective of this study was to develop and validate a questionnaire to evaluate the quality of life in patients with HS.
Material and methodsA multicentre study was carried out in Spain between 2016 and 2017 to develop the questionnaire. Both the conceptual framework and understanding of the patient's situation were considered through a review of the literature, consensus of professionals from different related health areas, and in-depth interviews with patients. The resulting questionnaire was passed to a group of 30 patients with 30±10 days of interval between both assessments.
ResultsThe reliability analysis shows a good internal consistency and reproducibility with Cronbach's alpha score of 0.920 (test) and 0.917 (retest) and intraclass correlation coefficient with DLQI and Skindex-29 of 0.698 IC 95% (0.456-0.844) and 0.900 IC 95% (0.801-0.951) respectively. Cut-off points were established for its use and the instrument was found to be sensitive to change.
ConclusionsThe HSQoL-24 is the first disease-specific self-administered instrument to assess quality of life in patients with HS in Spanish. It is user friendly, and easy to score. This study shows that the instrument is reliable, valid and sensitive to change, pending confirmatory study with a larger sample of 100 patients with HS.
La hidradenitis supurativa (HS) es una enfermedad cutánea inflamatoria crónica con afectación negativa a nivel físico y psicosocial1,2.
La calidad de vida se ve afectada por la HS3. Matusiak et al.4 realizan un análisis de las esferas de calidad de vida alteradas en la HS y describen una marcada alteración en las relaciones interpersonales del paciente con la pareja, con las relaciones sexuales, y con la familia, el desarrollo en algunos casos de ideas suicidas, y una frecuente pérdida de trabajo asociada a la enfermedad.
La aparición reciente de nuevos procedimientos «no invasivos» para el diagnóstico precoz de la enfermedad5, así como la de nuevas dianas terapéuticas van a revolucionar el abordaje de la HS6. En este nuevo escenario, se hace importante contar con un instrumento que mida la calidad de vida de los pacientes con HS, por ser una enfermedad que tiene su propia especificidad. Sin embargo, la revisión bibliográfica realizada mostró que no existe un instrumento en español para hacer esta medición.
El objetivo del presente estudio fue el desarrollo de un nuevo cuestionario psicométrico para evaluar la calidad de vida en pacientes con HS –el HSQoL-24– de acuerdo con los estándares actuales para su desarrollo.
Material y métodosSe incluyeron en el estudio 30 pacientes adultos diagnosticados de HS. Todos firmaron documento de consentimiento informado. Para el presente estudio PI16/020 se obtuvo el Dictamen Favorable por parte del Comité Ético de Investigación Clínica de Aragón (CEICA) el 10 de febrero de 2016, así como los dictámenes favorables de los tres restantes hospitales. Los hospitales que reclutaron los pacientes fueron: Royo Villanova (Zaragoza), Infanta Sofía (Madrid), Santa Creu i Sant Pau (Barcelona) y Doctor Negrín (Las Palmas de Gran Canaria).
Generación de ítemsEn primer lugar, se realizó una revisión bibliográfica en PubMed para identificar los determinantes psicosociales relevantes en la HS; estos sirvieron para identificar las áreas a explorar en las entrevistas. En segundo lugar, se realizaron entrevistas semiestructuradas a 12 pacientes (5 mujeres y 7 hombres con edades comprendidas entre 18 y 61 años) diagnosticados por un dermatólogo de HS. En tercer lugar, tras la transcripción y codificación de las entrevistas, se constituyó un panel de 20 expertos profesionales, con amplia experiencia clínica, para generar nuevos ítems. Con todo ello se elaboró un instrumento psicométrico de 24 ítems (HSQoL-24). La temporalización de las preguntas es referida a las 4 semanas previas a la cumplimentación del cuestionario, ya que el curso evolutivo de la HS es relativamente estable a lo largo del tiempo en comparación con otras patologías cutáneas. Los ítems del cuestionario se agruparon en 6 dominios: psicosocial, económico, laboral, relacional, personal y clínico.
Evaluación psicométricaPara la validación psicométrica de HSQoL-24 se utilizaron el Dermatology Life Quality Index (DLQI)7, cuestionario específico para la evaluación de la calidad de vida en enfermos dermatológicos, y el cuestionario Skindex-29 en su versión adaptada y validada al español por Jones-Caballero et al.8 que evalúa también calidad de vida dermatológica.
La fiabilidad se evaluó mediante análisis de consistencia interna con el estadístico alpha de Cronbach (es aceptable si el valor obtenido supera 0,7), y mediante análisis de reproductibilidad, evaluado con el coeficiente de correlación intraclase (CCI), (considerándose adecuado si el valor obtenido supera 0,7). La validez de contenido se evaluó por medio del juicio crítico de los 20 profesionales. La validez de constructo se realizó mediante análisis de correlación y regresión con los cuestionarios de calidad de vida DLQI y Skindex-29. Los valores de corte se calcularon mediante análisis de curvas de características operativas del receptor (COR) y comparación con las categorías de Skindex-29. La sensibilidad al cambio se analizó con las correlaciones entre las diferencias en las puntuaciones de los tres cuestionarios y con el tamaño del efecto.
Este cuestionario ha sido desarrollado por un grupo de expertos miembros del Grupo Aragonés de Investigación en Psicodermatología (GAI+PD) y del Grupo Español de Investigación en Dermatología y Psiquiatría (GEDEPSI) de la Academia Española de Dermatología y Venereología (AEDV). Se planteó una fase inicial de desarrollo en 30 pacientes, objeto del presente artículo y una posterior de confirmación en 100 pacientes. El cuestionario resultante, HsQoL-24 con 24 ítems y cinco posibles respuestas para cada uno (fig. 1), demostró ser factible y sencillo de realizar por los pacientes que invirtieron aproximadamente 10 min en sus respuestas.
ResultadosSe realizó la validación en una muestra de 30 pacientes, completando el HSQoL-24 en dos ocasiones con 30±10 días de diferencia entre ambas. De los 30 pacientes, 11 (36,7%) fueron hombres, la media de edad (± desviación estándar) fue de 36,8 (±11,2) años con una edad al inicio de 22,8 (±10,9) años y 13,6 (±11,3) años de duración de la enfermedad, 6 (20%) Hurley III, 14 (46,7%) Hurley II y 10 (33,3%) Hurley I.
Propiedades de HSQoL-24Los diferentes ítems se han agrupado en seis dominios: psicosocial: ítems 1, 3, 5, 7, 10, 12, 15, 17, 20, 22, 23 y 24; económico: ítem 2; laboral: ítems 4 y 8; relacional: ítems 6, 9, 13 y 18; personal; ítems 11 y 14; y clínico: ítems 16, 19 y 21. Para el cálculo de las puntuaciones, es necesario tener en cuenta que como norma general cada ítem se puntúa entre 0 y 4, puntuando 0 la respuesta «nunca», 1 «raramente», 2 «a veces», 3 «a menudo» y 4 «siempre». Los ítems 9, 12 y 16 se puntúan de forma inversa respecto a los demás. Finalmente, las puntuaciones de cada dominio y la puntuación general se deben ajustar a 100, que se obtiene multiplicando el valor obtenido por una constante. Estas constantes se pueden ver en la tabla 1.
Fiabilidad: consistencia interna y reproductibilidadConsistencia internaLa consistencia interna medida con el estadístico alpha de Cronbach presentó los valores de 0,920 en la validación inicial (o test) y 0,917 en la validación posterior (o retest).
ReproductibilidadLa reproductibilidad se midió con el CCI en una intervención test retest. Esta valoración se realizó para las puntuaciones totales y para los diferentes dominios. Los diferentes valores de los CCI de los cuestionarios DLQI y Skindex-29 suministrados a los pacientes fueron 0,698 IC 95% (0,456 - 0,844) y 0,900 IC 95%: (0,801 - 0,951) respectivamente. Los resultados se presentan en la tabla 2.
Coeficiente de correlación intraclase
| Dominio | CCI (IC 95%) | Media±DE, test | Media±DE, retest | p-valor, test retest* |
|---|---|---|---|---|
| Global | 0,842 (0,694 - 0,921) | 50,87±20,695 | 47,60±19,866 | 0,098 |
| Psicosocial | 0,872 (0,750 - 0,937 | 49,38±22,346 | 45,76±21,949 | 0,088 |
| Económico | 0,709 (0,474 - 0,850) | 40,00±40,258 | 40,00±40,258 | 0,546 |
| Laboral | 0,682 (0,431 - 0,835) | 51,67±34,072 | 46,25±30,469 | 0,259 |
| Relacional | 0,760 (0,555 - 0,878) | 63,33±25,360 | 59,79±23,309 | 0,260 |
| Personal | 0,718 (0,487 - 0,855) | 27,92±24,715 | 29,17±24,197 | 0,712 |
| Clínico | 0,702 (0,462 - 0,846) | 58,61±19,013 | 55,28±19,264 | 0,227 |
CCI: coeficiente de correlación intraclase; IC: intervalo de confianza; DE: desviación estándar.
La validez de constructo se realizó mediante análisis de correlación y regresión con los cuestionarios de CVRS DLQI y Skindex-29. Los valores de correlación del cuestionario HSQoL-24 con el cuestionario DLQI y con el cuestionario Skindex-29 tanto en valoración pre- como en valoración pos- se presentan en la tabla 3. En esta tabla se puede constatar cómo los valores de correlación son mayores en la comparación con Skindex-29 y que se encuentran próximos a 0,9 (0,863 y 0,898 para test y retest respectivamente).
Análisis de correlaciones
| Análisis test | Análisis retest | |||
|---|---|---|---|---|
| Correlación con DLQI (p-valor) | Correlación con Skindex-29 (p-valor) | Correlación con DLQI (p-valor) | Correlación con Skindex-29 (p-valor) | |
| Dominio global | 0,708 (<0,001) | 0,863 (<0,001) | 0,691 (<0,001) | 0,898 (<0,001) |
DLQI: Dermatology Life Quality Index.
Se han realizado análisis de regresión del cuestionario HSQoL-24 con los cuestionarios DLQI y Skindex-29 en la valoración inicial y en la final. Los resultados de la regresión en los cuestionarios iniciales (test), se presentan en la tabla 4. Los valores de R2 presentados con Skindex-29 indicaban una adecuada bondad del ajuste del modelo (0,7452 y 0,7548 para el modelo test y retest respectivamente). De lo expuesto, se comprobó que el cuestionario DLQI permite predecir el 47-50% del valor de la varianza en HSQoL-24 y el cuestionario Skindex-29 presenta un ajuste del modelo mayor, explicando el cuestionario Skindex-29 un 75-80% de la varianza en HSQoL-24.
Puntos de cortePara delimitar los puntos de corte se compararon los rangos de valores de HSQoL-24 y Skindex-29 por ser con este último con quien presenta mejores valores de correlación y regresión. Los resultados del estudio descriptivo de los valores de HSQoL-24 en las diferentes categorías del cuestionario Skindex-29 se presentan en la tabla 5. En esta tabla se puede ver que únicamente 8 y 10 pacientes no presentaron afectación en su calidad de vida y 14 y 13 pacientes presentaron afectación grave.
Valores de HSQoL-24 en categorías de Skindex-29
| Categoría | Test | Retest | ||||
|---|---|---|---|---|---|---|
| Casos | Media±DE | Rango | Casos | Media±DE | Rango | |
| Sin afectación (0-24) | 8 | 29,82+6,51 | 16 - 35 | 10 | 27,90±10,35 | 13-41 |
| Afectación leve (25-31) | 1 | 44,79 | 45 | 2 | 40,00±14,14 | 30-50 |
| Afectación moderada (32-43) | 6 | 37,33±6,12 | 31 - 47 | 2 | 39,00±5,65 | 35-43 |
| Afectación grave (≥44) | 14 | 67,63±20,67 | 35 - 83 | 13 | 66,31±11,09 | 45-83 |
DE: desviación estándar.
El análisis de los valores de las curvas COR determinan que los valores comprendidos entre 0-32 de HSQoL-24 corresponden a sujetos sin afectación en su CVRS con una sensibilidad de 0,909 y una especificidad de 0,5. El área bajo la curva es de 0,943 IC 95% (0,865 -1,000). En cuanto a los pacientes con afectación grave, el punto de corte de la curva propuesto es de 42 con una sensibilidad de 0,933 y una especificidad de 0,867. El área bajo la curva es de 0,967 IC 95% (0,909 - 1,000). La separación en las categorías leve y moderada se propuso con el punto de corte 36 con sensibilidad 0,810 y especificidad 0,889 y área bajo la curva 0,910 IC 95% (0,807 -1,000) (fig. 2).
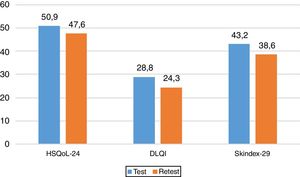
Sensibilidad al cambioPara analizar la sensibilidad al cambio se calculó la variación de los tres cuestionarios y se realizó un análisis de correlación entre las mismas. Los resultados presentaron correlación estadísticamente significativa entre el cambio en HSQoL-24 y Skindex-29 (r de Pearson=0,504, p=0,004) y no presentó correlación estadísticamente significativa, pero sí una tendencia con DLQI (r de Pearson=0,355, p=0,055). El tamaño del efecto de la variación de HSQoL-24, calculado como diferencia de medias dividido por la desviación del momento inicial fue de 0,33 (50,87 - 47,60/20,695), lo que indica una variación reducida en la CVRS. A parecidas conclusiones llegaba el cuestionario Skindex-29 con un valor de 0,17 (43,2-38,6/25,865); lo que indica en ambos casos una escasa variación en la CVRS en este tipo de pacientes en ambos cuestionarios.
Los valores en los tres cuestionarios demostraron diferencias en su puntuación global y en su puntuación final, los valores medios se presentan en la figura 3 y en ella se ve cómo los valores se reducen en los tres valores medios.
DiscusiónEl presente artículo analiza las características del cuestionario HSQoL-24 como predictor de calidad de vida en pacientes con HS. En la elaboración previa del cuestionario se han considerado tanto el marco conceptual como el conocimiento de la situación del paciente mediante la revisión de la bibliografía, reuniones de profesionales de diferentes áreas y entrevistas con pacientes. Esta metodología de trabajo es consistente con la de otros autores y habitual en el desarrollo de un cuestionario de calidad de vida9,10.
La pertinencia de los estudios de calidad de vida en HS se ha puesto de manifiesto en varios estudios. Los pacientes más allá de sus manifestaciones clínicas ven afectada su calidad de vida y se deben analizar estas mermas11,12 así como los factores que influyen en las mismas13. Además de esta pertinencia existe la necesidad de generar cuestionarios aplicables a poblaciones específicas, en este caso la población española con HS, lo que justifica la necesidad de esta investigación en el momento actual de estudio de la enfermedad. Los cuestionarios disponibles actualmente sobre HS no son aplicables a población española hasta su traducción y validación y no se encontraban publicados en el momento del diseño y posterior recogida de datos del presente estudio. Ello explica que no se pudiera contemplar la traducción de los mismos y se optara por la realización de un cuestionario de novo9,14,15.
Las características psicométricas analizadas en el presente artículo han sido la fiabilidad, validez y capacidad pronóstica, medidas igualmente aceptadas en las diferentes enfermedades con afectación de la calidad de vida en España16.
La fiabilidad se midió como consistencia interna y/o reproductibilidad/repetibilidad. La consistencia interna se midió con el estadístico alpha de Cronbach17. Los resultados presentaron un valor superior a 0,9 lo que indica una consistencia interna excelente que se mantiene aun cuando se elimine alguna de las cuestiones. Parecidos valores fueron hallados por McLellan et al.16 que presentaron valores de alpha de 0,955 en la función física y 0,900 en el dominio de los síntomas en un cuestionario de calidad de vida en HS. Pinnard et al., notificaron asimismo valores elevados, 0,93615.
La reproductibilidad o repetibilidad se midió con el CCI en una intervención test-retest, asumiendo que resultan adecuados valores superiores a 0,7. Esta valoración se realizó para las puntuaciones totales y para los diferentes dominios. Los valores del CCI superaron el valor de 0,7 en todos los dominios salvo en el laboral (0,68). Estos valores son similares a los localizados en otros cuestionarios o métodos empleados en Dermatología, como pueda ser la determinación computadorizada de la medición Psoriasis Area and Severity Index (PASI) en psoriasis que alcanzaba valores de 0,86 IC 95% (0,80 - 0,90)18.
Los diferentes valores de los CCI de los cuestionarios DLQI y Skindex-29 presentaron amplios solapamientos con el IC 95% de CCI de HSQoL-24, de lo que se dedujo que los valores de CCI de los tres cuestionarios presentaron valores comparables.
La validez de constructo se constató mediante análisis de correlación y regresión con los cuestionarios de CVRS DLQI y Skindex-29. Los valores elevados de los coeficientes de correlación y el adecuado ajuste de modelos de regresión indicaron adecuada validez, presentando una mayor correlación (r>0,85) y mejor ajuste de regresión (R2>0,7). Al igual que otros autores en sus investigaciones15,16, HSQoL-24ha mostrado correlaciones adecuadas con estos cuestionarios lo que indica una validez adecuada.
Los valores de los puntos de corte presentaron una adecuada sensibilidad (entre 0,88 y 0,90) y una elevada área bajo la curva (superior a 0,9) en el análisis de curvas COR lo que indicaba una adecuada capacidad predictiva para detectar individuos con alteraciones en su CVRS. Estos valores fueron similares a los reportados por otros autores en otros cuestionarios en HS o Dermatología19,20. No obstante, no se pudieron calcular de forma adecuada los valores de especificidad. Ello puede ser atribuido al reducido tamaño de muestra, por lo que en la fase posterior de valoración se podrán analizar con mayor coherencia los valores de sensibilidad y especificidad del cuestionario HSQoL-24.
Además de las variaciones paralelas en las escalas de calidad de vida test y retest comentadas con anterioridad, la sensibilidad al cambio se analizó con el estudio de correlaciones entre las diferencias en las puntuaciones de los cuestionarios y con el tamaño del efecto. Los resultados presentaron correlación estadísticamente significativa entre el cambio en HSQoL-24 y Skindex-29, pero no con DLQI con un bajo valor de p, p=0,055. Los valores de correlación en torno a 0,5 fueron significativos y ligeramente inferiores a otros cuestionarios en Dermatología como el cuestionario Urticaria Activity Score que en su fase de validación alcanzaba valores de 0,6-0,7 en relación con otros cuestionarios21. No obstante, los resultados de HSQoL-24 se han considerado como indicadores de buena sensibilidad al cambio.
ConclusionesLos resultados del análisis de las propiedades psicométricas de HSQoL-24, primer test específico autoadministrado para evaluar calidad de vida en pacientes con HS en español, demostraron unos valores adecuados de fiabilidad y validez lo que, a falta de los resultados de la validación en 100 pacientes, hacen de este cuestionario un elemento de amplia validez clínica en cuanto a resultados percibidos por los pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.