Los betabloqueantes (BB) se han convertido en el tratamiento de elección para los hemangiomas infantiles (HI)1. El propranolol es, de entre los fármacos de esta clase, el que se ha posicionado en primera línea, al demostrar su eficacia y seguridad2, siendo el único aprobado para esta indicación3. La existencia de pacientes con escasa respuesta terapéutica o que presentan efectos adversos durante su uso han llevado a recurrir a otros betabloqueantes como alternativa4.
Revisamos los pacientes con HI tratados con nadolol oral en el Servicio de Dermatología del Hospital Costa del Sol desde el año 2010 hasta el año 2022. El nadolol era administrado en una formulación tipo solución oral preparado por el Servicio de Farmacia de este centro a una concentración de 10mg/ml. La dosis inicial era de 1mg/kg/día, repartido en 2 dosis cada 12h, aumentándose 1mg/kg/día/cada 10 días (siendo la dosis máxima a utilizar de 3mg/kg/día) en función de la respuesta al fármaco y su tolerabilidad.
La respuesta al tratamiento se midió mediante una escala visual analógica validada5. La escala valora el grosor y el tamaño medidos en milímetros (una reducción de 5mm equivale a un 10% de la escala) y la coloración de la piel. Se considera una buena respuesta la involución total o la reducción de más del 80%, una respuesta parcial la reducción del 50-80% y una respuesta incompleta la reducción de menos del 50%.
Un total de 7 pacientes recibieron nadolol, de los cuales 6 eran mujeres. Las características demográficas y de los hemangiomas se describen en la tabla 1. En todos los casos el nadolol fue prescrito tras el empleo previo del propranolol.
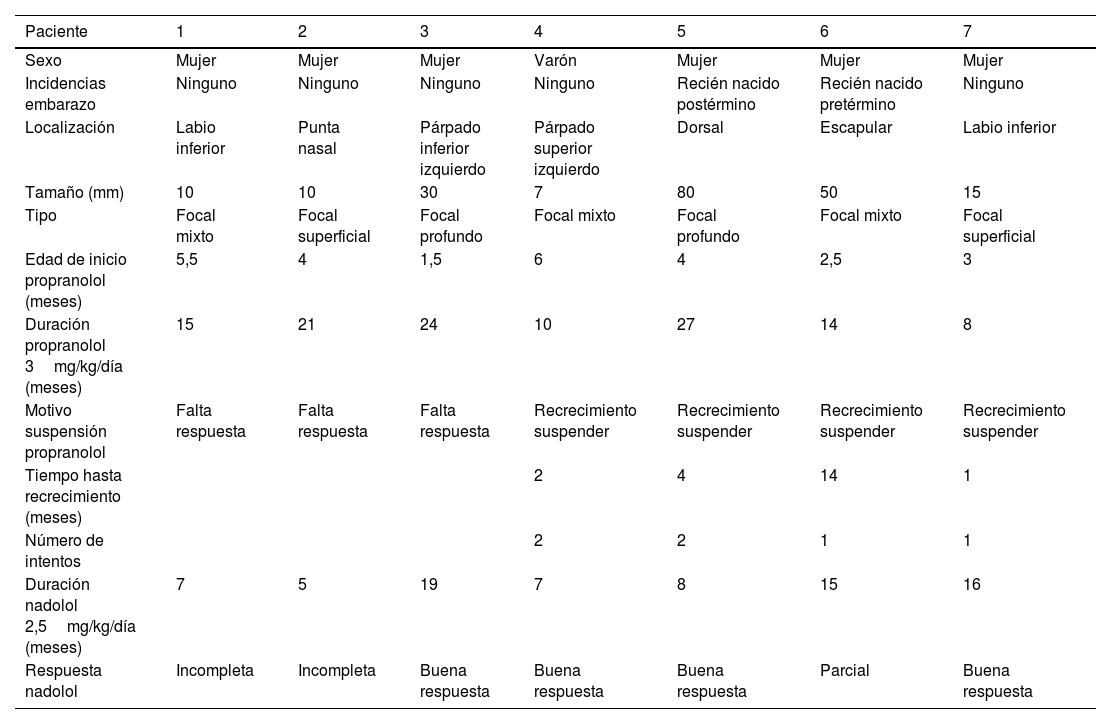
Características demográficas de los pacientes y cronología del tratamiento
| Paciente | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|---|---|---|---|---|---|---|---|
| Sexo | Mujer | Mujer | Mujer | Varón | Mujer | Mujer | Mujer |
| Incidencias embarazo | Ninguno | Ninguno | Ninguno | Ninguno | Recién nacido postérmino | Recién nacido pretérmino | Ninguno |
| Localización | Labio inferior | Punta nasal | Párpado inferior izquierdo | Párpado superior izquierdo | Dorsal | Escapular | Labio inferior |
| Tamaño (mm) | 10 | 10 | 30 | 7 | 80 | 50 | 15 |
| Tipo | Focal mixto | Focal superficial | Focal profundo | Focal mixto | Focal profundo | Focal mixto | Focal superficial |
| Edad de inicio propranolol (meses) | 5,5 | 4 | 1,5 | 6 | 4 | 2,5 | 3 |
| Duración propranolol 3mg/kg/día (meses) | 15 | 21 | 24 | 10 | 27 | 14 | 8 |
| Motivo suspensión propranolol | Falta respuesta | Falta respuesta | Falta respuesta | Recrecimiento suspender | Recrecimiento suspender | Recrecimiento suspender | Recrecimiento suspender |
| Tiempo hasta recrecimiento (meses) | 2 | 4 | 14 | 1 | |||
| Número de intentos | 2 | 2 | 1 | 1 | |||
| Duración nadolol 2,5mg/kg/día (meses) | 7 | 5 | 19 | 7 | 8 | 15 | 16 |
| Respuesta nadolol | Incompleta | Incompleta | Buena respuesta | Buena respuesta | Buena respuesta | Parcial | Buena respuesta |
La edad mediana de inicio de propranolol fue de 4 meses (rango intercuartílico [RIC]: 2,5-5,5], alcanzándose la dosis máxima de 3mg/kg/día en todos los pacientes, y una duración mediana del tratamiento de 15 meses (RIC: 10-24). El motivo para suspender el propranolol fue la falta de respuesta en 3 pacientes y el recrecimiento de la lesión tras suspender el fármaco en múltiples ocasiones, en los otros 4. En ninguno de nuestros pacientes el propranolol fue suspendido por la presencia de eventos adversos (alteraciones del sueño o hipoglucemia). La edad media de inicio de nadolol fue de 21 meses (RIC: 16-36) con una dosis de 2,5mg/kg/día (RIC: 2-3) y una duración media de 8 meses (RIC: 7-16). Respecto a la efectividad; 4 pacientes tuvieron una buena respuesta, en un paciente la respuesta se consideró parcial (fig. 1) y en otros 2 pacientes la respuesta fue incompleta. La tasa de respuesta se situó en 5 de 7 pacientes. Ningún paciente tuvo que suspender el tratamiento con nadolol por efectos adversos de la medicación. En la tabla 1 se muestra la cronología de los tratamientos, su duración y la respuesta.
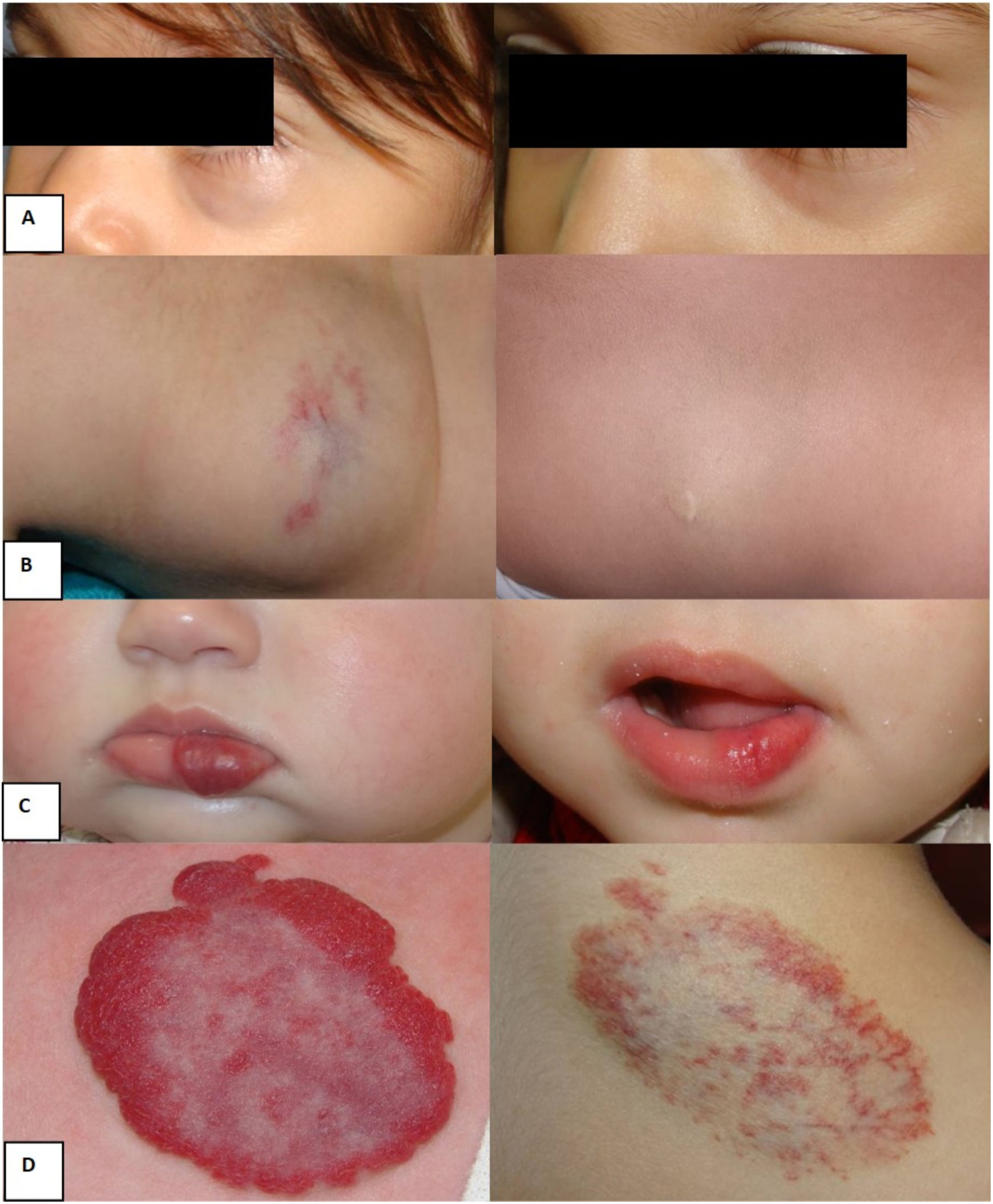
Ejemplos de respuesta al tratamiento con nadolol: A) Hemangioma focal profundo en el párpado inferior izquierdo, edad inicio nadolol: 24 meses, edad fin nadolol: 43 meses. Buena respuesta. B) Hemangioma dorsal focal profundo, edad inicio nadolol: 40 meses, edad fin nadolol: 48 meses. Buena respuesta. C) Hemangioma focal superficial labio inferior, edad inicio nadolol: 11 meses, edad fin nadolol: 27 meses. Buena respuesta. D) Hemangioma escapular focal mixto, edad inicio nadolol: 30 meses, edad fin nadolol: 45 meses. Respuesta parcial.
En nuestra serie de 7 casos, el motivo principal para cambiar el propranolol por nadolol fue el recrecimiento del hemangioma tras la suspensión del mismo después de varios intentos, un fenómeno bien acreditado en la literatura6. Se produce aproximadamente en el 25% de los casos. Los factores de riesgo son el sexo femenino, la localización en cabeza y cuello, el carácter segmentario, aquellos con componente profundo y una duración de tratamiento con BB inferior a 9 meses4. La falta de respuesta inicial al propranolol fue de 3 pacientes, una proporción similar a la reportada. Se desconoce la causa de esta ineficacia, pero se aconseja prolongar el tratamiento más de 6 meses para incrementar la tasa de éxito6. En nuestra serie la duración media superó con creces esa recomendación (hasta llegar a los 15 meses). En ningún caso la razón del cambio a nadolol fue la existencia de efectos adversos con el propranolol.
El nadolol es un fármaco BB hidrosoluble, con una vida media de 12-24h. Estas propiedades farmacocinéticas le confieren ciertas ventajas teóricas sobre el propranolol a la hora de su administración a pacientes de corta edad. Al no atravesar la barrera hematoencefálica tiene menos efectos adversos sobre el sistema nervioso central, provocando menos alteraciones del sueño respecto al propranolol. Sin embargo, al igual que el propranolol, es un BB no cardioselectivo, por lo que puede producir los mismos efectos adversos debido a su actividad beta 2 y beta 3 adrenérgica como son las hipoglucemias y el broncoespasmo7. El hecho de que su principal vía de eliminación sea a través del tracto gastrointestinal (hasta un 70%) obliga a controlar el ritmo deposicional de los lactantes, especialmente tras el caso reportado en la literatura de la muerte de un paciente por intoxicación por nadolol que sufría de estreñimiento8. Por otro lado, su vida media es el doble que la del propranolol, por lo que se relaciona con unos niveles más estables del fármaco en la sangre9. Esta es la principal hipótesis por la cual nos planteamos que tenga un inicio de acción más rápido y que sea más efectivo que el propranolol. Recientemente, se ha publicado un estudio doble ciego prospectivo de no inferioridad que compara la eficacia y la seguridad del nadolol frente al propranolol10. El nadolol se demuestra un 59% más rápido que el propranolol en alcanzar el 75% de la disminución de tamaño y un 105% más rápido en alcanzar la desaparición del hemangioma, todo ello sin un aumento de los efectos adversos.
Como conclusiones, podemos decir que el nadolol ha demostrado ser un fármaco efectivo y seguro, con un buen perfil farmacocinético y tasas de respuesta no inferiores y más tempranas que el propranolol. Esto lo puede hacer posicionarse cada vez más como primera opción terapéutica, especialmente en los subtipos de hemangiomas de alto riesgo con factores asociados a recidiva.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.