El término lupus eritematoso inducido por fármacos (LEIF) hace referencia a una entidad caracterizada por la aparición de manifestaciones clínicas, histopatológicas e inmunológicas similares a aquellas que aparecen en el lupus eritematoso idiopático, pero que cronológicamente coinciden con la toma de ciertos fármacos y que se resuelven tras la retirada de los mismos. Más de 90 fármacos se han asociado con la aparición de LEIF. Esta lista de fármacos implicados sigue aumentando. Al igual que el lupus eritematoso idiopático, el LEIF se puede subclasificar en lupus eritematoso sistémico inducido por fármacos, lupus eritematoso cutáneo subagudo inducido por fármacos y lupus eritematoso cutáneo crónico inducido por fármacos. Reconocer estas entidades es de gran interés, ya que este cuadro suele revertir tras la retirada del fármaco implicado.
Drug-induced lupus erythematosus (DILE) refers to a condition whose clinical, histological, and immunological features are similar to those seen in idiopathic lupus erythematosus but that occurs when certain drugs are taken and resolves after their withdrawal. Over 90 drugs have been linked to DILE to date and the list is growing. Like idiopathic lupus erythematosus, DILE has systemic, subacute cutaneous, and chronic cutaneous forms. A correct diagnosis is very important, as this condition usually resolves after withdrawal of the offending drug.
Los procesos de autoinmunidad se producen por una alteración en la regulación de uno o más componentes de la respuesta inmune. El desarrollo de autoinmunidad es un fenómeno multifactorial, donde factores genéticos, epigenéticos y ambientales desempeñarían un papel importante en la iniciación y mantenimiento del proceso.
Los síndromes autoinmunes inducidos por fármacos han sido descritos desde hace varios años, siendo el lupus eritematoso inducido por fármacos (LEIF) el ejemplo clásico.
El lupus eritematoso sistémico (LES) es una enfermedad sistémica autoinmune de etiología desconocida. No obstante, se ha observado que múltiples fármacos pueden inducir un cuadro clínico similar al del LES, conocido como LEIF, síndrome lupus-like, lupus eritematoso medicamentoso o lupus relacionado con fármacos1. Este cuadro se desarrolla en pacientes sin historia previa de esta enfermedad autoinmune y supone el 10-15% de los casos de LES2.
En la última década ha habido un aumento significativo de casos de autoinmunidad inducida por fármacos. Hasta la fecha más de 90 fármacos han sido implicados en el desarrollo de LEIF. El número de medicaciones involucradas ha aumentado exponencialmente, quizás debido al desarrollo y uso de nuevos fármacos en la última década. Fármacos como los biológicos, que han sido creados para interferir en pasos específicos de la respuesta inmune, pueden acarrear alteraciones significativas en esta respuesta inmunitaria. La evidencia de una relación causal es indudable para fármacos como la hidralacina, la procainamida, la isoniacida, la quinidina y la clorpromacina. Los fármacos con mayor riesgo asociado son procainamida e hidralacina, con aproximadamente una incidencia del 20% para la procainamida3 y un 5-8% para la hidralacina4 durante tratamientos de al menos un año a las dosis estándar. El resto de fármacos tiene un riesgo bajo basándonos en la escasez de los casos descritos en la literatura.
ConceptoAunque no existen en la actualidad criterios bien establecidos para su diagnóstico, está ampliamente aceptada la definición del lupus eritematoso sistémico inducido por fármacos (LESIF) como una patología consistente en el desarrollo de unos síntomas parecidos a los del LES (normalmente fiebre, afectación musculoesquelética y serositis) que ocurren paralelamente con la toma continuada de un fármaco (al menos durante un mes) y que se resuelve tras la interrupción del mismo. Este cuadro se acompaña normalmente de hallazgos serológicos, con una positividad de anticuerpos antinucleares (ANA) así como de anticuerpos antihistona. La diferenciación del LES idiopático del LESIF puede ser en ocasiones muy difícil, ya que ambas entidades suelen tener las mismas manifestaciones clínicas y similares hallazgos serológicos e histopatológicos. Algunos hallazgos serológicos, y sobre todo la completa recuperación tras la suspensión del fármaco responsable, son datos que servirán de ayuda para realizar un correcto diagnóstico.
EpidemiologíaLa incidencia del LEIF se ha estimado entre 15.000 y 30.000 casos nuevos por año en Estados Unidos, lo que podría suponer hasta un 10-15% de los casos de la forma idiopática de LES1. Al contrario de lo que ocurre en el LES idiopático, donde la proporción de mujeres afectadas es claramente superior a la de hombres, en el LESIF la proporción entre hombres y mujeres es similar5. Además, en el LESIF la edad de los afectados es más avanzada, ya que es este grupo de edad el que más frecuentemente recibe los fármacos implicados. Asimismo, se ha observado una prevalencia hasta 6 veces mayor en personas de raza blanca sobre la raza negra6. La procainamida es el fármaco que hasta la fecha se ha asociado con mayor frecuencia al LESIF3.
Mecanismos etiopatogénicosLa etiopatogenia del LEIF es desconocida en la actualidad. Probablemente sea la consecuencia de una conjunción de factores dependientes del fármaco responsable, así como de los propios pacientes.
El LEIF se diferencia de otras reacciones de hipersensibilidad a fármacos por varios motivos. En primer lugar, no existe evidencia de la existencia de linfocitos T-fármaco específicos o anticuerpos, y los autoantígenos diana no se afectan directamente por el fármaco inductor. Además, se necesitan meses o años para que se desarrolle el LEIF dependiendo de la dosis acumulada del fármaco. Finalmente, la recurrencia de la sintomatología después de la reintroducción del fármaco generalmente ocurre al cabo de uno a 2 días, indicando la ausencia de hipersensibilidad inmune. Se piensa que es necesaria cierta susceptibilidad genética para que se produzca un LEIF. Este hecho está apoyado por la observación de que los pacientes con familiares con LES tienen mayor probabilidad de desarrollar un LEIF. Además, se conoce que el desarrollo de un LEIF se ha asociado con el estatus de acetilador del individuo, el cual está predeterminado genéticamente7. Los individuos que son acetiladores lentos son homocigotos para el gen recesivo que controla la actividad de la enzima hepática acetil-transferasa. Esta enzima está implicada en el metabolismo de ciertos fármacos que provocan LEIF como la procainamida, la isoniacida y la hidralacina. Se ha descrito que los acetiladores lentos tratados con hidralacina o procainamida desarrollan ANA más rápidamente y a títulos más altos que los acetiladores rápidos, y además presentan con mayor frecuencia síntomas de LEIF. Recientemente la hipótesis de la susceptibilidad genética ha adquirido mayor relevancia por el descubrimiento del complejo mayor de histocompatibilidad (HLA). Se ha visto que ciertos haplotipos del HLA como el HLA-DR2, HLA-DR4 y HLA-DR3, además del estado de acetilador lento y el alelo C4 nulo podrían estar asociados con el desarrollo de autoinmunidad8. Por otra parte, se piensa que son necesarios varios eventos secuenciales para el desarrollo del LEIF9. En primer lugar, parece que ocurre una biotransformación del fármaco implicado en un producto reactivo. Estos metabolitos reactivos tendrían la capacidad de formar complejos estables con macromoléculas propias, o directamente de estimular a los linfocitos y se iniciaría una anomalía inmunológica que provocaría una importante alteración del sistema inmune. En la biotransformación del fármaco se ha demostrado que los neutrófilos activados en la sangre periférica son capaces de participar en el metabolismo oxidativo de muchos fármacos que inducen LEIF como la procainamida, la hidralacina, la quinidina, la fenitoína, la sulfona, el propiltiuracilo, la penicilamina, la clorpromacina, la isoniacida y la carbamacepina, lo que favorecería la formación de metabolitos que provocarían autoinmunidad10. Se ha demostrado que existe una gran correlación entre la susceptibilidad de un fármaco a su transformación oxidativa mediada por la mieloperoxidasa y la tendencia del mismo a inducir un lupus eritematoso10.
La formación de metabolitos reactivos con características similares podría explicar porqué diversos fármacos química y farmacológicamente distintos pueden inducir manifestaciones clínicas similares y son capaces de provocar autoinmunidad.
En la segunda parte del proceso se produciría una autoinmunidad por los fármacos o sus metabolitos. Se han propuestos varias hipótesis para explicar cómo se produciría este proceso. Una de ellas postula que algunos fármacos podrían inducir LEIF a través de alteraciones en la metilación del ADN de los linfocitos T11. La metilación del ADN tiene un papel primordial en la regulación de la expresión de los genes y la diferenciación celular. Fármacos como la procainamida o la hidralacina son inhibidores de la ADN metil-transferasa y disminuyen la metilación del ADN. La hipometilación del ADN de los linfocitos T alteraría los perfiles de expresión génica de los linfocitos T y su función. La segunda hipótesis afirma que los linfocitos T específicos para el fármaco podrían activar linfocitos B autorreactivos. La última hipótesis propone que el fármaco no estimularía directamente el linfocito T maduro, sino que previene la adquisición de novo de autotolerancia si está presente en el timo durante el desarrollo de la célula T12,13. Se ha demostrado que los linfocitos T se generan en el timo durante toda la vida, y se ha observado que la inyección de un metabolito de la procainamida en el interior del timo produce de forma tardía anticuerpos anti-([H2A-H2B]-ADN)14. Por otra parte, se piensa que muchos fármacos tienen la capacidad de interaccionar con proteínas nucleares como las histonas15. Esta interacción determina la formación de moléculas que expresarían nuevos determinantes antigénicos y favorecerían la producción de anticuerpos antihistona. Además, la estructura molecular de ciertos fármacos es similar a aquellas de las bases purínicas, lo que favorecería una reactividad cruzada con el ADN16. El mecanismo por el cual se produce autoinmunidad con los anti-TNFα parece que difiere del resto de los fármacos causantes de LEIF. Según algunas hipótesis la unión del anticuerpo anti-TNFα a la superficie celular induciría la apoptosis en las células17. Esto provocaría una liberación de autoantígenos nucleosomales y la inducción de anticuerpos anti-ADNds. Otra hipótesis señala que estos fármacos provocarían el cambio de perfil de linfocitos T helper. En el LES se considera que existe un perfil de citocinas de linfocitos T helper tipo 2 con una activación significativa de los linfocitos B. Los anti-TNFα bloquean la citocina de Th1 TNF-α, lo que podría provocar un cambio en el sistema inmunológico a un perfil Th2 con la producción de autoanticuerpos y el desarrollo de clínica lupus-like. La última hipótesis postula que el papel de las infecciones bacterianas favorecidas por la terapia anti-TNFα podría ser un estimulante que conduciría a una activación policlonal de los linfocitos B y a una producción de anticuerpos18.
Respecto a la correlación etiopatológica del lupus eritematoso cutáneo subagudo inducido por fármacos (LECSIF), en un reciente artículo publicado por Sontheimer et al., se pone de manifiesto que la mayoría de los fármacos inductores de LECSIF a la vez producen reacciones de fotosensibilidad y fotoliquenoides. Eso justifica que recientemente se describa el LECSIF como un ejemplo de respuesta isomórfica fotoinducida en un paciente inmunogenéticamente predispuesto19. Otra posibilidad siguiendo el mismo esquema etiológico es que una inflamación cutánea producida por un fármaco fotosensible pueda modificar la respuesta inmune innata resultando en un aumento local de la producción de interferón (IFN) clase i por parte de las células dendríticas. La disregulación en su producción y el disbalance resultante en la cascada (por ejemplo, la producción de CXCL9-11 con el consiguiente reclutamiento de linfocitos citotóxicos T CXCR3) se produce en la mayoría de dermatitis de interfase incluyendo el LES.
Manifestaciones clínicasEl espectro clínico del LEIF incluye desde una afectación cutánea limitada a una afectación sistémica que generalmente es leve2. El inicio suele ser normalmente insidioso. Además, las manifestaciones clínicas serán muy variadas en función de la forma clínica de LEIF.
Lupus eritematoso sistémico inducido por fármacosEn las manifestaciones clínicas del LESIF predominan la sintomatología musculoesquelética (artralgias y mialgias), así como serositis y sintomatología constitucional como fiebre, astenia y anorexia. Estos síntomas suelen ser generalmente leves.
La artritis suele ser simétrica y no deformante, y afecta sobre todo a pequeñas articulaciones como las manos. La artritis suele ser un fenómeno constante en los casos inducidos por hidralacina. Las mialgias son también muy frecuentes en pacientes con LESIF. Estos síntomas empeoran característicamente conforme se prolonga el tiempo de administración del fármaco causante20.
Las manifestaciones mucocutáneas clásicas como el eritema malar, la erupción discoide, la alopecia o las ulceraciones orales son muy infrecuentes en el LESIF. La serositis es también una manifestación frecuente del LESIF. La pericarditis suele tener un curso benigno en estos pacientes, aunque se han descrito casos de pericarditis constrictiva, taponamiento cardiaco y derrames pericárdicos graves21–23. La pleuritis, el derrame pleural y los infiltrados pulmonares no son infrecuentes en el LEIF causado por fármacos como la procainamida24. Por el contrario, las manifestaciones renales o neurológicas suelen ser muy infrecuentes en el LESIF, a diferencia del LES idiopático. La hidralacina es el fármaco que con mayor frecuencia se ha asociado a alteraciones renales25.
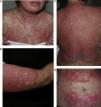
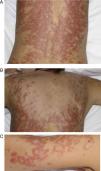
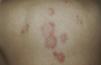
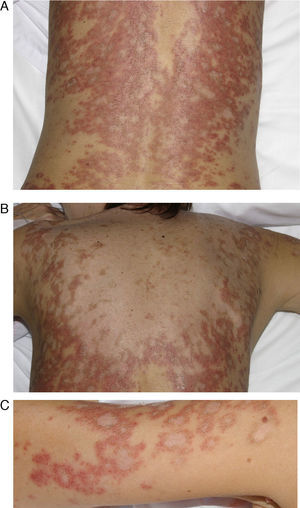
Lupus eritematoso cutáneo subagudo inducido por fármacosEl LECSIF es similar al LECS idiopático en términos de manifestaciones clínicas y hallazgos serológicos. Al igual que la forma idiopática es más prevalente en mujeres, aunque la población afectada suele ser de mayor edad26. El tiempo de latencia entre la toma del fármaco y el inicio de las lesiones oscila entre 4 y 20 semanas. Las manifestaciones cutáneas se caracterizan por la aparición de una erupción cutánea localizada en zonas fotoexpuestas como la cara, el escote y la cara extensora de los brazos, constituida por lesiones descamativas con patrón papuloescamoso (fig. 1) o anular (figs. 2 y 3), que curan en semanas o meses sin dejar cicatriz27. En el LECSIF las lesiones pueden ser más diseminadas y extenderse a áreas no fotoexpuestas como el tercio inferior de la espalda.
Mujer de 29 años con antecedente de epilepsia y lupus eritematoso subagudo inducido por carbamazepina de 9 años de evolución. Nótese la intensa afectación cutánea con lesiones pápulo-escamosas psoriasiformes en el tórax y en la región facial. (A) Gran afectación de los brazos y los antebrazos (B) con zonas poiquilodérmicas. Grandes placas eritemato-descamativas que comprenden toda la superficie de la espalda (C) y gran parte del abdomen. (D) Ha sido imposible retirar el fármaco debido al mal control de las crisis epilépticas con otros fármacos.
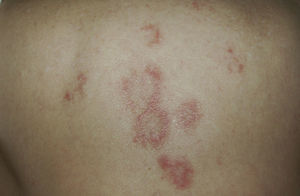
Mujer de 54 años con antecedente de epilepsia y lupus eritematoso subagudo de 2 meses de evolución tras la toma de oxcarbazepina. Lesiones eritematosas y descamativas de morfología anular en la región lumbar (A), en la espalda (B) y en los brazos (C). La sintomatología desapareció 3 meses después de suspender el antiepiléptico.
Paciente mujer de 79 años con antecedente de carcinoma de ovario metastásico. Lesiones compatibles clínica e histopatológicamente con lupus eritematoso subagudo de 2 meses de evolución en la espalda. En los últimos meses refería la toma de bisoprolol. Las lesiones desaparecieron tras retirar el fármaco.
Algunos autores señalan que en el LECSIF las formas ampollosas son más frecuentes que en el LECS idiopático28. En cuanto a las manifestaciones extracutáneas como artritis, serositis y afectación visceral hay que resaltar que suelen estar ausentes en el LECSIF29. Las manifestaciones hematológicas como anemia, leucopenia y plaquetopenia suelen ser muy raras. La mayoría de los pacientes mejoran su sintomatología tras 8 semanas de la suspensión del fármaco y los anticuerpos anti-Ro suelen desaparecer en un periodo de 8 meses26.
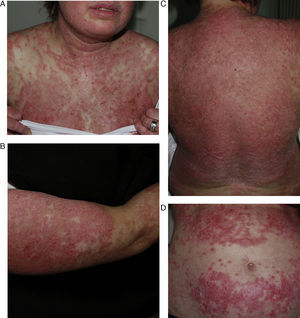
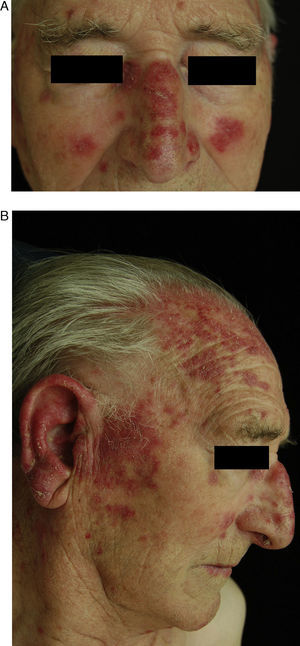
Lupus eritematoso cutáneo crónico inducido por fármacosLas manifestaciones clínicas suelen ser las clásicas lesiones discoides cutáneas en zonas fotoexpuestas como la cara, el tronco superior y los brazos (fig. 4). Las manifestaciones sistémicas, al igual que en la variante idiopática, suelen estar ausentes. Según la literatura el tiempo trascurrido desde la toma del fármaco hasta el desarrollo de los síntomas es de unos 8 meses. Las manifestaciones clínicas suelen resolverse en unas 5 semanas tras la retirada del fármaco30.
A y B. Paciente de 82 años con lesiones eritemato-descamativas en la región facial y en los brazos de 9 meses de evolución. El diagnóstico histopatológico fue compatible con un lupus discoide crónico. Previamente había empezado a tomar hidroclorotiazida. Las lesiones desaparecieron varios meses después de retirar el fármaco.
Los fármacos capaces de inducir LESIF pueden subdividirse en 3 categorías (tabla 1):
- 1.
Primera categoría: son aquellos fármacos en los que está bien demostrado que pueden ser causantes de LESIF. Existen evidencias convincentes de LESIF como la hidralacina, la procainamida, la isoniacida, la metildopa, la quinidina y la clorpromacina.
- 2.
Segunda categoría: son fármacos que potencialmente pueden causar LESIF. Entre ellos están los anticonvulsivantes, los antitiroideos, la D-penicilamina, la sulfasalacina, los bloqueadores beta y los diuréticos tiazídicos.
- 3.
Tercera categoría: son fármacos descritos en la literatura como causantes de algún caso de LESIF. Entre ellos se encuentran la minociclina y algunas tetraciclinas, el ácido valproico, el IFN-α, la interleucina-2 (IL-2), el clobazam, la lamotrigina, el infliximab, los inhibidores de la enzima convertidora de angiotensina (IECA), la ticlopidina, la amiodarona, los hipolipidemiantes, las sales de oro, la penicilina, la estreptomicina, la fenilbutazona, los estrógenos y los anticonceptivos orales, el ácido paraaminosalicílico y la reserpina.
Fármacos descritos como inductores de lupus eritematoso sistémico inducido por fármacos
| Fármacos | Alto riesgo | Riesgo moderado | Bajo riesgo | Riesgo muy bajo |
| Antiarrítmicos | Procainamida (15-20%) | Quinidina (<1%) | Disopiramida, propafenona | |
| Antihipertensivos | Hidralacina (5-8%) | Metildopa, captopril, acebutol | Clonidina, enalapril, labetalol, minoxidil, pindolol, prazosin, atenolol, timolol | |
| Antipsicóticos | Clorpromacina | Clorprotixeno, carbonato de litio, fenelcina, perfenacina | ||
| Antibióticos | Isoniacida | Minociclina | Nitrofurantoína | |
| Anticonvulsivantes | Carbamacepina | Etosuximida, fenitoína, primidona, trimetadiona | ||
| Antitiroideos | Propiltiouracilo | |||
| Antiinflamatorios | Sulfasalacina | D-penicilamina, sulfonamida | fenilbutazona | |
| Diuréticos | 5-Aminosalicilato | Clortalidona, hidroclorotiacida | ||
| Hipolipidemiantes | Atorvastatina, fluvastatina, lovastatina, pravastatina, simvastatina | |||
| Biológicos | Etanercept, infliximab, adalimumab, IFN-α, IL-2 | |||
| Neurolépticos | Levodopa | |||
| Antiadrenales | Aminoglutetimida |
La hidralacina es un vasodilatador periférico que se utiliza desde los años 50 para la hipertensión arterial. En la actualidad ha sido sustituido por otros nuevos fármacos con un perfil de efectos secundarios más tolerable. La hidralacina es junto con la procainamida el fármaco con mayor riesgo asociado de desarrollar un LESIF, con una incidencia del 5-8% de los pacientes tratados durante un año a dosis estándar31. La hidralacina se absorbe en el tracto gastrointestinal y es metabolizada en el hígado por la enzima N-acetiltransferasa, proceso que está determinado genéticamente. En función de cómo sea la velocidad de este proceso de acetilación se distinguen 2 tipos de acetiladores: los lentos y los rápidos. Los acetiladores lentos de hidralacina suelen desarrollar ANA con dosis más bajas de fármaco y en un periodo de tiempo más breve. La posibilidad de desarrollar un LEIF no solo viene determinada por la velocidad de acetilación, sino también por la dosis del fármaco y el tipo de HLA del paciente. Muchos pacientes desarrollan un LEIF con dosis tan bajas de hidralacina como 100 mg32. La posibilidad de desarrollar un LEIF podría estar determinada genéticamente, ya que se ha asociado este hecho a la presencia del HLA-DR433. Aunque hasta un 50% de los pacientes que toman hidralacina a dosis de 200mg/d desarrollan ANA2, solo un 10% de los pacientes tratados con hidralacina desarrollan un LESIF. Al contrario de lo que ocurre con otros fármacos, con la hidralacina parece que existe una correlación entre la dosis del fármaco y el desarrollo de autoinmunidad. Según algunos estudios el 5,4% de los pacientes que toman 100mg/d de este fármaco desarrollan un LESIF, mientras que el 10,4% de los pacientes que toman 200mg/d lo desarrollan2. Es muy frecuente que los casos de LESIF por este fármaco desarrollen sintomatología articular como artritis, llegando a afectar al 63% de los pacientes. Aunque la afectación renal es infrecuente, la hidralacina es el fármaco que se ha implicado con más frecuencia en el desarrollo de complicaciones renales25. La afectación pulmonar, incluyendo la pleuritis, la enfermedad vascular pulmonar o la neumonitis, es muy infrecuente en el LESIF inducido por hidralacina, siendo muy escasos los casos descritos34. La afectación cutánea es más prevalente en los casos producidos por hidralacina que por procainamida, aunque no suelen manifestarse como el típico eritema malar35.
Por último, las anomalías serológicas que se suelen observar incluyen positividad de ANA y de anticuerpos antihistona en un 95% de los pacientes y negatividad de los anti-ADNds, salvo en un 5% de los casos y cifras normales de complemento35.
ProcainamidaLa procainamida es un fármaco antiarrítmico utilizado desde los años 50. Casi el 90% de los pacientes tratados con procainamida, uno de los fármacos que más comúnmente causan autoinmunidad inducida por fármacos, desarrollan títulos detectables de ANA, pero solamente un 30% desarrolla clínica de LEIF36. El intervalo de tiempo entre la introducción del fármaco y el desarrollo de la sintomatología oscila entre 3 meses y 2 años. Como hemos comentado previamente, las manifestaciones cutáneas y renales son muy infrecuentes en el LESIF inducido por hidralacina35. Por el contrario, la afectación pleural y pericárdica es especialmente frecuente en los casos de LESIF inducidos por este fármaco35. Las anomalías inmunológicas son similares a las observadas en los casos provocados por hidralacina. Sin embargo, en los casos por procainamida se observa en un porcentaje muy alto de pacientes anticuerpos antihistona frente a la partícula del subnucleosoma (H2A-H2B)-ADN37.
IsoniacidaLa isoniacida es un fármaco tuberculostático. Hasta un 25% de los pacientes tratados con este fármaco desarrollan positividad de ANA, pero solo un 1% de los pacientes presentan un LESIF2. Para desarrollar un LESIF es necesario estar recibiendo una dosis de 300-900mg/d durante un tiempo comprendido entre 4 semanas y 14 meses. Al igual que en el caso de la hidralacina, los acetiladores lentos tienen un riesgo mayor de desarrollar la enfermedad. Las manifestaciones clínicas más frecuentes son las artralgias/artritis junto con anemia. La fiebre y la pleuritis ocurren en un 50% de los pacientes, mientras que la pericarditis aparece en un 30% de los casos.
El anticuerpo IgG frente al complejo (H2A-H2B)-ADN parece ser específico del LESIF por isoniacida.
MetildopaLa metildopa es un fármaco antihipertensivo. Ha sido ampliamente utilizado, aunque tiene múltiples efectos adversos. Un 15% de los pacientes desarrollan ANA, mientras menos del 1% de los pacientes tratados desarrollan un LESIF2,38.
ClorpromacinaLa clorpromacina es un fármaco antipsicótico ampliamente utilizado en la práctica clínica. Hasta un 50% de los pacientes presentan ANA positivos a las dosis de 400mg/d, aunque menos de un 5% de los pacientes desarrollan un LESIF39.
Los signos clínicos más frecuentes son parecidos al LES idiopático e incluyen fiebre, artralgias y erupciones cutáneas. Se han descrito casos de afectación cardiaca severa.
QuinidinaEs un fármaco empleado para el tratamiento de las arritmias cardiacas. Su uso se ha asociado al desarrollo de LESIF en ausencia de ANA. La quinidina podría ser considerada de un riesgo intermedio40. El LEIF causado por quinidina parece estar asociado a un descenso en los niveles del complemento, lo que es inusual en el LESIF causado por otros fármacos.
Segunda categoríaSulfasalacinaLa sulfasalacina o la salazopirina es un compuesto formado por el ácido-5-aminosalicílico y sulfapiridina que se utiliza en un amplio número de enfermedades reumatológicas41–43. Aunque infrecuentes, también se han descrito casos de LESIF con positividad de anticuerpos antihistona y negatividad de los anti-ADNds.
AnticonvulsivantesSon fármacos utilizados en la epilepsia. Existen casos de LESIF por la carbamacepina, la fenilhidantoína y la etosuximida asociados o no a ANA positivos.
Los casos de LESIF por carbamacepina se consideran raros, con una incidencia de menos del 0,001% de los casos tratados44.
AntitiroideosEl propiltiouracilo, el tiouracilo y el metiltiouracilo son fármacos ampliamente utilizados para el tratamiento del hipertiroidismo. Se han descrito casos de LEIF por estos fármacos asociados a ANA positivos, leucopenia, anti-ADNds positivos, ANCA positivos y púrpura cutánea45.
D-penicilaminaEs un fármaco quelante del cobre usado en la enfermedad de Wilson, en la esclerodermia y en la artritis reumatoide. La inducción de LESIF es un efecto adverso muy poco frecuente46. Este LESIF puede manifestarse de manera asintomática asociado a ANA positivos e hipocomplementemia o como un cuadro clínico severo caracterizado por artralgia/artritis, serositis, erupción cutánea, malestar general y pérdida de peso.
Diuréticos tiazídicosSon fármacos antihipertensivos con un perfil bastante seguro en cuanto a efectos adversos. Se han descrito casos de LECSIF con ANA positivos, anti-ADNds y antihistona negativos43,47.
Bloqueadores betaEntre ellos se encuentran el propanolol y el atenolol. Son fármacos con uso muy extendido en la hipertensión arterial, en la profilaxis de la angina de pecho y en las arritmias cardiacas. Se han descrito casos de LESIF con positividad de ANA y anticuerpos antihistona48.
Tercera categoríaMinociclinaLa minociclina es una tetraciclina semisintética utilizada entre otras aplicaciones para el tratamiento del acné. El LESIF por minociclina es relativamente infrecuente. Un estudio controlado reciente ha mostrado que los pacientes tratados con minociclina para el acné que habían recibido más de 50.000mg del fármaco tenían un mayor riesgo de desarrollar LESIF49. Las mujeres tienen mayor probabilidad que los hombres de desarrollar esta patología. No se ha encontrado asociación entre el desarrollo de autoinmunidad y la toma de otros tipos de tetraciclinas50. El LESIF debido a minociclina se caracteriza por las características típicas de LESIF, como artralgias y artritis, y también por afectación cutánea inusual (fenómeno de Raynaud, poliarteritis nodosa, eritema nodoso), afectación hepática y raramente antihistona positivos51. Un porcentaje pequeño de pacientes presentan úlceras orales, livedo reticularis, erupción cutánea, alopecia y vasculitis, siendo muy difícil de diferenciar del LES idiopático52. Es rara la afectación neurológica, pulmonar y hematológica. Se suelen observar ANA, anti-Sm, anticuerpos antifosfolípidos y anti-ADN positivos52. La remisión del cuadro clínico ocurre tras la suspensión del fármaco, aunque en ocasiones es necesario que transcurra un tiempo de 2 años.
Ácido valproicoEs un fármaco antiepiléptico. El LESIF que puede provocar se caracteriza por fiebre, artromialgias, leucopenia, plaquetopenia, afectación del SNC, positividad de antihistonas y anti-ADNds e hipocomplementemia.
Interferón-αLos fármacos biológicos como los IFN-α y β, usados como antivirales en la hepatitis C, tienen la capacidad de alterar las funciones del sistema inmunológico y pueden inducir varios fenómenos autoinmunes53. Existen muy pocos casos descritos en la literatura de lupus inducidos por IFN-α54,55.
Estos casos son distintos de otros LESIF por su alta incidencia de afectación mucocutánea y renal, así como una positividad de los anti-ADNds en el 50% de los pacientes.
Interleucina-2Es una citocina producida por los linfocitos T helper usada como un agente inmunoterápico para el tratamiento del melanoma y del carcinoma renal, con casos aislados descritos de LESIF en la literatura56.
ClobazamEs una benzodiacepina usada para el tratamiento de la epilepsia. Se han comunicado casos de LESIF debidos a este fármaco57.
LamotriginaEs un fármaco antiepiléptico. Recientemente se ha detallado algún caso de LESIF58.
Anti-factor de necrosis tumoral αDesde su comercialización los anti-TNFα han sido ampliamente utilizados para varias enfermedades muy prevalentes como la artritis reumatoide, la psoriasis, la espondiloartropatías y la enfermedad inflamatoria intestinal. El desarrollo de autoanticuerpos en los pacientes tratados con anti-TNFα es un hecho bien conocido, pero el desarrollo de LESIF es relativamente raro59. En los ensayos clínicos y registros poscomercialización60 se ha evidenciado que casi en 2/3 de los pacientes tratados se producen autoanticuerpos, aunque menos del 1% de ellos desarrollan un LEIF. En los últimos años se han descrito múltiples casos de LESIF inducidos por los inhibidores del TNFα. Estos casos se presentan con una clínica muy diversa que incluye artritis/artralgias, erupciones cutáneas, serositis y alteraciones analíticas como citopenias. Los casos de LESIF inducidos por los anti-TNFα difieren en varias características del LESIF clásico. En primer lugar, la incidencia de la afectación cutánea es mayor en los casos de LESIF debidos a estos agentes que en los clásicos. Hasta un 72% de los LEIF inducidos por anti-TNFα presentan manifestaciones cutáneas17. Además, en la mayoría de los casos de LESIF clásicos la afectación visceral es infrecuente, mientras que en los casos provocados por los anti-TNFα no es tan extraña la afectación visceral, sobre todo la renal61–63. Así mismo, los niveles bajos de complemento y los anti-ENA, así como los anti-ADNds que están raramente presentes en los casos de LESIF clásico, se suelen detectar hasta en la mitad de los casos de LESIF causados por anti-TNFα17. Por el contrario, los anticuerpos antihistona se detectan en una proporción mayor en los LESIF clásicos. La mayoría de los casos descritos de LESIF secundarios a los anti-TNFα son causados por etanercept, infliximab y muy raramente, adalimumab. Según un estudio publicado en 2007 se habían descrito hasta la fecha un total de 92 casos de LESIF (40 de infliximab, 37 de etanercept y 15 de adalimumab)64. De forma similar, la leflunomida, que es un tratamiento efectivo para el LES, puede causar casos de LESIF65–67. No se ha establecido si el desarrollo de un LESIF en un paciente tratado con anti-TNFα predispone al desarrollo de esta enfermedad con la toma de otro anti-TNFα.
Lupus eritematoso cutáneo subagudo inducido por fármacosLos fármacos que con mayor frecuencia causan esta enfermedad suelen ser los antihipertensivos como las tiazidas68,69, los IECA70, los bloqueadores beta71, y los bloqueadores de los canales del calcio (tabla 2). Más recientemente se han descrito casos de LECSIF por terbinafina72–74, bupropión75, fármacos antineoplásicos76–78, leflunomida65,66, efalizumab79, inhibidores de la bomba de protones80, tamoxifeno81, neurolépticos (fenitoína82, oxcarbazepina83), benzodiacepinas84 (tetrazepam, lormetazepam), procainamida84 y etanercept85.
Fármacos descritos como potencialmente implicados en casos de lupus eritematoso cutáneo subagudo inducido por fármacos
| Fármacos | Alto riesgo (>5%) | Bajo riesgo (<5%) | |
| Antifúngicos | GriseofulvinaTerbinafina | ||
| Antihipertensivos | Antagonistas de los canales del calcio | Diltiazem, verapamilo, nifedipino nitrendipino | Inhibidores de la enzima conversora de la angiotensina (cilazapril, captopril) |
| Betabloqueantes | Oxprenolol, acebutolol | ||
| Diuréticos | Hidroclorotiazida, espironolactona | ||
| Quimioterápicos | Docetaxel | 5-Fluorouracilo, capecitabina | |
| Antiácidos | Omeprazol, lansoprazol, ranitidina | ||
| Antiepilépticos | Fenitoína, oxcarbamazepina | ||
| Antimaláricos | Hidroxicloroquina | ||
| Inmunomoduladores | Etanercept, infliximab, efalizumab, INF-α, leflunomida | ||
| Hipolimemiantes | Pravastatina, simvastatina | ||
| Antiinflamatorios | Naproxeno, piroxicam | ||
| Antidepresivos | Bupropión | ||
| Antidiabéticos | Sulfonilurea (gliburida) | ||
| Antiarrítmicos | Procainamida | ||
| Benzodiacepinas | Tetrazepam, lormetazepam | ||
| Antiagregantes | Ticlopidina | ||
| Antiestrógenos | Tamoxifeno | ||
| Miscelánea | D-Penicilamina, insecticida | ||
El lupus eritematoso cutáneo crónico inducido por fármacos (LECCIF) es muy infrecuente y normalmente está provocado por la toma de fluorouracilo, especialmente tegafur y uraciltegafur o sus derivados más modernos como la capecitabina30,86. También se han descrito casos aislados con antiinflamatorios no esteroideos (AINE) o diuréticos tiazídicos. Sin embargo, recientemente se han publicado casos de lupus tumidus inducidos por anti-TNFα como infliximab y adalimumab o IECA17,87–89.
DiagnósticoDeberemos sospechar un LESIF ante todo paciente que esté recibiendo un tratamiento con un fármaco de forma continuada durante meses o años y desarrolle ANA y al menos uno de los síntomas de LES idiopático. Para el diagnóstico es necesario que el afectado tenga una historia previa negativa de LES y que carezca de afectación renal o neurológica grave. Esta sospecha se confirmará cuando tras la retirada del fármaco implicado tanto las alteraciones clínicas como inmunológicas desaparezcan. La mayoría de los pacientes con LESIF no cumplen los 4 criterios de la Asociación Americana de Reumatología (AAR) para el diagnóstico del LES. Los hallazgos serológicos también son de importancia en el diagnóstico. Se suele observar la presencia en sangre periférica de anticuerpos antihistonas, en especial los anticuerpos dirigidos frente al complejo ([H2A-H2B]-ADN), y ausencia de anti-ADNds, anti-Sm, anti-RNP, anti-Ro y anti-La. Al contrario que en el LES idiopático no se suele observar hipocomplementemia. Aunque no existen criterios diagnósticos estandarizados, se han propuesto una serie de criterios diagnósticos para definir el LESIF:
- 1.
Tratamiento continuado con un fármaco durante al menos un mes.
- 2.
No tener historia previa de LES antes de utilizar el fármaco.
- 3.
Presencia de un cuadro caracterizado por fiebre, artritis, malestar general y mialgias.
- 4.
Positividad de los anticuerpos antihistona (en especial IgG frente al complejo ([H2A-H2B]- ADN) y anti-ADNss. Negatividad de los anticuerpos anti-ADNds y anti-ENA.
La positividad de estos anticuerpos suele desaparecer meses después de la retirada del fármaco culpable. La seroconversión a unos ANA positivos en un paciente en tratamiento con un fármaco que potencialmente puede inducir un LESIF no obliga a suspender el tratamiento, ya que solo un pequeño porcentaje de estos pacientes desarrollarán un LESIF. Respecto al diagnóstico del LECSIF y del LECCIF tampoco existen unos criterios bien definidos. Un test de provocación con el fármaco sospechoso que reproduzca las lesiones cutáneas es un hallazgo contundente, pero rara vez se ha comunicado en la literatura. El diagnóstico de estas entidades es más probable si se trata de un primer episodio de lesiones similares clínica e histológicamente a las del lupus cutáneo en pacientes de edad media y avanzada, coincidiendo con la toma de un fármaco de reciente incorporación, es decir, que exista una correlación temporal y una mejoría del cuadro tras su retirada. El estudio inmunológico en algunos de los casos revisados de LECSIF realza la importancia de los anticuerpos anti-Ro en detrimento de los anticuerpos antihistona, cuyo papel es más cuestionado en esta entidad.
Aunque la utilidad de las pruebas epicutáneas no ha sido evaluada en el diagnóstico del LEIF, sí nos pueden ser de ayuda en el diagnóstico diferencial con otras toxicodermias en su fase inicial, como el síndrome de Stevens-Johnson/necrólisis epidérmica tóxica y el síndrome DRESS. Un trabajo reciente ha demostrado su utilidad en el diagnóstico de estas patologías en casos producidos por carbamacepina, fármaco potencialmente causante también de LEIF90.
Alteraciones de laboratorioLupus eritematoso sistémico inducido por fármacosAunque la mayoría de los pacientes tienen típicamente una positividad de los ANA, su incidencia es variable91. El patrón de ANA en el LEIF es normalmente homogéneo, ya que estos anticuerpos tienen como diana las histonas. No obstante, un número no despreciable de pacientes con sintomatología de LES y en tratamiento con quinidina o minociclina no presentan ANA, por lo que la ausencia de ANA no excluye el diagnóstico de LEIF. Los anticuerpos antihistona son los más característicos del LESIF. Su positividad es un distintivo del LESIF, apareciendo en más del 90% de los casos, pero es menos frecuente con el uso de ciertos fármacos como la minociclina y los inhibidores del TNF-α92,93. Aunque los anticuerpos antihistona son muy prevalentes en el LESIF, no son patognomónicos de esta patología. Estos anticuerpos suelen tener una alta sensibilidad para el diagnóstico del LESIF, aunque una baja especificidad. En concreto, como hemos descrito previamente, se observan anticuerpos antihistona en el 90-95% de los casos de LESIF, aunque también en el 75% de los casos de LES y en el 32% de los casos de pacientes con ANA positivo sin signos clínicos de la enfermedad. Además también están presentes en algunos pacientes con artritis reumatoide, síndrome de Felty, artritis reumatoide juvenil (sobre todo en pacientes con ANA positivo y uveítis) y conectivopatías indiferenciadas94–97. Los anticuerpos antihistona son anticuerpos que reconocen epítopos de histonas solo presentes en la cromatina o de histonas libres o desnaturalizadas. Se ha demostrado la existencia de 2 tipos de anticuerpos antihistona, unos contra la histona simple H1, H2A, H2B, H3 y H4 y otros frente al complejo de histonas H2A-2B y H3-498. Los anticuerpos de tipo IgG que reaccionan con la cromatina nativa o el complejo H2A-H2B-ADN reconstituido, identificados mediante ELISA, parecen constituir un buen marcador de LEIF99. La presencia de títulos altos de anticuerpos antihistona de clase IgG suele ser un hallazgo casi constante en el LEIF, salvo en los casos de LEIF causado por procainamida, que suelen tenerlos de la subclase IgM100. Es un hecho conocido que muchos pacientes tratados con fármacos que pueden causar LESIF presentan anticuerpos antihistona sin evidencia clínica de enfermedad101. Normalmente el título de anticuerpos disminuye cuando se suspende el fármaco, aunque pueden pasar varios meses hasta que se hagan indetectables102. La positividad de anticuerpos anti-ADNds es un hallazgo raro en el LESIF93. Por tanto, la presencia de este tipo de autoanticuerpos debería hacernos pensar que se trata de una forma idiopática. No obstante, se han observado títulos mayores de anti-ADNds en pacientes tratados con inhibidores del TNF-α. Según algunos autores hasta el 90% de los LEIF inducidos por anti-TNFα tienen anticuerpos anti-ADNds positivos. Otra diferencia del LESIF respecto al LES idiopático es que los ANA del LEIF no tienen capacidad para fijar complemento103. En las formas cutáneas del LEIF puede existir positividad de los autoanticuerpos anti-Ro, siendo infrecuente en las formas sistémicas104,93. Las alteraciones hematológicas tales como leucopenia leve, anemia normocítica normocrómica, plaquetopenia y elevación de la velocidad de sedimentación globular suelen observarse en algunos pacientes con LESIF. Estas alteraciones suelen ser menos frecuentes que en la forma idiopática.
Lupus eritematoso cutáneo subagudo inducido por fármacosA diferencia de lo que sucede en el LESIF, en el LECSIF el perfil inmunológico incluye con frecuencia la positividad de los anticuerpos anti-Ro, junto con los ANA y en ocasiones los anti-La. Algunos autores señalan que los anticuerpos antihistona no deberían ser considerados un marcador serológico del LECSIF, aunque existe controversia respecto a este tema104. En la serie de casos de 71 pacientes de Sontheimer et al., menos del 50% presentaban anticuerpos antihistona. Los anti-ADNds suelen ser también negativos. La mayoría de los pacientes mejoran su sintomatología en 8-12 semanas tras la suspensión del fármaco, pero los anticuerpos anti-Ro persisten después de la resolución de las lesiones y permanecen positivos alrededor de un periodo de 8 meses26, aunque se ha publicado su persistencia hasta los 6 años después del episodio.
Lupus eritematoso cutáneo crónico inducido por fármacosEn la mayoría de los casos de LECCIF se observa una positividad de los ANA, mientras los anti-ENA y los anti-ADNds suelen ser negativos, salvo raras excepciones105.
Los ANA suelen negativizarse en unas 10 semanas tras la retirada del fármaco implicado. Así mismo, los anticuerpos antihistona suelen ser negativos106,107.
TratamientoEl manejo del LEIF consiste en la retirada del fármaco implicado. El tratamiento farmacológico debería estar reservado a los casos refractarios, los cuales realmente suelen ser casos de lupus preexistentes exacerbados por un fármaco concreto. Aunque las manifestaciones cutáneas del LEIF desaparecen normalmente después de unas semanas tras la retirada del fármaco, la resolución completa puede demorarse varios meses, haciendo necesario el uso de un tratamiento farmacológico. Las manifestaciones cutáneas del LESIF como la vasculitis cutánea, además de las lesiones cutáneas de LECSIF, pueden ser transitoriamente tratadas con corticoides sistémicos a las dosis indicadas para las formas idiopáticas, corticoides tópicos e hidroxicloroquina. En los casos más resistentes podrían utilizarse fármacos inmunosupresores como la talidomida, la azatioprina, la ciclofosfamida y el micofenolato mofetilo. En el LECCIF los corticoides tópicos en combinación con la hidroxicloroquina suelen ser efectivos. En esta forma clínica los esteroides sistémicos y la talidomida deben reservarse para casos refractarios.
ConclusionesEl LEIF es un síndrome semejante al lupus idiopático que ocurre como consecuencia de la exposición a un número cada vez mayor de fármacos. Con el desarrollo de nuevos tratamientos para multitud de patologías se prevé que la incidencia de esta entidad aumente de forma significativa, especialmente con el auge de los fármacos que modulan la respuesta inmunológica. Sus manifestaciones clínicas o serológicas se resuelven normalmente después de la retirada del fármaco. Además del LESIF existen 2 formas cutáneas bien establecidas denominadas LECCIF y LECSIF. Aunque la forma crónica cutánea es muy infrecuente, la variante cutánea subaguda está considerada como la forma más frecuente de LEIF.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido la información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de la correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.