Sr. Director:
Aunque la dermatitis alérgica de contacto (DAC) por corticoides es un fenómeno bien conocido y relativamente frecuente, raramente pueden producirse reacciones cutáneas tras su uso sistémico (dermatitis sistémicas de contacto [DSC]). Presentamos el caso de un paciente con DAC a diversos corticoides, que posteriormente presentó DSC a múltiples corticoides sistémicos.
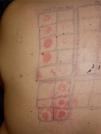
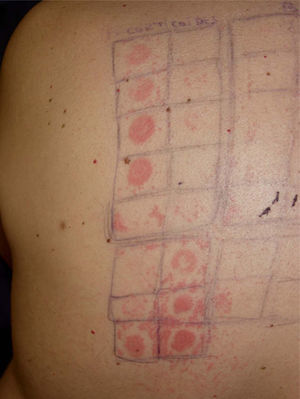
Se trata de un varón de 47 años que acudió a nuestra consulta por presentar una placa de alopecia areata en el cuero cabelludo. Se pautó metilprednisolona aceponato 0,1 % en emulsión, surgiendo a los 4 días lesiones maculosas, eritematodescamativas y pruriginosas en los párpados, el cuello y alrededor de la placa de alopecia. Con diagnóstico de sospecha de DAC por corticoide se pautó pimecrolimus crema al 1 % y se realizaron pruebas epicutáneas con True Test®, batería de corticoides y productos propios (Lexxema emulsión®). Se realizó la lectura los días 2, 5 y 7 obteniéndose positividad a múltiples corticoides (tabla 1, fig. 1). Se realizó la prueba de punción e intradermorreacción con hidrocortisona, prednisona, metilprednisolona, prednisolona, dexametasona y deflazacort, que fueron negativos, procediéndose posteriormente a su administración oral a dosis terapéuticas. Tras un periodo de 6–24 horas en todos los casos aparecieron lesiones eritematosas, pruriginosas que afectaban al cuello, las axilas, las ingles y el periné (baboon-like). En la provocación con placebo no se reprodujeron lesiones. La biopsia cutánea de una de dichas reacciones mostró una dermatitis espongiótica con infiltrado inflamatorio perivascular superficial y edema dérmico. Se realizó el diagnóstico de DAC y DSC por corticoides con polisensibilización a los mismos. Se llevó a cabo un test de uso con una crema de mometasona fuorato 0,1 %, sin producirse lesiones tras 10 días, por lo que se indicó como tratamiento en caso de necesidad de un corticoide tópico.
Pruebas realizadas al paciente y resultados
| Corticoide | Concentración (vaselina) | Grupo corticoide | Epicutáneas | Provocación |
| Tixocortol pivalato | 1 | A | − | |
| Budesonida | 0,1 | B | ++ | |
| Hidrocortisona acetato | 25 | A | − | |
| Hidrocortisona 17-butirato | 1 | D2 | ++ | |
| Triamcinolona acetónido | 1 | B | + | |
| Triamcinolona acetónido | 5 | B | ++ | |
| Prednisolona | 5 | A | − | ++ |
| Betametasona-17-valerato | 1 | D1 | ++ | |
| Clobetasol 17 dipropionato | 1 | D1 | + | |
| Dexametasona 21 fosfato disódico | 1 | C | ++ | |
| Dexametasona valerato | 1 | C | ++ | |
| Dexametasona base | 1 | C | +/− (D7) | ++ |
| Hidrocortisona base | 12,5 | A | − | ++ |
| Betametasona base | 1 | C | − | |
| Betametasona dipropionato | 0,5 | D1 | ++ | |
| Betametasona valerato | 1 | D1 | + | |
| Fluocinolona acetónido | 0,25 | B | + (D7) | |
| Lexxema® emulsión | Tal cual | D2 | + | |
| Mometasona fuorato | 1 % | D1 | − | |
| Metilprednisolona (Urbason®) | Tal cual | A | − | ++ |
| Prednisona (Dacortin®) | Tal cual | A | − | ++ |
| Deflazacort (Zamene®) | Tal cual | A | − | ++ |
La DAC por corticoides debe sospecharse cuando se produce un empeoramiento, una cronificación de la dermatitis previa o cuando no tiene lugar la mejoría que era esperable. Gonul y Gul demuestran mediante pruebas epicutáneas una sensibilización en el 22 % de los pacientes diagnosticados de DAC no respondedores a corticoides tópicos1. Las cifras de positividades a corticoides en las pruebas epicutáneas oscilan del 0,52 al 6 %, lo que ha llevado a incluir dichos alergenos en las diversas baterías estándar2-4. En nuestro medio el Grupo Español de Investigación de Dermatitis de Contacto (GEIDC) introdujo inicialmente tixocortol pivalato 1 % en vaselina, añadiéndose posteriormente la budesonida 0,1 % vaselina. Desde el año 2007 en el True Test® además se ha añadido hidrocortisona-17 butirato. En el estudio epidemiológico de DAC en España en el año 2001, publicado por el GEIDC5, se obtenían positividades para corticoides únicamente en el 1,01 %. Desconocemos las cifras actuales con los nuevos corticoides usados como cribado.
En un estudio retrospectivo de 1.188 pacientes parcheados con una batería específica de corticoides se demostró que si sólo hubieran utilizado tixocortol pivalato habrían detectado menos de un 50 % de las sensibilizaciones6. Con los tres corticoides actuales como cribaje presentes en el True Test® se detectarían un 71 %. No obstante, quedaría un grupo significativo sin diagnosticar. Por ello la NACDG (North American Contact Dermatitis Group) ha añadido dos corticoides más a su batería estándar: acetónido de triamcinolona 1 % vaselina y clobetasol-17-propionato 1 % vaselina 3. Si se obtiene una positividad o hay sospecha de sensibilización debe parchearse una batería de corticoides para detectar posibles reacciones cruzadas. Las baterías de corticoides deberían incluir los más comúnmente utilizados en ese país. No obstante, corticoides tan utilizados como mometasona fuorato, prednicarbato o metilprednisolona aceponato, entre otros, no están incluidos en las baterías específicas comercializadas. Por ello, para minimizar la pérdida de casos es importante parchear los productos propios usados por el paciente.
Es recomendable realizar una lectura tardía en el día 6–7. Algunos estudios muestran pérdidas del 30 % sin esta lectura tardía, mientras que en otros es menor del 1 %6,7.
Las sensibilizaciones múltiples (correacciones o reacciones cruzadas) son relativamente frecuentes. Coopman et al en 1989 clasificaron los corticoides en 4 grupos, en función de su estructura química y de las reacciones cutáneas que se observaban con las pruebas del parche8 (tabla 2). No obstante, esto tiene un valor limitado, pues se han descrito reacciones cruzadas entre todos los grupos. Mucho menos frecuente es encontrar, como en nuestro caso, sensibilización a una gran cantidad de corticoides incluyendo todos los grupos9. El mecanismo no está claro, ya que puede deberse a una sensibilización a la estructura básica del corticoide o a un metabolito común.
Clases de corticoides
| Grupo | Estructura | Componentes | Reacciones cruzadas típicas |
| A | Sin metil sustitución en C16, ni cadena lateral en C17. Posible cadena lateral corta en C21 | Tixocortol pivalato | Con D2 |
| Hidrocortisona | |||
| Prednisolona | |||
| Metil prednisolona | |||
| Prednisona | |||
| B | Estructura cis-quetal o diol en C16 y C17; posible cadena lateral en C21 | Budesonida | Budesonida con D2 |
| Triamcinolona | |||
| Acetónido de triamcinolona | |||
| Acetónido de fluocinolona | |||
| Fluocinónido | |||
| Halcinónido | |||
| C | Sustitución metil en C16, no cadena lateral en C17, posible cadena lateral en C21 | Betametasona | |
| Dexametasona | |||
| Desoximetasona | |||
| Fluocortolona | |||
| D1 | Sustitución metilo en C16, cadena lateral éster en C17/C21 | Propionato de clobetasol | |
| Betametasona dipropionato | |||
| Betametasona-17 valerato | |||
| Mometasona fuorato | |||
| Diflucortolona valerato | |||
| D2 | Sin sustitución metilo ni halogenación en C16, cadena lateral éster en C17, posible cadena lateral en C21 | Hidrocortisona-17 butirato | Con A y con budesonida |
| Hidrocortisona-17 aceponato | |||
| Metilprednisolona aceponato | |||
| Prednicarbato |
La molécula usada como cribado se resalta en negrita.
Dada la sensibilización a múltiples corticoides y la posibilidad de una reacción tras su administración sistémica, se decidió provocación oral controlada. Con todos los corticoides probados se produjo una reacción cutánea pruriginosa tipo baboon, que se trata de un patrón clínico conocido de DSC. Aunque el paciente puede utilizar de forma tópica pimecrolimus/tacrolimus o mometasona fuorato, no hemos podido encontrar un corticoide sistémico seguro en caso de que el paciente lo precise en un futuro, debiendo valorarse cuidadosamente el balance riesgo-beneficio. Dicha circunstancia es excepcional, y aunque hay descritos casos de DAC a múltiples corticoides, sólo hemos encontrado en la literatura un caso similar al que se presenta en este artículo10.
Queremos resaltar la importancia de sospechar una DAC en aquellos casos que no respondan de forma adecuada al tratamiento esteroideo, debiendo ser estudiados en Unidades específicas de Contacto, tanto para confirmar el diagnóstico como para ofrecer alternativas terapéuticas seguras.
Conflicto de intereses
Declaramos no tener ningún conflicto de intereses.