El imiquimod 5% es un fármaco aprobado por la Food and Drug Administration (FDA) para el tratamiento tópico de los condilomas acuminados, queratosis actínicas y carcinomas basocelulares. Se trata de un medicamento de uso habitual en la práctica clínica diaria, sin embargo no se han descrito hasta el momento casos de alteraciones de la cicatrización después de la aplicación de dicho fármaco.
Se presentan 2 casos de cicatrización anormal aparecidos después del tratamiento con imiquimod al 5% en crema.
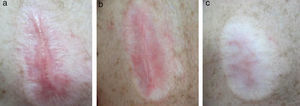
Caso 1Varón de 32 años sin alergias medicamentosas ni antecedentes personales médicos ni quirúrgicos de interés, que consultó por la presencia de una lesión en la región pectoral derecha de 2 años de evolución, tratada con antifúngicos por sospecha de micosis. En la exploración se objetivaba una placa eritemato-descamativa de 2cm de diámetro compatible con enfermedad de Bowen, por lo que se decidió instaurar tratamiento con imiquimod 5% crema una vez al día de lunes a viernes durante 6 semanas. A los 60 días de haber iniciado el tratamiento el paciente presentaba en la zona tratada una lesión lineal sobreelevada, perlada y con telangiectasias en la superficie, rodeada de un halo de piel atrófica e hipopigmentada (fig. 1A). Ante tales hallazgos se decidió realizar una biopsia cutánea de la lesión para estudio histopatológico, que reveló que se trataba de un proceso inflamatorio crónico inespecífico focalmente granulomatoso, con fibrosis de aspecto cicatricial y ausencia de elementos neoplásicos malignos, descartando la presencia de un proceso tumoral y llegando al diagnóstico de cicatriz hipertrófica.
El tratamiento con corticoides tópicos y bandas de silicona consiguió una disminución del prurito, aplanamiento de la lesión y disminución de las telangiectasias, pero persistencia de la hipocromía y atrofia a los 9 meses de tratamiento (fig. 1B y C).
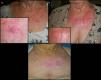
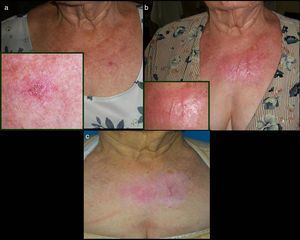
Caso 2Mujer de 71 años, sin alergias medicamentosas conocidas y con antecedentes personales de dislipidemia, espondiloartrosis y polinosis. No refería antecedentes quirúrgicos previos. La paciente consultaba por una lesión perlada de 1cm de diámetro, con queratosis central y telangiectasias gruesas a la dermatoscopia, localizada en la región pectoral izquierda, de 2 años de evolución (fig. 2A). Se estableció el diagnóstico de carcinoma basocelular superficial y se pautó imiquimod al 5% crema una vez al día de lunes a viernes durante 6 semanas.
Dos meses después se observó la presencia de una placa eritematosa de 7cm de diámetro, infiltrada y ligeramente dolorosa, que contenía 3 elementos lineales ramificados de consistencia elástica, que sobrepasaban la zona inicial tumoral, llegándose al diagnóstico clínico de queloide después de la aplicación de imiquimod 5% crema (fig. 2B).
Con el tratamiento con corticoides tópicos, a los 2 meses únicamente se consiguió disminuir el grado de eritema (fig. 2C).
La crema de imiquimod al 5% está indicada en los condilomas acuminados, el carcinoma basocelular superficial (CBCs) y las queratosis actínicas1. Sin embargo, su empleo fuera de ficha técnica en numerosos procesos dermatológicos ha demostrado resultados favorables2,3.
Los efectos secundarios locales habituales son eritema, prurito, ardor, ulceración, erosión, descamación y costra, y dentro de los síntomas sistémicos más comunes se han descrito cefalea, fatiga, fiebre, malestar general, algias, náuseas, diarrea y artralgias4,5.
Imiquimod se ha sugerido como alternativa a la cirugía en zonas quirúrgicas complejas precisamente por los mejores resultados estéticos obtenidos. En este sentido, incluso se ha propuesto en el tratamiento de cicatrices hipertróficas y queloides6,7. Sin embargo, es preciso tener en cuenta la habitual inflamación asociada a la aplicación de imiquimod. Esta reacción inflamatoria, de intensidad y naturaleza variable, puede llegar a ser intensa hasta el punto de que en áreas anatómicas predispuestas (región pectoral, preesternal, clavicular, etc.) puede ocasionar una cicatriz hipertrófica o un queloide.
En los casos presentados las lesiones estaban localizadas en la superficie anterior del tórax, área anatómica con tendencia natural a la cicatrización hipertrófica y al queloide; este factor debe ser tenido en cuenta a la hora de prescribir imiquimod en estas localizaciones.
Por otra parte, los pacientes descritos no contaban con antecedentes quirúrgicos ni traumáticos relevantes, por lo que no fue posible conocer su predisposición a la mala cicatrización; sin embargo, ambos presentaron una intensa inflamación en regiones con tendencia al queloide, lo cual parece justificar la evolución.