Etanercept (ETN) es un fármaco antagonista del factor de necrosis tumoral que ha demostrado ser eficaz y seguro en el tratamiento de la psoriasis1–3. Sin embargo, su posible relación con la aparición de infecciones es discutida4.
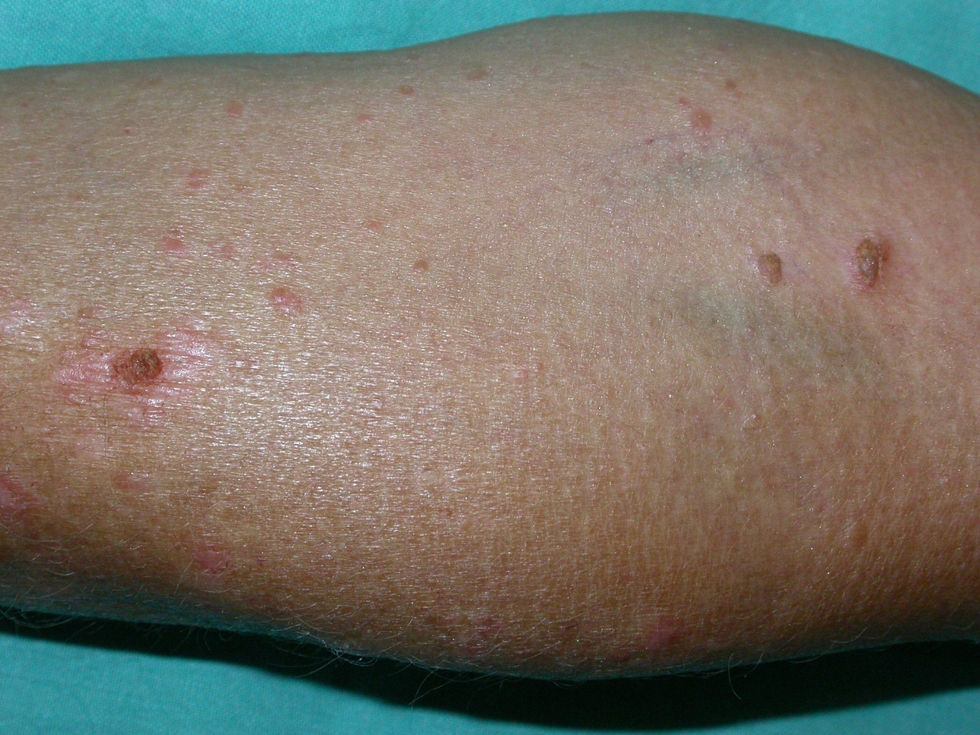
Presentamos el caso de una mujer de 70 años diagnosticada de psoriasis crónica en placas resistente a terapia sistémica convencional. La paciente cuando acudió a la consulta presentaba numerosas placas diseminadas por el tronco y las extremidades (Psoriasis Area and Severity Index [PASI] basal: 17,9), por lo que se decidió comenzar con ETN subcutáneo en dosis de 50mg 2 veces por semana. A los 3 meses se obtuvo una buena respuesta al tratamiento alcanzando un PASI de 1,8, descendiendo la dosis de ETN a 50mg por semana como terapia de mantenimiento. La paciente refería la aparición brusca de múltiples lesiones asintomáticas un mes después de comenzar el tratamiento con ETN, que no había presentado previamente. En la exploración física se observaban numerosas pápulas del color de la piel normal o ligeramente hiperpigmentadas de 2 a 5mm, localizadas en la región facial, el cuello, los miembros superiores y las piernas. Algunas lesiones presentaban una superficie queratósica, rugosa, y otras un aspecto filiforme (fig. 1).
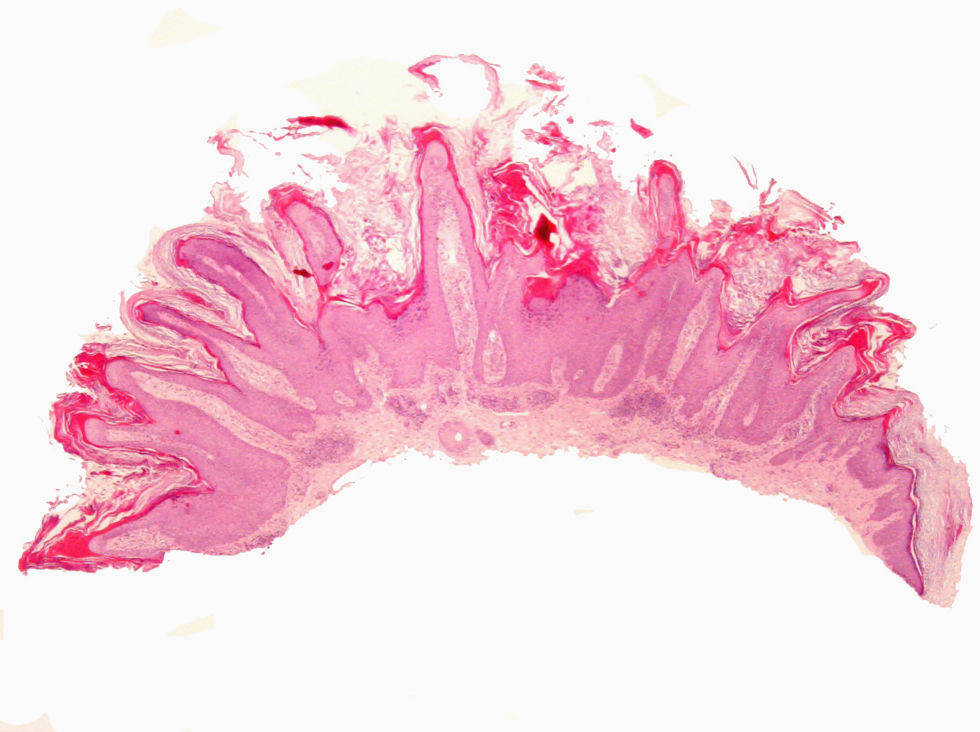
Se realizaron 4 biopsias de diferentes localizaciones en los miembros superiores e inferiores que mostraban una histología similar: marcada hiperqueratosis y acantosis, paraqueratosis sobre proyecciones papilomatosas, dilatación de los vasos en las papilas dérmicas y una típica incurvación de las crestas interpapilares en los extremos de las lesiones (fig. 2), hallazgos característicos de verrugas vulgares y filiformes. Las pruebas analíticas practicadas (hematología, bioquímica y analítica de orina) se encontraban dentro de la normalidad. Las serologías para el virus de la inmunodeficiencia humana (VIH), hepatitis B y C y la prueba de la tuberculina fueron negativas. La radiografía de tórax no mostraba alteraciones significativas.
Durante el tratamiento con ETN continuaron apareciendo nuevas lesiones verrugosas, siendo tratadas mediante electrocoagulación. Después del aclaramiento casi completo de las placas de psoriasis se suspendió el tratamiento con ETN, manteniéndose bajo control con terapia tópica. Durante los primeros meses sin tratamiento sistémico antipsoriásico aparecieron algunas verrugas, pero con menor frecuencia. Posteriormente estas dejaron de aparecer. No se observó otro acontecimiento adverso durante el tratamiento con ETN. La paciente no contaba con historia de verrugas virales previas al tratamiento con ETN, ni con antecedentes de infecciones frecuentes u otros síntomas de inmunosupresión.
Los ensayos clínicos y nuestra experiencia han mostrado que ETN es un fármaco seguro y bien tolerado en el tratamiento de la psoriasis, aunque debemos estar atentos a los posibles efectos adversos infrecuentes. No se ha comunicado un aumento de las tasas ajustadas de infecciones en los estudios aleatorizados, multicéntricos y controlados con placebo, aunque se han descrito casos de infecciones por bacterias, micobacterias, virus y hongos5. Existen escasas referencias que investiguen la relación de enfermedades virales durante el tratamiento con ETN6. Se han publicados algunos casos de tratamiento con ETN en pacientes con hepatitis C y VIH, sin observarse complicaciones7. No obstante, se considera recomendable, antes de empezar el tratamiento con ETN, determinar el estado serológico del paciente frente al VIH, hepatitis B y hepatitis C6–8.
La asociación entre ETN y el riesgo de infección por el virus de papiloma humano (VPH) es desconocida. No obstante, se ha estudiado que la proteína E6 del VPH-16 se une directamente al receptor 1 del factor de necrosis tumoral (TNF) y este induce la apoptosis de la célula huésped9,10. Por otra parte, ETN es una proteína de fusión que actúa inhibiendo la acción del TNF. Sin embargo, la asociación entre ETN y la aparición de verrugas solo se ha descrito excepcionalmente en la literatura. Se ha publicado la aparición de verrugas recalcitrantes en un paciente con artritis reumatoide juvenil, en tratamiento con metotrexato y ETN, que desaparecieron un mes después de suspender el tratamiento11. Posteriormente, se ha publicado el caso de un paciente con artritis psoriásica y psoriasis que presentó un nuevo brote de condilomas perianales durante la terapia con ETN12. Además, en el Registro Español de Acontecimientos Adversos de Terapias Biológicas en Enfermedades Reumáticas (Biobadaser), que incluye 9.352 pacientes, solo hay registrados dos casos de infección por el VPH13.
En nuestro caso la aparición brusca de verrugas virales en un paciente inmunocompetente, cronológicamente coincidiendo con el inicio del tratamiento con ETN, junto con su desaparición progresiva tras la suspensión del fármaco, sugiere una asociación entre el tratamiento con ETN y el desarrollo de las verrugas. Aunque la experiencia clínica muestra que esta relación es muy infrecuente, debemos estar atentos ante este riesgo potencial durante el tratamiento con ETN que, por otra parte, no exigió la suspensión del mismo.