La morfea o esclerodermia localizada es una enfermedad inflamatoria distintiva que conduce a la esclerosis de la piel y los tejidos subyacentes. Incluye una serie de entidades que pueden distinguirse basándose en las manifestaciones clínicas y la estructura de la piel y los tejidos subyacentes involucrados en el proceso fibroso. Sin embargo, la clasificación de estos procesos resulta difícil desde el momento en que los límites entre ellos no siempre son claros y es frecuente el solapamiento. En esencia, se distingue entre la morfea en placas, la esclerodermia lineal, la morfea generalizada y la panesclerótica. Si bien no tiene, salvo excepciones, una repercusión sistémica grave, sí que puede ser causa de una gran morbilidad. Si las lesiones asientan en el polo cefálico, pueden acompañarse de complicaciones neurológicas y oculares. No existe un tratamiento realmente eficaz y universal por lo que es importante realizar una evaluación correcta de la extensión y la gravedad de la enfermedad antes de tomar una decisión terapéutica.
Morphea or localized scleroderma is a distinctive inflammatory disease that leads to sclerosis of the skin and subcutaneous tissues. It comprises a number of subtypes differentiated according to their clinical presentation and the structure of the skin and underlying tissues involved in the fibrotic process. However, classification is difficult because the boundaries between the different types of morphea are blurred and different entities frequently overlap. The main subtypes are plaque morphea, linear scleroderma, generalized morphea, and pansclerotic morphea. With certain exceptions, the disorder does not have serious systemic repercussions, but it can cause considerable morbidity. In the case of lesions affecting the head, neurological and ocular complications may occur. There is no really effective and universal treatment so it is important to make a correct assessment of the extent and severity of the disease before deciding on a treatment approach.
El término «morfea» es sinónimo de «esclerodermia localizada» y ambos hacen referencia a una enfermedad inflamatoria distintiva que afecta de forma primaria a la piel y los tejidos subyacentes y que conduce finalmente a la esclerosis. Se diferencia de la esclerodermia sistémica por la ausencia de esclerodactilia, fenómeno de Raynaud, anomalías en los capilares del lecho ungueal y afectación de los órganos internos1. Es un proceso infrecuente con unas cifras de incidencia que oscilan entre los 0,34 y 2,7 casos/100.000 habitantes/año2,3. Es más frecuente en las mujeres de origen caucásico con un predominio respecto al varón de 2,4 a 4,2:13–6, y su prevalencia es similar en los niños y los adultos6.
ClasificaciónIncluye una serie de entidades que pueden distinguirse por las manifestaciones clínicas y la estructura de la piel y los tejidos subyacentes involucrados en el proceso fibroso. Sin embargo, la clasificación de estos procesos resulta difícil desde el momento en que los límites entre ellos no siempre son claros y es frecuente el solapamiento. Peterson et al.7 en 1995 tras realizar una revisión de la literatura médica propusieron una clasificación de la esclerodermia localizada que ha sido adaptada con leves modificaciones en la mayoría de los artículos de revisión posteriores8–14. En ella, los autores utilizan el término morfea de manera uniforme para cada uno de los tipos clínicos y hablan de morfea en placa, morfea generalizada, morfea ampollosa, morfea lineal y morfea profunda7. A su vez, en cada uno de estos grupos se distinguen diferentes subtipos (tabla 1). Por otro lado, los autores proponen incluir diversas entidades cuya relación con la esclerodermia localizada había sido apuntada con anterioridad pero que eran, y en algún caso continúan siendo, motivo de discusión como la atrofodermia de Pasini y Pierini y el liquen escleroso y atrófico en el grupo de las morfeas en placa, la hemiatrofia facial progresiva en el grupo de las morfeas lineales y la fascitis eosinofílica en el grupo de las morfeas profundas. Finalmente, introducen la idea de que esta clasificación no distingue entidades estancas de forma que las diferentes categorías no se excluyen unas de otras y, con frecuencia, los diferentes subtipos pueden observarse a la vez en un mismo paciente7.
Clasificación de la morfea o esclerodermia localizada
| Morfea en placa |
| Morfea en placa |
| Morfea guttata |
| Atrofodermia de Pasini y Pierini |
| Morfea queloidea (morfea nodular) |
| (Liquen escleroso y atrófico) |
| Morfea generalizada |
| Morfea ampollosa |
| Morfea lineal |
| Morfea lineal (esclerodermia lineal) |
| En coup de sabre |
| Hemiatrofia facial progresiva |
| Morfea profunda |
| Morfea profunda |
| Morfea subcutánea |
| Fascitis eosinofílica |
| Morfea panesclerótica de la infancia |
Tomada de Peterson et al.7
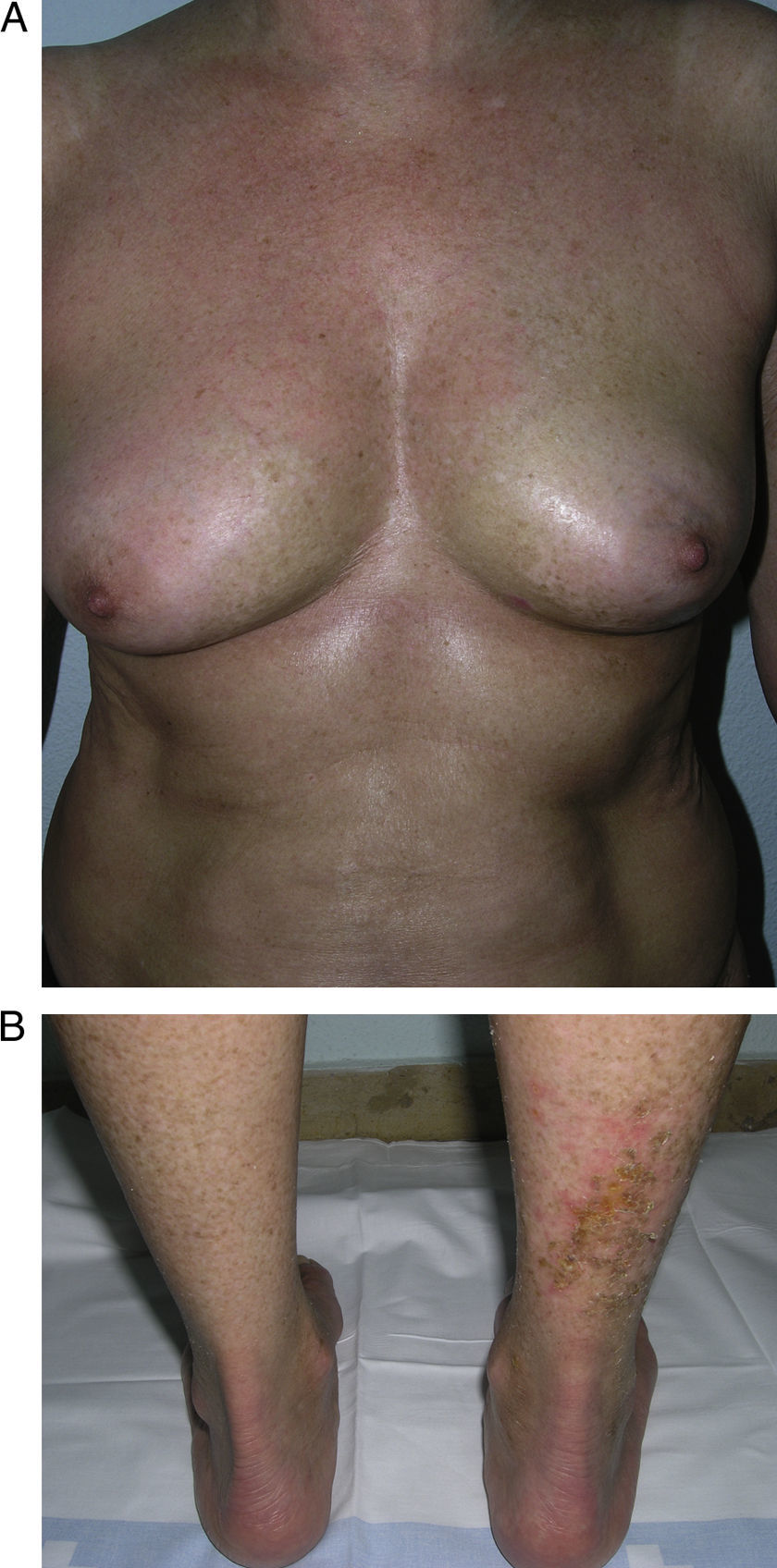
Un grupo de trabajo de la Sociedad Europea de Reumatología Pediátrica15 hace en 2004 una nueva propuesta de clasificación de la esclerodermia localizada juvenil con el fin de, según su criterio, corregir algunas deficiencias de la anterior propuesta por Peterson et al. Para ello, excluyen de nuevo de la clasificación condiciones como la atrofodermia de Pasini y Pierini, el liquen escleroso y atrófico y la fascitis eosinofílica, y proponen pequeñas modificaciones en el ordenamiento de los diferentes subtipos, que no varían en esencia de los de la anterior clasificación, a la vez que incluyen el concepto de morfea mixta para identificar aquellos pacientes que presentan una combinación de 2 o más tipos de lesiones (tabla 2). En un estudio del mismo grupo de trabajo publicado en 2006 que reúne un amplio número de niños con esclerodermia localizada, se subraya la necesidad de incluir el concepto de morfea mixta ya que hasta el 15% de los niños presentaron una combinación de lesiones distintas de morfea (fig. 1)5. Esta misma idea es trasladable a los adultos y, de hecho, la clasificación de Peterson et al. lleva implícito el reconocimiento de este subgrupo desde el momento en que aceptan la posibilidad de que un mismo paciente desarrolle a la vez diferentes subtipos de morfea7.
Clasificación de la morfea o esclerodermia localizada
| Morfea circunscrita |
| (a) Superficial |
| (b) Profunda |
| Esclerodermia lineal |
| (a) Tronco/extremidades |
| (b) Cabeza |
| Morfea generalizada |
| Morfea panesclerótica |
| Morfea mixta |
Tomada de la Conferencia Consenso de Padua (Italia), 200415.
La morfea en placas es la forma más superficial ya que con frecuencia el proceso fibroso se limita a la dermis, mientras que en la esclerodermia lineal la fibrosis afecta no solo a la dermis sino también al tejido adiposo, el músculo y, a menudo, el hueso. En la morfea profunda la fibrosis también afecta a la dermis profunda, el tejido adiposo y el músculo, pero a diferencia de la forma lineal, las lesiones son más difusas y no siguen un patrón lineal.
Si bien la esclerodermia localizada o morfea no tiene, salvo excepciones, una repercusión sistémica grave, sí que puede ser causa de una gran morbilidad ya que las lesiones, muchas veces localizadas en la cara y en las extremidades, pueden ser muy deformantes y ocasionar importantes limitaciones físicas. En general, cuanto más extensa y profunda es la afección del proceso escleroso, mayor es la probabilidad de detectar alguna anomalía visceral acompañante. Y esto es lo que puede ocurrir fundamentalmente en la esclerodermia lineal, la morfea generalizada y la morfea profunda. Las complicaciones sistémicas más frecuentes son las artralgias y, en el caso de que las lesiones asienten en el polo cefálico, las manifestaciones neurológicas y oculares. Los pacientes con morfea también tienen un mayor riesgo de enfermedad autoinmune entre sus familiares5,6.
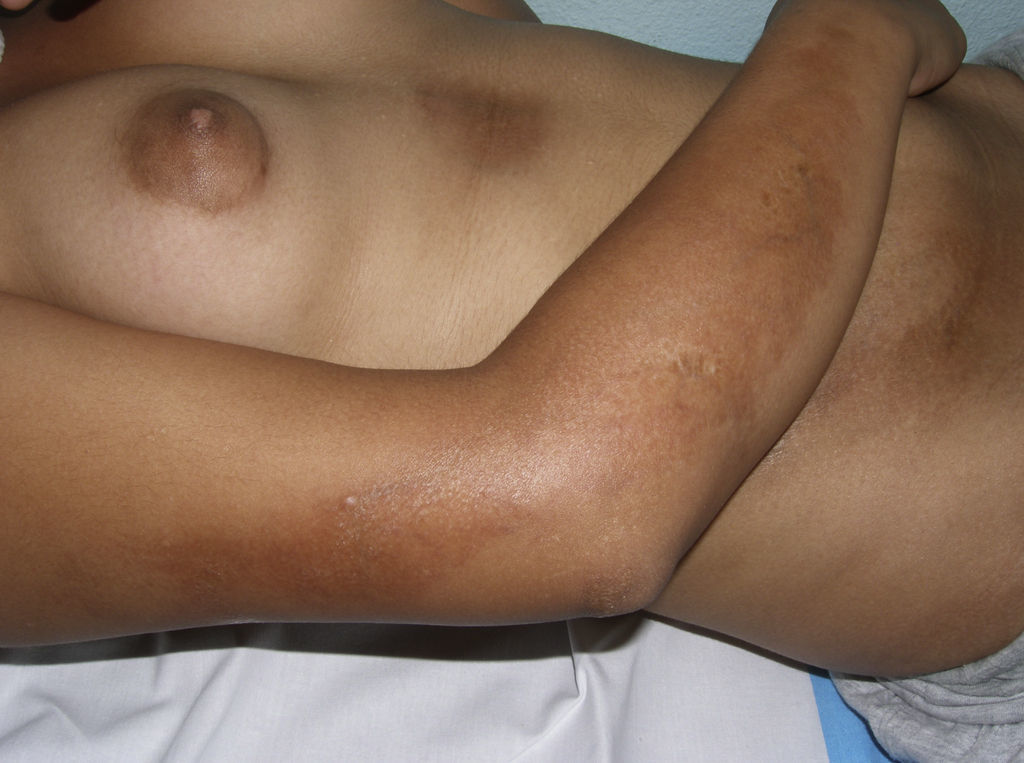
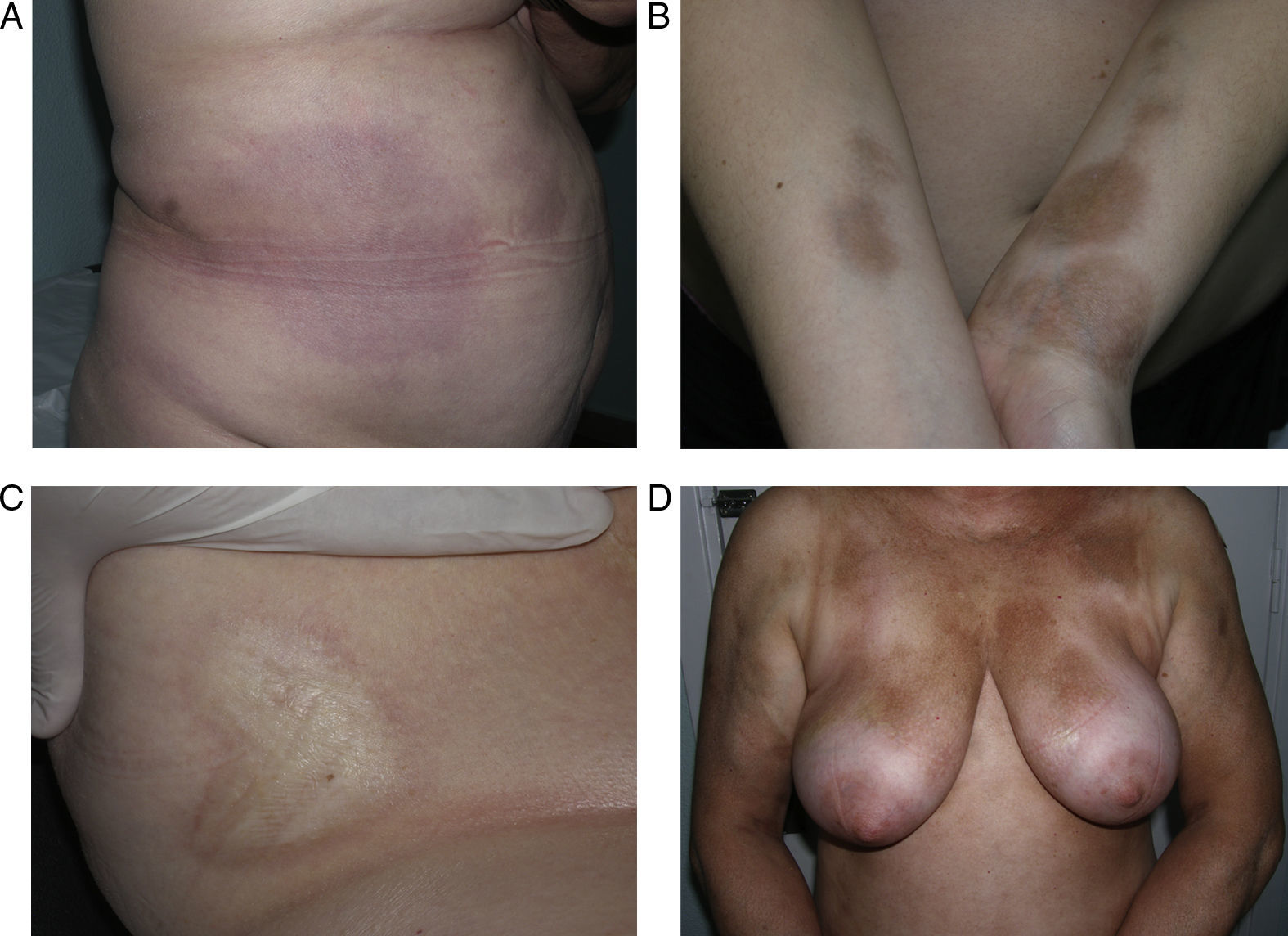
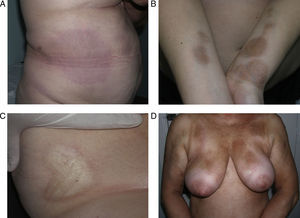
Variantes clínicasMorfea en placas (circunscrita)La morfea en placas constituye la variante más frecuente de esclerodermia localizada en los adultos3,4,6. El trastorno escleroso asienta preferentemente en la dermis reticular. Se manifiesta en forma de áreas bien circunscritas de piel endurecida y brillante, de silueta oval o redondeada, que asientan en uno o como máximo 2 territorios anatómicos, con más frecuencia en el tronco o las extremidades (fig. 2). En las fases más iniciales es posible observar un halo violáceo muy característico alrededor de la placa y que traduce la fase más inflamatoria de la morfea. Cuando las lesiones se instauran desde el inicio como placas levemente deprimidas de tonalidad marrón-grisácea se habla de atrofodermia de Pasini y Pierini. Con frecuencia las lesiones asientan en el tronco o la porción proximal de las extremidades9,13. La mayoría de los autores aceptan que este tipo de lesiones, en las que no hay endurecimiento de la piel, constituye una variante de morfea, ya sea como una forma abortiva de la misma9,16 o bien una variante aún más superficial en la que el trastorno escleroso asienta en la dermis papilar o superficial17. En este sentido, algunas evidencias apoyan su relación con la morfea. Por un lado, la coexistencia en el 20% de los casos de lesiones tipo atrofodermia de Pasini y Pierini y morfea en placas típicas16 y, por otro, la demostración microscópica, en los pacientes con morfea en placas, de que cuando la esclerosis se limita a las capas más superficiales de la dermis reticular, en la clínica esta esclerosis se traduce en placas más delgadas en las que predomina la pigmentación y el endurecimiento es mínimo18.
Diferentes aspectos clínicos de la morfea en placas: placa de coloración violácea indicativa de una lesión más inicial e inflamatoria (a); placas hiperpigmentadas con escaso endurecimiento de la piel en las fases más tardías (b); placa de color blanco marfileño, endurecida al tacto (c); múltiples placas hiperpigmentadas de bordes mal definidos en el tronco (d).
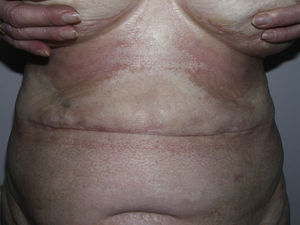
De forma muy inusual, sobre las placas de morfea pueden formarse ampollas o erosiones dando lugar a la llamada morfea ampollosa. Es curioso que en la mayoría de los casos descritos el sustrato anatomopatológico observado es de tipo liquen escleroso y atrófico (fig. 3)19, si bien en algunos otros se ha atribuido a la obstrucción linfática por el mismo proceso escleroso20 o la asociación a una enfermedad ampollosa autoinmune21.
Múltiples placas algunas de coloración blanco marfileño uniforme con clínica y microscopia de morfea y otras de aspecto moteado con clínica y microscopia tipo liquen escleroso y atrófico, coincidentes en una misma paciente. En algunas de las placas se observa la formación de pequeñas ampollas y costras.
La observación de cambios microscópicos tipo liquen escleroso y atrófico en casos de morfea ampollosa19, así como la coincidencia infrecuente pero bien documentada en un mismo paciente de placas de morfea clásica y liquen escleroso y atrófico22–25, conducen a plantear si esta última entidad debe considerarse una forma superficial de morfea en placa. Este es un tema también controvertido y para el que no existe aún una respuesta clarificadora. A pesar de la coexistencia, como acabamos de comentar, de lesiones de ambos tipos en algunos pacientes y la dificultad que, en algunas ocasiones, existe para distinguirlas desde el punto de vista clínico y microscópico, algunos estudios han querido demostrar diferencias en su microscopia óptica y ultraestructural24,26,27.
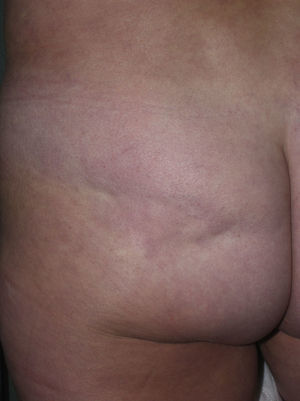
En ocasiones, el proceso escleroso que sigue circunscrito a una determinada área de piel no se limita a la dermis sino que puede afectar al tejido adiposo y otros tejidos subyacentes como la fascia o el músculo. Se habla entonces de morfea subcutánea o morfea profunda solitaria (este último término también se ha aplicado cuando las lesiones son más extensas y generalizadas; véase más adelante)28–31. En la clínica se manifiesta, muchas veces, a modo de una lesión única, con frecuencia localizada en la parte alta del tronco junto a la columna vertebral. La piel suprayacente puede tener un aspecto normal o bien ser atrófica o estar endurecida, pero casi siempre se mostrará deprimida y adherida a los planos profundos (fig. 4). De forma ocasional, se ha descrito el desarrollo de ampollas32. En general, es asintomática y no se asocia a alteraciones viscerales. Además de una densa esclerosis del colágeno y una marcada inflamación subcutánea con linfocitos y células plasmáticas como hallazgos microscópicos más llamativos de esta forma de morfea, se ha observado ocasionalmente la formación de hueso en la dermis profunda33,34. En algunos casos, la morfea profunda solitaria o lesiones similares se han descrito en relación con las vacunas35 o la inyección intramuscular de vitamina K36,37.
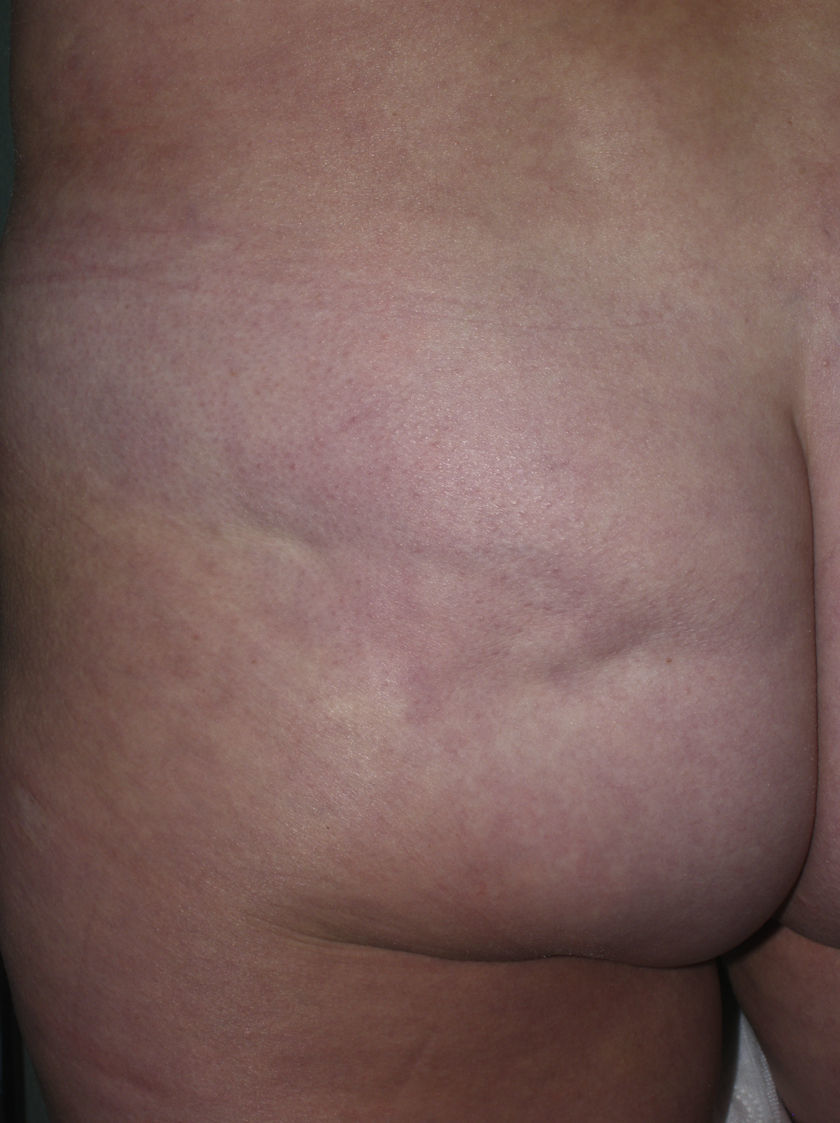
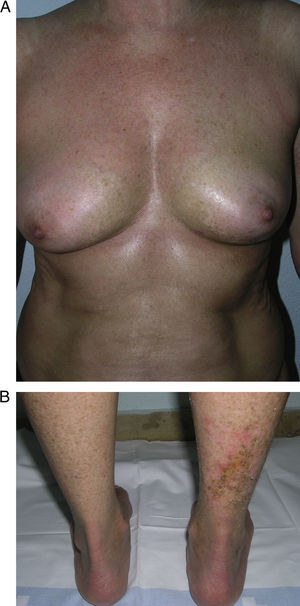
Morfea generalizada, morfea profunda y fascitis eosinofílicaCuando las placas de morfea afectan a más de 2 territorios anatómicos se habla de morfea generalizada7. Esta situación clínica se ha descrito con más frecuencia en las mujeres que en los varones y se ha invocado al ejercicio físico como posible factor desencadenante. En la clínica, aparecen placas suavemente inflamadas, pigmentadas, mal definidas, en unas zonas, con frecuencia en el tronco, mientras que en otras áreas, muchas veces en las extremidades, la piel se palpa engrosada y adherida a los planos profundos, la fascia y el músculo (fig. 5a). El inicio de la esclerosis suele ser gradual y relativamente rápido durante el periodo de unos meses. Los signos de inflamación aguda, como edema y eritema, suelen estar ausentes. Es posible, aunque infrecuente, la coexistencia con lesiones tipo liquen escleroso y atrófico y la formación de ampollas en la superficie de las placas (fig. 5 b)20,32.
Morfea generalizada: múltiples placas de piel endurecida, brillante, turgente, que confluyen hasta afectar a la práctica totalidad de la piel del tronco y las extremidades (a); erosiones y costras en las placas que afectan a la parte distal de la extremidad inferior (b). En 2 biopsias realizadas en esta paciente se observaron cambios de morfea en una de ellas y de liquen escleroso y atrófico en la otra.
Una revisión detallada de la literatura médica permite comprobar que los casos descritos con una clínica similar a la que acabamos de definir aparecen referenciados de manera indistinta como «morfea generalizada» y «morfea profunda»38–46. Ambos términos, por tanto, se han utilizado en la literatura para describir una misma situación clínica en la que el proceso escleroso afecta fundamentalmente a la dermis profunda y el tejido adiposo, pero también la fascia y el músculo superficial, de una manera extensa. El término «morfea generalizada» hace referencia a la vasta extensión que el trastorno fibroso puede alcanzar en esta entidad, mientras que el término «morfea profunda» pretende describir que los cambios microscópicos asientan fundamentalmente en el músculo superficial, la fascia, el tejido adiposo y la dermis más profunda.
La morfea generalizada debe distinguirse de la esclerodermia sistémica. A diferencia de esta, en la morfea generalizada, si bien los pacientes pueden desarrollar esclerosis de los dedos, no suelen presentar ulceraciones, reabsorción de las falanges, cambios en los capilares del pliegue ungueal o fenómeno de Raynaud. Por otro lado, la cara suele respetarse, ello quiere decir que aunque los cambios esclerosos de la piel pueden ser muy extensos en la morfea generalizada, el paciente no suele presentar los cambios típicos de la facies en la esclerodermia sistémica, como la desaparición de las arrugas de expresión, el adelgazamiento de los labios, los pliegues radiales alrededor de la boca, etc. Sí que, por el contrario, son frecuentes las contracturas en flexión de las articulaciones y las manifestaciones músculo-articulares39,46. De forma muy ocasional, se han documentado anomalías pulmonares, esofágicas o, incluso, renales o cardiacas4,6,46–48. Es usual detectar una eosinofilia periférica, que a veces puede ser muy importante, aumento de las gammaglobulinas o alteraciones inmunológicas como la presencia de ANA, anti-ADN de cadena simple, hipocomplementemia o, incluso, anticuerpos antifosfolípidos39,46,49,50. Los anticuerpos antihistona y la elevación en el suero del procolágeno tipo iii se han demostrado indicadores de enfermedad grave en la esclerodermia localizada por lo que no es infrecuente detectar dichas anomalías en el contexto de estas formas extensas y profundas de morfea51–54.
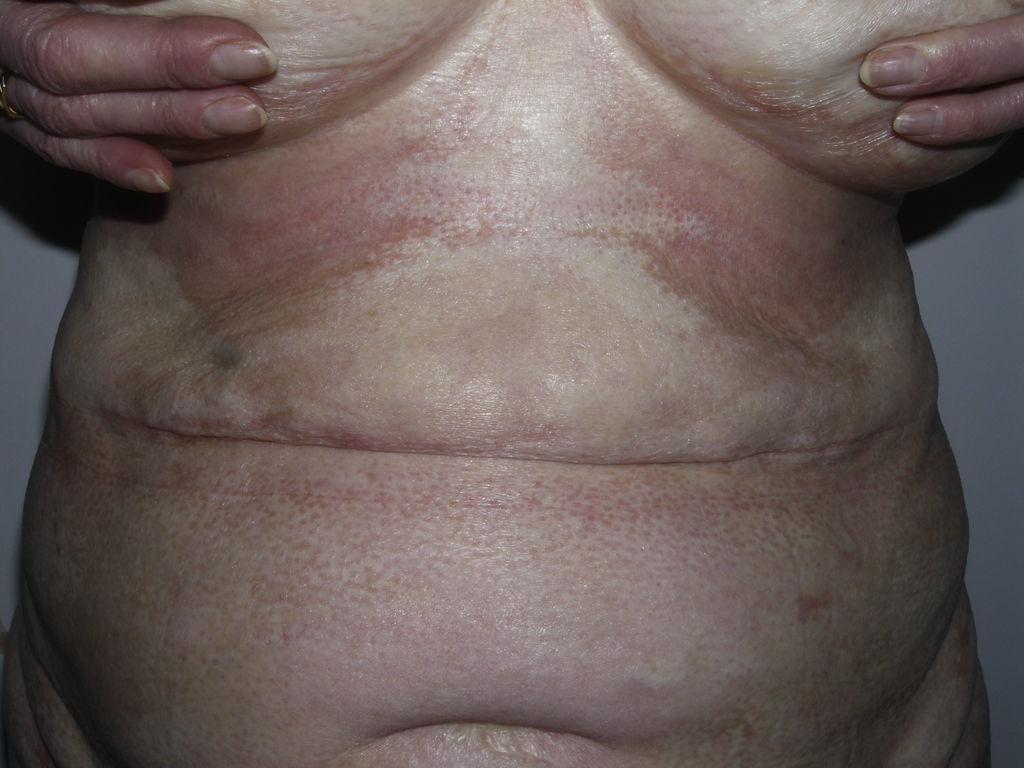
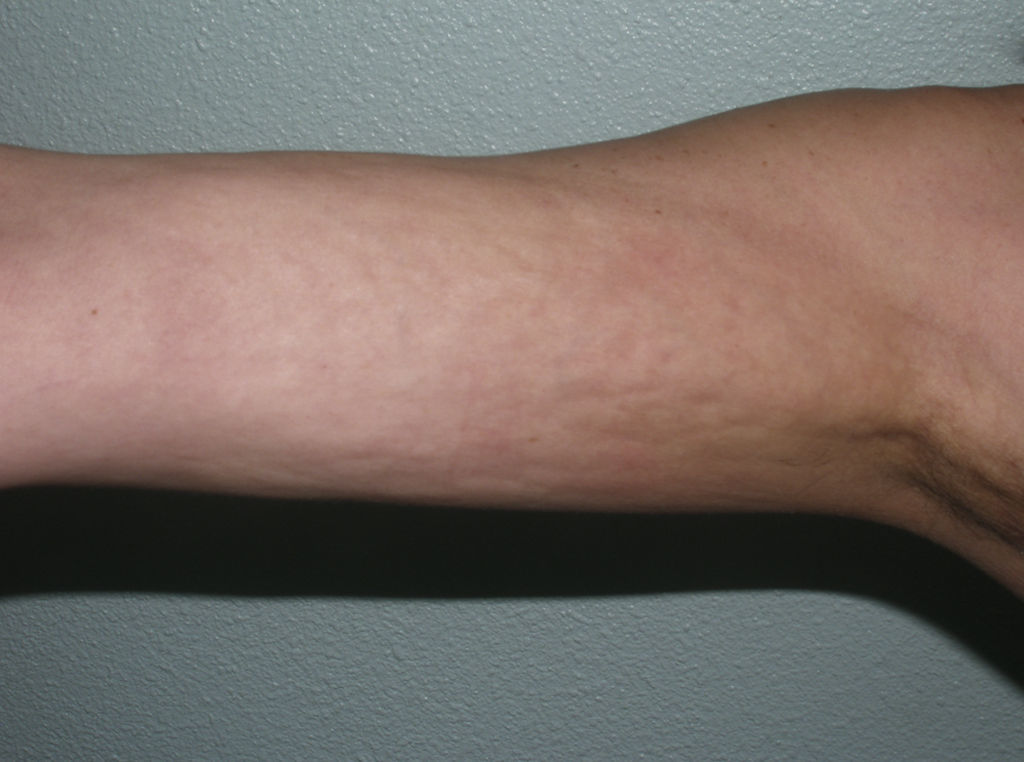
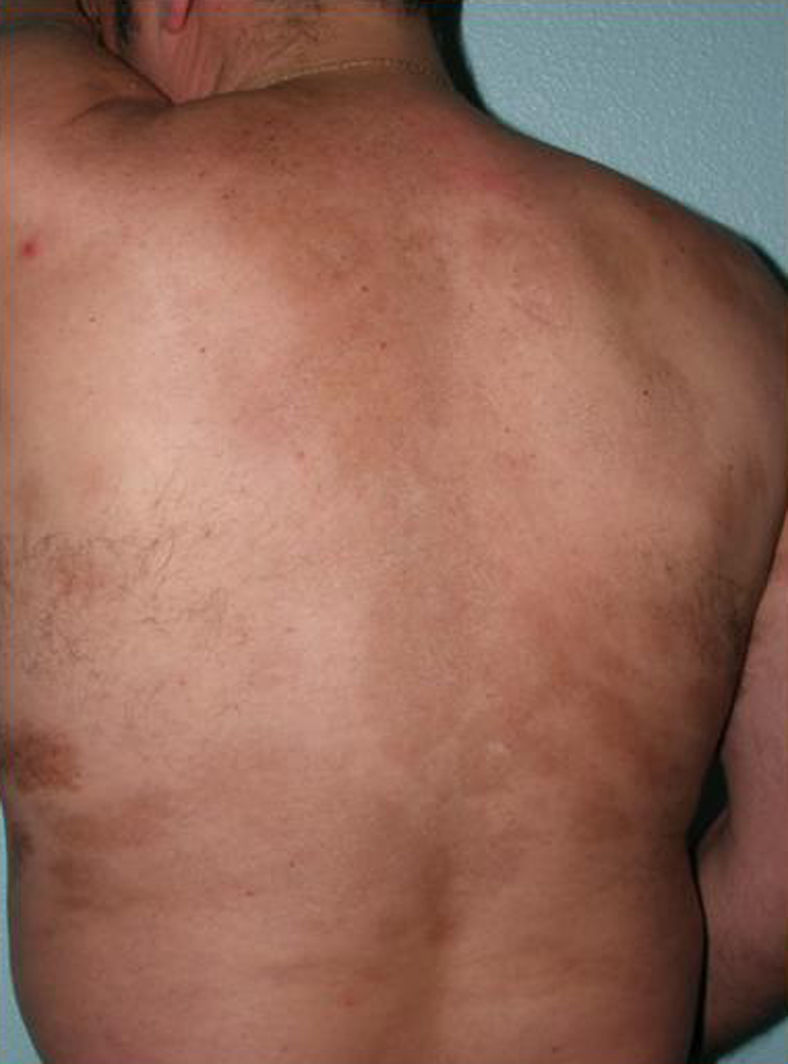
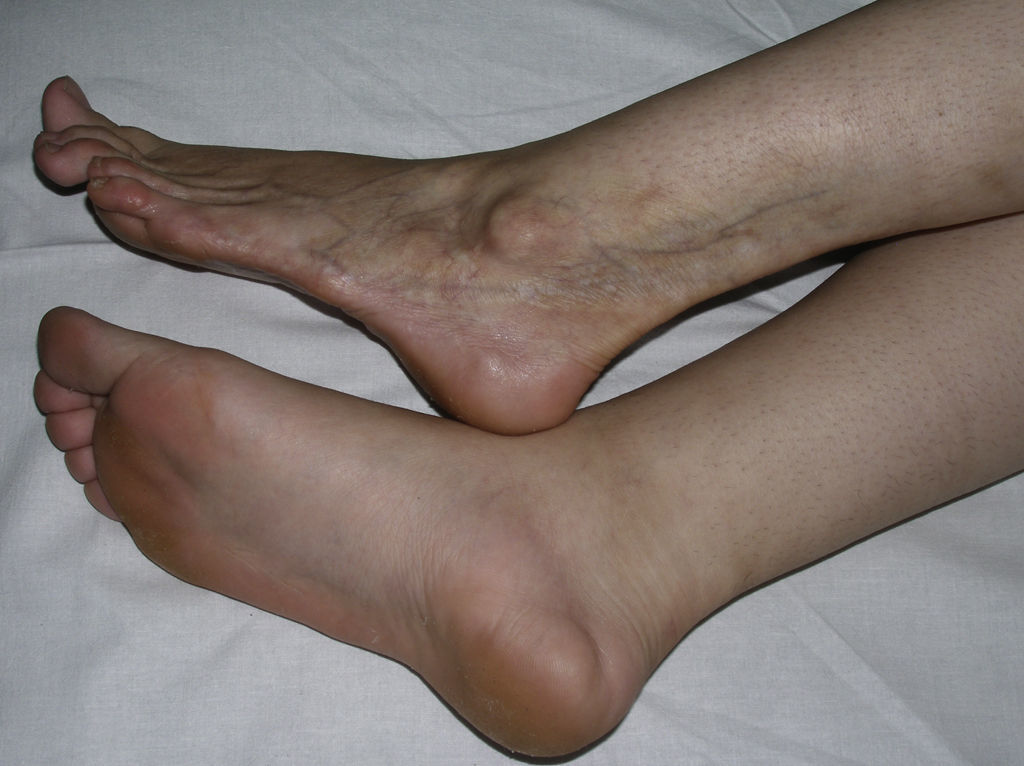
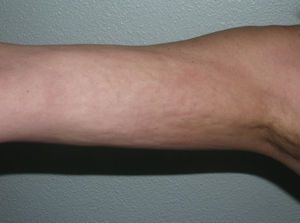
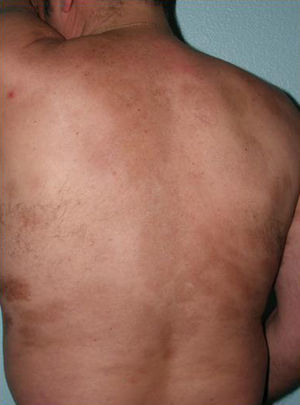
Toda esta clínica cutánea y sistémica que puede estar presente en la morfea generalizada solapa en gran medida con otra entidad, la fascitis eosinofílica, cuya inclusión dentro del grupo de las morfeas, en concreto dentro de las morfeas profundas según la clasificación de Peterson et al.7, ha sido y sigue siendo motivo de discusión en la literatura médica. Sin ir más lejos en algunos textos de Dermatología actuales y de gran prestigio, la fascitis eosinofílica se contempla como un síndrome esclerodermiforme55. Tampoco se contempla en la última clasificación propuesta por Zulian et al.5,15. En la clínica se caracteriza por el endurecimiento de la piel de las 4 extremidades de manera bilateral y simétrica. La mayoría de los pacientes inician el cuadro con una fase edematosa que se expresa con una sensación de tirantez en la piel y áreas de eritema tenue y difuso en las extremidades. Esta fase, que suele ser de corta duración y suele pasar desapercibida, es seguida de otra en la que la piel ya tersa y más dura muestra una superficie irregular y abollonada –esto resulta sobre todo evidente en la zona media de las extremidades superiores y cara interna de muslos– como consecuencia del desarrollo de unas bandas de esclerosis que atravesando de forma perpendicular el panículo adiposo unen focalmente la dermis más profunda con la fascia (fig. 6). En un estadio final la piel aparece completamente lisa, endurecida y adherida a los planos más profundos56–59. Lesiones típicas de morfea en placas se observan en otras áreas del cuerpo, fundamentalmente en el tronco, en un porcentaje significativo de los pacientes descritos con fascitis eosinofílica (30%) (fig. 7)59–62. En general, estas lesiones no son sincrónicas a la fascitis y pueden aparecer antes o después de la inflamación de la fascia. Es característica la presencia en sangre periférica de anomalías como eosinofilia, hipergammaglobulinemia y aumento de la velocidad de sedimentación globular. Sin embargo, su ausencia no descarta el diagnóstico ya que estas alteraciones suelen ser transitorias59. De forma similar, aunque la presencia de inflamación microscópica rica en eosinófilos de la fascia es característica, no es un requisito para el diagnóstico63. Finalmente, las manifestaciones extracutáneas más frecuentes son la sinovitis o tenosinovitis, la artritis, las contracturas o el síndrome del túnel carpiano. Las complicaciones viscerales en el pulmón, el esófago o el corazón, aunque descritas, son muy poco frecuentes. Quizá destacan las anomalías hematológicas que se han descrito en estos pacientes que además de la eosinofilia, pueden desarrollar aplasia megacariocítica64, anemia aplásica65–67, trombocitopenia, anemia hemolítica68 y trastornos mielo y linfoproliferativos69,70.
La mayor parte de la bibliografía en la que se recogen las características clínicas y microscópicas de la fascitis eosinofílica está descrita por reumatólogos que son los que utilizan fundamentalmente este término. Sin embargo, a tenor de sus descripciones vemos que comparte muchos de los rasgos clínicos tanto cutáneos como extracutáneos de la entidad que fundamentalmente se recoge en la literatura dermatológica como morfea generalizada o profunda. Es probable que todos estos términos (morfea generalizada, morfea profunda y fascitis eosinofílica) hagan referencia, en realidad, a una misma situación clínica. Sin embargo, la existencia de pacientes «tipo» o «puros» de cada una de estas situaciones clínicas justifica probablemente la conservación de la terminología.
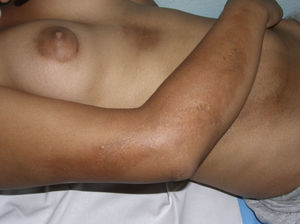
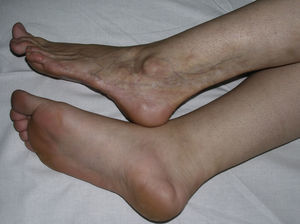
Morfea linealLa morfea o esclerodermia lineal con frecuencia se observa en la infancia o la juventud y se trata probablemente de la variante de morfea más común en este grupo de la población, afectando entre el 40 y el 70% de los niños estudiados5,6,48. En general, es una lesión única, unilateral y de distribución lineal, que con frecuencia asienta en las extremidades, la cara o el cuero cabelludo (fig. 8). Muchas veces, estas lesiones lineales siguen las líneas de Blaschko, por lo que se ha propuesto que un posible mosaicismo genético sea el factor determinante de la distribución lineal del proceso escleroso71. A menudo, son lesiones profundas que interfieren en el crecimiento de la extremidad y ocasionan deformidades por la atrofia del músculo y el hueso subyacente, así como contracturas articulares. En superficie aparecen como bandas de piel deprimida, mal delimitadas, con trastornos de la pigmentación.
Cuando se localizan en el cuero cabelludo originan una placa alopécica de disposición lineal, muchas veces atrófica y ligeramente deprimida, de piel lisa, brillante, marfileña, endurecida y a veces pigmentada. El carácter unilateral de estas lesiones, su preferencia por la región parietal y la tendencia a deformar el hueso dando lugar a lesiones deprimidas, ha propiciado denominaciones tan descriptivas como la de esclerodermia en coup de sabre. A veces, pueden extenderse o afectar de forma exclusiva a la mejilla, la nariz o el labio superior. En esta localización, a menudo, solo se observa en la superficie de la piel una leve pigmentación lineal, pero en profundidad puede ser responsable de deformidades del macizo facial, asimetrías y alteraciones en la implantación de los dientes.
Cuando el trastorno escleroso afecta a la mitad completa de la cara se denomina hemiatrofia facial progresiva o síndrome de Parry-Romberg. Se ha discutido mucho su relación con la esclerodermia localizada, pero la coexistencia de este cuadro con lesiones de esclerodermia lineal en forma de coup de sabre o, incluso, de morfea en placas, permite afirmar que se trata de una variante de esclerodermia lineal72–74. El proceso afecta sobre todo al tejido adiposo e, incluso, al músculo y el hueso, lo que en la sintomatología se traduce por la práctica ausencia de cambios en la piel, pero sí una evidente atrofia de la grasa y el músculo, junto a deformidades del macizo facial. Ello favorece la aparición de alteraciones oculares como endoftalmos, parálisis de la musculatura ocular, ptosis o síndrome de Horner, y deformaciones de la mandíbula con la consecuente mala oclusión dental, implantación inadecuada de los dientes, atrofia de las raíces o retraso en la aparición de los dientes74.
En la esclerodermia lineal, sobre todo cuando las lesiones asientan en el polo cefálico (tipo coup de sabre y/o hemiatrofia facial progresiva), se ha destacado la frecuencia con que subyacen las complicaciones neurológicas, casi el 20%5,73,74, y las oftalmológicas (15%)75. Entre las anomalías neurológicas sobresalen la epilepsia, la migraña, la neuralgia y/o parestesias de diversos pares craneales y las anomalías electroencefalográficas y en diversas pruebas de imagen. Entre las oftalmológicas predomina la esclerosis de las estructuras anexiales, seguida de la inflamación del segmento anterior y la uveítis anterior; estas 2 últimas complicaciones son, en muchas ocasiones, asintomáticas y unilaterales75. También se ha demostrado un mayor riesgo de asociación de otras complicaciones extracutáneas, sobre todo las neurológicas, cuando están presentes las lesiones oculares75.
Morfea panesclerótica de la infanciaEs una variante muy inusual de morfea profunda a la vez que muy agresiva y mutilante76. De forma característica se desarrolla en la infancia aunque se ha descrito su inicio en la vida adulta77. La sintomatología es similar a la de la morfea generalizada, pero en la que existiría una mayor y más extensa afectación no solo de todas las capas de la piel y el tejido celular subcutáneo sino también de las estructuras más profundas como el músculo, el tendón y el hueso. Es típico que las placas de esclerosis se originen en la superficie de extensión de las extremidades y el tronco, para de forma progresiva afectar a la completa totalidad de la piel, incluyendo la cara, el cuello y el cuero cabelludo. Se respeta la punta de los dedos de las manos y los pies y no hay fenómeno de Raynaud76–78. Como resultado de la afectación esclerótica de toda la piel y los tejidos subyacentes, se desarrollan importantes contracturas articulares, deformidades, ulceraciones muy dolorosas y calcificaciones. De forma ocasional, se ha descrito la aparición de carcinomas escamosos sobre las placas panescleróticas de larga evolución79,80. Las complicaciones sistémicas y las anomalías en los análisis observadas en esta entidad son superponibles a las que ya se han descrito en el resto de procesos relacionados (eosinofilia, hipergammaglobulinemia, aumento de la velocidad de sedimentación globular, presencia de ANA, anomalías en las pruebas de funcionalismo pulmonar, alteraciones esofágicas, etc.).
TratamientoDesde el momento en que no existe un tratamiento realmente eficaz y universal para la esclerodermia localizada, este debe plantearse en función de la extensión y la gravedad de la enfermedad, que viene determinada fundamentalmente por el riesgo de deformaciones y limitación de la movilidad81. El tratamiento resulta ineficaz para revertir tales complicaciones, por lo que este debería iniciarse antes de que aparezcan. Sin embargo, en muchas ocasiones resulta difícil decidir en qué casos y en qué momento debe iniciarse una terapia sistémica, ya que no es fácil reconocer en la clínica cuándo las lesiones están activas y van a progresar o si el proceso está estable y el daño ya hecho se verá modificado por el tratamiento. Por otro lado, también es difícil definir y evaluar la mejoría de las lesiones ya sea en la evolución natural de la enfermedad o tras iniciar un determinado tratamiento. Existen numerosos aparatos más o menos sofisticados que intentan medir de una manera objetiva la evolución de la morfea (cutometer, durometer, ultrasonidos, termografía, imágenes computadorizadas, etc.), pero ninguno de ellos ha sido aceptado de forma universal. Además, tampoco existe un sistema de puntuación capaz de medir la actividad y el daño de la enfermedad que haya sido validado de forma definitiva. En este sentido, el recientemente publicado LoSCAT (del inglés Localized Scleroderma Cutaneous Assessment Tool) puede constituir una herramienta de medida prometedora ya que parece que es capaz de diferenciar entre actividad y daño, es sensible a los cambios y no requiere un equipamiento complementario82. Consiste en la cuantificación del daño cutáneo y extracutáneo en un paciente con esclerodermia localizada mediante la evaluación de una serie de síntomas y signos clínicos de actividad (endurecimiento de la piel, eritema) y daño (atrofia y trastorno de la pigmentación), así como diversos parámetros de laboratorio. Es evidente que disponer de un sistema de medida útil resulta imprescindible para poner en marcha estudios multicéntricos y realizar metanálisis, por otro lado, necesarios en el estudio de enfermedades que como la morfea son infrecuentes.
De todo ello se desprende que no se dispone hoy por hoy de estudios aleatorizados y a doble ciego que demuestren la eficacia real de la mayor parte de los fármacos propuestos en el tratamiento de la morfea. Si atendemos al tratamiento sistémico, se ha demostrado mediante sendos estudios aleatorizados con placebo que ni el interferón γ intralesional83 ni el calcitriol oral84 constituyen alternativas eficaces en el tratamiento de la morfea.
Los fármacos más aceptados como útiles en el tratamiento de esta enfermedad son el metotrexato y los glucocorticoides sistémicos, casi siempre administrados en combinación. Respaldan esta afirmación varios estudios prospectivos85–87 y retrospectivos88–91, aunque ninguno de ellos es aleatorizado y a doble ciego con placebo. Estos estudios incluyen tanto adultos como niños y las dosis de metotrexato administrado oscilan entre 0,3 y 0,4mg/kg por semana en los niños, y entre 15 y 25mg por semana en los adultos. Se prefiere la administración de los glucocorticoides en forma bolus de altas dosis de metilprednisolona por vía intravenosa seguidos o no de prednisona oral en pauta descendente. Existe el acuerdo general de que la administración de altas dosis de glucocorticoides en forma de bolus proporciona el efecto antiinflamatorio e inmunomodulador deseado con un menor riesgo de los efectos secundarios que pueden aparecer cuando los glucocorticoides se administran durante un tiempo prolongado. En los adultos la pauta de bolus más empleada es la de 1 g de metilprednisolona al día, durante 3 días consecutivos al mes, hasta un máximo de 6 meses, y, en los niños, 30mg/kg/día, máximo 500mg/día, de metilprednisolona por vía intravenosa durante 3 días consecutivos, en 2 o máximo 3 bolus de administración semanal o mensual86,87. En la mayoría de estos estudios, la mejoría que se describe en más del 80% de los casos se documenta mediante la impresión clínica del médico que pauta el tratamiento. En solo 2 de los estudios prospectivos realizados en adultos se demuestra una mejoría significativa tras el tratamiento basada en el sistema de puntuación no validado Modified Skin Score (MSS) y en las medidas tomadas mediante ultrasonografía de la piel esclerosada85,86. La naturaleza retrospectiva y no controlada de los estudios no permite conocer si los resultados en los pacientes tratados con metotrexato y glucocorticoides fueron similares a los de aquellos tratados únicamente con metotrexato. Los glucocorticoides por vía oral como único fármaco, en dosis entre 0,5 y 1mg/kg/día, se han demostrado asimismo eficaces en algún estudio aislado pero el riesgo de recaída tras dejar el tratamiento es probablemente mayor92.
La radiación ultravioleta en sus diferentes modalidades constituye también una opción que se debe considerar entre el arsenal terapéutico disponible en el tratamiento de la morfea. Incluye la luz ultravioleta A (UVA) de banda ancha asociada o no a psoraleno en baño, crema u oral, el UVA1 y el ultravioleta B (UVB) de banda estrecha. El mecanismo por el que la fototerapia puede resultar eficaz en la morfea es desconocido. La mayor parte de los estudios que analizan este aspecto se centran en el UVA1. El UVA1 es capaz de ocasionar la apoptosis de las células de Langerhans y los linfocitos T, a la vez que disminuye la síntesis de colágeno, aumenta la producción de colagenasas y altera la concentración local de citocinas que como la IL-6, el factor transformador del crecimiento beta (transforming growth factor-beta, TGFβ) y el interferón γ, influyen en la producción del colágeno y los glicosaminoglicanos, el crecimiento de los fibroblastos y la cantidad de metaloproteinasas de la matriz93,94.
La mayor experiencia y eficacia se ha obtenido con el uso de UVA1. Desde que en 1995 Kerscher et al.95 introdujeran esta modalidad de fototerapia en la morfea, varios estudios prospectivos han permitido evaluar la eficacia de este tratamiento en más de un centenar de pacientes96–102. En el 90% de los pacientes se describe una mejoría documentada mediante el examen clínico, un sistema de puntuación cutáneo, ultrasonografía, biopsia, cutometer o una combinación de estos sistemas de medida. En opinión de algunos autores, la terapia UVA1 resulta especialmente beneficiosa en la fase más tardía y fibrótica de la morfea. Sin embargo, será poco útil en aquellos pacientes con formas de la enfermedad especialmente agresivas con afectación del tejido subcutáneo y el músculo y rápidas en su evolución81,86,103. Las principales dificultades en el uso estandarizado del UVA1 radican en que, por un lado, su administración precisa de un aparataje especial no disponible en la mayoría de los centros de fototerapia, a la vez que el tiempo de exposición necesario es prolongado (entre 30 y 60 min, 3 veces por semana). Por otro lado, no se han establecido de forma clara las pautas de tratamiento más eficaces. Probablemente, las dosis altas de UVA1 (130 J/cm2 por sesión con una dosis total de 3.900 J/cm2) resultan más eficaces que las dosis medias (70 J/cm2 por sesión con una dosis total de 2.100 J/cm2) o las bajas (20 J/cm2 por sesión con una dosis total de 600 J/cm2), aunque la mayoría de los pacientes han sido tratados con estas últimas82. Finalmente, no se ha demostrado que esta modalidad de fototerapia resulte igualmente eficaz en pacientes con fototipo alto (fototipo iv o más alto), ya que la mayoría de los estudios se han llevado a cabo en países donde la mayor parte de la población tiene la piel clara (fototipos i a iii). Aún más, Wang et al.104 demostraron mediante diversas observaciones experimentales que tras la administración de altas dosis de UVA1, la disminución de los colágenos 1 y 3 y el incremento de las metaloproteinasas de la matriz fueron superiores en los pacientes con fototipo más claro. Asimismo, la producción de los colágenos 1 y 3 que se consiguió reducir fue mayor tras un tratamiento de altas dosis de UVA1 que en aquellos pacientes que ya habían recibido 3 sesiones previas de altas dosis de UVA1 antes de realizar las determinaciones. Estos hallazgos sugieren que el UVA1 debería administrarse bien en forma de pulsos (una dosis única y alta separada por semanas de la siguiente sesión) o bien en dosis bajas con el fin de prevenir el bronceado e incrementar así su eficacia.
La experiencia acumulada con otras formas de fototerapia, en especial con UVA de banda ancha asociado o no a psoralenos, ha sido mucho menor, aunque algunos estudios prospectivos han descrito mejorías clínicas con o sin mediciones con ultrasonografías o biopsias, en alrededor del 80% de los pacientes tratados105–107. Los autores de algunos de estos estudios señalan que el tratamiento con psoraleno-UVA (PUVA) tópico, ya sea mediante baños o crema, puede resultar especialmente útil en la fase inflamatoria más inicial de la morfea81. Mucho más limitada es la experiencia con el uso de UVB de banda estrecha, cuya eficacia referida solo en casos aislados, está aún por demostrar en estudios controlados o en series de pacientes más largas108.
A partir de su utilización en la esclerodermia sistémica, se han propuesto otros inmunosupresores en el tratamiento de la morfea, cuyo beneficio se ha descrito únicamente en casos aislados. Este es el caso de la d-penicilamina, fármaco poco recomendable por su pobre perfil de seguridad, la ciclosporina, utilizada en 2 niños afectados de una morfea lineal109, y la fotoféresis extracorpórea, en algún caso combinada con micofenolato mofetilo110,111. Este último inmunosupresor que, en general, es bien tolerado, se ha observado eficaz en el tratamiento de niños con morfea que no habían respondido previamente a la combinación de glucocorticoides y metotrexato112. El estudio es retrospectivo y recoge un total de 10 niños con diversas formas graves de esclerodermia localizada (morfea panesclerótica, morfea generalizada y morfea lineal), describiéndose en todos ellos una mejoría clínica que permitió suspender o reducir las dosis de glucocorticoides y metotrexato. Recientemente, se ha demostrado la eficacia de micofenolato mofetilo en reblandecer la piel en un estudio prospectivo realizado en pacientes afectados de una esclerodermia sistémica difusa113. Así pues, teniendo en cuenta el buen perfil de seguridad de este fármaco, es una buena alternativa de tratamiento en caso de fracaso con las opciones más clásicas antes comentadas.
También se ha descrito en sendos casos de morfea generalizada una mejoría significativa con infliximab, un anti-TNF114, e imatinib, un inhibidor de la actividad tirosina cinasa115.
Respecto al tratamiento tópico, que debe limitarse a las formas más superficiales y limitadas de morfea como la morfea en placas, se dispone de varias opciones. Es clásico recomendar la aplicación tópica de corticoides, en especial de alta potencia, en las placas de morfea, sobre todo si se encuentran en la fase inicial más inflamatoria. Sin embargo, no existe ningún estudio que haya demostrado la eficacia real de este tratamiento82. En un único estudio piloto, aleatorizado con placebo y a doble ciego, realizado en 10 pacientes con morfea en placa, se demostró la eficacia de tacrolimus en este proceso116. La aplicación de imiquimod, 3 veces por semana, se ha demostrado eficaz en reducir el eritema y el endurecimiento de las placas de morfea en 12 pacientes que de manera prospectiva se incluyeron en un único estudio117. Más tarde, se han descrito 2 casos aislados que mejoraron las placas de morfea tras la aplicación de imiquimod, 5 veces por semana, durante 16 semanas118. Calcipotriol en combinación con betametasona también se ha demostrado eficaz en un estudio prospectivo en el que se incluyeron 6 pacientes con morfea en placas119. Finalmente, se ha demostrado la total ineficacia de la terapia fotodinámica en el tratamiento de la morfea120.
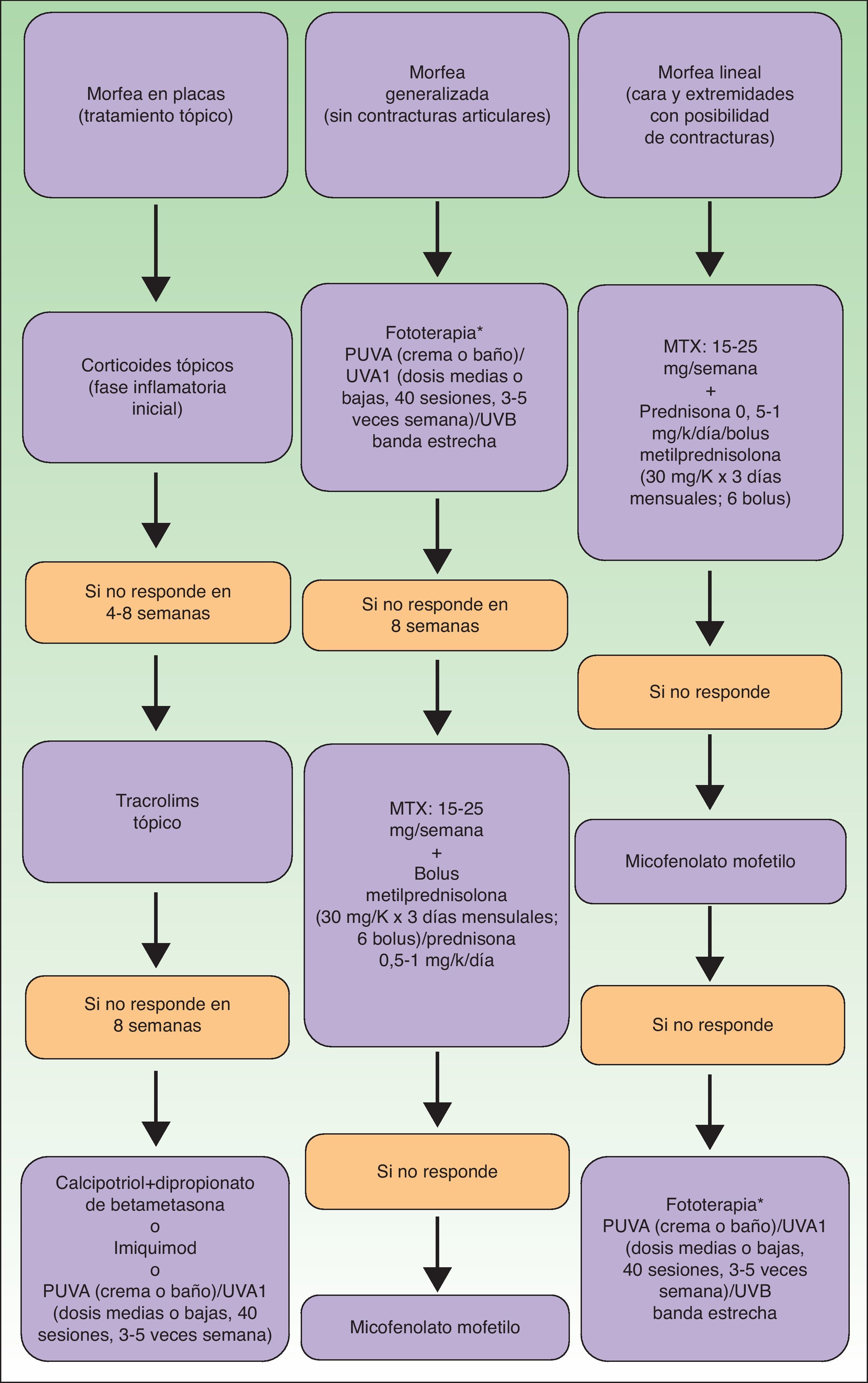
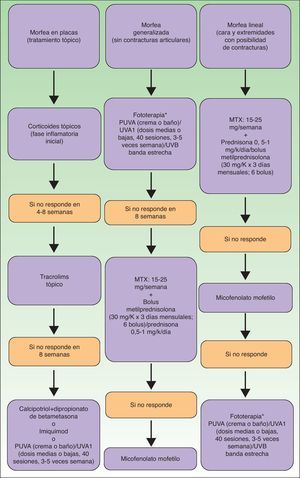
A modo de resumen se propone en la figura 9 un algoritmo terapéutico de la esclerodermia localizada, inspirado en la experiencia personal y la de otros autores81 y en las últimas revisiones al respecto82.
Algoritmo terapéutico de la esclerodermia localizada81,82.
*Según disponibilidad.
La fisioterapia puede tener interés recomendarla en aquellos pacientes que como consecuencia de la morfea sufren limitaciones en la movilidad de las extremidades y contracturas articulares, aunque tampoco existen estudios que demuestren su utilidad real. En cualquier caso, parece que no exacerba la enfermedad y que, por tanto, puede indicarse82.
Sea cual sea el régimen terapéutico que se instaure parece que la morfea, cualquiera que sea su tipo, tiene tendencia a progresar y recurrir, en especial, cuando su inicio tiene lugar durante la infancia121. Es por ello que no resulta extraño que un mismo paciente precise recibir, a lo largo de su vida, diversas tandas de tratamiento ante los nuevos brotes de actividad de la enfermedad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.