Presentamos 2 casos de tumores neuroendocrinos citoqueratina 20 negativos distintos del carcinoma de células de Merkel con afectación cutánea.
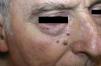
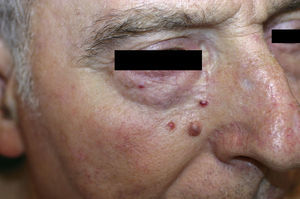
Caso 1: Varón de 72 años con 3 lesiones papuloeritematosas asintomáticas, de 2-3mm en la región paranasal derecha de 20 días de evolución (fig. 1). Se extirpó una observándose un tumor epitelial de patrón difuso constituido por nidos sólidos de células poligonales, irregulares y atípicas, con abundantes figuras de mitosis, sin rasgos de diferenciación morfológica, que no establecían conexión con la epidermis. Estaba constituido por células queratinas AE1-AE3, sinaptofisina, cromogranina y enolasa neuronal específica positivas, negativas para citoqueratina 20, TTF1, CD30, S100 y HMB45 (fig. 2). El diagnóstico fue de carcinoma intradérmico con diferenciación neuroendocrina. Se encontraron niveles plasmáticos elevados de cromogranina A (124,2 ng/ml) (valores normales: 19,4-98,1), siendo el resto de determinaciones hormonales en sangre y orina normales. La radiografía de tórax, la resonancia magnética abdominal, la gammagrafía con octreótido marcado con 111In y la PET fueron normales. En la gastroscopia no había hallazgos significativos y en la colonoscopia un pólipo adenomatoso. Se realizó una extirpación simple de las 3 lesiones sin otro tratamiento adyuvante, y los niveles de cromogranina A se normalizaron.
A. Tumor constituido por nidos de células poligonales (hematoxilina-eosina [H-E] × 5). B. Estas células eran irregulares y atípicas y no establecían conexión con la epidermis (H-E × 20). C. Se aprecian abundantes figuras de mitosis (H-E × 40). D. Estas células eran sinaptofisina positivas (H-E × 40).
El paciente permanece asintomático tras 5 años de seguimiento.
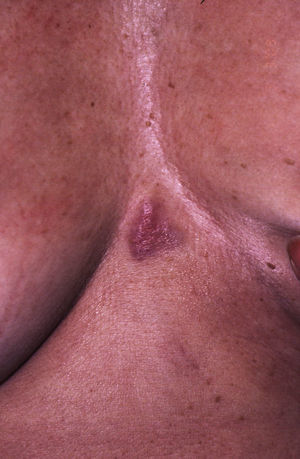
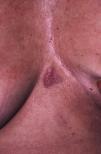
Caso 2: Mujer de 62 años con una lesión preesternal de 2 años de evolución, de crecimiento progresivo. En la exploración presentaba una placa eritematoviolácea, de 3×2cm (fig. 3). Se realizó una biopsia encontrando en la dermis una tumoración en forma de nidos dispersos de células de apariencia epitelial, monomorfas y escasamente atípicas, de citoplasma mal definido con microcalcificaciones ocasionales y muy escasa actividad mitótica. Estas células eran positivas para queratinas AE1-AE3 y citoqueratina 8, sinaptofisina, cromogranina y enolasa neuronal específica, siendo S100, MELAN-A, HMB45 y citoqueratina 20 negativas. El diagnóstico histológico fue de metástasis cutánea de neoplasia neuroendocrina bien diferenciada. Se encontró una cifra elevada de somatostatina en sangre (27,3pmol/l) (valores normales: hasta 16), siendo el resto de determinaciones hormonales en plasma y orina normales. Ante el diagnóstico de metástasis cutánea de un tumor neuroendocrino productor de somatostatina se realizó una gammagrafía con octreótido, encontrando captación en la región preesternal y en la axilar izquierda. En el resto de pruebas de imagen únicamente se observó litiasis biliar y una lesión hepática sugestiva de hemangioma.
La placa preesternal fue extirpada practicándose también una linfadenectomía parcial axilar izquierda, sin objetivarse infiltración tumoral en los 10 ganglios linfáticos extirpados. Tras esta intervención la cifra de somatostatina se redujo a 19,9pmol/l (hasta 16) pero sin normalizarse. En la nueva gammagrafía con octreótido realizada después continuaba observándose un foco de captación en el cuadrante superoexterno de la mama izquierda —cola de la mama—. Se solicitó una resonancia magnética, un escáner y una ecografía mamaria para filiar esa lesión, siendo interpretada como un ganglio intramamario de 9mm. Revisando la historia encontramos una mamografía realizada 16 años antes con una lesión de 4mm en la misma localización diagnosticada de adenopatía benigna.
Previa localización radiológica se extirpó esta lesión demostrando una infiltración de tejido fibroadiposo y ganglionar por un carcinoma de origen neuroendocrino. Tras la intervención las cifras de somatostatina se normalizaron, manteniéndose dentro de los límites normales tras sucesivas determinaciones realizadas a lo largo de 2 años de seguimiento. Durante este tiempo la paciente ha permanecido asintomática, sin aparición de nuevas lesiones ni aumento de captación con la gammagrafía con octreótido.
Los tumores neuroendocrinos cutáneos pueden originarse en múltiples órganos. En su mayoría corresponden a tumores de células de Merkel, siendo muy raras las metástasis cutáneas de neoplasias endocrinas y los tumores neuroendocrinos cutáneos primarios de otro origen1–4. Estos 2 últimos grupos comparten marcadores neuroendocrinos como la sinaptofisina, la enolasa neuronal específica y la cromogranina, siendo por el contrario citoqueratina 20 negativos5,6.
Su diagnóstico se basa en la clínica, la determinación hormonal y en pruebas de imagen. Entre estas últimas cabe destacar la gammagrafía con octreótido marcado con 111In. El octreótido es un análogo de la somatostatina, y debido a la expresión de receptores de somatostatina en la mayoría de estos tumores esta prueba presenta una capacidad de detección de estos de entre el 67-91%. Esta técnica se emplea para el diagnóstico, estadificación y control evolutivo de los pacientes7,8. Algunos tumores pueden mostrar un comportamiento agresivo, aunque la mayoría presentan un crecimiento lento y comportamiento indolente1.
Entre los diagnósticos diferenciales clínicos destacan el carcinoma basocelular o el linfoma cutáneo, e histológicamente los tumores de células pequeñas como las metástasis de carcinoma indiferenciado de célula pequeña de tipo oat cell pulmonar, tumores neuroendocrinos de célula pequeña como el sarcoma de Ewing, el rabdomiosarcoma o linfomas de bajo grado. El carcinoma de células de Merkel se diferencia de los carcinomas neuroendocrinos con afectación cutánea secundaria porque sus células tienen basofilia, menos citoplasma y a menudo compromenten la epidermis en forma de enfermedad de Bowen.
El tratamiento de elección de los tumores neuroendocrinos con compromiso cutáneo o no es el quirúrgico, siendo este el único curativo1.
Hemos descrito 2 casos con tumores neuroendocrinos que afectan a la piel. En ninguno de ellos hemos encontrado una neoplasia neuroendocrina primaria en otra localización. Esto no descarta su existencia, porque podría ser tan pequeña que escapara a las pruebas de imagen o a la endoscopia como sucede, por ejemplo, con los tumores neuroendocrinos duodenales9. Es importante, por tanto, un estudio multidisciplinar y seguimiento a largo plazo de estos pacientes10.


![A. Tumor constituido por nidos de células poligonales (hematoxilina-eosina [H-E] × 5). B. Estas células eran irregulares y atípicas y no establecían conexión con la epidermis (H-E × 20). C. Se aprecian abundantes figuras de mitosis (H-E × 40). D. Estas células eran sinaptofisina positivas (H-E × 40). A. Tumor constituido por nidos de células poligonales (hematoxilina-eosina [H-E] × 5). B. Estas células eran irregulares y atípicas y no establecían conexión con la epidermis (H-E × 20). C. Se aprecian abundantes figuras de mitosis (H-E × 40). D. Estas células eran sinaptofisina positivas (H-E × 40).](https://static.elsevier.es/multimedia/00017310/0000010500000001/v1_201401250106/S0001731012004887/v1_201401250106/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w9/t1/zx4Q/XH5Tma1a/6fSs=)