El tumor fibroso solitario (TFS) es un tumor mesenquimal que se desarrolla típicamente en la cavidad pleural. Las localizaciones extrapleurales, como la piel, son extremadamente raras1. En la piel forman parte del grupo de neoplasias fusocelulares que expresan CD34: dermatofibrosarcoma protuberans (DFSP), lipoma de células fusiformes, fibromixolipoma dendrítico y fibromixoma acral superficial2,3.
Una mujer de 44 años consultó por presentar una lesión de 2 años de evolución de crecimiento lentamente progresivo en la ingle derecha. A la exploración física la paciente presentaba un tumor pediculado de base ancha de 1,2cm de diámetro de tacto firme. Se procedió a su extirpación.
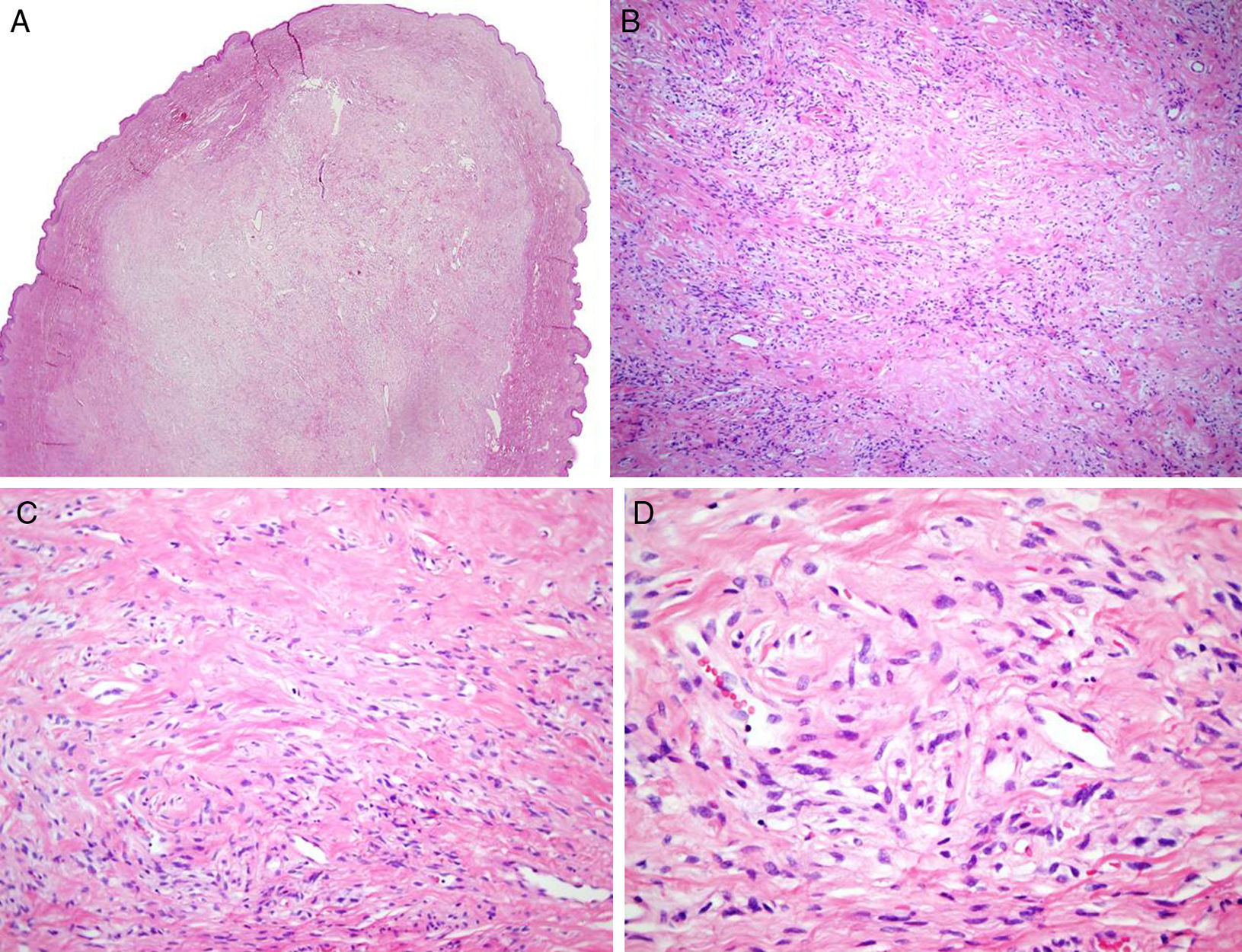
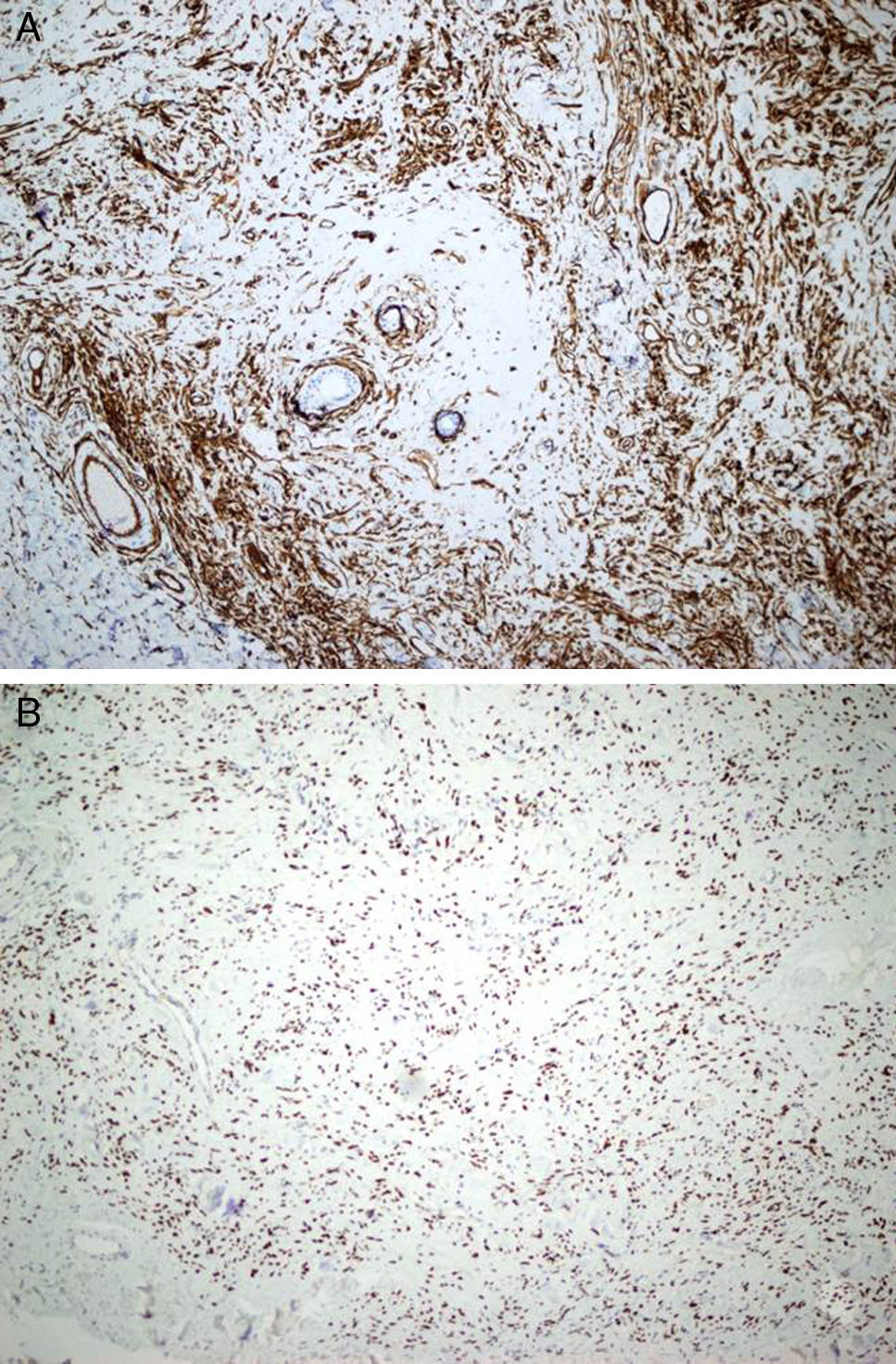
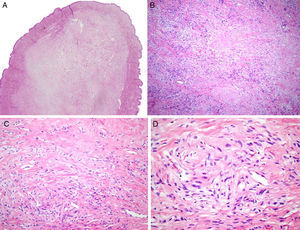
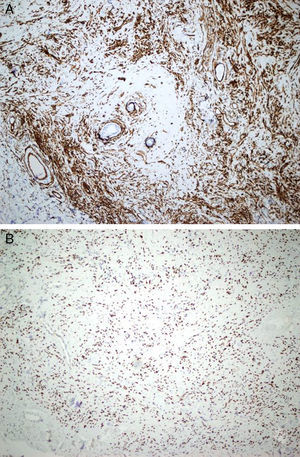
El estudio dermatopatológico reveló una lesión polipoide, con una proliferación dérmica bien delimitada, no encapsulada, de densidad celular variable compuesta por células elongadas y ovaladas, monomorfas, sin atipia, con escaso citoplasma, sin evidencia de necrosis (figs. 1A-D). Se observa una mitosis en 10CGA. El estudio inmunohistoquímico mostró positividad para CD34, BCL-2, CD 99 y STAT-6 (figs. 2A y B). El EMA, actina de músculo liso, desmina y S100 fueron negativos. Ki67 mostró una positividad del 1%.
A. Lesión polipoide con una proliferación dérmica bien delimitada, no encapsulada (hematoxilina-eosina ×20). B y C. En algunas áreas presencia de abundante matriz colágena extracelular (hematoxilina-eosina ×100, hematoxilina-eosina ×200). D. Detalle de la celularidad con núcleos elongados y ovalados monomorfos (hematoxilina-eosina ×400).
El TFS cutáneo aparece principalmente en adultos, con una distribución predominante en hombres 4:1 y con predilección por la piel de la cabeza y el cuello1. Desde el punto de vista dermatopatológico el patrón más característico de los tumores fibrosos solitarios es un «patrón fusocelular sin patrón» donde los haces están dispuestos de forma irregular sin llegar a definirse ni como un patrón estoriforme claro, ni como un patrón de haces rectilíneos y/o perpendiculares, ni de tipo ondulante. Se acompaña siempre de matriz extracelular tipo colágena o material amorfo hialinizado y es frecuente encontrar vasos de tipo hemangiopericitoide en algún área de la tumoración. El diagnóstico de esta entidad es un reto debido a la variabilidad histológica de su presentación. El diagnóstico diferencial principal hay que realizarlo con el DFSP. El TFS expresa además de CD34, vimentina, bcl-2 y CD99 (estas 2 últimas en un rango de positividad que oscila entre el 40% al 100% de los tumores) y es negativo para el antígeno de membrana epitelial, actina de músculo liso, desmina y proteína s-100. Sin embargo, algunos DFSP también pueden expresar CD34 y CD994,5. Recientemente se ha descrito que los genes de fusión NAB2-STAT6 son específicos para los TFS y su estudio puede ser de utilidad en los casos overlap2. Se ha demostrado que la inmunotinción nuclear con STAT6 es altamente sensible y específica, oscilando su porcentaje de positividad entre el 91% en los TFS de meninges y el 100% de los TFS de partes blandas2,6,7. Los marcadores inmunohistoquímicos son muy importantes para el diagnóstico de este tumor, y al igual que en otras localizaciones anatómicas STAT6 es de gran valor para su correcto diagnóstico. En su localización cutánea no se han observado metástasis a distancia, pero en 3 casos se han observado recidivas locales1,8,9, por lo que es considerado un «tumor borderline» como en el resto de localizaciones anatómicas, por lo que se recomienda su extirpación quirúrgica completa1.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.