Hasta hace pocos años las guías clínicas y revisiones sobre tratamientos de la hiperhidrosis consideraban que no existía evidencia de la utilidad de los tratamientos sistémicos, y que se asociaban a un perfil intolerable de efectos adversos, siendo desaconsejados. Sin embargo, en los últimos años diferentes estudios han ido mostrando la eficacia de los mismos, asociándose a un perfil de efectos adversos por lo general aceptable cuando se usan de forma apropiada, convirtiéndose en una alternativa terapéutica más en el tratamiento de la hiperhidrosis, de especial relevancia en casos de hiperhidrosis generalizada, multifocal o resistente a otros tratamientos. Mediante esta revisión, la primera centrada en este tema, se repasarán los diferentes tratamientos sistémicos actualmente disponibles para la hiperhidrosis, incluyendo antihipertensivos, psicofármacos y, fundamentalmente, los anticolinérgicos orales, aunque ninguno tiene indicación aprobada en el tratamiento de la hiperhidrosis.
Until quite recently, clinical guidelines and reviews on the treatment of hyperhidrosis advised against the use of systemic therapies based on their unacceptable adverse effects and a lack of evidence of usefulness. Numerous studies published over the past few years, however, have shown that, when used appropriately, these treatments are effective and in general have a favorable tolerability profile, making them an additional option for the treatment of hyperhidrosis, particularly for disease that is widespread, multifocal, or resistant to other treatments. In this review, the first of its kind, we examine the systemic therapies available for hyperhidrosis, including antihypertensives, psychoactive agents, and in particular oral anticholinergics, although none of these drugs are currently approved for this indication.
Se entiende por hiperhidrosis la producción de sudor de forma excesiva respecto a las necesidades fisiológicas, y se estima que la hiperhidrosis afecta aproximadamente al 3% de la población general1.
De forma breve, y para poder comprender mejor los tratamientos posibles, conviene recordar el mecanismo de producción del sudor. Las glándulas sudoríparas son activadas por el sistema nervioso simpático. Las señales son transmitidas desde el «centro termorregulador», en el hipotálamo, a través de nervios preganglionares y posganglionares simpáticos, hacia las glándulas sudoríparas. En estas sinapsis la acetil-colina es el neurotransmisor fundamental, estimulando tanto los receptores nicotínicos localizados en las sinapsis entre fibras pre y posganglionares, como los receptores muscarínicos (fundamentalmente M3) localizados en las glándulas sudoríparas1.
Existen múltiples alternativas terapéuticas en el tratamiento de la hiperhidrosis, como son el uso de antitranspirantes tópicos —sobre todo a base de sales de aluminio—, de anticolinérgicos tópicos —glicopirrolato fundamentalmente—, la toxina botulínica, la iontoforesis, la simpatectomía y técnicas quirúrgicas ablativas del tejido glandular sudoríparo, aunque actualmente no existe consenso respecto al algoritmo terapéutico a seguir en cada caso1–7. En cualquier caso la elección del tratamiento para cada paciente dependerá de la localización afecta, la intensidad de la sudoración y cómo afecta a la calidad de vida del paciente, la respuesta (eficacia, tolerancia…) a los tratamientos previamente utilizados, los antecedentes personales del paciente (otras enfermedades, edad, medicación habitual…) y cómo no, según el coste y disponibilidad de recursos, y en general lo aconsejable sería comenzar siempre por los tratamientos menos agresivos y costosos.
A pesar de todas estas alternativas, ya sea por la falta de respuesta a las mismas, por mala tolerancia asociada, por el miedo a sus potenciales efectos secundarios o complicaciones, o simplemente por la no disponibilidad o el coste de algunas, frecuentemente no se obtiene un control óptimo de la sudoración.
Una alternativa más previamente no mencionada sería el tratamiento sistémico de la hiperhidrosis (TSH), en el cual nos centraremos. Este actúa sobre los receptores muscarínicos de las glándulas sudoríparas de todo el cuerpo, por lo cual no existe riesgo de hiperhidrosis compensatoria, y suelen ser habitualmente tratamientos baratos y de fácil cumplimiento. Existen diferentes tipos, resumidos en la tabla 1 (incluyendo niveles de evidencia según la tabla 2)8, que a continuación iremos repasando:
Resumen de los principales tratamientos sistémicos usados en hiperhidrosis
| Fármaco | Principales contraindicaciones y precauciones* | Posología habitual | Principales efectos adversos potenciales | Grados de evidencia (jerarquía) |
|---|---|---|---|---|
| Antihipertensivos | ||||
| Clonidina | Contraindicado en enfermedad del nodo sinusal | 0,2mg/día (0,1mg/12h o parches de 0,2mg/día) | Hipotensión, xerosis oral, mareo, estreñimiento, somnolencia | III |
| Diltiazem | Evitar en BAV y bradicardia | 30-60mg, 4v/día | Hipotensión, edemas en piernas, astenia, palpitaciones | III |
| Propranolol | Contraindicado en BAV, bradicardia, asma, bronquoespasmo, hipotensión, ICC mal controlada, enfermedad del seno, predisposición a hipoglucemiaPrecauciones: medir previamente Ta y Fc | 5-20mg/día (1h antes de proceso estresante) | Hipotensión, bradicardia, hipoglucemia, fatiga, extremidades frías, fenómeno de Raynaud, trastornos del sueño | III |
| Psicofármacos | ||||
| Paroxetina | Fundamentalmente a tener en cuenta posibles interacciones medicamentosas | 10-20mg/día | Hipercolesterolemia, anorexia, trastornos del sueño, mareos, cefalea, temblores, visión borrosa, trastornos gastrointestinales (como en anticolinérgicos), disfunción sexual, astenia, ganancia de peso | III |
| Clonazepam | Contraindicado en drogodependientes, miastenia gravis, insuficiencia respiratoria grave | 1,5-6mg/día | Confusión, desorientación, somnolencia, astenia, riesgo de dependencia a fármacos | III |
| Anticolinérgicos orales | ||||
| Oxibutinina | Contraindicaciones: alteraciones gastrointestinales obstructivas, atonía intestinal, ileo paralítico, megacolon tóxico, colitis ulcerosa, miastenia gravis, glaucoma de ángulo estrechoPrecauciones: alteraciones de la motilidad intestinal, obstrucción vesical significativa, neuropatía autonómica, Parkinson, deterioro cognitivo | 2,5-20mg/día (divididos en 1-3 dosis/día) | Xerosis oral, estreñimiento, náuseas, molestias abdominales, astenia, cefalea, somnolencia, taquicardia, arritmias, visión borrosa, dificultad para micción, faringitis | I |
| Glicopirrolato | 1-8mg/día (divididos en 1-3 dosis/día) | I | ||
| Metantelina | 50mg 2-3 veces/día | I | ||
BAV: bloqueo cardíaco aurículo-ventricular; Fc: frecuencia cardíaca; h: hora; ICC: insuficiencia cardíaca; Ta: tensión arterial; v: veces.
Niveles de evidencia en terapéutica
| Nivel de jerarquía | Diseño de estudios | Sesgo |
|---|---|---|
| I | Revisión sistemática y metaanálisis | + |
| I | Estudios clínicos aleatorizados | ++ |
| II | Estudios observacionales: cohortes y casos-controles | +++ |
| III | Reporte de series y casos clínicos | ++++ |
| IV | Opinión de expertos | +++++ |
Esta jerarquía se establece según el tipo de diseño que ofrece la menor posibilidad de sesgo.
-Tratamientos sistémicos «etiológicos»: Dirigidos a la causa de la hipersudoración (casos de hiperhidrosis secundaria). Un ejemplo podría ser la terapia hormonal sustitutiva en el caso de hiperhidrosis posmenopáusica2, por otro lado no exenta de posibles efectos adversos asociados.
No hablaremos más al respecto de estos, sino que nos centraremos en aquellos que actúan sobre los mecanismos de producción del sudor, los más importantes, pues la gran mayoría de pacientes presentan hiperhidrosis primaria, aunque ninguno de los siguientes tiene indicación aprobada en el tratamiento de la hiperhidrosis, por lo que es fundamental la firma de un consentimiento informado para su uso fuera de ficha técnica.
-Antihipertensivos. Entre estos los más usados son la clonidina, el diltiazem y el propranolol.
La clonidina es una sustancia con acción agonista sobre receptores alfa-adrenérgicos, originando una reducción de flujo del sistema nervioso simpático y un predominio del sistema nervioso parasimpático. Su uso en hiperhidrosis se remonta a 1984, aunque solo se han publicado casos aislados mostrando su utilidad9–13, y en un estudio reciente14 se trataron 13 pacientes, de los que respondieron 6, mientras que fracasó en los 7 restantes (en 3 por no respuesta y en 4 por hipotensión, efecto adverso a tener en cuenta). Según algunos autores, su mayor utilidad podría estar en hiperhidrosis craneofacial posmenopaúsica o acompañada de flushing13,14, aunque también ha sido ocasionalmente usada con éxito en forma de parches en el manejo de la hiperhidrosis facial gustatoria11.
El diltiazem es un calcioantagonista indicado en el tratamiento de hipertensión arterial esencial leve-moderada, en determinadas arritmias y en el tratamiento y prevención de cardiopatía isquémica. Su utilidad en hiperhidrosis se ha descrito de forma prácticamente anecdótica15, con dosis de 30-60mg 4 veces al día, achacándose su efecto sobre la sudoración a la importancia del calcio en la estimulación de la secreción de sudor.
El propranolol, fármaco de gran uso en dermatología desde hace unos años tras conocerse su utilidad en el tratamiento de hemangiomas infantiles16, es un bloqueador beta con indicación aprobada para su uso en hipertensión, cardiopatía isquémica y taquicardias, aunque probablemente su utilidad en la hiperhidrosis se deba a su efecto ansiolítico1.
-Psicofármacos. Incluyendo antidepresivos, ansiolíticos, antipsicóticos y anticonvulsivantes: su utilidad es en cierta forma paradójica, teniendo en cuenta que entre sus efectos adversos pueden originar hipersudoración. Su eficacia podría explicarse al originar en el paciente una cierta indiferencia ante los factores emocionales que actúan como estímulo que desencadena la sudoración en muchos casos1, aunque probablemente también a su efecto anticolinérgico o noradrenérgico17–19.
Destaca el uso de la paroxetina (inhibidor selectivo de la recaptación de serotonina), con dosis de 10-20mg/día20,21.
Entre las benzodiacepinas utilizadas en el tratamiento de la hiperhidrosis destaca el uso de clonazepan, un antiepiléptico22.
Otros psicofármacos de eficacia descrita son la quetiapina17 y el topiramato18,19.
-Anticolinérgicos orales: suponen el grupo de fármacos más utilizados en el TSH, por lo cual profundizaremos más al respecto. Desarrollan su efecto inhibiendo la activación simpática al ocupar de forma competitiva los receptores de acetilcolina de las glándulas sudoríparas.
Sus efectos adversos más comunes se producen a nivel gastrointestinal (el más frecuente es la xerosis orofaríngea, aunque puede originarse estreñimiento, o incluso parálisis intestinal), ocular (midriasis, ciclopejía, pudiendo originarse un glaucoma de ángulo estrecho) y genitourinario (polaquiuria e incluso retención urinaria aguda). Los efectos adversos a nivel del sistema nervioso central (somnolencia, insomnio, nerviosismo, cefalea, náuseas, astenia…) son relativamente poco habituales, al igual que los efectos adversos a nivel cardiovascular como taquicardia, palpitaciones…
Así, antes de pautarlos, es fundamental una correcta historia clínica recogiendo antecedentes personales y medicación actual, y explicando los posibles efectos adversos, existiendo contraindicación (absoluta o relativa) para su uso en individuos que presenten (o tengan riesgo de presentar) retención urinaria (por ejemplo, pacientes con hiperplasia benigna de próstata), trastornos gastrointestinales graves (como enfermedad inflamatoria intestinal), trastornos neuromusculares como la miastenia gravis, o alteraciones oculares como el glaucoma.
En cualquier caso, por norma general las dosis de anticolinérgicos orales usadas como TSH suelen ser mucho menores a las usadas «para sus indicaciones aprobadas», por lo que aparte de la xerosis orofaríngea (que sí se aprecia frecuentemente), no suelen darse otros efectos adversos, o suelen ser bien tolerados.
En nuestra opinión es oportuno recomendar a las pacientes en edad fértil que mientras utilicen dichos tratamientos tomen medidas anticonceptivas (al no existir datos suficientes respecto a su seguridad en el embarazo), eviten la ingesta de alcohol (sus efectos pueden potenciarse ante la toma de esta medicación) y realicen una higiene oral meticulosa (la xerosis oral puede favorecer el desarrollo de caries).
Se han usado en el TSH diferentes anticolinérgicos orales como la metantelina23,24, el glicopirrolato25–30, la oxibutinina31–55, la propantelina56, la tolterodina1 o la solifenacina1, aunque nos centraremos en los 3 primeros sobre los cuales se desarrollaron la mayoría de los estudios en los últimos años, y que presentan escasos efectos adversos asociados neurólogicos gracias a su limitado paso a través de la barrera hematoencefálica. Por otro lado, la no respuesta o no tolerancia a alguno de ellos no implica que otro pueda ser útil.
El bromuro de metantelina tiene como indicaciones aprobadas el uso adyuvante en la úlcera péptica (como antisecretor) y como tratamiento de la vejiga irritable en mayores de 12 años. En España no se encuentra disponible. Se ha utilizado en 2 estudios clínicos aleatorizados23,24, controlados contra placebo, doble ciego, en casos de hiperhidrosis focal (todos adultos), usándose metantelina en forma de comprimidos de 50mg. En el primero23 se indicó un comprimido 2 veces al día. En el segundo24, multicéntrico, más amplio y reciente, de 339 pacientes, se pautó en forma de un comprimido/8h, consiguiéndose en ambos solo una mejoría moderada, y casi exclusivamente a nivel axilar. Se postula que probablemente no fuese útil a nivel palmar, ya que esta sustancia es excretada a través de glándulas sebáceas, que no existen a nivel palmoplantar y sí a nivel axilar. Los efectos adversos fueron leves y tolerables (xerosis oral fundamentalmente).
El glicopirrolato (bromuro de glicopirronio) tiene indicación aprobada en el perioperatorio digestivo (para disminuir las secreciones gástricas), como tratamiento adyuvante de la úlcera péptica y para inhibir una excesiva salivación en mayores de 12 años. Existe comercializado en forma de comprimidos de uno o 2mg, aunque en España solo está disponible (como «medicación extranjera») como comprimidos de 1mg. Su precio es de aproximadamente 150 euros por 100 comprimidos de 1mg. Así, un año de tratamiento para un paciente con una dosis media de 3mg/día supondría un coste de unos 1.600 euros.
Su uso como TSH viene avalado por diferentes estudios desde 200713,25–30, aunque ya existían estudios defendiendo su utilidad en la hiperhidrosis (fundamentalmente craneofacial) mediante formulación tópica57–63. En el primer estudio25 se utilizó para 24 pacientes (hiperhidrosis generalizada en 9 y localizada en 15), con dosis progresivamente crecientes según la respuesta comenzando con 2mg/12h (4mg/día) y llegando a un máximo de 4mg/12h (8mg/día). De los 19 evaluables hubo respuesta en 14 y efectos adversos (fundamentalmente xerosis oral) en la misma proporción, y de estos 14 que respondieron 5 abandonaron por los efectos adversos y 4 por ineficacia. En otro estudio más reciente14 se indicó en 45 pacientes con dosis habitual de 1-4mg/día (habitualmente 1-2mg/día), respondiendo 2/3 de los pacientes. De los 15 «fracasos» 9 fueron por efectos adversos limitantes y 6 por ineficacia.
Un grupo coreano describió recientemente su experiencia con glicopirrolato26,27 usando dosis iniciales de 2mg/día, incrementadas hasta un máximo de 8mg/día: mediante un estudio en 36 pacientes con hiperhidrosis primaria obtuvieron buena respuesta en el 75%, y se produjeron efectos adversos en el 36%, y en otro estudio en 19 pacientes con hiperhidrosis compensatoria (postsimpatectomía) obtuvieron buena respuesta en el 79% y efectos adversos en el 42%; En ningún caso los efectos adversos (boca seca fundamentalmente) originaron abandono del tratamiento. También se usó con éxito en un caso aislado29 de hiperhidrosis secundaria a antidepresivos orales.
Además, aunque el glicopirrolato no tiene indicación aprobada para menores de 12 años, la Dra. Paller et al. publicaron28 el uso de glicopirrolato en 31 niños y adolescentes de entre 9 y 18 años con hiperhidrosis con dosis iniciales de 1-2mg/día, aumentada según la eficacia y tolerancia hasta un máximo de 3mg/12h, con buena respuesta en el 90% y efectos adversos en el 29% (xerosis oral principalmente), y en otro estudio aún más reciente30, de 12 niños/adolescentes entre 11 y 17 años con dosis de 0,5-3mg/día, obtuvieron resultados parejos.
El anticolinérgico oral con el que actualmente se tiene mayor experiencia de uso en hiperhidrosis es sin duda el hidrocloruro de oxibutinina, de indicación aprobada en el tratamiento sintomático de la incontinencia urinaria de urgencia y/o del aumento de la frecuencia urinaria, incluso en niños mayores de 5 años (aunque se utiliza frecuentemente en niños incluso menores). Su valor en el tratamiento de la hiperhidrosis se describió en 198831, encontrándose de forma casual al prescribirse a un paciente con síndrome de hiperhidrosis e hipertermia episódicos asociado a urgencia miccional, aunque no volvió a describirse tal utilidad hasta 199632, en que volvió a apreciarse su eficacia (igualmente de forma casual) al prescribirse en una mujer con urgencia urinaria e hiperhidrosis.
Desde entonces sucesivos estudios han descrito su utilidad en el TSH33–55 en sus diferentes formas, tanto generalizada como multifocal31,33–38, en formas puramente focales39–48, en formas compensatorias (o no respondedoras) tras simpatectomía33,49,50, de origen posmenopáusico32,51 o secundarias a fármacos antidepresivos tricíciclos50 o inhibidores selectivos de la recaptación de la serotinina35,53. En cambio, se ha demostrado no eficaz en el tratamiento de la sudoración (fisiológica) secundaria a ejercicios físicos54,55.
La mayoría de los últimos estudios referentes al uso de oxibutinina en hiperhidrosis han sido publicados por Wolosker et al., recogiendo más de 500 pacientes adultos37–43,45–48 y 45 niños46 tratados. Estos la prescriben en dosis progresivamente crecientes, con las cuales promulgan una mejor tolerancia al tratamiento, comenzando en 2,5mg/día, llegando a una dosis final de 10mg/día repartidos en 2 tomas diarias (excepto en niños menores de 40kg, en que la dosis final fue de 5mg/día repartidos en 2 tomas). Otros autores recomiendan comenzar por 1,25mg/día, incrementándola progresivamente hasta estabilizar la dosis diaria en la «mínima dosis eficaz» con un máximo de 7,5mg/día repartido en 3 tomas36. En cualquier caso, las dosis utilizadas en la gran mayoría de estudios son consideradas bajas, ya que en el caso de la indicación aprobada por ficha técnica la oxibutinina se usa en adultos en dosis de hasta 15mg/día, y en niños de hasta 10mg/día. De nuevo el efecto adverso más frecuentemente asociado fue la xerosis oral, y no se apreciaron efectos adversos graves o irreversibles. Otra gran ventaja de la oxibutinina es su precio: el coste de un año de tratamiento de un paciente tomando 7,5mg/día sería de aproximadamente 36 euros.
La mayoría de los estudios sobre TSH tienen diversas limitaciones, como son las pérdidas de seguimiento de un número no desdeñable de pacientes (que en muchos casos podrían corresponder a fracasos terapéuticos con abandonos por intolerancia o falta de eficacia), y el escaso periodo de seguimiento de los pacientes tratados (pocas semanas por lo general), y además falta por discernir cuál es la dosis óptima a utilizar para cada caso.
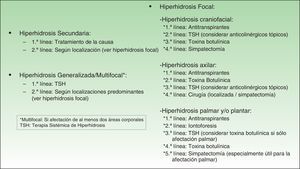
A pesar de ello, en nuestra opinión (fig. 1) los TSH podrían llegar a considerarse tratamiento de 1.ª o 2.ª línea (tras los antitranspirantes) en casos de hiperhidrosis generalizada, multifocal o compensatoria, de 2.ª línea (tras los antitranspirantes) en casos de hiperhidrosis craneofacial (aunque también podrían plantearse anticolinérgicos tópicos) y de 3.ª línea en casos de hiperhidrosis palmoplantar (tras antitranspirantes e iontoforesis) y en casos de hiperhidrosis axilar (tras antitranspirantes y toxina botulínica), y en cualquier caso, estos tratamientos pueden combinarse con otros con el objeto de lograr un mejor control de la sudoración en determinadas áreas corporales, o ante determinadas situaciones.
Según nuestro parecer actualmente el TSH de primera elección debería ser la oxibutinina, por existir respecto a su uso una mayor experiencia, pero también por su disponibilidad (no es medicación extranjera), e incluso por su precio. Sería de segunda elección el glicopirrolato oral, reservándose los antihipertensivos para casos asociados a hipertensión, el caso del propranolol ante síntomas de ansiedad (temblor, taquicardia) y la clonidina en caso de flushing, y la dosis óptima a usar debería individualizarse para cada paciente, según respuesta y tolerancia, realizándose aumento de dosis de manera progresiva; los ansiolíticos podrían plantearse cuando los episodios de hiperhidrosis se produzcan fundamentalmente en relación con situaciones de estrés, y los antidepresivos ante un trastorno depresivo asociado, que pueda estar originando o agravando el cuadro de hipersudoración.
En conclusión, existen suficientes estudios que avalan la utilidad de los TSH, sobre todo en el caso de los anticolinérgicos orales, y estos cuentan con diversas ventajas como pueden ser su versatilidad, al ser potencialmente útiles en prácticamente todos los tipos (y localizaciones) de hiperhidrosis, su bajo precio (en la mayoría de casos), su fácil seguimiento y el no producir irritación local o hiperhidrosis compensatoria, favoreciendo todo ello una buena adherencia al tratamiento. Entre sus desventajas, como comentábamos previamente, estarían su uso fuera de ficha técnica y sus frecuentes efectos adversos (xerosis oral fundamentalmente) —que por otro lado son por lo general leves y tolerables—. En cualquier caso, son necesarios estudios más amplios, aleatorizados, frente a placebo y con mayores periodos de seguimiento.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.