El síndrome del nevus azul en tetina de goma, síndrome de Bean o Blue Rubber Bleb Nevus Syndrome (BRBNS) es una enfermedad congénita poco frecuente, caracterizada por la presencia de múltiples malformaciones venosas cutáneas y viscerales, sobre todo digestivas, que progresivamente van aumentando en número y tamaño1. Habitualmente, sobre todo en los casos severos, estos pacientes desarrollan una anemia ferropénica crónica grave secundaria a los sangrados gastrointestinales recurrentes, siendo necesarias transfusiones repetidas y ferroterapia mantenida. No existe actualmente un tratamiento curativo. El tratamiento quirúrgico de las lesiones mediante enteroscopia y fulguración con arco de argón2 o resecciones término-terminales del intestino3, puede ser necesario en los casos severos. También se ha descrito, con resultados poco satisfactorios, el tratamiento con fármacos antiangiogénicos como corticoides, propranolol o interferón alfa. Recientemente se ha publicado la eficacia de la rapamicina oral en 2 casos de BRBNS4,5.
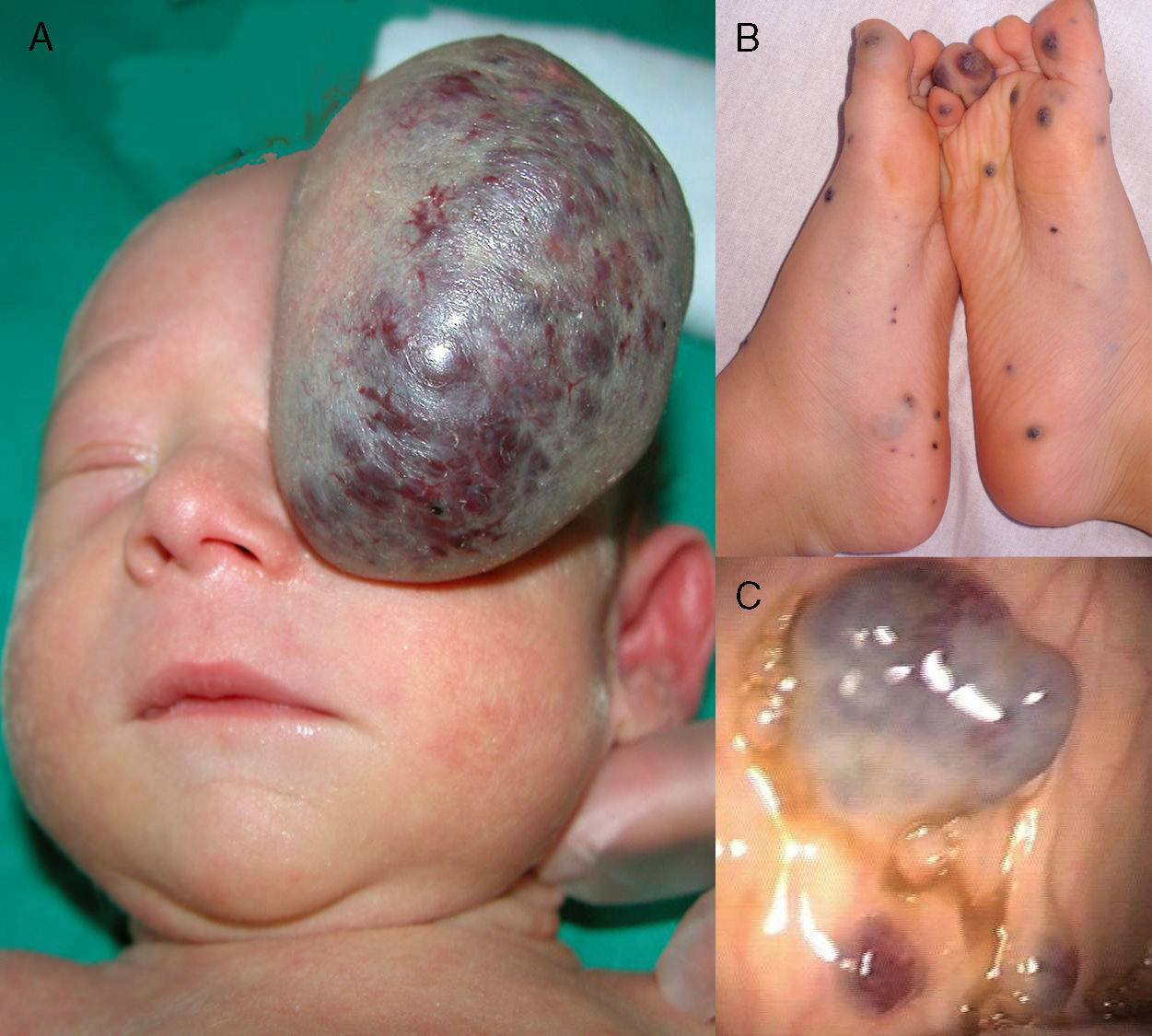
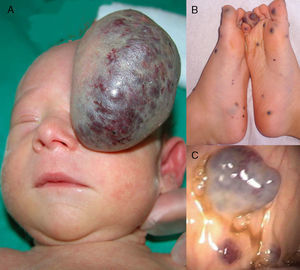
Presentamos el caso de un recién nacido a término con una tumoración congénita de 7cm localizada en la región fronto-orbitaria. La lesión ocluía el ojo izquierdo (fig. 1A) y fue extirpada a los 5 días de vida. La histología evidenció la presencia de vasos dilatados de endotelio fino, calcificaciones y reacción granulomatosa. La anamnesis descartó problemas durante la gestación o el parto, así como antecedentes familiares de anomalías vasculares. No se realizó estudio histológico de la placenta.
A) Tumor vascular grande pediculado con telangiectasias superficiales, de color azul-purpúrico en el centro y pálido en la periferia, semejando un hemangioma tipo RICH. B) Múltiples lesiones cutáneas azuladas típicas del síndrome del nevus azul en tetina de goma en los pies. C) Malformaciones venosas en el tubo digestivo.
A los 4 meses apareció una tumoración subcutánea azulada y blanda en la zona de la cicatriz, asociada a múltiples pápulas azuladas de 0,2-0,5cm de diámetro de predominio en tronco y extremidades. Con la sospecha de síndrome del nevus azul en tetina de goma, se realizó una endoscopia digestiva que reveló múltiples malformaciones vasculares localizadas a lo largo de todo el intestino. En los años sucesivos las lesiones cutáneas (fig. 1B) e intestinales (fig. 1C) fueron aumentando progresivamente en número y tamaño causando dolor y limitación de la marcha, compromiso nervioso y articular, así como episodios recurrentes de hemorragia digestiva severa. Secundariamente a los sangrados digestivos el paciente desarrolló una anemia ferropénica grave, precisando transfusiones repetidas y ferroterapia oral y endovenosa. Algunas de las lesiones cutáneas sintomáticas fueron tratadas mediante exéresis o esclerosis. A los 6 años se realizó ablación por láser de las malformaciones intestinales, consiguiendo una respuesta parcial con recidiva posterior. Dada la mala evolución del paciente y la persistencia de la anemia, que hizo necesaria la administración de ferroterapia endovenosa y más de 3 transfusiones en el último año, se decidió a los 8 años de edad iniciar tratamiento con rapamicina oral a una dosis inicial de 0,05mg/kg. La dosis se tuvo que reducir rápidamente a la mitad (0,025mg/kg) debido a la presencia de niveles de rapamicina elevados en sangre, consiguiendo entonces niveles en rango adecuado. La tolerancia al tratamiento fue buena sin ser objetivados efectos adversos. Las lesiones cutáneas mejoraron discretamente, mientras que los niveles de hemoglobina se normalizaron desde el primer mes, sin ser necesarias más transfusiones sanguíneas tras 12 meses de tratamiento mantenido.
La rapamicina (sirolimus) es un fármaco inmunosupresor que actúa inhibiendo la vía mTOR (del inglés mammalian target of rapamycin), utilizado clásicamente por vía oral para evitar el rechazo en el trasplante renal. Dadas sus propiedades antineoplásicas al inhibir la neoangiogénesis y la proliferación de células tumorales, se ha evidenciado su utilidad en la disminución del número y tamaño de los tumores en los pacientes afectos de esclerosis tuberosa6–8 y también de algunas anomalías vasculares severas9,10. En abril de 2012 se publicó por primera vez la eficacia de rapamicina a dosis de 0,05-0,1mg/kg en la reducción del tamaño de las lesiones cutáneas y reducción del sangrado digestivo en un paciente afecto de BRBNS. Más recientemente, en noviembre de 2013, se ha reportado su uso exitoso a una dosis de 4mg en la resolución de una anemia crónica en una paciente de 18 años afecta de BRBNS.
En nuestro caso una dosis menor de rapamicina (0,025mg/kg) también ha sido efectiva, consiguiendo frenar las hemorragias digestivas, normalizando las cifras de hemoglobina y evitando la necesidad de posteriores transfusiones.
Es posible que, en el futuro, el estudio de la expresión de las proteínas de la vía mTOR en las lesiones cutáneas permita predecir la respuesta a los fármacos que frenan su activación como rapamicina, temsirolimus, everolimus u otros.
ConclusiónLa rapamicina parece ser una alternativa terapéutica en el síndrome del nevus azul en tetina de goma. Sin embargo, son necesarios más estudios que corroboren su eficacia y permitan establecer la pauta de dosificación en esta rara entidad.