INTRODUCCION
La poroqueratosis, descrita por Mibelli en 18931, es una enfermedad específica de la queratinización, con diferentes formas de presentación clínica entre las que se encuentra la poroqueratosis actínica superficial diseminada (PASD). Su etiología aún es desconocida, a pesar de que en ciertas formas se ha demostrado un carácter autosómico dominante. Los últimos estudios sugieren que esta alteración en la queratinización se debe a una apoptosis prematura de los queratinocitos2. Actualmente se considera que las diversas formas clínicas de poroqueratosis, caracterizadas histopatológicamente por la llamada laminilla cornoide, pueden tratarse de diferentes expresiones fenotípicas de una misma alteración genética, debido a la coexistencia de dos diferentes tipos de poroqueratosis en el mismo paciente o en varios miembros de una familia3.
El linfedema es la aparición de un edema crónico e indoloro en las extremidades secundario al drenaje inadecuado del líquido intersticial por los vasos linfáticos, y puede clasificarse como primario o secundario a procesos muy diversos (tabla 1).
El linfedema crónico primario adquirido afecta fundamentalmente a mujeres adolescentes (precoz), o a partir de la cuarta década de la vida (tardío)4. Se instaura de forma lenta e insidiosa y afecta con mayor frecuencia a los miembros inferiores con tumefacción bilateral de intensidad variable, desde una fase leve con edema reversible limitado al tobillo, hasta un edema irreversible de consistencia dura y fibrosa que conlleva una hinchazón monstruosa de toda la extremidad (elefantiasis)5.
Presentamos un caso de linfedema primario idiopático asociado a PASD, en el que las lesiones de PASD coincidían con lesiones verrugosas debidas al linfedema.
DESCRIPCION DEL CASO
Una mujer de 74 años de edad, con antecedentes personales de hipertensión arterial, padecía un linfedema crónico idiopático desde los 30 años, sin relación con traumatismo o cirugía previa y en tratamiento con diuréticos tiacídicos y nifedipino. Carecía de hábitos tóxicos y había trabajado en el campo tan sólo durante su juventud.
Consultó por presentar, junto a las manifestaciones crónicas del linfedema, lesiones en ambas piernas y brazos de unos 20 años de evolución aproximadamente, que se habían hecho más prominentes y le ocasionaban discreto prurito coincidiendo con períodos de exacerbación durante los meses de verano.
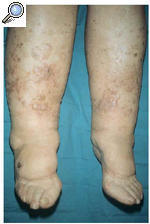
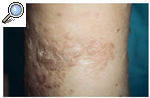
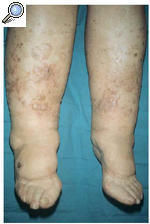
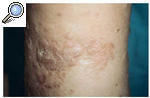
A la exploración física se observó una piel rugosa, áspera, con edema duro, sin fóvea e irreductible en ambas extremidades inferiores (linfedema crónico en fase III) conjuntamente con numerosas pápulas hiperqueratósicas, redondeadas de pequeño tamaño (1-3 mm de diámetro), discretamente hiperpigmentadas (fig. 1). Estas lesiones papulosas habían crecido adoptando un aspecto circinado de bordes netos, queratósicos, delimitados por un pequeño surco acanalado, dejando un centro atrófico de aproximadamente 1 a 3 cm de diámetro con coloración marronácea. Algunas de estas lesiones circinadas estaban ocupadas total o parcialmente por áreas hipertróficas con perfecta delimitación de la piel sana circundante, manteniendo un borde lesional de aspecto queratósico (fig. 2). En algunas áreas, principalmente en el tercio inferior, estas lesiones hipertróficas presentaban un componente vegetante y verrugoso de aspecto tumoral, de consistencia firme y de bordes bien delimitados, que borraban las lesiones hiperqueratósicas previas.
Fig. 1.--Linfedema crónico en fase III en ambas extremidades inferiores conjuntamente con múltiples pápulas hiperqueratósicas, redondeadas de pequeño tamaño discretamente hiperpigmentadas.
Fig. 2.--Áreas hipertróficas dentro de las lesiones circinadas que delimitan perfectamente la piel sana circundante y manteniendo en el borde lesional el aspecto típico de una poroqueratosis.
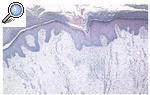
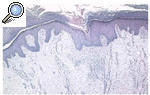
Se tomaron biopsias de las diferentes lesiones cutáneas objetivadas clínicamente. En primer lugar se realizó una biopsia de un borde de la lesión maculosa, apreciándose una delgada columna de células paraqueratósicas estrechamente apiladas que se extendía a través del estrato córneo, es decir, una laminilla cornoide, con un infiltrado inflamatorio linfocítico sublamelar. En segundo lugar, se biopsió una lesión hipertrófica bajo una lesión hiperqueratósica, apreciándose además de la laminilla cornoide y una notable elevación de la epidermis por un intenso edema dérmico (fig. 3). En tercer lugar, se biopsió una lesión verrugosa, en la que estaba también presente la laminilla cornoide, junto con atrofia epidérmica en sus proximidades y un importante daño solar. La paciente fue valorada por el servicio de cirugía vascular y tras realizar un estudio con eco-Doppler se confirmó el diagnóstico de linfedema crónico, con ausencia de alteraciones en el sistema venoso profundo y en el sistema arterial.
Fig. 3.--Estudio histopatológico de una lesión hipertrófica superpuesta a la poroqueratosis, apreciándose además de la laminilla cornoide una notable elevación de la epidermis por un intenso edema dérmico. (Hematoxilina-eosina, x40.)
Se instauró tratamiento conservador para el linfedema, evitando el ortostatismo, el sobrepeso y los largos períodos de sedestación y manteniendo reposo con piernas elevadas. Se realizó tratamiento con ácido retinoico en crema al 0,05 %, lubricantes con urea al 20 % y protección solar para la poroqueratosis junto con un tratamiento antibiótico de amplio espectro. Después de 3 meses de tratamiento la paciente presentaba un aplanamiento importante de las lesiones más hipertróficas y no presentaba molestias.
DISCUSION
La PASD, descrita en 1966 por Chernoski y Freeman6, es la forma más frecuente de poroqueratosis que comienza hacia la tercera o cuarta década de la vida. Se transmite con un patrón de herencia autosómica dominante, con penetrancia reducida en edades jóvenes y con una incidencia similar en ambos sexos7. Se observa con mayor frecuencia en áreas geográficas con mayor grado de exposición solar8, y es extremadamente rara en la raza negra9. Su etiología es aún desconocida; Reed y Leone en 197010 postularon la existencia de un clon mutante de células epidérmicas que se extiende hacia la periferia originando la laminilla cornoide. Esta tendencia a desarrollar clones anómalos sería hereditaria, y como factores desencadenantes del desarrollo de las manifestaciones clínicas se encuentran la luz ultravioleta, bien sea natural11, artificial12-14 o de fototerapia15 y la inmunodepresión producida por trasplante de órganos16-19 o por infección por el virus de la inmunodeficiencia humana (VIH)14,15. La inmunodepresión grave reduciría la inmunovigilancia20, facilitando el surgimiento de clones de queratinocitos anómalos y su transformación maligna21. Recientemente se ha mapeado el defecto genético de PASD en el cromosoma 15q 25.1-26.122 y se cree que es una reacción inmunológica debida a la presentación de antígenos desconocidos como se comprueba en el incremento en las células de Langerhans en el epitelio sublamelar y en íntimo contacto con el infiltrado inflamatorio linfocítico subyacente23,24.
Las lesiones de PASD son persistentes y no suelen resolverse de forma espontánea, carecen de tratamiento específico; sin embargo, resulta esencial considerar su potencial premaligno25. Se piensa que esta posible malignización está causada probablemente por una sobreexpresión de la proteína p5326, pudiendo aparecer carcinomas espinocelulares y basocelulares o enfermedad de Bowen. Las lesiones de mayor tiempo de evolución, las de gran tamaño y las que se presentan en pacientes de edad avanzada e inmunodeprimidos parecen asociarse a un mayor riesgo de degeneración maligna27.
Aunque la PASD típicamente se ha asociado con inmunosupresión y radiación solar, también se han descrito casos de asociados a cicatrices24, irradiación con baño de electrones28, psoriasis29,30 y con el tratamiento con tiazidas, fármacos potencialmente fototóxicos31. En nuestro caso, queremos destacar la coincidencia del desarrollo de lesiones típicas de PASD sobre un linfedema crónico primario idiopático de años de evolución, asociación no descrita hasta ahora, con la peculiaridad clínica de que todas las lesiones hipertróficas y verrugosas se desarrollaron selectivamente sobre las lesiones de poroqueratosis. Creemos que una posibilidad que explique este hecho es que en las lesiones de PASD existe un infiltrado inflamatorio con dilatación capilar y un edema dérmico, que conllevaría a una mayor filtración capilar por aumento de la presión hidrostática. Por otra parte, tampoco podemos descartar que las lesiones de PASD pudieran haber producido algún estímulo para la producción de lesiones verrugosas sobre un linfedema crónico de base.
No se ha encontrado en nuestra paciente degeneración maligna de estas lesiones, presentando hasta la actualidad una evolución favorable con el tratamiento. No obstante, la paciente está sometida a controles periódicos, dado el potencial riesgo añadido de malignización como consecuencia del linfedema crónico.