El plasma rico en plaquetas (PRP) aporta factores de crecimiento que inducen la síntesis de colágeno y otros componentes de la matriz extracelular, y estimula la activación de fibroblastos. El objetivo de este estudio es evaluar el efecto del PRP en el tratamiento del fotodaño en manos.
Material y métodosEstudio de tipo experimental. Se incluyeron individuos con envejecimiento en el dorso de las manos, de tipo 3 en la escala de fotodaño de Glogau o de clase II de la clasificación de arrugas y elastosis de Fitzpatrick, entre agosto de 2012 y enero de 2013. Se aplicó PRP en la piel del dorso de las manos y se tomaron biopsias cutáneas antes y después del tratamiento para la comparación histológica.
ResultadosSe trataron 18 mujeres con una edad media de 47,9 ± 4,3 años. El análisis histológico demostró un incremento en el número de fibroblastos (p = 0,000), número de vasos (p = 0,000) y cantidad de colágeno (p = 0,27), representado como un cambio en la escala de clasificación de arrugas y elastosis de Fitzpatrick (p < 0,001) y en la escala de fotodaño de Glogau (p = 0,01).
ConclusionesEl PRP indujo una reducción en los signos y síntomas del envejecimiento cutáneo, con mejoría en las arrugas y elastosis.
Platelet-rich plasma (PRP) provides growth factors that stimulate fibroblast activation and induce the synthesis of collagen and other components of the extracellular matrix. The objective of this study was to evaluate the effect of PRP in the treatment of photodamage of the skin of the hands.
Material and methodsExperimental study enrolling persons with photoaged skin on the dorsum of the hands (Glogau photoaging scale, type III, or Fitzpatrick wrinkle classification, type II) were included between August 2012 and January 2013. A histological comparison was made of skin biopsies taken before and after the application of PRP to the skin of the dorsum of the hands.
ResultsThe mean (SD) age of the 18 women enrolled was 47.9 (4.3) years. Histological analysis showed an increase in the number of fibroblasts (P<.001), number of vessels (P<.001), and collagen density (P=.27). These changes produced significant improvements in the Fitzpatrick wrinkle and elastosis scale (P<.001) and in the Glogau photoaging scale (P=.01).
ConclusionsPRP induced a reduction in the manifestations of skin aging, including an improvement in wrinkles and elastosis.
El envejecimiento cutáneo es el daño acumulado a nivel celular, resultado de la declinación gradual, biológica y funcional de las células con el paso del tiempo (envejecimiento intrínseco) o de factores ambientales como el tabaquismo, la exposición química y la radiación ultravioleta (envejecimiento extrínseco)1.
En la piel constantemente expuesta a los rayos ultravioleta, la degeneración del colágeno y el depósito alterado de elastina resultan en la discapacidad estructural de la integridad de la matriz extracelular, lo que causa pérdida de tono y elasticidad de la piel, y provoca su envejecimiento2.
La activación plaquetaria se presenta en respuesta al daño tisular y a la exposición vascular para proveer hemostasia y secretar proteínas biológicamente activas3-6. Dichas proteínas están a cargo de varias funciones como la quimiotaxis, la proliferación y diferenciación tisular, y la angiogénesis y regeneración de la matriz extracelular. In vitro existe una relación dosis-respuesta entre la concentración plaquetaria y la proliferación de células mesenquimales, fibroblastos y producción de colágeno de tipo i7-10.
Los factores de crecimiento en el plasma rico en plaquetas (PRP) pueden estimular la activación de los fibroblastos y lograr la regeneración de heridas del tejido blando y duro2,3. Sus efectos regenerativos son atribuidos a la presencia de factores biológicos, como el factor de crecimiento derivado de plaquetas, el factor de crecimiento transformante-ß, el factor de crecimiento epidérmico, el factor de crecimiento similar a la insulina y el factor de crecimiento endotelial vascular, los cuales se liberan localmente tras su aplicación11. El incremento en el grosor de la dermis y la epidermis, así como el aumento en el número y organización de los fibroblastos en la piel de pacientes con fotodaño, indica que estos factores actúan en la proliferación celular y en la reducción de la elastosis actínica12,13, incluso hasta 3 meses tras su aplicación6.
Aunque el PRP es muy utilizado en diversas enfermedades, existe un número limitado de estudios experimentales que confirman los efectos de la bioestimulación del PRP en el tratamiento del envejecimiento cutáneo6,14-17.
Material y métodoSe realizó un estudio de tipo experimental durante el periodo comprendido entre el 1 de agosto del 2012 y el 31 de enero del 2013. Se autorizó con el número R-2013-1301-142 del registro del Comité Local de Investigación y Ética en Investigación en Salud. Se incluyó a pacientes de 40-60 años de edad con envejecimiento cutáneo leve a moderado de acuerdo con la escala de fotoenvejecimiento de Glogau18. Los criterios de exclusión fueron el uso de tratamientos tópicos en los 6 meses previos al inicio del estudio, embarazo, infección cutánea, antecedentes de disfunción plaquetaria, uso de corticoesteroides, tabaquismo, cáncer, hemoglobina <10g/dL o recuento plaquetario <105×109/L.
Las pacientes recibieron 3sesiones de aplicación de PRP, con un intervalo de 30 días entre cada una de ellas.
La evaluación de los resultados se hizo de acuerdo con la Escala de Fotoenvejecimiento de Glogau, la Escala de Arrugas y Elastosis de Fitzpatrick19 y mediante el análisis histológico de las biopsias obtenidas antes y después del tratamiento. Se solicitó a las pacientes que no alteraran el cuidado rutinario de su piel durante el tiempo de duración del estudio.
Obtención del plasma rico en plaquetasMediante punción venosa con sistema Vacutainer (sistema de tubos al vacío) se extrajo sangre autóloga, que se depositó en 6 tubos estériles con citrato de sodio al 3,2%. Posteriormente se procedió al centrifugado de las muestras obtenidas utilizando una centrífuga digital MS 2000. El primer ciclo de centrifugado se realizó a 1.500rpm durante 10 min, logrando la separación de la sangre en sus diferentes componentes (células rojas, capa leucocitaria y plasma). El plasma fue separado en 3 partes: 2fracciones superiores conocidas como plasma pobre en plaquetas y una fracción inferior conocida como PRP. Mediante técnica estéril, se recolectaron las 2fracciones superiores del plasma de cada tubo con una jeringa de 10ml con aguja hipodérmica de 25G×16mm y se depositaron en 2 tubos estériles al vacío. Se realizó el mismo procedimiento con las fracciones inferiores del plasma y se depositaron en un tercer tubo. Finalmente, se colocaron los 3 tubos obtenidos y se procedió al segundo ciclo de centrifugado a 2.000rpm por 10 min20.
Técnica anestésicaSe realizó asepsia y antisepsia del dorso de las manos de cada paciente y con técnica estéril se efectuó bloqueo de los nervios radial y cubital mediante infiltración subcutánea de 3 cc de lidocaína simple al 2% proximales a la apófisis estiloides del radio (tabaquera anatómica) y de 2 cc de lidocaína simple al 2% a la altura de la apófisis estiloides del cúbito entre el tendón del flexor cubital del carpo y la arteria cubital.
Toma de biopsiaSe identificó la región con mayor fotodaño y se procedió a la toma de biopsia con un punch desechable de 2,5mm (Uni-Punch®). Se realizó la toma de biopsia en 2ocasiones: inmediatamente antes de la primera aplicación del tratamiento y 28 días después de la última.
Aplicación del plasma rico en plaquetasLa activación de las fracciones superiores del plasma se realizó administrando gluconato de calcio al 10%, en una concentración 10:1 y mezclando el contenido del tubo con movimientos uniformes; el producto de la mezcla se extrajo por medio de una aguja hipodérmica de 25G×16mm a jeringas de insulina de 100 unidades. Se realizaron incisiones puntiformes con una hoja de bisturí n.° 11 a nivel de la superficie dorsal del segundo, tercer y cuarto espacios interdigitales y se introdujo una cánula de lipoinfiltración de 17mm de punta roma, con la que el plasma se administró subcutáneamente de forma radiada y cruzada21,22. Posteriormente se procedió a la activación de la fracción inferior del plasma siguiendo los pasos ya mencionados y su aplicación se llevó a cabo por medio de inyecciones de aproximadamente 1,5ml en la dermis del dorso de las manos con una aguja de 25G×16mm con distancia de 1,5 a 2mm entre cada zona de aplicación.
Análisis clínicoLas participantes fueron evaluadas y clasificadas, antes del inicio del tratamiento y un mes después de la última aplicación, de acuerdo con la escala de fotoenvejecimiento de Glogau18 como de tipo 1, fotoenvejecimiento temprano sin arrugas; tipo 2, fotoenvejecimiento temprano a moderado con arrugas en movimiento; tipo 3, fotoenvejecimiento avanzado con arrugas en reposo o de tipo 4, fotoenvejecimiento severo, únicamente arrugas. De la misma forma, se clasificó a las pacientes de acuerdo con la Escala de Elastosis y Arrugas de Fitzpatrick19 como de clase I, elastosis leve con arrugas finas; de clase II, elastosis moderada con arrugas de finas a moderadas o de clase III, elastosis severa con arrugas de finas a profundas.
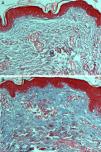
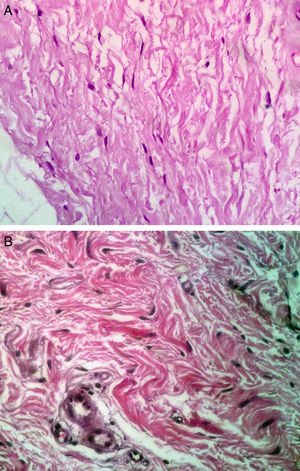
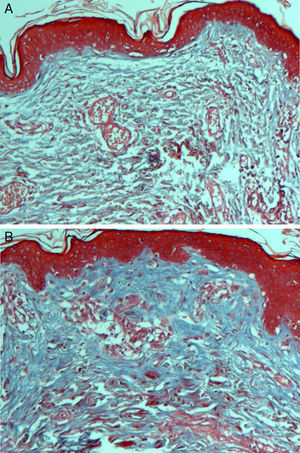
Análisis histológicoPara su evaluación, las muestras obtenidas fueron fijadas con formalina al 10% y se realizaron cortes de 6μm. Se utilizó tinción con hematoxilina-eosina para la visualización de los fibroblastos y sus características nucleares, tinción tricrómica de Masson para la visualización de las fibras de colágeno tipo I y reacción de Schiff (técnica de PAS) para la visualización de las membranas basales de los vasos sanguíneos.
El análisis de las imágenes fue realizado utilizando el software de análisis de imágenes ImageJ. La evaluación y análisis histológico de los vasos sanguíneos, colágeno y fibroblastos fue realizado cuantitativamente en 10 campos de seco fuerte, 2mm por debajo de la membrana basal del epitelio hacia la dermis profunda y en zonas no adyacentes a anexos cutáneos. Las características de atipia o reacción fibroblástica en el núcleo y la elastosis se evaluaron cualitativamente con base en su presencia o ausencia.
Análisis estadísticoLas variables cualitativas se describen con frecuencias y porcentajes; su análisis inferencial se realizó mediante la prueba exacta de Fisher o de chi cuadrado. Las variables cuantitativas se expresan como medias, desviaciones estándar o medianas; su análisis inferencial se realizó mediante la prueba de rangos de Wilcoxon. Todo valor de p<0,05 se consideró estadísticamente significativo.
ResultadosSe incluyeron 20 mujeres, 2de las cuales interrumpieron el tratamiento: una por presentar flebitis aislada de la extremidad superior y otra dislipidemia descontrolada. El resto (n=18) continuó hasta finalizar el estudio. La edad media fue de 47,90±4,3 años.
De acuerdo a la Escala de Elastosis y Arrugas de Fitzpatrick, hubo cambios significativos tras el tratamiento con PRP (p<0,001), con una media de puntuación antes y después del tratamiento de 4,94±0,80 y 2,78±0,42 respectivamente, lo cual se consideró como un cambio en la clasificación, de clase II a clase I.
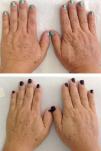
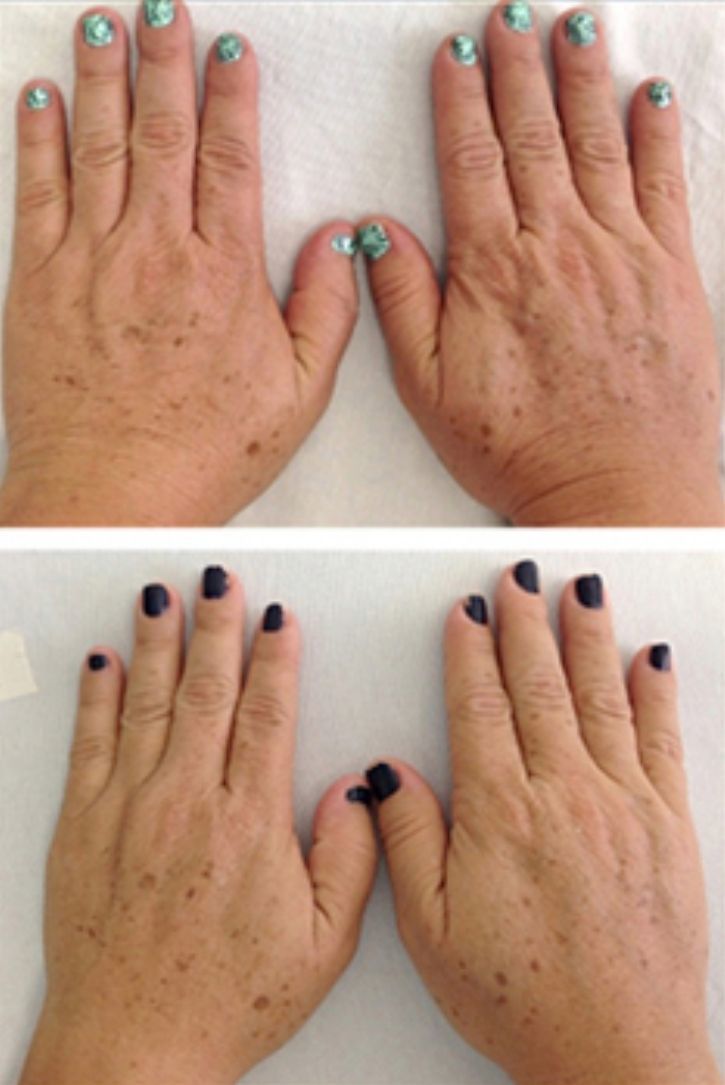
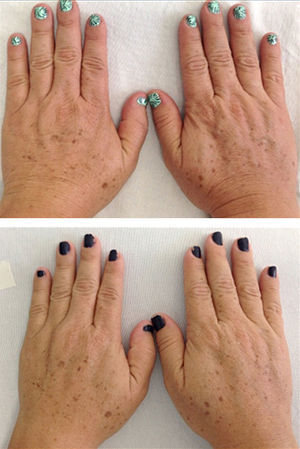
En cuanto a la Escala de Fotodaño de Glogau, 11 pacientes fueron clasificadas como tipo 3, y 7 como tipo 2 antes del inicio del estudio. Posteriormente al tratamiento, 7 (63,64%) de las pacientes que se clasificaron como tipo 3 fueron reclasificadas como tipo 2 (p=0,01); el resto de las pacientes se mantuvo dentro del grupo asignado antes del tratamiento (fig. 1).
Para el análisis y evaluación histológica, se valoró cuantitativamente el número de vasos sanguíneos y fibroblastos de acuerdo con el número de membranas basales y de núcleos de fibroblastos: este mostró un incremento significativo, así como un aumento en la cantidad de colágeno de la dermis papilar (figs. 2 y 3).
Con relación a la elastosis y la morfología de la membrana basal, no se encontraron cambios histológicos que pudieran asociarse al tratamiento con PRP. Tampoco se encontraron cambios atípicos evaluables en los fibroblastos, únicamente se notaron núcleos vesiculosos y nucléolos discretos, datos relacionados con reactividad fibroblástica leve.
El recuento y análisis del número de fibroblastos, de vasos sanguíneos y la cantidad de colágeno se expresan en la tabla 1 evidenciándose un incremento significativo en el número de los dos primeros.
Análisis histológico anterior y después del tratamiento con PRP
| Pretratamiento | Postratamiento | |||||||
|---|---|---|---|---|---|---|---|---|
| N | Media (DE) | Mediana | N | Media (DE) | Mediana | Z | p | |
| Fibroblastos/250μm2 | 18 | 2,78 (0,42) | 3 | 18 | 4,94 (0,80) | 5 | −3,77 | 0,000a |
| Fracción promedio de área con colágeno | 18 | 60,67 (2,78) | 62 | 18 | 63 (1,60) | 63 | −2,20 | 0,27a |
| Número de vasos sanguíneos /250μm2 | 18 | 6,72 (1,80) | 6,5 | 18 | 11,5 (2,3) | 11,5 | −3,49 | 0,000a |
Durante el proceso de envejecimiento cutáneo, la piel presenta múltiples cambios clínicos. Uno de los más importantes es la aparición de arrugas, que con la presencia de elastosis y la aparición de discromías y queratosis dan como resultado una apariencia no deseada de la piel. Estas manifestaciones clínicas tienen su fundamento en los cambios histológicos.
En diversos estudios se ha establecido que la aplicación del PRP de manera intradérmica estimula factores de crecimiento, los cuales favorecen la regeneración celular de la piel23,24. En nuestro estudio se observó un aumento considerable en el número de núcleos de fibroblastos y de membranas basales de vasos sanguíneos después de recibir el tratamiento con PRP. Si bien se encontraron cambios significativos en las variables valoradas, pudimos observar que los cambios producidos en el colágeno no fueron significativos en comparación con los resultados obtenidos en otros estudios6,17.
En el artículo publicado por Díaz-Ley6 se realizó un análisis histológico del uso de plasma rico en factores de crecimiento (PRGF) en la piel, y se encontró un incremento en el grosor de la dermis y epidermis, así como un aumento significativo en el número de fibroblastos y fibras de colágeno a los 3 meses de aplicación del tratamiento, por lo que el tiempo puede ser un factor importante para la visualización de cambios histológicos. Sin embargo, en nuestro estudio, así como en el realizado por Elnehrawy et al.25, las pacientes refirieron percibir un cambio en el grado de arrugas a pesar de la falta de incremento significativo en la cantidad de colágeno.
Debido a que los fibroblastos son los encargados de la síntesis de las fibras reticulares, colágenas y elásticas del tejido conjuntivo, el aumento de estos estimula la síntesis de las fibras antes mencionadas26,27. Por ello consideramos que si los procesos de cicatrización y regeneración tisular siguen llevándose a cabo posteriormente al tiempo en que realizamos nuestras mediciones, se podrían encontrar cambios histológicos significativos. Por lo que debemos considerar el tiempo en que se realizó la segunda biopsia una limitación en nuestro estudio.
Así mismo, las señales proangiogénicas liberadas por el PRP provocan que las células endoteliales sean capaces de cambiar su fenotipo para convertirse en células altamente proliferativas con capacidad de remodelar la matriz extracelular circundante, migrar hacia el foco angiogénico y diferenciarse para formar nuevos vasos sanguíneos8,28. Las líneas celulares encargadas de la angiogénesis también están involucradas en los procesos de reconocimiento, reparación y quimiotaxis para la regeneración celular, por lo que la angiogénesis podría sustentar los cambios clínicos que se presentan y ser un factor importante en los resultados obtenidos con la aplicación del PRP. Por esta razón, proponemos su medición en estudios clínicos posteriores.
De acuerdo con algunos autores29,30, la aplicación tópica o la inyección subcutánea del PRP y sus factores de crecimiento producen cambios significativos sobre la piel: restauran su elasticidad y vitalidad, aumentan su grosor y mejoran la circulación sanguínea, lo que indica que el PRP y sus factores de crecimiento regulan la remodelación de la dermis y epidermis facial. Sin embargo, un estudio señaló que el uso de la aguja en la aplicación del PRP podría ser, por sí mismo, un factor importante para el incremento del colágeno, posiblemente por el aumento en la actividad de los fibroblastos en la piel. Recientemente, Abuaf et al.17 comprobaron que hay un incremento en la cantidad de colágeno con el uso de la técnica de mesoterapia sin aplicación de PRP. Por la técnica utilizada en nuestro estudio podría considerarse que los cambios en el colágeno podrían ser aún mayores; sin embargo, nuestros resultados no fueron significativos.
Debido a que las manos generalmente se encuentran sometidas a una exposición solar continua, los resultados obtenidos en nuestro estudio pueden ser de utilidad para el tratamiento del fotodaño en zonas de menor exposición solar. Tras revisar la literatura, este es el primer estudio acerca del efecto rejuvenecedor del PRP en manos, por lo que proponemos que se realicen estudios similares que ayuden a entender y determinar los efectos de la aplicación del PRP en el tratamiento del fotodaño cutáneo.
ConclusionesLa aplicación del PRP demostró reducir los signos del envejecimiento cutáneo, favoreciendo la síntesis de colágeno y el incremento del número de fibroblastos y vasos sanguíneos en la dermis superficial.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.