El apremilast es un inhibidor vía oral de la fosfodiesterasa-4 con pocos datos de práctica clínica habitual. Nuestro objetivo fue evaluar la persistencia y la seguridad del apremilast en la práctica clínica en distintas formas clínicas de psoriasis. Se realizó un estudio observacional retrospectivo de los 30 pacientes con psoriasis que recibieron el fármaco entre enero de 2016 y diciembre de 2017 en nuestro centro, 10 con psoriasis en placas, 8 con placas predominantemente en el cuero cabelludo y 12 palmo-plantares. El tiempo global de probabilidad de supervivencia del 50% fue de 18,5meses. En nuestra experiencia, el apremilast es un fármaco efectivo y seguro para la psoriasis en placas y palmo-plantar, no así para la afectación del cuero cabelludo. Los efectos secundarios ocurren en casi dos tercios de los pacientes comprometiendo la persistencia del tratamiento.
Apremilast is a phosphodiesterase-4 inhibitor taken orally. Little information about its use in routine clinical practice is available. We aimed to assess treatment safety and persistence rates in patients on apremilast for different forms of plaque psoriasis. This observational retrospective study included 30 patients with psoriasis who were treated with apremilast between January 2016 and December 2017 in our hospital. Twelve patients had palmar-plantar psoriasis, 8 had plaque psoriasis mainly on the scalp, and 10 had plaque psoriasis in other locations. The probable period of treatment persistence in patients in the 50th percentile was 18.5 months according to survival analysis of the series overall. Our experience suggests that apremilast is effective and safe for treating palmar-plantar psoriasis and plaques at other locations but not for treating scalp psoriasis. Adverse effects that compromise treatment occur in nearly two-thirds of the patients.
El apremilast es un inhibidor oral de la fosfodiesterasa tipo 4 (PDE-4) aprobado en 2014 por la FDA y en 2015 por la EMA para el tratamiento de la psoriasis en placas en adultos. Esta inhibición produce un aumento del AMPc intracelular, que provoca una elevación de las citocinas antiinflamatorias y un descenso de las proinflamatorias (TNF-alfa, IL-6, IL-17 e IL-23)1,2.
Los ensayos clínicos (ESTEEM1 y ESTEEM2) han demostrado una eficacia PASI50 y PASI75 en el 55,5% y en el 33,1% de los pacientes con psoriasis en placas, respectivamente3,4. Un subanálisis de los ensayos ESTEEM1 y ESTEEM2, centrado en aquellos pacientes que concomitantemente a las placas presentaban lesiones hiperqueratósicas palmo-plantares, mostró que un 48% de pacientes con un PGA igual o superior a 3 alcanzaban un PGA0/1 tras las primeras 16semanas de tratamiento5. En otro subanálisis de los ensayos clínicos ESTEEM sobre la efectividad en las lesiones del cuero cabelludo, un 40-50% de los pacientes alcanzaron un PGA0/1 a las 16semanas de tratamiento, con un mantenimiento de la respuesta e incluso mejoría en la semana526. Estos resultados, aunque a través de subanálisis, postulan al apremilast como un fármaco efectivo en el tratamiento de las localizaciones especiales de la enfermedad. Sin embargo, en la actualidad existen pocos datos de práctica clínica que apoyen estos hallazgos. El objetivo del presente trabajo es evaluar los datos obtenidos de la persistencia y la seguridad en nuestra práctica clínica, tras 2años de empleo de apremilast en las diferentes formas clínicas de psoriasis.
Material y métodosSe diseñó un estudio observacional retrospectivo realizado en el Hospital Universitario y Politécnico La Fe de Valencia, España. Se incluyeron todos los pacientes con psoriasis, excluyendo las formas pustulosas, que habían recibido al menos una dosis de tratamiento con apremilast, entre enero de 2016 y diciembre de 2017. Se empleó la dosis según ficha técnica. Al tratarse de práctica clínica, se permitió el empleo de terapia tópica, así como el inicio del apremilast sin necesidad de un periodo de lavado previo.
Se analizó la persistencia y la seguridad del tratamiento, así como la influencia en las mismas de las variables epidemiológicas (sexo, edad, peso, talla, índice de masa corporal [IMC]) y clínicas (tiempo de evolución de la psoriasis, líneas de tratamiento previas, PASI y PGA inicial). Se consideró que un paciente pertenecía al subgrupo de placas predominantes del cuero cabelludo cuando presentaba más de un 20% de afectación del mismo y menos de un 3% de lesiones en tronco y/o extremidades. Establecimos como fallo primario la ausencia de mejoría PASI50 en la psoriasis en placas, o la ausencia de una reducción de al menos 2 puntos del PGA en las formas palmo-plantares (PP) y del cuero cabelludo. Se consideró un fallo secundario cuando una respuesta inicial adecuada se perdía en al menos 2 visitas consecutivas. En todos los pacientes se evaluó la presencia, la gravedad y la duración de los efectos secundarios.
El análisis descriptivo de las variables se analizó con las frecuencias absolutas y relativas, la media y la desviación tipo. El análisis inferencial de las variables cualitativas se realizó mediante las pruebas basadas en la ley de la ji cuadrado. El análisis de supervivencia se realizó mediante el método de Kaplan-Meier y las pruebas de los rangos logarítmicos, junto al percentil 50 y el percentil 75 para el cálculo del tiempo de la probabilidad de supervivencia, estableciendo como el evento a estudio la retirada del tratamiento por cualquier motivo. Para el análisis se utilizó el paquete estadístico SPSS tomando como límite de significación p<0,05.
Todas las historias clínicas de los pacientes fueron tratadas de forma anonimizada y cumpliendo las leyes de privacidad de datos, obteniéndose para la realización del estudio la clasificación de la AEMS como EPA-OD y la aprobación del comité ético del Hospital Universitario y Politécnico La Fe.
ResultadosSe incluyeron un total de 30 pacientes, 18 mujeres y 12 hombres con una mediana de edad de 44años (rango 22-71) y una mediana de IMC de 28,3 (rango 19-38). La mediana de seguimiento fue de 9meses (rango 0,5-18meses). Diez pacientes presentaban una psoriasis en placas, 8 una forma predominante del cuero cabelludo y 12 una PP. En 19 pacientes (63%) la indicación del apremilast se basó solo en el criterio clínico de la localización especial. El resto de indicaciones fueron: una ausencia del control con fármacos clásicos o una contraindicación de los mismos (4/30; 13%), una infección tuberculosa latente no tratada (2/30; 7%), una hepatitis B activa (2/30; 7%), un síndrome de Lynch (1/30; 3%), un antecedente de peritonitis bacteriana espontánea (1/30; 3%) y una hepatitis autoinmune (1/30; 3%). En 7 pacientes (23%) el apremilast fue el fármaco empleado como primer tratamiento sistémico, y 23 (77%) pacientes habían recibido algún tratamiento sistémico previamente: 19 pacientes fármacos clásicos (63%), 3 pacientes fármacos clásicos y biológicos (10%), y un paciente solo fármacos biológicos (3%).
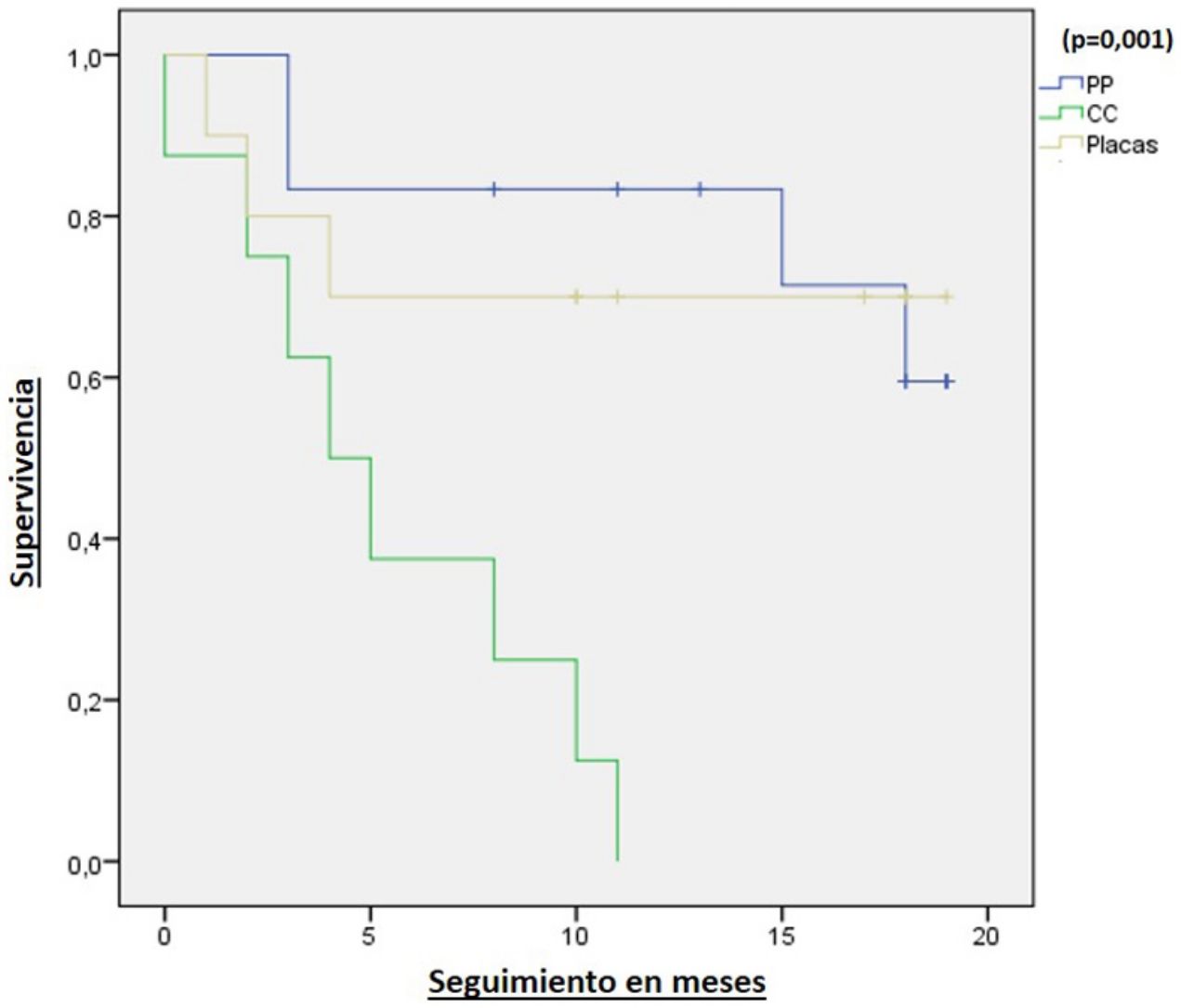
Al finalizar el periodo del estudio, solo 15 pacientes mantenían el tratamiento. El tiempo de probabilidad de supervivencia del 50% y del 75% fue de 18,5 y 4 meses, respectivamente, para el total de pacientes incluidos sin distinguir entre indicaciones. Ningún paciente con psoriasis en placas predominante del cuero cabelludo finalizó el periodo de estudio en tratamiento, con un tiempo de probabilidad de supervivencia del 50% y 75% de 5 y 2,5 meses, respectivamente. En la psoriasis en placas, el tiempo de probabilidad de supervivencia del 75% fue de 4meses, y en la PP de 15,6meses. La tabla 1 muestra las causas de retirada. De forma global, la mediana del tiempo hasta la retirada del fármaco por las reacciones adversas fue de 2meses (rango 0,5-4meses), para el fallo primario fue de 5,5meses (rango 4-8meses) y de 14,5meses (rango 11-18meses) para el fallo secundario. En los 3 tipos de psoriasis incluidos, no identificamos una asociación estadísticamente significativa entre una reducción en el PGA≥2 puntos y el IMC, el sexo, la edad y la toma de fármacos previos. En nuestro estudio, solo la forma clínica del cuero cabelludo se asoció de forma estadísticamente significativa con la retirada por un fallo primario y/o secundario, así como la ausencia de una reducción de al menos 2 puntos en el PGA (p=0,003). El análisis mediante curvas Kaplan-Meier demostró una reducción significativa de la supervivencia del tratamiento en los pacientes con psoriasis del cuero cabelludo (p=0,001) (fig. 1).
Causas de retirada y proporción de efectos secundarios acontecidos
| Todas las indicaciones(n=30) | Psoriasis en placas(n=10) | Psoriasis palmo-plantar(n=12) | Psoriasis de cuero cabelludo(n=8) | |
|---|---|---|---|---|
| Causas de retirada | ||||
| Fallo primario | 4 (13%) | 0 | 1 (8%) | 3 (38%) |
| Fallo secundario | 4 (14%) | 0 | 2 (16%) | 2 (24%) |
| Efecto secundario | 7 (23%) | 3 (30%) | 1 (8%) | 3 (38%) |
| Tipo de efecto secundario | ||||
| Cefalea | 11 (37%) | 4 (40%) | 5 (42%) | 2 (25%) |
| Diarrea | 10 (33%) | 4 (40%) | 4 (33%) | 2 (25%) |
| Náuseas | 8 (27%) | 1 (10%) | 3 (25%) | 4 (50%) |
| Astenia | 6 (20%) | 4 (40%) | 2 (17%) | 0 |
| Dolor abdominal | 3 (10%) | 0 | 1 (8%) | 2 (25%) |
| Mialgias | 2 (7%) | 2 (20%) | 0 | 0 |
| Calambres | 1 (3%) | 0 | 1 (8%) | 0 |
Un 73% de los pacientes (22/30) tuvieron efectos secundarios relacionados con la toma del fármaco, de los cuales un 60% (13/22) tuvo 2 o más efectos secundarios. En total se registraron 41 efectos secundarios (tabla 1). Ningún paciente presentó efectos secundarios severos ni infecciosos. En los 15 pacientes que finalizaron el estudio, el tiempo de duración de los efectos secundarios fue de 3,4meses de mediana (intervalo: 1-10meses), resolviéndose el 40% (6/15) durante el primer mes de tratamiento, y el 53% (8/15) durante los primeros 2meses. No encontramos una asociación estadísticamente significativa entre la aparición de los efectos secundarios y la edad, el IMC, la forma clínica, la respuesta al tratamiento o el sexo. No obstante, cabe señalar una tendencia (p=0,077) entre los pacientes con normopeso y la aparición de los efectos secundarios, de forma que el 100% de pacientes con normopeso presentaron efectos secundarios frente a solo el 50% de los pacientes con obesidad.
DiscusiónLa eficacia, persistencia y seguridad de los fármacos en la práctica clínica puede ser diferente a la descrita en los ensayos clínicos7,8. Por ello son necesarios estudios en las condiciones reales de su empleo. Nuestros resultados con el apremilast en la psoriasis en placas han sido similares a los recientemente publicados por Vujic et al. en un estudio de práctica clínica sobre 48 pacientes durante 2años9. Los autores no encontraron diferencias estadísticamente significativas entre la supervivencia del fármaco y el sexo, la edad, el tabaquismo, la presencia de artropatía, el PASI inicial ni tratamientos previos. Sin embargo, sí que hallaron una tendencia entre la probabilidad de alcanzar una respuesta igual o mayor al PASI75 y un IMC inferior a 30. En nuestra serie, únicamente identificamos una tendencia a presentar con mayor probabilidad efectos secundarios en aquellos pacientes en normopeso10. Con respecto a los efectos secundarios, nuestros resultados son similares a los obtenidos tanto en ensayos clínicos como en otros estudios de práctica clínica, siendo la diarrea, el dolor abdominal y la cefalea los más frecuentes, apareciendo en un 60-80% de pacientes. Por ello sería aconsejable evitar el fármaco o realizar controles estrechos en aquellos pacientes con problemas digestivos, cefaleas o migrañas de base. En nuestra serie, no hemos encontrado efectos secundarios graves o potencialmente graves, incluso en pacientes con comorbilidad infecciosa o neoplásica de base.
Nuestro estudio tiene una serie de limitaciones. Por un lado, se trata de un estudio de carácter retrospectivo, sin grupo comparativo y con un reducido número de pacientes, sobre todo teniendo en cuenta la subdivisión posterior según el tipo clínico. Además, el uso concomitante de corticoides tópicos no fue correctamente cuantificado.
En conclusión, en nuestra experiencia el apremilast es un fármaco efectivo y seguro en la psoriasis en placas y PP. En nuestra serie, las formas clínicas con afectación predominante de cuero cabelludo no mostraron una buena respuesta al tratamiento. Los efectos secundarios ocurren en casi dos tercios de los pacientes, principalmente en forma de problemas gastrointestinales o cefalea, y aunque son en su mayoría de carácter leve-moderado, pueden comprometer seriamente la persistencia al tratamiento.
Conflicto de interesesA. Sahuquillo-Torralba y R. Botella Estrada han ejercido como consultores y/o recibido honorarios como ponentes y/o participado en ensayos clínicos de compañías que desarrollan fármacos empleados en el tratamiento de la psoriasis incluyendo AbbVie, Celgene, Janssen-Cilag, LEO Pharma, Lilly, Novartis y Pfizer.
E. Monte Boquet ha ejercido como consultor y/o recibido honorarios como ponente de compañías que desarrollan fármacos empleados en el tratamiento de la psoriasis incluyendo AbbVie, Celgene, Janssen-Cilag, LEO Pharma, Lilly, Novartis y Pfizer.
El resto de los autores no tiene conflictos de intereses que declarar.