La psoriasis afecta a un gran porcentaje de mujeres en edad fértil. Nuestro objetivo fue conocer las inquietudes de las mujeres con psoriasis en relación con la planificación familiar.
Material y métodosEstudio observacional, descriptivo, transversal y multicéntrico realizado entre marzo del 2020 y octubre del 2021. Se recabaron datos sociodemográficos e inquietudes relacionadas con la planificación familiar de mujeres entre 18-45 años con psoriasis en placas y candidatas a recibir tratamiento sistémico.
ResultadosSe reclutaron 153 pacientes de 11 centros españoles (edad media: 35,4 ± 8 años, duración media de la enfermedad: 16,7 años); 38,4% de los casos tenían una enfermedad moderada/grave para los médicos, aunque la percepción de la actividad era significativamente superior para las pacientes. En una de cada tres mujeres, la enfermedad limitaba o retrasaba el deseo gestacional. Existía preocupación de que la enfermedad empeorara al tener que retirar o cambiar un fármaco o que los tratamientos perjudicaran al bebé. Alrededor de la mitad de las pacientes no había recibido información sobre planificación familiar en la consulta, especialmente aquellas mujeres sin embarazos previos. Las mujeres con tratamiento biológico (58,7%) tenían mejor situación clínica, mejor calidad de vida y menos alteraciones en la esfera sexual que las pacientes sin tratamiento biológico.
ConclusionesLas pacientes con psoriasis tienen numerosas preocupaciones relacionadas con la planificación familiar. En algunos casos, estos miedos podrían llevar a retrasar y/o limitar el deseo gestacional. Sería necesario incrementar la información que se da a las pacientes y mejorar la formación de los dermatólogos en este tema.
A significant proportion of women of childbearing age have psoriasis. The aim of this study was to examine family planning concerns in this population.
Material and methodsObservational, descriptive, cross-sectional, multicenter study conducted between March 2020 and October 2021. We collected sociodemographic data and analyzed responses to a family planning questionnaire administered to women aged 18 to 45 years with plaque psoriasis who were candidates for systemic treatment.
ResultsWe studied 153 patients (mean [SD] age, 35.4 [8.0] years; mean disease duration, 16.7 years) being treated at 11 Spanish hospitals. Overall, 38.4% of women were considered to have moderate to severe psoriasis by their physicians; perceived severity ratings were significantly higher among women. Psoriasis affected the women's desire to become pregnant or led to their delaying pregnancy in 1 in 3 respondents. They were concerned that their condition might worsen if they had to discontinue or switch treatment or that the treatment might harm the baby. Approximately half of the women had not received family planning counseling from their physicians, and this was more likely to be the case among never-pregnant women. Women on biologic therapy (58.7%) had better psoriasis control and a better quality of life than women on other treatments. Their sexual health was also less affected.
ConclusionsWomen with psoriasis have numerous family planning concerns, which in some cases can lead them to delay pregnancy or affect their desire to become pregnant. Dermatologists need to receive better training regarding family planning in women with psoriasis so that they can provide their patients with more and better information.
La psoriasis afecta negativamente la calidad de vida de los pacientes1. En España, la prevalencia es de 2,3%, con aproximadamente un millón de pacientes y una prevalencia similar entre géneros2. El debut ocurre entre la segunda y cuarta décadas de la vida en 75% de los casos. Por lo tanto, su aparición coincide con los años reproductivos de la mujer, lo que puede plantearle miedos e incertidumbres sobre la maternidad3,4 por falta de información sobre la planificación familiar, el embarazo o la lactancia5,6. Según el registro BIOBADADERM, las mujeres con psoriasis moderada-grave en España tienen menores tasas de embarazo7 y son menos proclives a la lactancia materna que la población general8.
La evolución de la psoriasis durante el embarazo es imprevisible. Aproximadamente la mitad de las mujeres mejoran de sus síntomas, otras mantienen una actividad similar y en más de 20% hay una exacerbación3. Además, 65% de las pacientes empeoran de los síntomas en el posparto9. La psoriasis no controlada en el embarazo se asocia a complicaciones tanto maternas como fetales3,10–12. Aunque hay numerosos tratamientos para la psoriasis potencialmente teratogénicos13–15, en la actualidad disponemos de opciones terapéuticas compatibles con el embarazo y la lactancia5,16–18.
El objetivo principal del estudio fue determinar el impacto de la enfermedad sobre el deseo gestacional y la lactancia, saber más de las inquietudes y miedos de las mujeres con psoriasis antes, durante o después del embarazo, así como la información sobre planificación familiar, embarazo y lactancia que reciben en las consultas, con el fin de que en un futuro puedan recibir información más completa, según sus necesidades por parte de su dermatólogo. Como objetivos secundarios se evaluó si existen diferencias en el impacto de la enfermedad, las preocupaciones o la información en función de haber tenido algún embarazo/hijo, el tratamiento con biológicos, o la actividad de la enfermedad según el médico o la paciente.
MétodosEstudio observacional, descriptivo, transversal y multicéntrico. La selección de las pacientes se realizó en consultas de dermatología de centros españoles. La inclusión de pacientes se realizó entre marzo del 2020 y octubre del 2021.
Población de estudioSe incluyeron mujeres con psoriasis en placas, de 18-45 años, candidatas a recibir tratamiento sistémico y que estaban de acuerdo en participar en el estudio. Se excluyeron pacientes con artritis psoriásica (para centrarnos en el dominio cutáneo de la psoriasis y minimizar la variabilidad) y pacientes que no querían participar o no podían escribir o leer apropiadamente.
Variables y recogida de datosSe recogieron variables clínicas, incluyendo Psoriasis Area Severity Index (PASI), Body Surface Area (BSA), percepción de la actividad de la psoriasis por parte del médico en una escala visual analógica (EVA) de 0-10, comorbilidades y tratamientos previos y actuales. Se evaluó la calidad de vida con una escala cualitativa (material suplementario) y por medio del Dermatology Life Quality Index (DLQI)19.
Las pacientes respondieron anónimamente en papel un cuestionario con datos sociodemográficos y percepción de la actividad de la psoriasis. Cumplimentaron un cuestionario de 27 preguntas sobre planificación familiar diseñado para el estudio (material suplementario). Los investigadores elaboraron el cuestionario ad hoc para este proyecto teniendo en cuenta los objetivos del estudio. Las preocupaciones e información antes del embarazo, así como el impacto de la enfermedad se abordaron en los ítems 1-16 y 24. En el ítem 2 se evalúa el impacto de la enfermedad en la vida sexual. Las preocupaciones e información durante el embarazo se trataron en los ítems 17-21 y después del embarazo en los ítems 22, 23 y 25. Dos ítems adicionales (26 y 27) analizan la información por parte del médico u otros medios.
Con los resultados, se elaboró una tabla con aspectos para tratar en las consultas.
Estudio estadísticoLas variables se describieron mediante distribución de frecuencias, mínimo, máximo, media y desviación estándar (DE) o mediana y rango intercuartílico (RIC). Para determinar los objetivos secundarios, se realizaron subanálisis evaluando diferencias por el hecho de haber tenido algún embarazo/hijos, la actividad de la enfermedad (leve: EVA = 0-2 vs. moderada o grave: EVA = 3-10), y el uso actual de tratamientos biológicos. Las comparaciones de variables cualitativas se realizaron mediante la prueba chi-cuadrado y las de variables cuantitativas independientes o pareadas mediante la prueba de Mann-Whitney o de Wilcoxon, respectivamente (nivel de significación: 5%; paquete estadístico SPSS 25.0 [IBM Corp., Armonk, NY, EE. UU.]).
Aspectos éticosSe siguió la Declaración de Helsinki y la legislación española en materia de investigación clínica y de protección de datos. Las participantes firmaron un consentimiento informado. El estudio fue aprobado por el Comité Ético de Investigación Clínica del Hospital Ramón y Cajal (acta N°373).
ResultadosSe incluyeron 153 mujeres de 11 centros españoles (edad media: 35,4 ± 8 años). Las características sociodemográficas y clínicas se resumen en la tabla 1. La mayoría de las pacientes (51,6%) no habían estado nunca embarazadas. De las 74 pacientes que habían estado embarazadas, la mayoría habían tenido uno o dos hijos (51,4 y 27%, respectivamente), y 35,1% había sufrido al menos un aborto; 23,9% recibieron atención en unidades de embarazo de alto riesgo.
Características sociodemográficas y clínicas
| nEdad media ± DE (años) | 15335,4 ± 8,0 |
| Nivel de estudios, (%) | |
| Educación primaria o secundaria | 28 (18,3) |
| Bachillerato o superior | 125 (81,7) |
| Comorbilidades, n (%) | |
| Diabetes mellitus en tratamiento | 4 (2,6) |
| Hipertensión en tratamiento | 11 (7,2) |
| Hiperlipidemia | 17 (11,2) |
| Obesidad mórbida (IMC ≥ 35) | 8 (5,3) |
| Síndrome metabólico en tratamiento | 5 (3,3) |
| Enfermedad inflamatoria intestinal | 3 (2%) |
| Hígado graso no alcohólico | 4 (2,6) |
| Insuficiencia cardiaca | 0 |
| Insuficiencia renal | 0 |
| Ansiedad / depresión | 23 (15,1) |
| Otras comorbilidades | 26 (17,1) |
| Duración media de la psoriasis ± DE (años)Media de PASI ± DEMedia de BSA ± DECalidad de vida media ± DE (escala DLQI de 0 a 30) | 16,7 ± 8,03,1 ± 4,02,9 ± 4,46,5 ± 5,9 |
| Calidad de vida (cualitativo), n (%) | |
| CV no afectada | 1 (0,7) |
| CV poco afectada | 89 (58,2) |
| CV moderadamente afectada | 35 (22,9) |
| CV muy afectada | 21 (13,7) |
| CV extremadamente afectada | 7 (4,6) |
| Percepción de la actividad según las pacientes (EVA media ± DE) | 3,6 ± 3,2 |
| Percepción de la actividad según los médicos (EVA media ± DE) | 2,7 ± 2,6 |
| Actividad de la enfermedad según las pacientes, n (%) | |
| Leve (EVA: 0-2) | 76 (51,0) |
| Moderada (EVA: 3-7) | 50 (33,6) |
| Intensa (EVA: 8-10) | 23 (15,4) |
| Actividad de la enfermedad según los médicos, n (%) | |
| Leve (EVA: 0-2) | 90 (61,6) |
| Moderada (EVA: 3-7) | 50 (34,2) |
| Intensa (EVA: 8-10) | 6 (4,1) |
| Tratamiento actual, n (%) | |
| Tratamiento tópico | 73 (48,7) |
| Corticoides sistémicos | 6 (4,0) |
| Tratamiento sistémico convencional | 26 (17,3) |
| Apremilast u otros tratamientos orales | 13 (8,7) |
| Anti-TNF | 29 (19,3) |
| Anti-IL 17 | 28 (18,7) |
| Anti-IL 23 | 9 (6,0) |
| Anti-IL 12/23 | 22 (14,7) |
BSA: Body Surface Area; DE: desviación estándar; EVA: escala visual analógica; IL: interleucina; IMC: índice de masa corporal; PASI: Psoriasis Area Severity Index; TNF: factor de necrosis tumoral.
La mediana de la duración de enfermedad era de 16 años (RIC: 9-22; mínimo: 1; máximo: 41 años). La mayoría de las pacientes presentaban una enfermedad leve en el momento de la valoración (81,4% BSA < 5%). Sin embargo, la percepción de la gravedad de la enfermedad por las pacientes era moderada-grave (EVA 3-10) en 49% de los casos y de 38,4% casos según los médicos. La percepción de la actividad era significativamente superior para las pacientes que para los médicos (EVA media 3,6 vs. 2,7 y mediana de 2 vs. 1,5; p < 0,001). Respecto a la calidad de vida, 41,2% refería que estaba moderada, muy o extremadamente afectada (tabla 1).
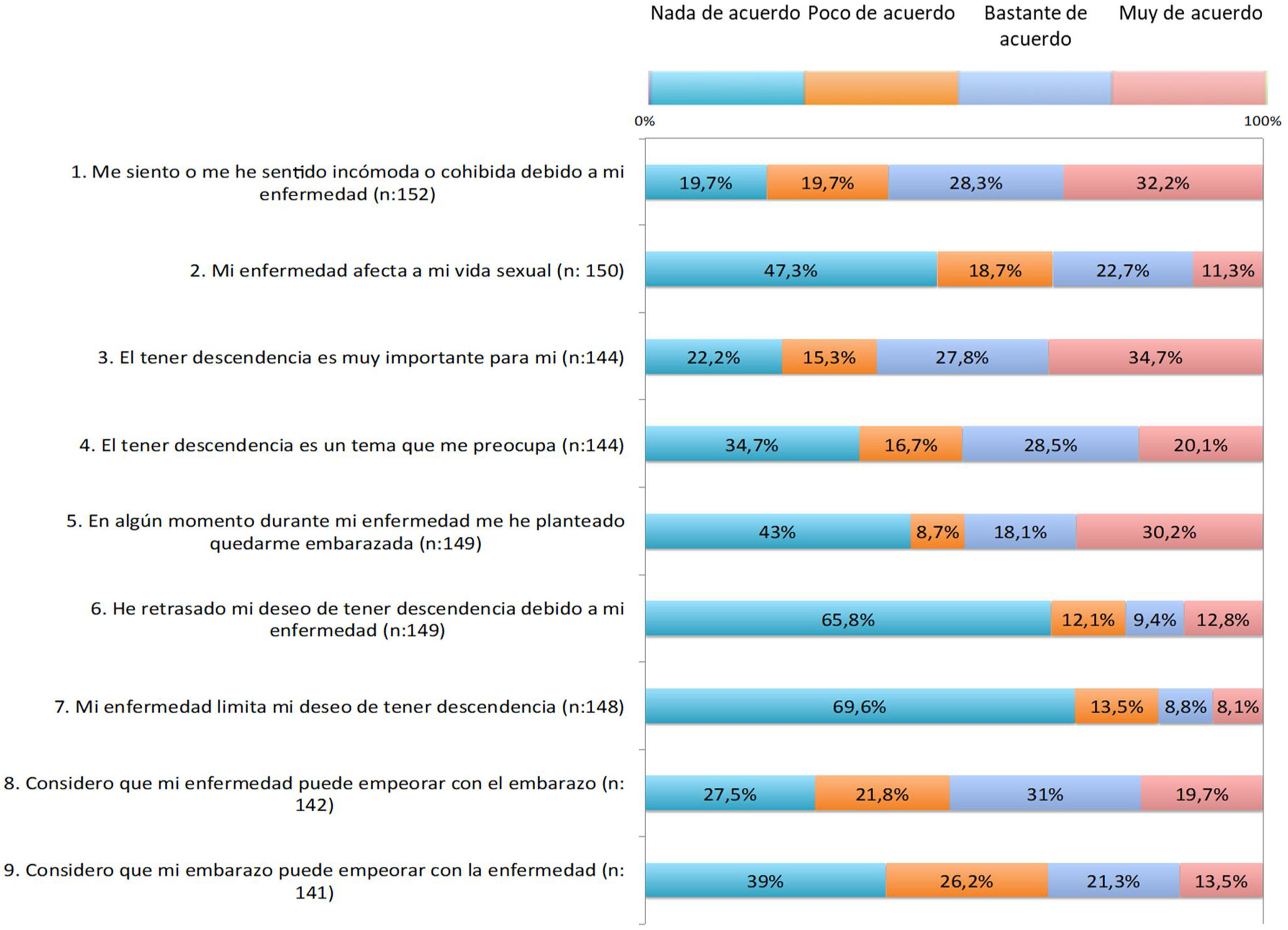
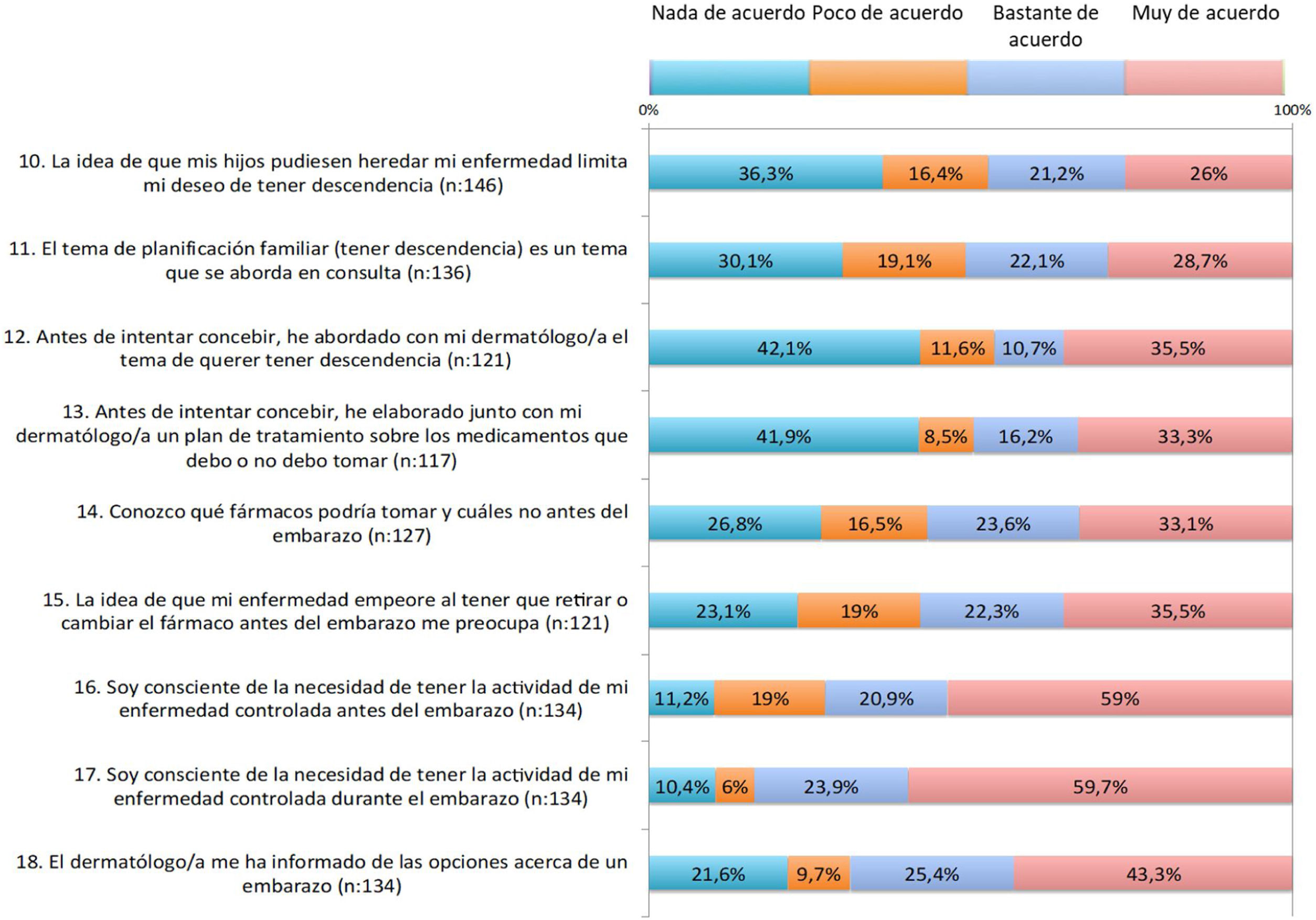
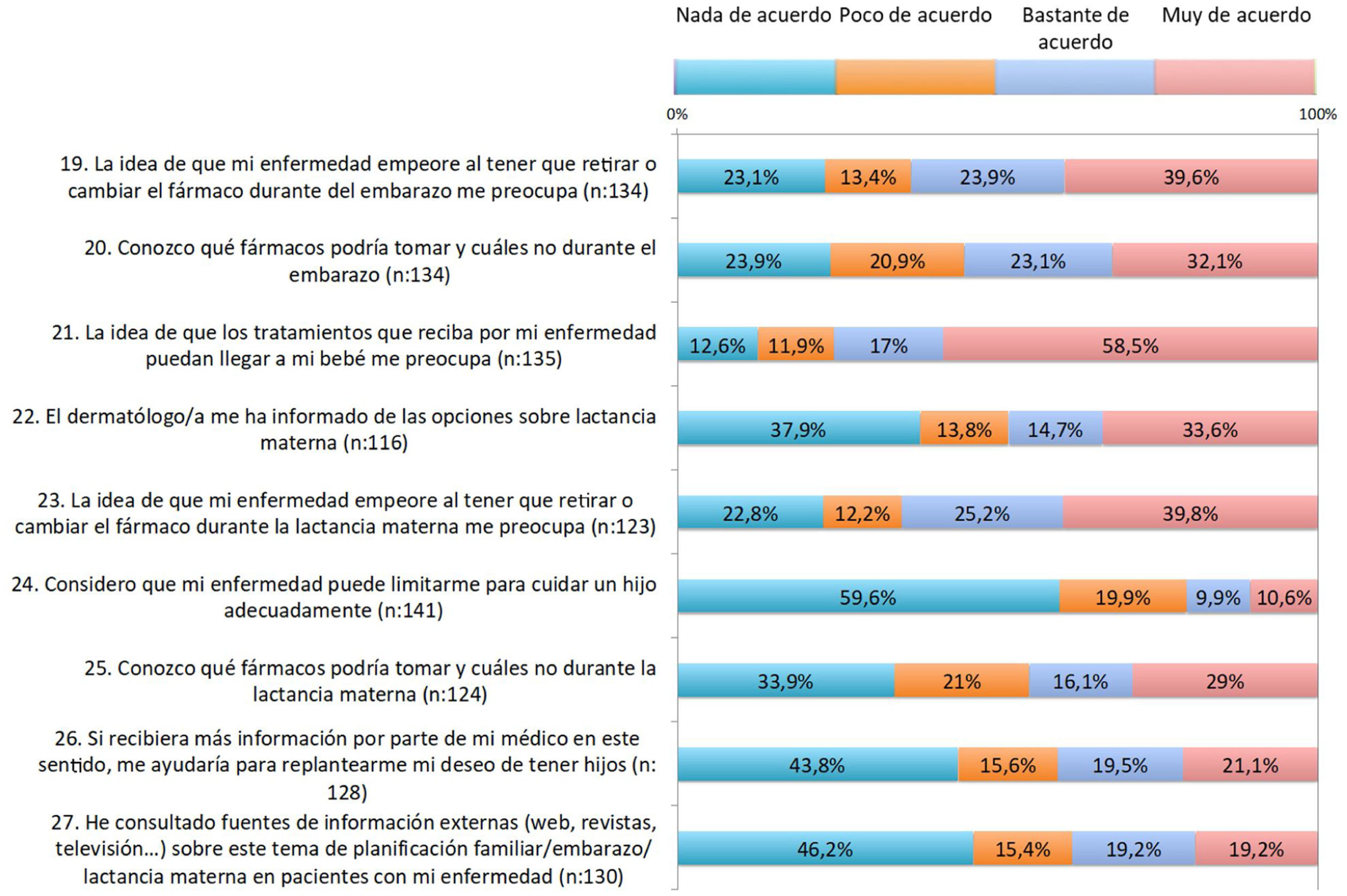
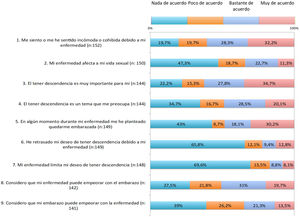
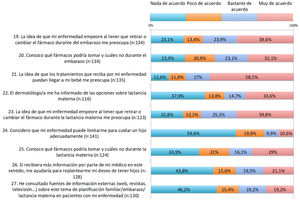
Los resultados del cuestionario sobre planificación familiar se resumen en las figuras 1, 2, 3.
Respecto impacto de la enfermedad, más de 30% de las pacientes estaba bastante o muy de acuerdo con la afirmación de que la enfermedad puede afectar a su vida sexual (ítem 2). Para 35%, la enfermedad retrasa o limita su deseo de descendencia (ítems 6-7); 20,5%, considera que la enfermedad puede limitarle para cuidar un hijo adecuadamente (ítem 24).
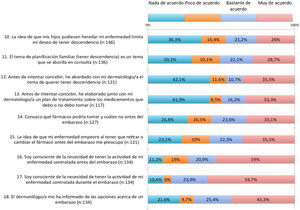
Respecto a las preocupaciones, en 55-65% existía preocupación de que la enfermedad empeore al tener que retirar o cambiar un fármaco antes del embarazo, durante el embarazo o durante la lactancia (ítems 15, 19 y 23). A alrededor de 60% le preocupaba que los tratamientos puedan dañar al bebé (ítem 21).
Respecto a la información recibida, cerca de la mitad de las pacientes consideraba que no se abordan en la consulta temas como la planificación familiar, el deseo gestacional o los tratamientos antes de concebir (ítems 11-13). Un tercio consideraba que conocía los fármacos que puede tomar y cuáles no antes del embarazo (ítem 14). Cerca de 60% era consciente de que la psoriasis tiene que estar controlada antes y durante el embarazo (ítems 16 -17). Una proporción relevante de pacientes no había recibido información sobre las opciones en el embarazo o la lactancia (ítems 18 y 22). Casi la mitad estaba bastante o muy de acuerdo con que si recibiera más información por parte del médico se replantearía el deseo de tener hijos.
Análisis en función de haber tenido algún embarazo/hijoLa actividad de la enfermedad medida por PASI o BSA, así como la calidad de vida por el DLQI, no era estadísticamente diferente en pacientes con o sin embarazos/hijos. La percepción de la actividad de la enfermedad según la paciente era superior a la percepción del médico tanto en aquellas que habían tenido embarazo/hijos (EVA media de la paciente 4,2 vs. 3,1 del médico; p = 0,001) como en las que no (EVA media de la paciente 3,1 vs. 2,3 del médico; p = 0,002).
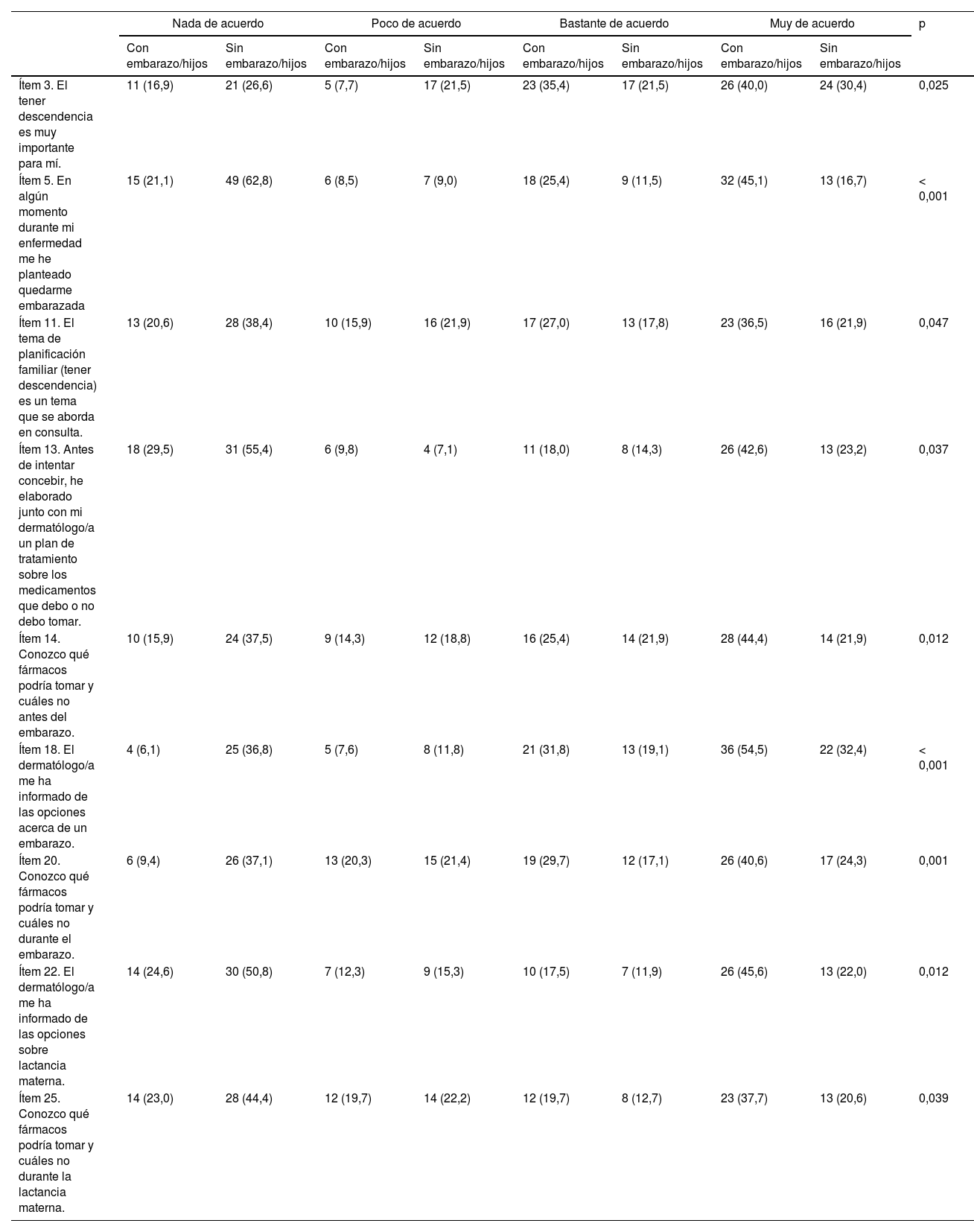
Había diferencias estadísticamente significativas en nueve cuestiones del cuestionario de planificación familiar entre las pacientes con o sin embarazos/hijos (tabla 2). Las diferencias indican una menor información de las pacientes sin embarazos/hijos sobre planificación familiar (ítem 11) o sobre la seguridad de los tratamientos antes del embarazo, durante el embarazo o durante la lactancia materna (ítems 14, 20 y 25) (tabla 2).
Diferencias entre mujeres con o sin embarazos/hijos en el cuestionario de planificación familiar
| Nada de acuerdo | Poco de acuerdo | Bastante de acuerdo | Muy de acuerdo | p | |||||
|---|---|---|---|---|---|---|---|---|---|
| Con embarazo/hijos | Sin embarazo/hijos | Con embarazo/hijos | Sin embarazo/hijos | Con embarazo/hijos | Sin embarazo/hijos | Con embarazo/hijos | Sin embarazo/hijos | ||
| Ítem 3. El tener descendencia es muy importante para mí. | 11 (16,9) | 21 (26,6) | 5 (7,7) | 17 (21,5) | 23 (35,4) | 17 (21,5) | 26 (40,0) | 24 (30,4) | 0,025 |
| Ítem 5. En algún momento durante mi enfermedad me he planteado quedarme embarazada | 15 (21,1) | 49 (62,8) | 6 (8,5) | 7 (9,0) | 18 (25,4) | 9 (11,5) | 32 (45,1) | 13 (16,7) | < 0,001 |
| Ítem 11. El tema de planificación familiar (tener descendencia) es un tema que se aborda en consulta. | 13 (20,6) | 28 (38,4) | 10 (15,9) | 16 (21,9) | 17 (27,0) | 13 (17,8) | 23 (36,5) | 16 (21,9) | 0,047 |
| Ítem 13. Antes de intentar concebir, he elaborado junto con mi dermatólogo/a un plan de tratamiento sobre los medicamentos que debo o no debo tomar. | 18 (29,5) | 31 (55,4) | 6 (9,8) | 4 (7,1) | 11 (18,0) | 8 (14,3) | 26 (42,6) | 13 (23,2) | 0,037 |
| Ítem 14. Conozco qué fármacos podría tomar y cuáles no antes del embarazo. | 10 (15,9) | 24 (37,5) | 9 (14,3) | 12 (18,8) | 16 (25,4) | 14 (21,9) | 28 (44,4) | 14 (21,9) | 0,012 |
| Ítem 18. El dermatólogo/a me ha informado de las opciones acerca de un embarazo. | 4 (6,1) | 25 (36,8) | 5 (7,6) | 8 (11,8) | 21 (31,8) | 13 (19,1) | 36 (54,5) | 22 (32,4) | < 0,001 |
| Ítem 20. Conozco qué fármacos podría tomar y cuáles no durante el embarazo. | 6 (9,4) | 26 (37,1) | 13 (20,3) | 15 (21,4) | 19 (29,7) | 12 (17,1) | 26 (40,6) | 17 (24,3) | 0,001 |
| Ítem 22. El dermatólogo/a me ha informado de las opciones sobre lactancia materna. | 14 (24,6) | 30 (50,8) | 7 (12,3) | 9 (15,3) | 10 (17,5) | 7 (11,9) | 26 (45,6) | 13 (22,0) | 0,012 |
| Ítem 25. Conozco qué fármacos podría tomar y cuáles no durante la lactancia materna. | 14 (23,0) | 28 (44,4) | 12 (19,7) | 14 (22,2) | 12 (19,7) | 8 (12,7) | 23 (37,7) | 13 (20,6) | 0,039 |
Los resultados se muestran como n (%) dentro de cada grupo: «Con embarazo/hijos» o «Sin embarazo/hijos».
La percepción de la actividad de la enfermedad según la paciente era superior a la del médico tanto en aquellas pacientes que recibían tratamiento biológico (EVA media de la paciente 2,6 vs. 1,9 del médico; p = 0,009) como en las que no (EVA 5,3 vs. 3,9; p < 0,001).
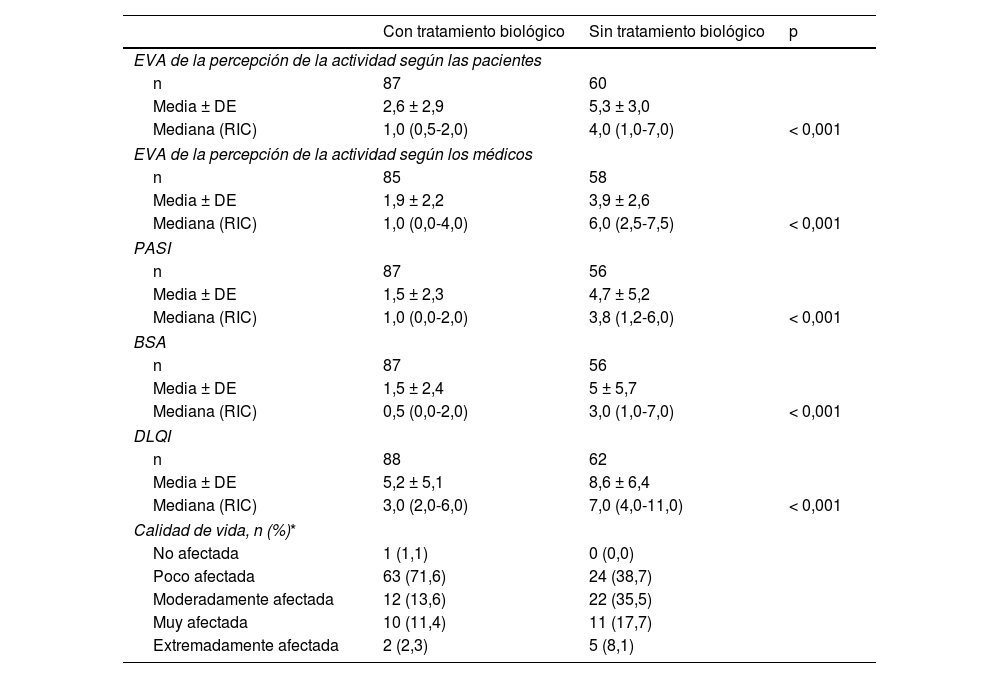
La percepción de la actividad por parte de la paciente y del médico, así como la gravedad medida por PASI y por BSA, era estadísticamente inferior en las pacientes que recibían tratamiento biológico (tabla 3). La calidad de vida medida por DLQI era significativamente mejor en pacientes en tratamiento con biológicos. Cualitativamente también se observa que la calidad de vida era superior en las pacientes que recibían tratamiento biológico (tabla 3).
Diferencias en la actividad de la psoriasis y la calidad de vida en mujeres con o sin tratamiento biológico
| Con tratamiento biológico | Sin tratamiento biológico | p | |
|---|---|---|---|
| EVA de la percepción de la actividad según las pacientes | |||
| n | 87 | 60 | |
| Media ± DE | 2,6 ± 2,9 | 5,3 ± 3,0 | |
| Mediana (RIC) | 1,0 (0,5-2,0) | 4,0 (1,0-7,0) | < 0,001 |
| EVA de la percepción de la actividad según los médicos | |||
| n | 85 | 58 | |
| Media ± DE | 1,9 ± 2,2 | 3,9 ± 2,6 | |
| Mediana (RIC) | 1,0 (0,0-4,0) | 6,0 (2,5-7,5) | < 0,001 |
| PASI | |||
| n | 87 | 56 | |
| Media ± DE | 1,5 ± 2,3 | 4,7 ± 5,2 | |
| Mediana (RIC) | 1,0 (0,0-2,0) | 3,8 (1,2-6,0) | < 0,001 |
| BSA | |||
| n | 87 | 56 | |
| Media ± DE | 1,5 ± 2,4 | 5 ± 5,7 | |
| Mediana (RIC) | 0,5 (0,0-2,0) | 3,0 (1,0-7,0) | < 0,001 |
| DLQI | |||
| n | 88 | 62 | |
| Media ± DE | 5,2 ± 5,1 | 8,6 ± 6,4 | |
| Mediana (RIC) | 3,0 (2,0-6,0) | 7,0 (4,0-11,0) | < 0,001 |
| Calidad de vida, n (%)* | |||
| No afectada | 1 (1,1) | 0 (0,0) | |
| Poco afectada | 63 (71,6) | 24 (38,7) | |
| Moderadamente afectada | 12 (13,6) | 22 (35,5) | |
| Muy afectada | 10 (11,4) | 11 (17,7) | |
| Extremadamente afectada | 2 (2,3) | 5 (8,1) | |
No puede realizarse ningún test de significación estadística porque 40% de las celdas tienen una frecuencia esperada inferior a 5.
BSA: Body Surface Area; DE: desviación estándar; DLQI: Dermatology Life Quality Index; EVA: escala visual analógica; PASI: Psoriasis Area Severity Index; RIC: rango intercuartílico.
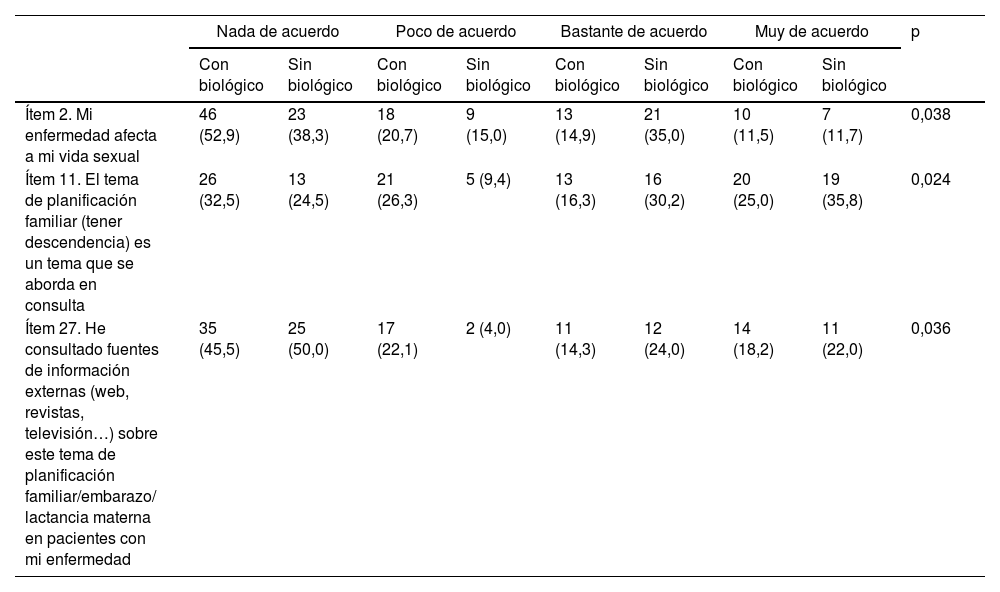
Hubo diferencias estadísticamente significativas en tres ítems del cuestionario de planificación familiar (tabla 4). Las pacientes sin tratamiento biológico referían una mayor afectación de la vida sexual (ítem 2) y una mayor necesidad de búsqueda de información externa (ítem 27) (tabla 4).
Diferencias entre mujeres con o sin tratamiento biológico en el cuestionario de planificación familiar
| Nada de acuerdo | Poco de acuerdo | Bastante de acuerdo | Muy de acuerdo | p | |||||
|---|---|---|---|---|---|---|---|---|---|
| Con biológico | Sin biológico | Con biológico | Sin biológico | Con biológico | Sin biológico | Con biológico | Sin biológico | ||
| Ítem 2. Mi enfermedad afecta a mi vida sexual | 46 (52,9) | 23 (38,3) | 18 (20,7) | 9 (15,0) | 13 (14,9) | 21 (35,0) | 10 (11,5) | 7 (11,7) | 0,038 |
| Ítem 11. El tema de planificación familiar (tener descendencia) es un tema que se aborda en consulta | 26 (32,5) | 13 (24,5) | 21 (26,3) | 5 (9,4) | 13 (16,3) | 16 (30,2) | 20 (25,0) | 19 (35,8) | 0,024 |
| Ítem 27. He consultado fuentes de información externas (web, revistas, televisión…) sobre este tema de planificación familiar/embarazo/ lactancia materna en pacientes con mi enfermedad | 35 (45,5) | 25 (50,0) | 17 (22,1) | 2 (4,0) | 11 (14,3) | 12 (24,0) | 14 (18,2) | 11 (22,0) | 0,036 |
Los resultados se muestran como n (%) dentro de cada grupo: «Con tratamiento biológico» o «Sin tratamiento biológico».
El PASI y la BSA eran estadísticamente inferiores en el grupo de pacientes que perciben la actividad como leve vs. moderada/intensa (PASI medio 1,5 vs. 4,8 puntos; p < 0,001; BSA medio 1,0 vs. 4,9 puntos; p < 0,001). La calidad de vida era mejor en el grupo de pacientes que percibían la actividad como leve (DLQI medio 3,4 vs. 9,9; p < 0,001). En el cuestionario de planificación familiar solo hubo diferencias en relación con el impacto de la enfermedad en la vida sexual (ítem 2), siendo mayor en las que presentaban enfermedad moderada/intensa que leve (46 vs. 24%, respectivamente).
Análisis en función de la actividad de la psoriasis según el médicoEl PASI y la BSA fueron estadísticamente inferiores en el grupo de pacientes con actividad leve vs. actividad moderada/intensa (PASI medio 1,4 vs. 5,9; p < 0,001; BSA medio: 0,8 vs. 6,5; p < 0,001). La calidad de vida media era mejor en el grupo de pacientes con actividad leve (DLQI medio: 4,4 vs. 10; p < 0,001). No hubo diferencias significativas en ninguna cuestión del cuestionario de planificación familiar.
DiscusiónEstudios recientes indican que las mujeres con psoriasis moderada-grave en España tienen menores tasas de embarazo7 y son menos proclives a la lactancia materna que la población general8. Las causas de esto pueden ser múltiples: causas psicológicas, sentimientos de baja autoestima, estigmatización y disminución de la confianza que conduzca a una disfunción sexual, factores sociales y familiares, preocupación por la seguridad de los tratamientos para el feto, etc.7,8 En nuestra encuesta, más de 40% de las pacientes consideraban que si recibieran más información por parte del médico se replantearían el deseo de tener hijos. Por ello, en línea con consensos recientes13, consideramos que se debería ser más proactivos en facilitar esta información (tabla 5).
Puntos a discutir en la consulta relacionados con la planificación familiar
| Antes de la concepción | Relacionados con el embarazo | Tras el parto |
|---|---|---|
| • Problemas en la esfera sexual relacionados con la psoriasis• Retrasos o limitaciones en el deseo gestacional debido a la psoriasis o sus tratamientos• Necesidad de tener la enfermedad controlada antes de la concepción• Tratamientos a evitar antes de la concepción | • Necesidad de tener la enfermedad controlada durante el embarazo• Preocupaciones por:° La evolución de la psoriasis durante el embarazo° La evolución de la psoriasis si se retira un tratamiento° Complicaciones para la madre secundarias a la psoriasis o su tratamiento° Complicaciones para el feto secundarias a la psoriasis o su tratamiento• Tratamientos a evitar durante el embarazo | • Evolución de la psoriasis después del embarazo• Posibilidad de lactancia materna• Preocupaciones por si los hijos heredan la psoriasis• Preocupaciones por si la psoriasis limita el cuidado adecuado del hijo• Tratamientos a evitar durante la lactancia |
Fuentes de información fidedigna sobre la planificación familiar en mujeres con psoriasis (como información proveniente de sociedades científicas o asociaciones de pacientes con información contrastadas por especialistas).
En mujeres, la psoriasis se diagnostica de media a los 28 años y el inicio del tratamiento se produce entre los 28-45 años, lo que coinciden con los años de máxima actividad reproductiva5. En nuestro estudio, las pacientes tienen una edad media de 35,4 años y llevan 16,7 años de evolución de la psoriasis, así que es un grupo representativo de mujeres en plena edad reproductiva. La enfermedad tiene un gran impacto físico y emocional en las mujeres y afecta a su calidad de vida (en mayor medida que a los hombres), a sus relaciones íntimas y produce mucha incertidumbre sobre los posibles efectos de la enfermedad en la maternidad3,5. Estos aspectos son poco conocidos y podrían estar infravalorados en la práctica clínica5,6.
Nuestra cohorte reúne pacientes con una carga significativa de enfermedad. En aproximadamente un 1/3 de las pacientes el impacto de la enfermedad retrasa o limita su deseo de tener hijos. La encuesta pone en evidencia algunas preocupaciones que podrían explicar estos miedos, relacionados principalmente con la seguridad de los tratamientos, la evolución de la enfermedad y la falta de información. A la gran mayoría de las mujeres les preocupaba que los tratamientos pudieran dañar al bebé, pero también les preocupaba que la enfermedad empeore al tener que retirar o cambiar el tratamiento antes o durante el embarazo o en la lactancia.
Los datos sugieren que la información que se da en la consulta de dermatología sobre planificación familiar, deseo gestacional o seguridad de los tratamientos es insuficiente tanto antes de concebir, como durante la gestación o la lactancia, especialmente en mujeres sin embarazos previos. Consideramos que todas las mujeres en edad fértil deberían recibir información suficiente en la consulta. Además, hasta 50% de los embarazos no son planificados, por ello, en línea con otros autores5, consideramos que puede ser recomendable un plan de tratamiento compatible con el embarazo en las mujeres en edad fértil, independientemente de las intenciones de planificación familiar. Además, sería importante capacitar y mejorar el papel informador de los dermatólogos sobre la planificación familiar.
Los resultados sugieren que las mujeres en tratamiento biológico están mejor controladas y tienen mejor calidad de vida y menos impacto de la enfermedad en la vida sexual que las pacientes sin tratamiento biológico. El tratamiento de la psoriasis durante el embarazo y la lactancia supone un reto para el clínico3,13,14. Aunque hay numerosas terapias con potencial efecto teratogénico que hay que retirar antes de la concepción13, existen tratamientos disponibles que se pueden utilizar de forma segura durante el embarazo y la lactancia, y deberíamos informar a las pacientes al respecto. Entre los tratamientos biológicos, certolizumab pegol es la opción más segura tanto en embarazo como en la lactancia, dada su transferencia mínima o nula a través de la placenta y a la leche materna16,17,20. En mujeres embarazadas tratadas con biológicos, se puede mantener el tratamiento durante el primer y segundo trimestres y valorar con la paciente los riesgos y beneficios de continuar con ellos durante el tercer trimestre. Sin embargo, las pacientes que reciben certolizumab pegol podrían usarlo durante todo el embarazo si se considera clínicamente necesario, así como durante la lactancia13.
Tanto en mujeres sanas20 como en mujeres con otras enfermedades crónicas21 existen evidencias de que el comportamiento en relación con el embarazo está influido por su percepción del riesgo22. Las diferentes enfermedades crónicas introducen diversos riesgos de embarazo y la percepción del riesgo es única para cada individuo y no se basa únicamente en información objetiva sobre el riesgo20. Por ello se necesita más investigación para comprender las percepciones de riesgo de las mujeres en enfermedades crónicas específicas y mejorar la información que se proporciona a las pacientes sobre los riesgos objetivos20. En el caso concreto de la psoriasis existen guías recientes para el manejo de las pacientes13.
Nuestro estudio tiene limitaciones. Es un estudio observacional, descriptivo y transversal que carece de grupo de control con mujeres sin psoriasis o pacientes con psoriasis varones. Sin embargo, creemos que es una muestra representativa de las mujeres en edad fértil atendidas en las consultas de dermatología en España y que dan algunas claves de sus necesidades e inquietudes en relación con la planificación familiar. Con estos resultados, consideramos fundamental incrementar la información que se da a las pacientes en las consultas.
ConclusionesLos resultados de nuestro estudio sugieren que la psoriasis tiene un impacto en la planificación familiar y en el deseo gestacional de las pacientes. Existen preocupaciones que podrían llevar a retrasar o limitar el deseo gestacional. La información proporcionada sobre estos temas durante el seguimiento no resulta completa.
FinanciaciónEste estudio estuvo financiado con una beca sin restricciones de la Cátedra Universidad Francisco de Vitoria-UCB en Inflamación y Salud Ósea.
Conflicto de interesesNatalia Jiménez Gómez ha actuado como asesora y/o investigadora y/o ponente para: Abbvie, Almirall, BMS, Celgene, Janssen, LEO Pharma, Lilly, MSD, Novartis y UCB.
Ricardo Ruiz-Villaverde ha recibido honorarios por consultoría de Abbvie, Novartis, UCB, Celgene y Janssen.
María Luisa Alonso Pacheco de Abbvie, Novartis, Lilly, LEO Pharma, UCB, Celgene y Janssen.
Rosa María Izu ha sido consultor, asesor, impartido ponencias o participado en ensayos clínicos para Almirall, Novartis, Abbvie, Lilly, LEO Pharma, UCB, Sanofi, Celgene, Pfizer, Janssen y Kyowa-Kirin.
Raquel Rivera-Díaz ha recibido honorarios como investigador/consultor para: Abbvie, Boehringer Ingelheim, Celgene, Janssen, LEO Pharma, Lilly, Novartis, Pfizer, Novartis, UCB.
Jordi Mollet Sanchez ha recibido honorarios como investigador/consultor para: Abbvie, Amgen, Boehringer Ingelheim, Celgene, Janssen, LEO Pharma, Lilly, Novartis, Pfizer, Sanofi, UCB.
Mar Llamas-Velasco ha recibido honorarios como investigador/consultor para Abbvie, Boehringer Ingelheim, Celgene, Janssen, LEO Pharma, Lilly, Kyowa Kirin, Novartis, Pfizer, Novartis, UCB.
Álvaro González-Cantero ha recibido honorarios como investigador/consultor para Abbvie, Amgen, Celgene, Janssen, LEO Pharma, Lilly, Novartis, Novartis, UCB.
Pablo de la Cueva ha actuado como asesor y/o investigador y/o ponente de Abbvie, Almirall, BMS, Boehringer, Celgene, Janssen, LEO Pharma, Lilly, MSD, Novartis, Pfizer, Roche, Sanofi, UCB.
Elena Martínez Lorenzo ha recibido honorarios como consultor para Abbvie, Almirall, Janssen, LEO Pharma, Novartis, UCB. Además, ha impartido ponencias o participado en formaciones con Abbvie, Almirall, Celgene, Janssen, LEO Pharma, Lilly, Novartis, Roche, UCB.
Ofelia Baniandrés Rodríguez ha recibido honorarios como investigador/consultor para: Abbvie, Amgen, Celgene, Janssen, LEO Pharma, Lilly, Novartis, Pfizer, UCB.
Gerard Pitarch Bort ha participado en estudios y ensayos clínicos de Abbvie, Janssen, Novartis y UCB. Ha recibido honorarios como ponente de Abbvie, Janssen, LEO Pharma, Novartis y ayudas para formación de Abbvie, Almirall, Janssen, Novartis y UCB.
Agradecemos a la Cátedra de Inflamación y Salud Ósea UFV-UCB su apoyo en la difusión de los resultados del presente estudio.
Agradecemos al Dr. Pablo Rivas el soporte editorial prestado en la redacción de este artículo en nombre de la Universidad Francisco de Vitoria (Madrid).