La psoriasis es una enfermedad inflamatoria crónica de la piel de carácter sistémico que presenta múltiples comorbilidades, como artritis psoriásica y enfermedades cardiovasculares que pueden incluso reducir la esperanza de vida, y se acompaña de una gran carga física, mental y social1. Actualmente el arsenal terapéutico para la psoriasis moderada-grave es muy extenso: fototerapia, fármacos sistémicos convencionales (ciclosporina, metotrexato, acitretina, fumaratos), moléculas sintéticas de nueva generación (apremilast y próximamente deucravacitinib) y terapias biológicas incluyendo algunos biosimilares (adalimumab, etanercept, infliximab, certolizumab, ustekinumab, secukinumab, ixekizumab, brodalumab, tildrakizumab, guselkumab, risankizumab y próximamente bimekizumab). Sin embargo, no todos los pacientes responden igual al tratamiento y, por otro lado, el acceso a los tratamientos más eficaces (la terapia biológica) suele estar restringido a un número pequeño de pacientes con psoriasis moderada-grave. Además, el alto impacto económico de las nuevas terapias biológicas ha favorecido que actores no clínicos, como gestores y pagadores, sean elementos de peso en la elección de estos tratamientos2. Para la prescripción de la terapia biológica hay establecidos una serie de requisitos que para algunos pacientes suponen un retraso en recibir su primer fármaco biológico; esto puede suponer una pérdida de oportunidad de conseguir respuestas más permanentes e incluso de evitar la progresión a formas más graves de la enfermedad, como la afectación articular3.
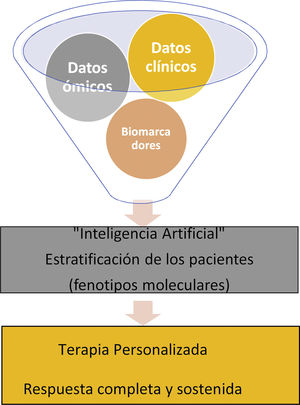
La medicina de precisión o medicina estratificada persigue la elección del tratamiento según las características individuales del paciente, como un traje a medida4. Esta estrategia es bien conocida desde hace años en el mundo de la oncología, como el uso de inhibidores de BRAF en pacientes con melanoma BRAF mutado que han demostrado un aumento en la supervivencia en fases avanzadas combinados con un inhibidor de MEK5, pero no tanto en las enfermedades inflamatorias inmunomediadas, mucho más heterogéneas y que requieren un tratamiento crónico a veces de por vida y con frecuencia de alto coste. La medicina tradicional se basa en el uso de patrones clínicos para diagnosticar una enfermedad y en el método ensayo-error para seleccionar el tratamiento. En la medicina de precisión, en función de múltiples datos multi-ómicos combinados con datos clínicos obtenidos y analizados gracias a los avances tecnológicos actuales, se clasifican a los pacientes en distintos fenotipos moleculares (o endotipos) para la elección de tratamientos dirigidos y personalizados, que permitan un aclaramiento prolongado de la enfermedad en todos los pacientes y de una manera coste-efectiva. La medicina de precisión se basa en la idea de que hay subpoblaciones dentro de una categoría de enfermedad que pueden ser identificadas por biomarcadores, preferiblemente antes de iniciar el tratamiento o en las fases más iniciales6 (fig. 1).
Los avances en el conocimiento en diferentes aspectos de la psoriasis, así como el desarrollo de la inteligencia artificial, permiten que esta individualización pueda empezar a aplicarse en la práctica diaria. Por ejemplo, en el campo de la genética la presencia del alelo Human Leukocyte Antigen (HLA)-Cw6 se ha relacionado con una afectación cutánea más extensa, con un comienzo precoz de la enfermedad y con un menor riesgo de desarrollar artritis psoriásica7; también con una mejor respuesta a metotrexato8 y ustekinumab9 y su ausencia con una mejor respuesta a adalimumab10. Respecto a secukinumab, hay resultados discordantes, estudios que no encuentran asociación11 frente a otros que sí observan una excelente respuesta en pacientes con HLA-Cw612. Con los nuevos inhibidores de IL23 hay poca información, nosotros no hemos encontrado relación entre la efectividad y la presencia o no de HLA-Cw6 (observación personal). Por otro lado, el hallazgo de mutaciones en formas de psoriasis pustulosa en los genes IL36RN, AP1S3 y CARD14, ha permitido encontrar nuevas dianas terapéuticas frente a IL-1 e IL-36 que están en fases avanzadas de investigación13. En relación al tratamiento, los niveles de adalimumab y ustekinumab en una fase temprana podrían usarse para predecir y mejorar los resultados en los pacientes14–15. Respecto al fenotipo de los pacientes, también puede ser de utilidad al seleccionar el tratamiento; en el registro BIOBADADERM, las mujeres tenían más riesgo de acontecimientos adversos, pero la supervivencia de los tratamientos era similar a la de los varones16. También en este registro español encontramos que el aumento de índice de masa corporal se asociaba a una mayor discontinuación del tratamiento por falta de efectividad y mayor riesgo de acontecimientos adversos17. Por otro lado, la influencia del exposoma (ambiente + estilo de vida) en el curso de la enfermedad y la respuesta al tratamiento también es interesante, por ser factores potencialmente modificables. Hay una relación directa entre el tabaco y la prevalencia y gravedad de la psoriasis18, también fumar se asocia a una menor eficacia de las terapias biológicas19. Respecto al alcohol, también es más frecuente en pacientes con psoriasis y, además, puede ser un desencadenante de brotes20.
El disponer de biomarcadores, que probablemente surgirán de una combinación de datos demográficos, fenotípicos, genómicos y bioquímicos ayudará a comprender mejor la historia natural de la psoriasis, los factores pueden predecir su aparición y los brotes, el desarrollo de comorbilidades y la respuesta a la terapia de cada individuo. Hoy en día tenemos la oportunidad de aprovechar los datos de registros y el uso de la salud digital, permitirá la recopilación de datos en remoto y/o continuo que, junto con los avances en la inteligencia artificial, permitirán desarrollar algoritmos para enfocar de forma individualizada el manejo de los pacientes con psoriasis, como ya recomendaba la Organización Mundial de la Salud en el año 2016, en su informe global dedicado a esta enfermedad21. Se trata, en definitiva, de seleccionar el fármaco correcto, para el paciente correcto y en el momento correcto.
Conflictos de interesesEl Dr. Rivera-Díaz ha participado como asesor/ponente/investigador en ensayos clínicos promovidos por compañías que producen fármacos para el tratamiento de psoriasis, incluyendo Janssen Pharmaceuticals Inc, Almirall SA, Boehringer-Ingelheim, Lilly, AbbVie, Novartis, Celgene, Biogen Amgen, Leo-Pharma y UCB.
El Dr. Belinchón ha participado como asesor/ponente/investigador en ensayos clínicos promovidos por compañías que producen fármacos para el tratamiento de psoriasis, incluyendo Janssen Pharmaceuticals Inc, Almirall SA, Lilly, AbbVie, Novartis, Celgene, Biogen Amgen, Leo-Pharma, Pfizer-Wyeth, MSD y UCB.