La leiomiomatosis cutánea y uterina múltiple (MCUL) o síndrome de Reed se caracteriza por la presencia de leiomiomas cutáneos de origen pilar, leiomiomas uterinos en las mujeres y, en algunos casos, asociación con carcinoma renal. Este síndrome, de herencia autosómica dominante, se produce por una mutación heterocigótica en la línea germinal del gen de la fumarato hidratasa, una enzima del ciclo de Krebs que actúa como supresor tumoral.
ObjetivoRevisar los casos de MCUL diagnosticados en 2 hospitales universitarios durante un periodo de 5 años (2008-2013).
Material y métodosEstudio retrospectivo de 13 casos de MCUL, en el que se recogieron características demográficas, clínicas e histológicas, así como posibles asociaciones con otras enfermedades y tratamientos recibidos.
ResultadosTrece pacientes fueron diagnosticados de MCUL (10 mujeres y 3 hombres, con una edad media al diagnóstico de 53 años). El 100% de los casos presentaba leiomiomas cutáneos múltiples, distribuidos de forma difusa (69%), agrupada (92%) y/o lineal (7,7%). El 90% de las mujeres presentaba además miomas uterinos y todas ellas habían precisado histerectomía por ese motivo. No encontramos ningún caso de carcinoma renal en los pacientes explorados (9/13), pero sí lesiones renales benignas (4/9).
ConclusiónDescribimos 13 casos de MCUL, que presentan características clínicas e histológicas similares a las descritas en la literatura, siendo la manifestación cutánea más frecuente la segmentaria tipo 2. Es importante que el dermatólogo identifique los casos de leiomiomas cutáneos y conozca su posible relación con MCUL.
Multiple cutaneous and uterine leiomyomatosis (MCUL), or Reed syndrome, is characterized by the presence of cutaneous leiomyomas arising from the arrector pili muscles and, in women, by uterine leiomyomas. In some cases, MCUL is associated with renal cell carcinoma. This syndrome is an autosomal dominant disorder caused by a heterozygous germline mutation of the gene that encodes fumarate hydratase, a Krebs cycle enzyme that acts as a tumor suppressor.
ObjectiveTo review the cases of MCUL diagnosed at 2 university hospitals over a 5-year period (2008-2013).
Material and methodsThis was a retrospective study of 13 cases of MCUL that investigated demographic, clinical, and histologic characteristics, as well as possible associations with other diseases and treatments received.
ResultsWe identified 13 patients (10 women and 3 men) who had been diagnosed with MCUL. The mean age at diagnosis was 53 years. All the patients had multiple cutaneous leiomyomas; in 12 (92%) the distribution was clustered and 9 (69%) also had disseminated solitary lesions. In 1 patient (7.7%), the pattern of distribution was linear. Uterine fibroids requiring hysterectomy were present in 90% of the women. Nine patients were screened for renal lesions; no cases of renal cell carcinoma were detected but benign renal lesions were found in 4 patients.
ConclusionThe clinical and histologic characteristics of the 13 cases of MCUL reviewed were similar to those reported in the literature. The most common cutaneous manifestation was a type 2 segmental pattern. It is important for dermatologists to identify cutaneous leiomyomas and be aware of the possible association with MCUL.
La leiomiomatosis cutánea y uterina múltiple (MCUL), también conocida como leiomiomatosis múltiple, síndrome de Reed y leiomiomatosis cutis et uteri, fue descrita en 1973 por Reed et al. Se caracteriza por presentar leiomiomas cutáneos de origen pilar en ambos sexos y leiomiomas uterinos en las mujeres. Además, existe una variante asociada al carcinoma renal que se conoce como leiomiomatosis hereditaria y carcinoma de células renales (HLRCC)1.
Tanto la MCUL como la HLRCC se deben a una mutación heterocigótica del gen de la fumarato hidratasa (FH), localizado en el cromosoma 1q42.3-q432,3.
El objetivo de este estudio es presentar nuestra experiencia en MCUL, discutiendo sus características, asociaciones y tratamientos.
Material y métodosPacientes diagnosticados de MCUL en los servicios de dermatología del Hospital Universitari Sagrat Cor y del Hospital del Mar durante el periodo 2008-2013, considerando como criterio diagnóstico los pacientes con lesiones clínicamente compatibles con leiomiomas cutáneos múltiples (≥10 lesiones) y confirmación histológica de una lesión o más.
Se determinaron características demográficas, clínicas e histológicas, y los antecedentes personales y familiares de leiomiomas uterinos, lesiones renales y neoplasias renales. Los datos se recogieron de la historia clínica, y en algunos casos se contactó con los pacientes para ser visitados, pudiendo reevaluar las lesiones y completar la historia.
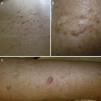
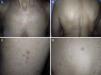
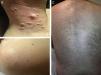
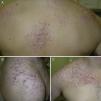
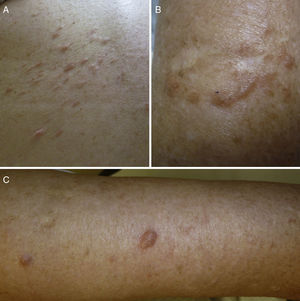
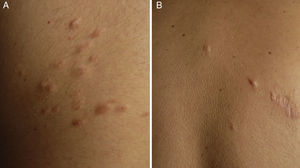
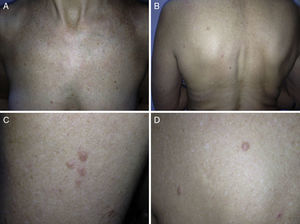
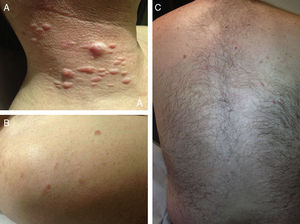
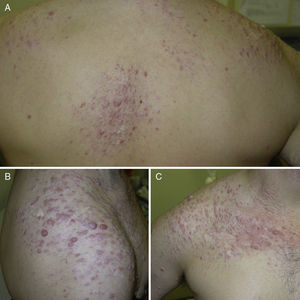
ResultadosIdentificamos 13 pacientes (10 mujeres y 3 hombres) con leiomiomas cutáneos múltiples. La media de edad del diagnóstico fue de 53 años (36-76). Todos los pacientes presentaban lesiones cutáneas, que en el 92% de los casos fueron el motivo de consulta (12/13 pacientes). La media de edad de aparición de las lesiones cutáneas fue 40 años (14-53), si bien en 4 pacientes no se pudo determinar la edad de aparición. En 12 pacientes los leiomiomas cutáneos estaban distribuidos agrupados en forma de placa y 9 de ellos presentaban además lesiones aisladas dispersas. Las placas de leiomiomas agrupados estaban localizadas en la zona pectoral (5 casos), el cuello (4 casos), la espalda (3 casos), la extremidad superior (3 casos) y el abdomen (un caso), y las lesiones aisladas se localizaban en el tronco, las extremidades superiores e inferiores (figs. 1–4). Cabe destacar que el caso número 7 era muy extenso, presentando múltiples placas en el tronco (fig. 5). En un caso las lesiones estaban distribuidas de forma lineal únicamente en la zona del deltoides. En cuanto a la sintomatología de los leiomiomas cutáneos 5 casos eran dolorosos (uno de ellos especialmente con el frío y otros 2 de manera constante), un caso presentaba molestias y prurito ocasional y el resto eran asintomáticos.
El tipo histológico más frecuente fue el piloleiomioma (12/13), encontrándose un caso de leiomioma vascular. La inmunohistoquímica fue positiva para actina y desmina en los 2 casos en los que se realizó.
En cuanto a los leiomiomas uterinos, 9 de 10 mujeres (90%) habían desarrollado miomas, todas ellas habían precisado histerectomía previamente al diagnóstico de MCUL.
Se realizó screening de las lesiones renales en 9/13 pacientes, de los cuales 4 presentaban lesiones renales (quistes, litiasis o nódulo suprarrenal), pero no se encontró ningún caso de carcinoma renal. En 4 casos no se realizaron estudios de imagen para descartar afectación renal, pero los pacientes están asintomáticos.
Al revisar la asociación con otras enfermedades y procesos se encontró un caso afecto de hipogonadismo hipogonadotropo (caso 7), que consideramos asociación casual. Se registraron los antecedentes familiares en 12 pacientes, de los cuales el 92% (11/12) presentaban un familiar o más afecto de leiomiomas cutáneos y/o uterinos. No se encontró ningún caso de carcinoma renal, pero sí un caso de un familiar de primer grado que falleció a causa de un cáncer de origen indeterminado a los 35 años. En cuanto al tratamiento, el 30% (4/13) de los pacientes no precisaron tratamiento, al 38% (5/13) se les extirparon de una a 3 lesiones por sintomatología clínica o motivos estéticos, el 30% (4/13) recibió tratamiento con crioterapia, siendo esta de baja o nula efectividad, y 2 pacientes recibieron tratamiento ablativo con electrocoagulación o láser de CO2. Los 2 pacientes que presentaban afectación más extensa requirieron tratamientos múltiples para aliviar la sintomatología, incluyendo fármacos sistémicos como nifedipino, pregabalina, doxazosina y gabapentina, obteniéndose escasa mejoría. Las características de los pacientes se resumen en la tabla 1.
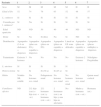
Características demográficas, clínicas y tratamiento de los 13 pacientes diagnosticados de MCUL
| Paciente | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|---|---|---|---|---|---|---|---|
| Sexo | M | M | M | M | M | H | H |
| Edad al Dx | 52 | 74 | 76 | 63 | 52 | 48 | 57 |
| L. cutáneos | Sí | Sí | Sí | Sí | Sí | Sí | Sí |
| Consulta por l. cutáneos? | Sí | No | Sí | Sí | Sí | Sí | Sí |
| Edad aparición | ND | ND | 50 | 40 | 49 | ND | ND |
| Dolor | Sí | No | Sí (frío) | No | Sí | ND | Sí |
| Distribución | Agrupados (3-4 en abdomen)+dispersos | Agrupados (placa en ES y espalda)+dispersos | Agrupados (placa en ES) | Agrupados (placa en espalda)+dispersos | Lineal en ES zona deltoides | Agrupados (placa en espalda)+dispersos | Agrupados (placas múltiples)+dispersos |
| Tratamiento | Exéresis 3 lesiones | No | No | No | No | Exéresis 2 lesiones | Nifedipino Pregabalina |
| L. uterinos | Sí | Sí | Sí | Sí | Sí | ||
| Histerectomía | Sí | Sí | Sí (30 a) | Sí (45 a) | Sí | ||
| Riñón | Nódulo SR, estable | No lesiones eco. renal | Poliquistosis renal | No lesiones eco. renal | No lesiones eco. renal | No lesiones eco. renal | Quiste renal cortical |
| Familiares afectos | ND | 2/2: hijo (cut.) e hija (cut.+ut.) | 2/2: hermano (cut.) y hermana (cut.+ut.) | 2 hermanas (cut.), un hijo y una hija no afectados | No | Madre y hermana (cut.+ut.) | Hermana (ut.) |
| Paciente | 8 | 9 | 10 | 11 | 12 | 13 |
|---|---|---|---|---|---|---|
| Sexo | M | M | M | M | M | H |
| Edad al Dx. | 48 | 51 | 37 | 55 | 36 | 40 |
| L. cutáneos | Sí | Sí | Sí | Sí | Sí | Sí |
| Consulta por l. cutáneos? | Sí | Sí | Sí | Sí | Sí | Sí |
| Edad aparición | 42 | 47 | 35 | 53 | 33 | 14 |
| Dolor | No (molestia y prurito ocasional) | No | No | No | No | Sí (los del cuello de forma constante) |
| Distribución | Agrupados (placa en ES)+dispersos (espalda y escote) | Agrupados (placa zona pectoral izq.) | Agrupados (placa zona pectoral y cuello+alguna dispersa (cuello) | Agrupados (cuello y zona pectoral izq.)+dispersas (cuello) | Agrupadas (zona pectoral der.) | Agrupados (placa laterocervical der.)+dispersos (tronco y EE) |
| Tratamiento | Exéresis una lesión | Exéresis una lesiónNitrógeno líquidoElectrocoagulación | Nitrógeno líquido | Nitrógenolíquido | Nitrógeno líquido | Exéresis 2 lesiones, láser de CO2, doxazosina, gabapentina vo. |
| L. uterinosHisterectomía | SíSí | SíSí | NoNo | SíSí | SíSí | |
| Riñón | No explorado | Litiasis izq. | Pendiente eco. renalCistitis | No lesiones eco. renal | No explorado | No explorado |
| Familiares afectos | Abuela (cut.+histerectomía), madre (falleció de cáncer indeterminado a los 35 años), 3 hijos sin lesiones | Una hermana (cut.+ut.) | Una hermana (ut.) | Una hija (histerectomía) | Una hermana (cut.+histerectomía) y 2 sobrinas (ut.) | Padre, abuela paterna (cut), tía paterna (cut). Hija sin lesiones |
Cut: cutáneos; Der: derecha; Dx: diagnóstico; Eco: ecografía; EE: extremidades; ES: extremidad superior; Izq: izquierda; L: leiomiomas; ND: no disponible; SR: suprarrenal; Ut: uterinos.
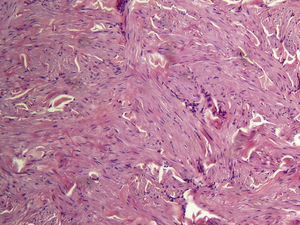
Los leiomiomas cutáneos son neoplasias benignas derivadas del músculo liso. Existen diferentes tipos, dependiendo de las fibras a partir de las que se originen: los angioleiomiomas (músculo liso vascular), los leiomiomas genitales (músculo liso de la piel genital) y los piloleiomiomas (músculo erector del pelo). Coincidiendo con lo observado en nuestro estudio, estos últimos son los que se encuentran de forma predominante en la MCUL4. Todos suelen ser solitarios (esporádicos), excepto los piloleiomiomas, que también pueden ser múltiples (esporádicos o familiares). Clínicamente las lesiones cutáneas de la MCUL son pápulas o nódulos de color piel, marronáceo o rosado, de 0,2-2cm, de crecimiento lento que aparecen a partir de la adolescencia hasta la cuarta década, pudiendo preceder, aparecer de forma simultánea o posterior a los leiomiomas uterinos. Afectan más frecuentemente al tronco o a la parte extensora de las extremidades, pudiendo presentarse en forma de lesiones aisladas, o diseminadas por diferentes zonas o agrupadas en un segmento cutáneo5,6. En línea con lo descrito previamente en la literatura7, la manifestación más frecuente que encontramos es la segmentaria tipo 2, con afectación más pronunciada de un segmento cutáneo y lesiones diseminadas distribuidas de forma simétrica. En nuestros pacientes hay un ligero predominio de lesiones asintomáticas, lo que contrasta con los casos publicados, en los que las lesiones eran más frecuentemente molestas o dolorosas8,9, sobre todo en respuesta a la presión, cambios de temperatura o estrés5. El diagnóstico se confirma con la histología, caracterizándose por fascículos de fibras de músculo liso entrelazadas con fibras de colágeno, distribuidos de forma irregular en la dermis y respetando la epidermis (fig. 6). Es característica la forma alargada del núcleo «en puro» de las células fusiformes. La inmunohistoquímica de estas células es positiva para actina y desmina10.
La mayoría de leiomiomas uterinos son esporádicos, siendo el tumor más frecuente en mujeres en edad reproductiva. Los que aparecen en la MCUL afectan al 76-100% de las mujeres con FH mutada8,9,11, se manifiestan de forma precoz antes de la cuarta década (media de 30 años, rango 18-52 años) y frecuentemente requieren histerectomía a edades tempranas (un estudio 44% ≤30 años)8. Esto coincide con lo observado en nuestras pacientes. Se ha descrito algún caso de transformación maligna a una variante muy agresiva de leiomiosarcoma12, no presente en nuestra serie.
Existe un aumento de incidencia de carcinoma renal entre familias de MCUL, siendo del 2 al 16% según diferentes autores8,13. Los casos de HLRCC presentan la misma mutación que los casos de MCUL2,3, pero todavía no se ha encontrado relación entre un determinado tipo de mutación y el aumento de riesgo de cáncer renal. El tipo más frecuente es el papilar tipo ii, de presentación más agresiva e inicio precoz (edad media de diagnóstico a los 44 años); afecta más frecuentemente a mujeres, suele ser unilateral y produce metástasis en el 50% de los casos. En comparación con el carcinoma renal esporádico, el asociado a HLRCC se presenta a edades más tempranas y tiene un mayor porcentaje de metástasis. También se han descrito otros tipos de tumores, como el carcinoma de conducto colector, el oncocitoma, el carcinoma de células claras y el tumor de Wilms14. Se diagnostica mediante pruebas de imagen, preferentemente TAC o RM, ya que el tipo papilar suele ser hipoecoico en la ecografía y puede ser interpretado como quiste. No encontramos ningún caso de carcinoma renal en nuestros pacientes, aunque como limitación, el cribado se realizó mediante ecografía. Si bien hubiera podido dejar algún caso infradiagnosticado, los pacientes que siguen controles ecográficos no han mostrado ningún cambio y se encuentran asintomáticos. Encontramos 4 casos de enfermedad renal benigna (quistes, litiasis y nódulo suprarrenal), hallazgo que no ha sido recogido previamente, por lo que desconocemos la posible relación con el síndrome.
Se han descrito casos aislados de otras asociaciones al síndrome de Reed, como MEN-1, artritis reumatoide, neoplasia mamaria, neoplasia de próstata, neoplasia vesical, quistes renales y ováricos y adenomas de glándulas adrenales15,16.
En cuanto a su etiopatogenia, la MCUL es causada por una mutación heterocigótica en el gen 1q42.3-43, que codifica la FH, una enzima mitocondrial del ciclo de Krebs que cataliza la conversión de fumarato en malato y podría actuar como supresor tumoral de la FH. La mayoría de casos son debidos a una mutación heterocigota de FH en la línea germinal, de herencia autosómica dominante, pero hay descritos algunos casos esporádicos o mosaicos de FH, en los que no se encuentra la mutación en la línea germinal y presentan leiomiomatosis cutánea segmentaria, sin miomas uterinos ni antecedentes familiares9,17. Se han descrito casos de manifestaciones segmentarias tipo 2 debido a la pérdida de heterocigosidad en el mismo locus que el que causa el fenotipo difuso; en estos casos, los pacientes muestran lesiones difusas pero más pronunciadas en un segmento cutáneo7. Si se produce una mutación de las 2 copias de la FH en la línea germinal (mutación homocigota) el resultado es un cuadro totalmente diferente, caracterizado por disfunción neurológica y supervivencia de meses o pocos años.
La serie más larga publicada de MCUL incluye 46 pacientes con leiomiomas cutáneos múltiples, de los cuales el 89% presentan mutación de la FH en la línea germinal con alta penetrancia. El mismo estudio también incluye a familiares de los casos índices (62 afectos y 42 aparentemente no afectos), encontrando 62% de FH mutada en el total de los individuos (n=150), de los cuales el 100% de los hombres presentaba leiomiomas cutáneos considerándose. En cuanto a las mujeres, el 69% presentaba leiomiomas cutáneos y uterinos, el 15% únicamente cutáneos, el 7% únicamente uterinos y el 9% no tenía lesiones, considerando que podía tratarse de una mutación sin penetrancia9. En nuestros pacientes no fue posible realizar la detección de la mutación de la FH.
Todavía no existe consenso sobre los criterios diagnósticos de la MCUL. Pithukpakorn et al., en una revisión de 2014, proponen una serie de criterios, recogidos en la tabla 218. Cuando no se conocía la mutación genética se consideraba diagnóstico los leiomiomas cutáneos múltiples con al menos uno confirmado por histología, o un solo leiomioma cutáneo con historia familiar de MCUL. Los criterios no han sido formalmente modificados, por lo que a pesar del descubrimiento de la mutación de FH, se sigue considerando diagnóstico clínico de MCUL lo descrito anteriormente, y se ha añadido como criterio los casos de mutación heterocigota de FH junto con carcinoma renal o leiomioma cutáneo confirmados por histología. Sin embargo, dada la alta prevalencia de leiomiomas uterinos, no es suficiente para el diagnóstico la presencia de un leiomioma uterino, aunque se detecte la mutación de la FH18. En los casos de diagnóstico clínico de MCUL podría estar indicada la detección de la mutación de la FH para confirmar el diagnóstico desde el punto de vista genético. Esto puede realizarse mediante test de genética molecular o midiendo la actividad de la enzima en cultivos de fibroblastos de piel o linfoblastos, mostrándose actividad reducida (≤60%)18.
Criterios diagnósticos de MCUL propuestos por Pithukpakorn et al. en 2014
| Diagnóstico clínico dermatológico si uno de los siguientes: | Múltiples leiomiomas cutáneos+≥1 confirmado por histología (no necesaria H.a familiar)Un leiomioma cutáneo+H.a familiar de MCUL/HLRCC |
| → En estos casos está indicada la detección de la mutación para confirmar el diagnóstico | |
| Diagnóstico confirmado: mutación heterocigota gen FH+uno de los siguientes: | Carcinoma renalLeiomioma cutáneoLeiomiomas uterinos múltiples(Todos confirmados por histología) |
| → Mutación heterozigota gen FH+leiomioma uterino solitario: no diagnóstico | |
H.a: historia.
Fuente: Pithukpakorn et al.18
Ante el diagnóstico de un caso de MCUL se debería ofrecer al paciente consejo genético para él y sus familiares.
Respecto al cribado de manifestaciones no cutáneas, ante un caso de leiomiomas cutáneos múltiples, debe valorarse la posibilidad de explorar a familiares de primer grado9,18 y se recomienda la exploración ginecológica con ecografía anual a las mujeres con lesiones cutáneas múltiples, para detectar precozmente miomas subclínicos y permitir la planificación familiar a la paciente. Existe controversia en cuanto al cribado de carcinoma renal, sobre si debe realizarse y con qué técnica, dada la baja sensibilidad de la ecografía renal para el carcinoma renal papilar tipo ii. Algunos autores contemplan la posibilidad de no hacer cribado9, mientras que otros plantean estrategias más agresivas en los casos de mutación de FH confirmada, realizando TAC o RM anual o bianual desde la adolescencia18,19.
Otros autores plantean una estrategia conservadora, realizando TAC o RM anual o bianual solo cuando además existen antecedentes de carcinoma renal en la misma familia13. Aunque algunos trabajos sugieren realizar exploración dermatológica cada uno o 2 años a los pacientes afectos y a familiares sin estudio genético, para evaluar la extensión de las lesiones y detectar cambios sugestivos de leiomiosarcoma, no hay casos descritos de malignización de las lesiones cutáneas18.
Respecto al tratamiento de los leiomiomas cutáneos la exéresis quirúrgica es el tratamiento de elección en los casos de lesión aislada sintomática, pudiendo considerarse también la ablación mediante electrocirugía o láser de CO2, aunque las recurrencias son más frecuentes. En los casos de lesiones múltiples sintomáticas se han propuesto diversos tratamientos sistémicos con la finalidad de calmar el dolor, pero su eficacia es limitada. Se utilizan fármacos que inhiben contracción de las fibras de músculo liso (nifedipino20,21, fenoxibenzamina22,23, doxazosina24,25 y nitroglicerina22), antiepilépticos (mirtazapina), opioides (oxicodona) y gabapentina26. Debe considerase la abstención terapéutica en los casos de lesiones asintomáticas, dada la benignidad de las lesiones.
ConclusiónDescribimos 13 casos de MCUL, que presentan características clínicas e histológicas similares a las descritas en la literatura, siendo la manifestación cutánea más frecuente la segmentaria tipo 2. Es importante que el dermatólogo identifique los casos de leiomiomas cutáneos y realice una historia clínica dirigida para valorar si se trata de un caso de MCUL, ya que existe una fuerte asociación a leiomiomas uterinos más agresivos que lo habitual y riesgo de desarrollar carcinoma renal. Sin embargo, la necesidad de realizar screening y el tipo de pruebas necesarias sigue siendo un tema de controversia.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.