Para estimar la carga real del melanoma y el impacto de las nuevas terapias adyuvantes sobre las recaídas y la supervivencia, se precisa conocer con mayor exactitud la incidencia por estadios y analizar la transición entre ellos. Este estudio pretende estimar dicha incidencia y determinar el número de pacientes en estadio III que podrían beneficiarse del tratamiento sistémico adyuvante en España.
Materiales y métodoSe elaboró un modelo epidemiológico basado en datos de pacientes diagnosticados de melanoma o en recaída, recogidos prospectivamente durante 2012-2016 por cuatro unidades de melanoma de centros sanitarios públicos.
ResultadosLas tasas brutas de incidencia estimadas para estadios I y II se situaron en 7 y 2,9 casos por 100.000 personas-año, respectivamente. Para estadio III se estimó en 1,9 (25,8% en IIIA, 47% en IIIB, y 27,3% en IIIC), siendo la de estadio IV de 1,3. La tasa de recaídas en estadio III se estimó en 1,1, siendo para estadio IV de 0,9. El 54% de recaídas a estadio III procedían de estadios I/II, mientras que el resto progresaban desde subestadios III. En estadio III, un 85% de nuevos diagnósticos y un 80% de recaídas fueron resecables, por tanto, candidatos a adyuvancia, de los cuales el 47% presentaba mutación en BRAF.
ConclusionesEstas estimaciones podrían tener un impacto importante en la planificación de los recursos sanitarios. La proyección en el número de potenciales candidatos a adyuvancia puede ayudar a decisores y clínicos a anticiparse a futuras necesidades en el manejo del melanoma.
Accurate information on the incidence of melanoma by stage and a better understanding of transition between stages are important for determining the burden of disease and assessing the impact of new adjuvant therapies on recurrence and survival. The aim of this study was to estimate the incidence rates of the various stages of melanoma in Spain and to estimate the number of patients with stage III disease who are eligible for adjuvant systemic therapies.
Materials and methodWe built an epidemiological model using prospectively collected data from patients diagnosed with de novo or recurrent melanoma between 2012 and 2016 in the melanoma units of 4 public hospitals.
ResultsThe estimated crude incidence rates for stage I and II melanoma were 7 and 2.9 cases per 100,000 person-years, respectively. The corresponding rates for stage III and IV melanoma were 1.9 and 1.3 cases per 100,000 person-years; 25.8% of patients with stage III melanoma were stage IIIA, 47% were stage IIIB, and 27.3% were stage IIIC. The respective estimated incidence rates for recurrent stage III and IV melanoma were 1.1 and 0.9 cases per 100,000 person-years. Overall, 54% of patients with recurrent stage III melanoma had progressed from stage I or II; the other cases corresponded to changes in substage. Of the patients with stage III melanoma, 85% of those with a de novo diagnosis and 80% of those who had relapsed had resectable disease, meaning they were eligible for adjuvant therapy; 47% of these patients had a BRAF mutation.
ConclusionsThe above estimates could have a major impact on health care resource planning. Assessing the number of patients with melanoma who are eligible for adjuvant therapies in melanoma could help decision-makers and clinicians anticipate future needs for the management of this disease.
El melanoma cutáneo representa aproximadamente un 4% de los cánceres dermatológicos a nivel mundial, siendo uno de los tumores con mayor carga mutacional1 y el responsable del 80% de las muertes por cáncer de piel2.
En los últimos años, su incidencia ha aumentado en España, desde una tasa bruta (TB) de incidencia de 8,8 casos por 100.000 personas-año en 20153 hasta 13,1 nuevos casos estimados en 20204. En regiones como Cataluña, la tasa de incidencia ajustada por edad es superior a la nacional, alcanzando los 13,8 casos5. Estos datos provienen de registros referentes a aproximadamente un 30% de la población española, por lo que la incidencia podría infraestimarse6. Tampoco discriminan la etapa patológica o estadio, ni la transición entre estadios a consecuencia de recaídas, por lo que es difícil precisar el número de pacientes de nuevo diagnóstico por estadio.
Actualmente, el estadio del tumor, considerado uno de los principales factores determinantes del pronóstico, se establece de acuerdo con el sistema TNM, propuesto por el American Joint Cancer Committee (AJCC)7. La evidencia previa muestra una importante reducción de la supervivencia en estadios avanzados, estimándose una supervivencia a los cinco años del 95-100% para el estadio I, frente a un 9-28% para el estadio IV8. Además, en la valoración del pronóstico, es importante considerar el riesgo de recaídas asociado a cada estadio, siendo mayor en estadios avanzados9. Por otra parte, la presencia de mutación en el gen BRAF, presente en cerca del 50% de los melanomas10, podría asociarse a la progresión. Tanto el número de ganglios linfáticos positivos como la presencia de mutación en BRAF se han identificado como factores pronósticos asociados de manera independiente y significativa a la supervivencia y a las recurrencias en pacientes en estadios IIIB/C con melanoma resecado11. La supervivencia específica de la enfermedad en estos pacientes es menor que en pacientes sin mutación, y su tasa de recaídas y riesgo de mortalidad resultan superiores11,12.
Con el objetivo de reducir el riesgo de recaída y mortalidad en pacientes con melanoma en estadio III y IV resecado, las guías clínicas recomiendan la administración de tratamiento sistémico adyuvante como terapia complementaria a la resección13,14. Un estudio de vida real llevado a cabo en esta población, demostró que la adyuvancia con interferón α-2b aumentaba significativamente la supervivencia libre de recaída frente a la estrategia «observar y esperar»15. Las nuevas terapias adyuvantes han demostrado en ensayos clínicos un mayor beneficio en la supervivencia libre de recaída del obtenido hasta el momento con interferón16. Por contra, la evidencia indica que las tasas de supervivencia específica de melanoma en estadio III sin tratamiento adyuvante se reducen significativamente en subestadios más avanzandos17.
Disponer de datos referentes a la incidencia del melanoma por estadio y subestadio permitiría analizar la transición a estadios más avanzados y, por tanto, proveer de información sobre su pronóstico, así como del impacto de las terapias adyuvantes sobre dicha transición. Sin embargo, estos datos en España son muy limitados. Asimismo, obtener información sobre la población candidata al tratamiento adyuvante en España, ayudaría en la estimación de la carga real de la enfermedad y establecer el impacto económico del manejo de estos pacientes para el sistema sanitario.
El presente estudio tiene como objetivo estimar la incidencia de melanoma por estadio y determinar el número de pacientes en estadio III que podrían beneficiarse de la adyuvancia en España, basándose en un modelo epidemiológico elaborado con datos de vida real previos a la introducción de nuevas terapias adyuvantes.
Materiales y métodoSe elaboró un modelo epidemiológico basado en datos recogidos prospectivamente durante cinco años por cuatro unidades de melanoma, pertenecientes a centros sanitarios públicos de referencia en el tratamiento y manejo del melanoma: el Instituto Valenciano de Oncología (IVO), el Hospital Universitario Virgen Macarena (HUVM), el Hospital Clínic de Barcelona (HCB) y el Hospital Universitario 12 de Octubre (HU12O). Dichos centros cubren una población de aproximadamente dos millones de habitantes.
Fuentes de datos utilizadasSe utilizaron los siguientes datos de los registros de las unidades de melanoma de pacientes diagnosticados de melanoma o en recaída, recopilados durante los años 2012-2016: incidencia de nuevos diagnósticos por estadio (estadios I/II/III/IV) y de nuevos casos en estadio III por subestadio (IIIA/IIIB/IIIC), de acuerdo con la séptima edición del AJCC18; incidencia de recaídas a estadios III y IV, y estadio de procedencia; porcentaje de pacientes con melanoma resecable de nuevo diagnóstico por estadio y en recaída a estadios III y IV; número de pacientes candidatos a adyuvancia (nuevo diagnóstico y recaída) y número de pacientes candidatos a adyuvancia con mutación BRAF. Estos centros realizaron de forma rutinaria el análisis de mutaciones BRAF en todos los pacientes en estadio III.
Se desarrolló el modelo con los datos disponibles de cada unidad. Los datos recogidos se analizaron de forma agregada y no se recogieron variables de resultados clínicos, de seguimiento de los pacientes, o de tratamientos utilizados.
Modelo epidemiológicoEl modelo se construyó sobre la base poblacional española de 2020, utilizando datos de publicaciones científicas y datos de vida real recopilados en cada unidad de melanoma. Se desarrolló a partir de los datos de incidencia de melanoma en los diferentes estadios, y el flujo de pacientes entre ellos, teniendo en cuenta los nuevos diagnósticos para cada estadio y las recaídas (tabla 1). Puesto que el modelo se construyó a partir de datos de diferentes comunidades autónomas, para la estimación de la incidencia de nuevos diagnósticos por estadio se tomó como base la aproximación para el año 2020 realizada por REDECAN, a partir de registros poblacionales para la TB de incidencia nacional de melanoma invasor4.
Evidencia empleada para las estimaciones realizadas en el modelo, según los datos de práctica clínica real y datos publicados en la literatura
| Datos de práctica clínica real | Datos publicados en la literatura |
|---|---|
| 1) Estimación de la incidencia de nuevos diagnósticos en los diferentes estadios de la enfermedad a nivel nacional. | |
| Incidencia y porcentaje promedio de pacientes de nuevo diagnóstico por estadio (incluyendo los subestadios IIIA, IIIB y IIIC)18. | Tasa bruta de incidencia del melanoma a nivel nacional en 2020 (13,1 nuevos casos por 100.000 personas-año), obtenida a partir de registros poblacionales de la Red Española de Registros de Cáncer (REDECAN)4.Población total residente en España en el año 2020, según datos del Instituto Nacional de Estadística (47.329.981 habitantes)19. |
| 2) Estimación de la incidencia de recaídas a los estadios III y IV a nivel nacional. | |
| Incidencia y el porcentaje de pacientes en recaída a estadios III y IV; y el porcentaje de pacientes que progresan a estadios III y IV desde otros estadios. | Población de referencia que abarcan los hospitales (500.000 habitantes cada uno)29–31.Población total residente en España en el año 2020, según datos del Instituto Nacional de Estadística19. |
| 3) Estimación del número de pacientes con melanoma resecable en estadio III que podrían beneficiarse de la adyuvancia en España. | |
| Número medio anual de recaídas a estadio III resecables.Número medio anual de nuevos casos en estadio III resecables. | Población total residente en España en el año 2020, según datos del Instituto Nacional de Estadística19. |
| 4) Estimación del número de pacientes candidatos a adyuvancia que presentaban mutación BRAF V600 a nivel nacional, considerando tanto los pacientes de nuevo diagnóstico en estadio III como las recaídas. | |
| Porcentaje promedio de pacientes candidatos a la adyuvancia que presentaban mutación BRAF V600. | -- |
Al tratarse de hospitales de referencia en el manejo del melanoma, cuyas cifras de resección en estadio III podrían ser superiores a la media nacional, se consideró conveniente aplicar un factor de corrección, acordado por consenso por los expertos participantes con base en su experiencia, con el fin de no sobreestimar los resultados y aproximarlo a la realidad nacional. Para ello se asumió que el porcentaje de resección de melanomas en estadio III en estos centros podía ser un 10% superior a la media nacional, por lo que se aplicó un factor de corrección del 10% a los melanomas, tanto de novo como en recaída.
Para cada una de las medias estimadas en la elaboración del modelo, se calculó su correspondiente desviación estándar como medida de dispersión de los datos. Los datos de cada registro fueron recogidos y analizados mediante Microsoft Excel®.
ResultadosDescripción de los datos registradosSe registraron datos de 1.795 pacientes de nuevo diagnóstico de melanoma en estadios I-IV (IVO: 279, HUVM: 286, HCB: 1.024, y HU12O: 206) y 402 pacientes en recaída a estadios III y IV (IVO: 86, HUVM: 27, HCB: 252, y HU12O: 37).
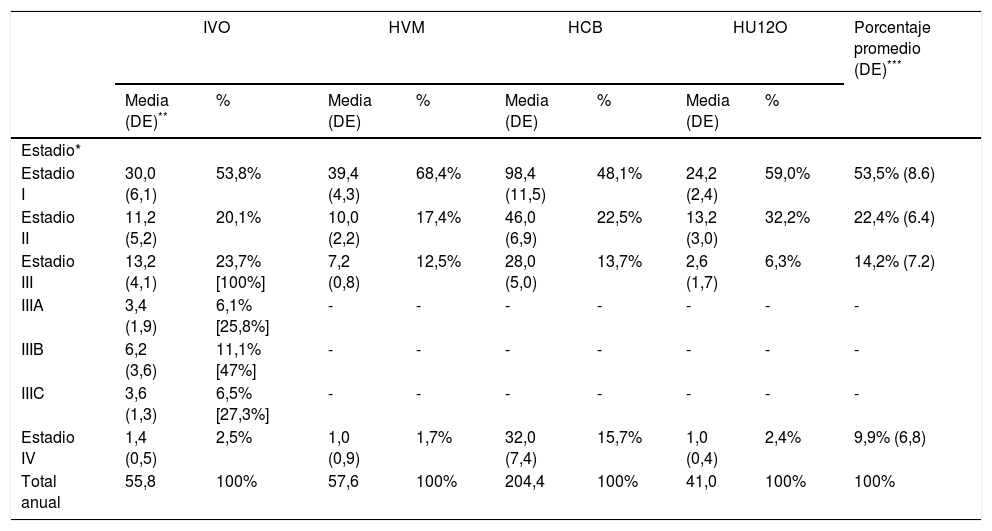
Incidencia de nuevos casos por estadioA partir de los datos recopilados se obtuvo la incidencia de pacientes de nuevo diagnóstico por estadio (tabla 2). El 53,5% de los nuevos casos diagnosticados de melanoma se encontraba en estadio I, el 22,4% en estadio II, el 14,2% en estadio III y el 9,9% en estadio IV.
Incidencia de pacientes de nuevo diagnóstico por estadio recopilados por las unidades de melanoma para el periodo 2012-2016
| IVO | HVM | HCB | HU12O | Porcentaje promedio (DE)*** | |||||
|---|---|---|---|---|---|---|---|---|---|
| Media (DE)** | % | Media (DE) | % | Media (DE) | % | Media (DE) | % | ||
| Estadio* | |||||||||
| Estadio I | 30,0 (6,1) | 53,8% | 39,4 (4,3) | 68,4% | 98,4 (11,5) | 48,1% | 24,2 (2,4) | 59,0% | 53,5% (8.6) |
| Estadio II | 11,2 (5,2) | 20,1% | 10,0 (2,2) | 17,4% | 46,0 (6,9) | 22,5% | 13,2 (3,0) | 32,2% | 22,4% (6.4) |
| Estadio III | 13,2 (4,1) | 23,7% [100%] | 7,2 (0,8) | 12,5% | 28,0 (5,0) | 13,7% | 2,6 (1,7) | 6,3% | 14,2% (7.2) |
| IIIA | 3,4 (1,9) | 6,1% [25,8%] | - | - | - | - | - | - | - |
| IIIB | 6,2 (3,6) | 11,1% [47%] | - | - | - | - | - | - | - |
| IIIC | 3,6 (1,3) | 6,5% [27,3%] | - | - | - | - | - | - | - |
| Estadio IV | 1,4 (0,5) | 2,5% | 1,0 (0,9) | 1,7% | 32,0 (7,4) | 15,7% | 1,0 (0,4) | 2,4% | 9,9% (6,8) |
| Total anual | 55,8 | 100% | 57,6 | 100% | 204,4 | 100% | 41,0 | 100% | 100% |
IVO: Instituto Valenciano de Oncología; HVM: Hospital Virgen Macarena; HCB: Hospital Clínic de Barcelona; HU12O: Hospital Universitario 12 de Octubre; DE: desviación estándar.
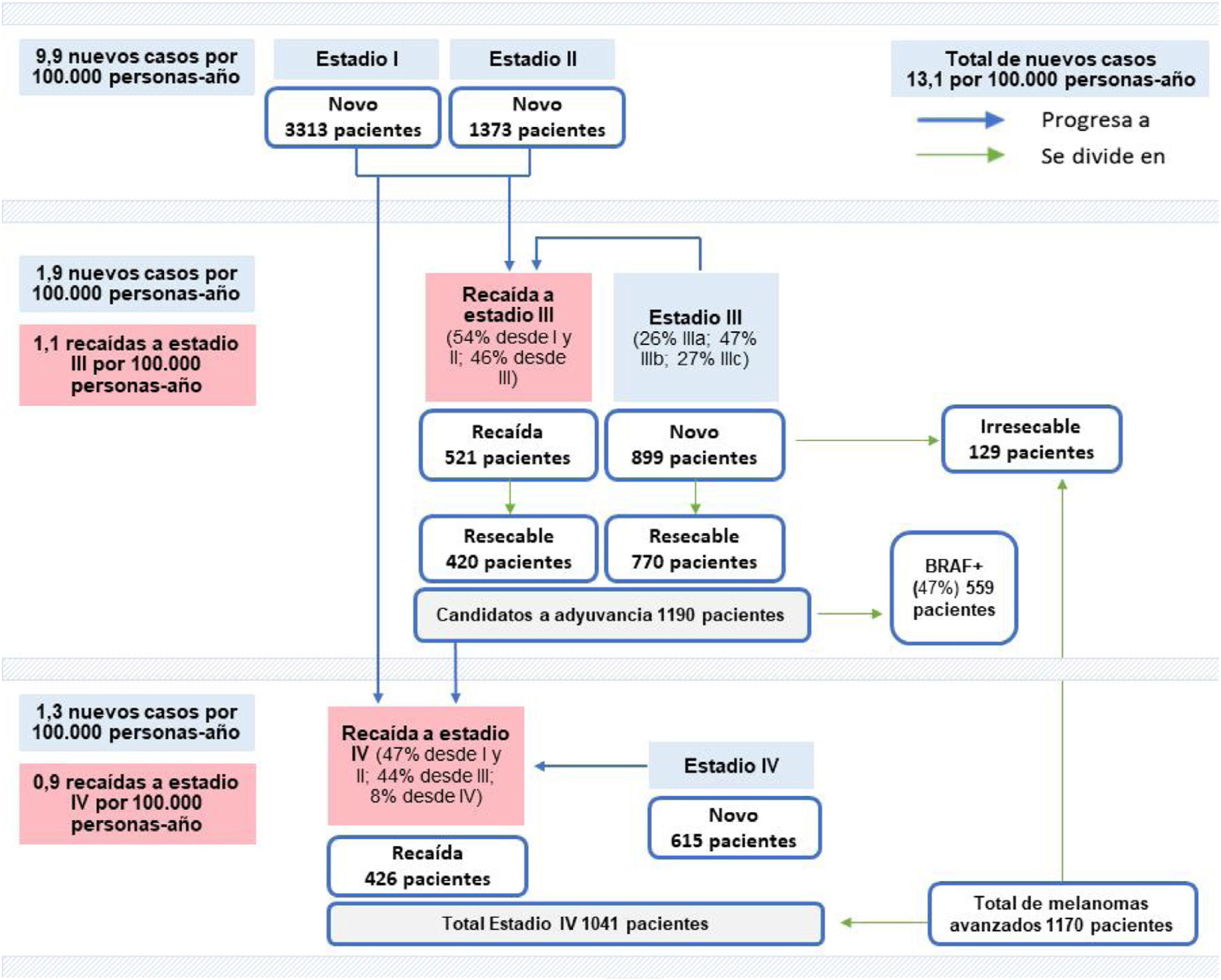
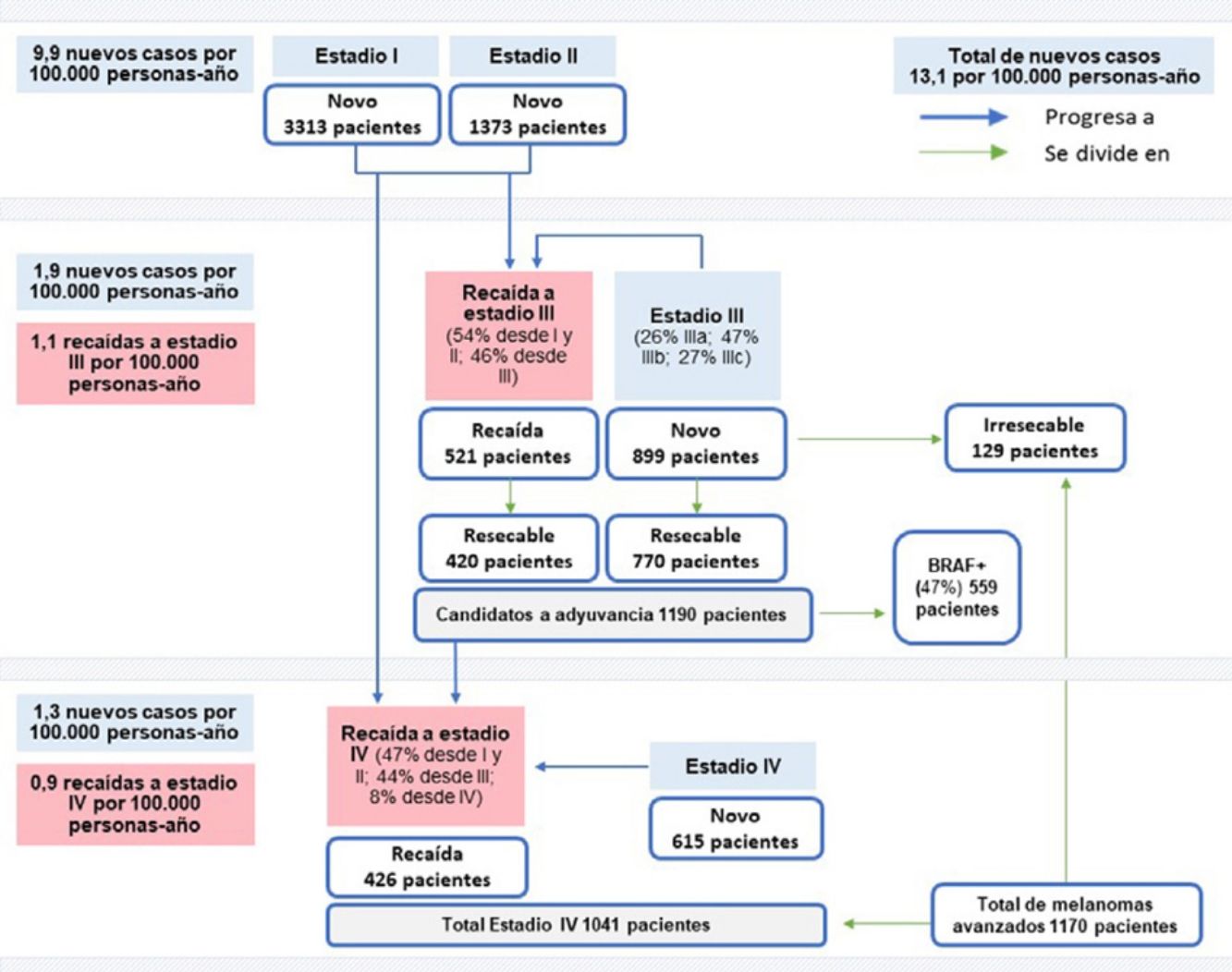
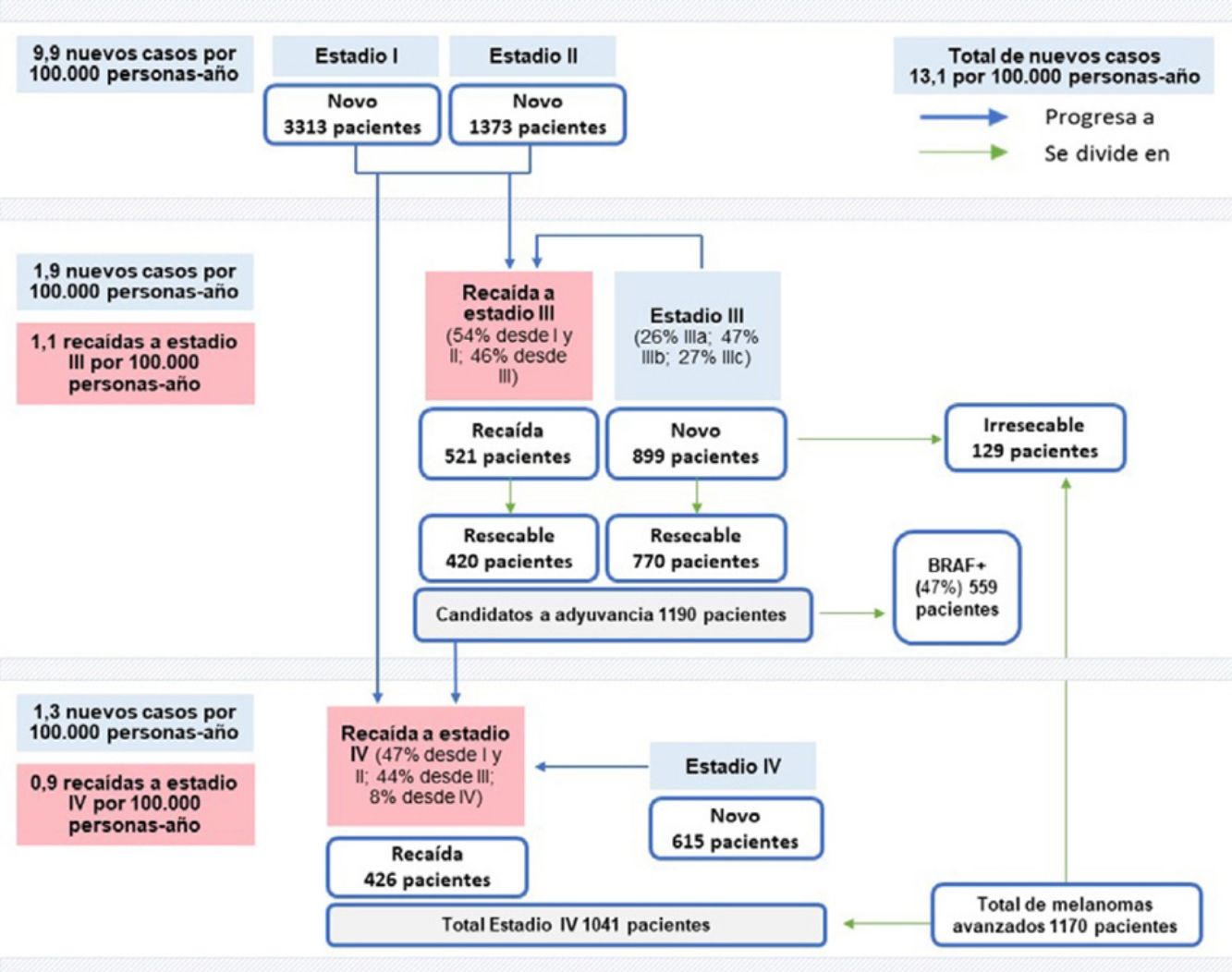
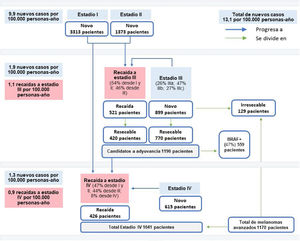
Con base en TB de incidencia nacional para 20204 y al porcentaje medio de pacientes por estadio, la TB de incidencia se estimó en siete nuevos casos por 100.000 personas-año para el estadio I, 2,9 para estadio II, 1,9 para estadio III y 1,3 para estadio IV. Trasladando estos datos a la población española censada en 202019, ese año se diagnosticarían 6.200 nuevos casos de melanoma, de los que 3.313 serían en estadio I, 1.373 en estadio II, 899 en estadio III y 615 en estadio IV (fig. 1).
Incidencia de novo: 6.200 pacientes (13,1 casos/100.000 personas-año X 47.329.981 habitantes), 3.313 pacientes en estadio I (7 casos/100.000 personas-año X 47.329.981 habitantes), 1.373 pacientes en II (2,9 casos/100.000 personas-año X 47.329.981 habitantes), 899 pacientes en III (1,9 pacientes/100.000 personas-año X 47.329.981 habitantes), y 615 pacientes en IV (1,3 casos/100.000 personas-año X 47.329.981 habitantes). Incidencia de recaídas: 521 pacientes en estadio III (1,1 casos/100.000 personas-año X 47.329.981 habitantes) y 426 pacientes en IV (0,9 casos/100.000 personas-año X 47.329.981 habitantes). Resecabilidad: 420 pacientes en recaída (521 pacientes X 80,7%), 770 pacientes de novo (899 pacientes X 85,7%), 1.190 pacientes en total resecable (420 + 770 pacientes), 129 pacientes de novo irresecable (899-770 pacientes). Candidatos a adyuvancia BRAF: 559 pacientes (1.190 pacientes X 47%). Total estadio IV: 1.041 pacientes (426 + 615 pacientes). Total melanomas avanzados: 1.170 pacientes (1.041 + 129 pacientes).
Considerando los datos disponibles por subestadios III (datos del IVO) y el número de nuevos diagnósticos en estadio III para 2020 (899), se estimó que (tabla 2): 232 pacientes se encontraban en subestadio IIIA; 422 pacientes en subestadio IIIB y 245 pacientes en subestadio IIIC.
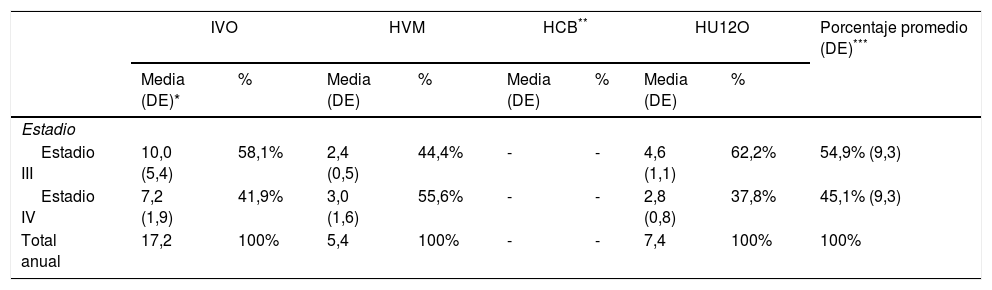
Incidencia de recaídas y procedenciaLa tabla 3 muestra la incidencia de pacientes en recaída a estadio III y IV. Se estimó que el 54,9% de las recaídas desde cualquier estadio fueron a estadio III, mientras el 45,1% progresaron a estadio IV.
Incidencia de pacientes en recaída a estadios III y IV recopilados por las unidades de melanoma para el periodo 2012-2016
| IVO | HVM | HCB** | HU12O | Porcentaje promedio (DE)*** | |||||
|---|---|---|---|---|---|---|---|---|---|
| Media (DE)* | % | Media (DE) | % | Media (DE) | % | Media (DE) | % | ||
| Estadio | |||||||||
| Estadio III | 10,0 (5,4) | 58,1% | 2,4 (0,5) | 44,4% | - | - | 4,6 (1,1) | 62,2% | 54,9% (9,3) |
| Estadio IV | 7,2 (1,9) | 41,9% | 3,0 (1,6) | 55,6% | - | - | 2,8 (0,8) | 37,8% | 45,1% (9,3) |
| Total anual | 17,2 | 100% | 5,4 | 100% | - | - | 7,4 | 100% | 100% |
IVO: Instituto Valenciano de Oncología; HVM: Hospital Virgen Macarena; HCB: Hospital Clínic de Barcelona; HU12O: Hospital Universitario 12 de Octubre; DE: desviación estándar.
Con base en la incidencia de pacientes en recaída a estadio III por centro, y teniendo en cuenta la población que abarca cada área de salud, se estimó una TB para esta población de 1,1 recaídas por 100.000 personas-año (IVO: dos recaídas; HUVM: 0,5 recaídas; HU12O: 0,9 recaídas).
A partir de los datos de recaídas a estadio IV (tabla 3), se calculó una TB de incidencia de recaídas a estadio IV de 0,9 recaídas por 100.000 personas-año.
Estos datos de incidencia se trasladaron a la población general española censada en 2020, obteniendo que 521 de pacientes presentarían una recaída locorregional (estadio III) y 426 pacientes una recaída a distancia (estadio IV) (fig. 1).
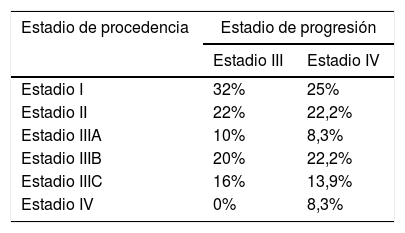
A partir de los datos recopilados del total de recaídas a estadio III y IV, se obtuvo la distribución de recaídas según el estadio de procedencia (tabla 4). En el 54% de los casos de recaída a estadio III los pacientes procedían de estadio I/II, mientras que el 46% restante progresaban siguiendo exclusivamente diseminación linfática, desde otro subestadio III. De los 521 pacientes en recaída a estadio III, 281 procederían de estadio I/II, y 240 recaerían desde otro subestadio III.
El 47,2% de recaídas a estadio IV progresaron desde estadios I y II, mientras que el 44,4% lo hicieron desde estadio III.
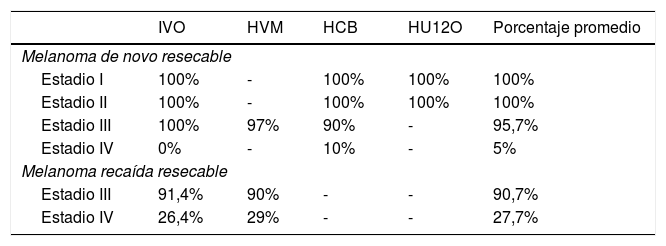
Pacientes en estadio III candidatos a adyuvanciaEl 100% de los melanomas de novo en estadio I y II fueron considerados resecables, mientras que en estadio III fueron el 95,7% (tabla 5). En la mayoría de los pacientes en estadio IV, no se consideró la resección quirúrgica.
Porcentaje del total de pacientes con melanoma resecable en cada estadio de la enfermedad para cada unidad de melanoma
| IVO | HVM | HCB | HU12O | Porcentaje promedio | |
|---|---|---|---|---|---|
| Melanoma de novo resecable | |||||
| Estadio I | 100% | - | 100% | 100% | 100% |
| Estadio II | 100% | - | 100% | 100% | 100% |
| Estadio III | 100% | 97% | 90% | - | 95,7% |
| Estadio IV | 0% | - | 10% | - | 5% |
| Melanoma recaída resecable | |||||
| Estadio III | 91,4% | 90% | - | - | 90,7% |
| Estadio IV | 26,4% | 29% | - | - | 27,7% |
IVO: Instituto Valenciano de Oncología; HVM: Hospital Virgen Macarena; HCB: Hospital Clínic de Barcelona; HU12O: Hospital Universitario 12 de Octubre.
Se aplicó una corrección del 10% al porcentaje de melanomas de novo en estadio III para aproximarlo a la media de resección nacional, obteniendo que un 85,7% de los melanomas de novo serían resecables en la población general española. Por lo tanto, 770 de los 899 nuevos casos en estadio III se consideraron resecables y, por tanto, candidatos a adyuvancia (fig. 1).
Atendiendo a las recaídas, un 90,7% de los melanomas en recaída a estadio III se consideraron resecables. Se aplicó una corrección del 10% para estos datos, obteniendo que 420 de las 521 recaídas a estadio III serían consideradas resecables.
Según estos datos, el número total de pacientes en estadio III candidatos a adyuvancia a nivel nacional en 2020 sería de 1.190 pacientes (770 + 420) (fig. 1).
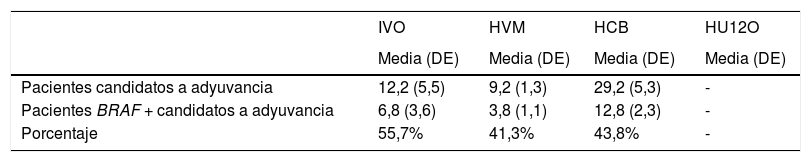
Pacientes candidatos a adyuvancia con mutación BRAF V600Atendiendo a la presencia de mutación en pacientes candidatos a adyuvancia, se estimó que el 47% de los casos de novo y recaída a estadio III resecables presentarían dicha mutación (tabla 6).
Número medio de pacientes candidatos a adyuvancia en cada centro y BRAF + candidatos a adyuvancia, en cada unidad de melanoma para el periodo 2012-2016
| IVO | HVM | HCB | HU12O | |
|---|---|---|---|---|
| Media (DE) | Media (DE) | Media (DE) | Media (DE) | |
| Pacientes candidatos a adyuvancia | 12,2 (5,5) | 9,2 (1,3) | 29,2 (5,3) | - |
| Pacientes BRAF + candidatos a adyuvancia | 6,8 (3,6) | 3,8 (1,1) | 12,8 (2,3) | - |
| Porcentaje | 55,7% | 41,3% | 43,8% | - |
IVO: Instituto Valenciano de Oncología; HVM: Hospital Virgen Macarena; HCB: Hospital Clínic de Barcelona; HU12O: Hospital Universitario 12 de Octubre.
Un total de 559 pacientes BRAF + serían candidatos a la adyuvancia (fig. 1).
DiscusiónActualmente, se consideran candidatos al tratamiento adyuvante aquellos pacientes con un riesgo alto de recaída. Las estimaciones llevadas a cabo en el presente trabajo permiten realizar una aproximación al número de pacientes con melanoma en estadio III en España que pueden ser candidatos a adyuvancia.
Los resultados obtenidos indican que el 14% de los pacientes con melanoma de nuevo diagnóstico se encuentran en estadio III. Estos datos son superiores a los estimados en un estudio previo realizado en España con base en datos poblacionales del registro nacional de melanoma desde 1997 hasta 2011 (9,9%)20, o a los publicados en EE. UU. entre 2008 y 2017 (8,5%)21. Estas diferencias podrían deberse a que nuestros datos provienen de centros de referencia en el manejo del melanoma situados en ciudades con alta densidad poblacional y que diagnostican un mayor número de melanomas en estadios avanzados que la media nacional. De manera similar, la proporción de melanomas en estadio IV en estos centros, cercana al 10%, también resulta superior a datos previos20,21.
Aunque nuestras estimaciones pueden no ser representativas de la realidad nacional, evidencian que cerca del 25% de los pacientes de nuevo diagnostico atendidos en estos centros se encuentran en estadios avanzados y, por tanto, en mayor riesgo de recaída. Un estudio realizado previamente a la introducción de los nuevos tratamientos para el melanoma avanzado, evidenció que la supervivencia libre de recaída a los cinco años en pacientes en subestadios IIIA, IIIB y IIIC, se encontraba entre un 10 y un 60%, siendo el subestadio IIIC el de mayor tasa de recaídas22. Otro estudio de 2018 sobre los patrones de recaída indicó que el 50% de recaídas desde estadio III progresaban a metástasis a distancia9. Según nuestro estudio, aproximadamente la mitad de las recaídas a estadio III progresan desde otros subestadios III, mientras que el 44% de recaídas a estadio IV lo hacen desde estadio III.
Respecto a la procedencia de las recaídas, estudios previos realizados en Europa con datos de vida real indican una mayor frecuencia de recurrencia a nivel regional para estadios I/II23, y de metástasis a distancia para estadio III9,24. Sin embargo, hay poca evidencia sobre la procedencia de la recaída. Según nuestros datos, tanto la incidencia de recaídas como su procedencia es similar en estadios III y IV, siendo ligeramente mayores las recaídas desde estadios I/II que desde estadio III en ambos casos, a pesar del mayor riesgo de metástasis a distancia desde estadio III.
Estos datos revelan la necesidad de introducción de nuevas estrategias terapéuticas para esta población. Estudios recientes en pacientes con melanoma resecado en estadio III indican que los nuevos tratamientos, tanto la inmunoterapia como las terapias dirigidas frente a mutaciones en BRAF reducen el riesgo de recaídas25, principalmente locorregionales26, mientras mantienen un perfil de seguridad aceptable10. Se ha estimado que 1.190 pacientes serían candidatos a la adyuvancia en 2020. Nuestros resultados indican que cerca del 50% de los pacientes en estadio III resecable presentan mutación BRAF, por lo que podrían beneficiarse del tratamiento adyuvante con terapias dirigidas.
Pese a los avances en la terapia, las diferencias en la disponibilidad de los fármacos a nivel regional y hospitalario, así como las barreras en la implementación de biomarcadores para una adecuada selección de los tratamientos podrían suponer un retraso en el acceso a estas nuevas terapias27. Estas diferencias podrían deberse en gran medida al elevado coste de los tratamientos, sin embargo, es necesario determinar si su introducción en la práctica clínica reduciría tanto el riesgo de recurrencias como los costes asociados al uso de recursos sanitarios. Los datos de incidencia de melanoma por estadio podrían servir para estimar el impacto económico de estas terapias sobre el sistema de salud y así optimizar la asignación de los recursos sanitarios.
El estudio presenta algunas limitaciones. Primero, al tratarse de centros de referencia, el uso de su información podría sobreestimar las cifras nacionales, por ello se aplicaron correcciones en los porcentajes de pacientes sometidos a resección para aproximarlo a la realidad nacional. En relación con la TB de incidencia de melanoma utilizada en el modelo, si bien un metaanálisis de Tejera-Vaquerizo et al.3 de 2016 estimó una incidencia inferior a 13,1 casos, los datos publicados por REDECAN4 en 2015 fueron similares. Del mismo modo, un estudio más reciente de Podlipnik5 et al. aportaba una cifra de incidencia inferior en Cataluña, sin embargo, se consideró utilizar en el modelo una cifra actualizada a nivel nacional (REDECAN). Segundo, este modelo fue elaborado previamente a la introducción de nuevas terapias adyuvantes, estando vigente la séptima edición del AJCC. En la actualidad, se utiliza la octava edición que introduce importantes cambios en la estadificación del estadio III, y que implican en algunos pacientes un cambio de estadio con respecto a la edición anterior26. No obstante, no cabe esperar cambios significativos en el manejo del melanoma en España hasta la actualidad, no habiendo cambiado los potenciales tratamientos adyuvantes. Con la introducción de nuevos tratamientos adyuvantes, se espera una reducción en el número de recaídas desde estadio III, por lo que se sugiere replicar el modelo tras su introducción. Tercero, cabe destacar que al no disponerse de datos concretos de carga tumoral, se consideró candidatos a adyuvancia a todos los pacientes en estadio IIIA, a pesar de que en los pacientes con un tamaño máximo de la metástasis ganglionar inferior a 1 mm no se recomienda el tratamiento adyuvante sistémico, por lo que nuestras cifras podrían sobreestimarse. Finalmente, no se ha tenido en cuenta la edad de la población estudiada, así como otros datos descriptivos, por lo que no se puede verificar su representatividad de la población nacional. Puesto que la edad avanzada sería un factor asociado al rechazo del tratamiento o a la existencia de comorbilidades que puedan contraindicar su administración, el número de candidatos a adyuvancia podría verse limitado en poblaciones más envejecidas. Sin embargo, la información proviene de hospitales geográficamente distantes, localizados en zonas de alta densidad poblacional, de manera que la población sea lo más representativa posible de la realidad.
Por último, cabe señalar que las estimaciones publicadas previamente a partir de registros no discriminaban el estadio del melanoma y podían subestimarse28, mientras este estudio presenta el cálculo de la incidencia por estadio a nivel nacional desde un nuevo enfoque.
ConclusiónTeniendo en cuenta la tasa de supervivencia de los pacientes con melanoma en estadio III y su elevado riesgo de recaídas, la indicación de tratamiento adyuvante para esta población adquiere especial relevancia. Las estimaciones del presente estudio podrían tener un impacto importante en la planificación de los recursos sanitarios. La proyección en el número de potenciales candidatos a la adyuvancia puede ayudar a decisores y clínicos a anticiparse a futuras necesidades en el manejo del melanoma.
FinanciaciónNovartis Farmacéutica S.A. ha financiado la publicación de este artículo. La compañía no ha intervenido en la obtención y el tratamiento de los datos.
Conflicto de interesesP. Ortiz-Romero ha recibido honorarios por labores de consultoría por parte de Kyowa, Takeda, 4SC, Helsinn, Recordati Rare Diseases, Innate Pharma y Miragen.
S. Puig ha recibido honorarios por labores de consultoría o conferenciante, y/o ha participado en ensayos clínicos patrocinados por Abbvie, Almirall, Amgen, BMS, Biofrontera, Canfield, Cantabria, Fotofinder, GSK, ISDIN, La Roche Posay, Leo Pharma, MSD, MEDA, Novartis, Polychem, y Roche.
E. Martín-Sánchez y A. Martínez-Fernández son empleados a tiempo completo de Novartis Farmacéutica S.A.
El resto de los autores declaran no tener ningún conflicto de intereses.
Los autores agradecen a Outcomes’10 su asesoramiento científico en el análisis de datos y la edición de este manuscrito.