Aunque los inhibidores de la Janus kinasa (JAKi) han demostrado eficacia en el tratamiento de diversas enfermedades dermatológicas, un subconjunto de pacientes podría no alcanzar un control sintomático adecuado. En estos casos se puede plantear el cambio de tratamiento o la combinación con otro fármaco.
Dada la escasa bibliografía disponible sobre el perfil de seguridad de la combinación de los JAKi con inmunomoduladores sistémicos en el tratamiento de enfermedades dermatológicas1,2, realizamos una revisión retrospectiva de los pacientes que recibieron tratamiento combinado en nuestro servicio de dermatología de un hospital universitario terciario.
Identificamos un total de 18 pacientes (edad media: 43 años; 7 varones y 11 mujeres) tratados con 22 combinaciones terapéuticas diferentes. Doce de estos pacientes recibieron un JAKi para el tratamiento de alopecia areata (AA), 5 para dermatitis atópica (DA) y uno para dermatitis granulomatosa intersticial (DGI), en este último caso como uso off-label. Un total de 15 pacientes fueron tratados con baricitinib a una dosis de 4mg/día durante una media de 21 meses (rango: 3-43 meses). En 4 casos se administró upadacitinib a una dosis de 15mg/día (en un caso, 30mg/día), con una media de duración de 20 meses (rango: 12-30 meses).
Las terapias sistémicas utilizadas en los regímenes combinados fueron variadas: metotrexato (12), prednisona (4), dupilumab (4), tacrolimus oral (1) y ciclosporina (1). Se decidió un tratamiento combinado por diversos factores, el más frecuente fue una respuesta parcial al JAKi, por lo que se añadió metotrexato en todos los casos, a una dosis media de 15mg por semana. Esta combinación se mantuvo durante una media de 18 meses. La segunda causa más común para iniciar un tratamiento combinado fue la falta de respuesta a la monoterapia con JAKi. En 2 casos se añadió metotrexato, y en otro caso la combinación incluyó dupilumab 300mg/cada 14 días y ciclosporina 100mg/2 veces al día/durante 6 meses (casos n.° 18 y 19; tabla 1). En otro caso, se prescribió tratamiento combinado en un paciente con trasplante renal, que ya recibía tacrolimus 2,5mg/día más prednisona oral 5mg/día (casos n.° 7 y 8; tabla 1). Otras causas incluyeron una recaída transitoria de la DA, para la que se prescribió prednisona oral 40mg/día con reducción progresiva durante 2 semanas, y una pérdida secundaria de eficacia tras la reducción de upadacitinib a 15mg/día debido a efectos adversos (EA), por lo que se prescribió un régimen de 6 meses de dupilumab 300mg en semanas alternas. En 6 casos, los pacientes que no lograron una respuesta completa con los tratamientos inmunosupresores clásicos o las terapias biológicas fueron tratados con JAKi. Dos casos de AA y uno de DGI que recibían metotrexato a dosis de 15mg/semana/durante un tiempo medio de 16 meses (rango: 7-33 meses) iniciaron tratamiento con baricitinib 4mg/día. Un paciente con DA había recibido prednisona oral 30mg/día/durante un mes antes de iniciar tratamiento con upadacitinib 30mg/día (caso n.° 16; tabla 1), y otro paciente atópico que llevaba un mes en tratamiento con dupilumab 300mg/cada 2 semanas recibió, además, upadacitinib 15mg/día para controlar un brote muy severo (caso n.° 17; tabla 1).
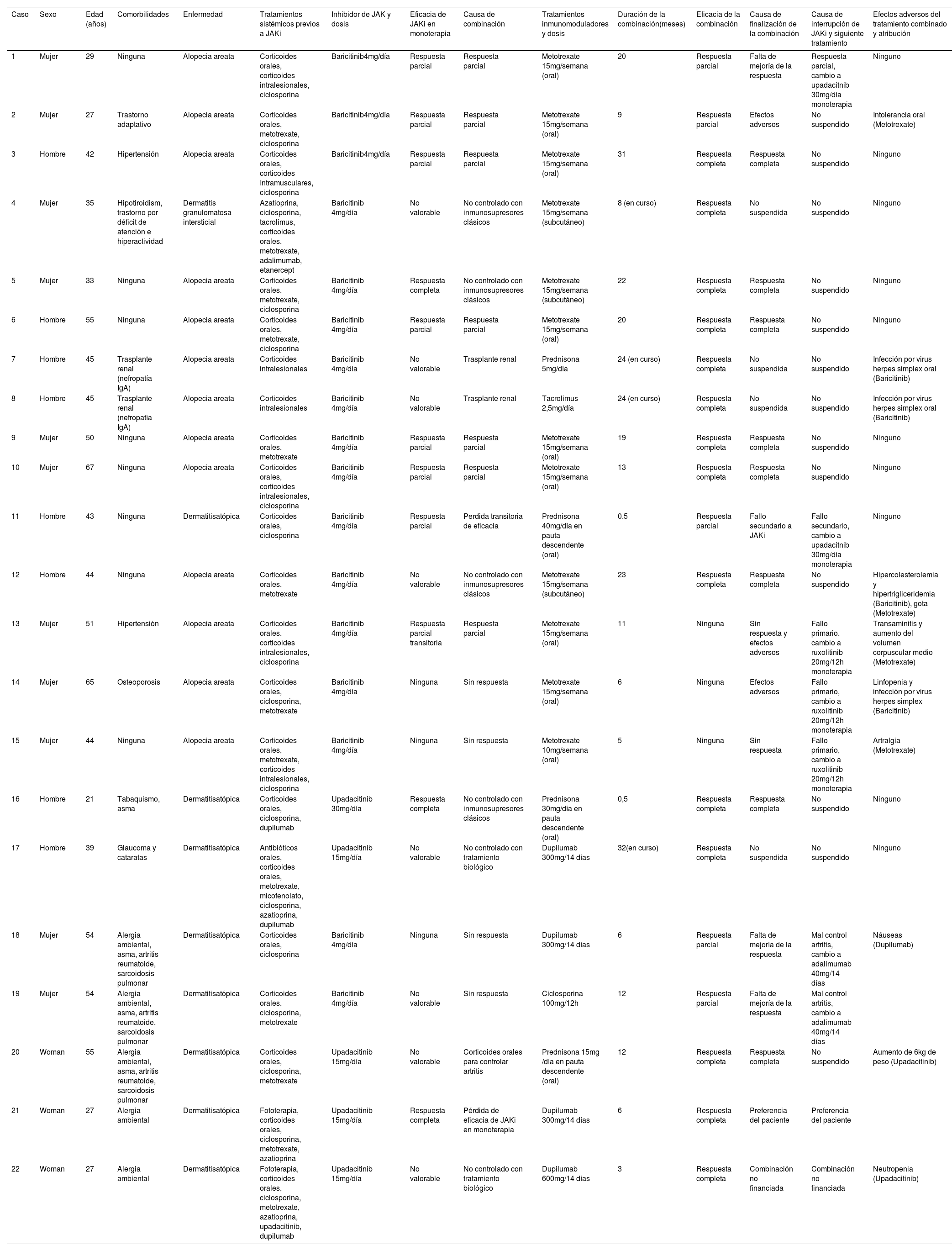
Pacientes en tratamiento con terapia combinada con inhibidores de JAK y otros tratamientos inmunomoduladores
| Caso | Sexo | Edad (años) | Comorbilidades | Enfermedad | Tratamientos sistémicos previos a JAKi | Inhibidor de JAK y dosis | Eficacia de JAKi en monoterapia | Causa de combinación | Tratamientos inmunomoduladores y dosis | Duración de la combinación(meses) | Eficacia de la combinación | Causa de finalización de la combinación | Causa de interrupción de JAKi y siguiente tratamiento | Efectos adversos del tratamiento combinado y atribución |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Mujer | 29 | Ninguna | Alopecia areata | Corticoides orales, corticoides intralesionales, ciclosporina | Baricitinib4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 20 | Respuesta parcial | Falta de mejoría de la respuesta | Respuesta parcial, cambio a upadacitnib 30mg/día monoterapia | Ninguno |
| 2 | Mujer | 27 | Trastorno adaptativo | Alopecia areata | Corticoides orales, metotrexate, ciclosporina | Baricitinib4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 9 | Respuesta parcial | Efectos adversos | No suspendido | Intolerancia oral (Metotrexate) |
| 3 | Hombre | 42 | Hipertensión | Alopecia areata | Corticoides orales, corticoides Intramusculares, ciclosporina | Baricitinib4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 31 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 4 | Mujer | 35 | Hipotiroidism, trastorno por déficit de atención e hiperactividad | Dermatitis granulomatosa intersticial | Azatioprina, ciclosporina, tacrolimus, corticoides orales, metotrexate, adalimumab, etanercept | Baricitinib 4mg/día | No valorable | No controlado con inmunosupresores clásicos | Metotrexate 15mg/semana (subcutáneo) | 8 (en curso) | Respuesta completa | No suspendida | No suspendido | Ninguno |
| 5 | Mujer | 33 | Ninguna | Alopecia areata | Corticoides orales, metotrexate, ciclosporina | Baricitinib 4mg/día | Respuesta completa | No controlado con inmunosupresores clásicos | Metotrexate 15mg/semana (subcutáneo) | 22 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 6 | Hombre | 55 | Ninguna | Alopecia areata | Corticoides orales, metotrexate, ciclosporina | Baricitinib 4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 20 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 7 | Hombre | 45 | Trasplante renal (nefropatía IgA) | Alopecia areata | Corticoides intralesionales | Baricitinib 4mg/día | No valorable | Trasplante renal | Prednisona 5mg/día | 24 (en curso) | Respuesta completa | No suspendida | No suspendido | Infección por virus herpes simplex oral (Baricitinib) |
| 8 | Hombre | 45 | Trasplante renal (nefropatía IgA) | Alopecia areata | Corticoides intralesionales | Baricitinib 4mg/día | No valorable | Trasplante renal | Tacrolimus 2,5mg/día | 24 (en curso) | Respuesta completa | No suspendida | No suspendido | Infección por virus herpes simplex oral (Baricitinib) |
| 9 | Mujer | 50 | Ninguna | Alopecia areata | Corticoides orales, metotrexate | Baricitinib 4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 19 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 10 | Mujer | 67 | Ninguna | Alopecia areata | Corticoides orales, corticoides intralesionales, ciclosporina | Baricitinib 4mg/día | Respuesta parcial | Respuesta parcial | Metotrexate 15mg/semana (oral) | 13 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 11 | Hombre | 43 | Ninguna | Dermatitisatópica | Corticoides orales, ciclosporina | Baricitinib 4mg/día | Respuesta parcial | Perdida transitoria de eficacia | Prednisona 40mg/día en pauta descendente (oral) | 0.5 | Respuesta parcial | Fallo secundario a JAKi | Fallo secundario, cambio a upadacitnib 30mg/día monoterapia | Ninguno |
| 12 | Hombre | 44 | Ninguna | Alopecia areata | Corticoides orales, metotrexate | Baricitinib 4mg/día | No valorable | No controlado con inmunosupresores clásicos | Metotrexate 15mg/semana (subcutáneo) | 23 | Respuesta completa | Respuesta completa | No suspendido | Hipercolesterolemia y hipertrigliceridemia (Baricitinib), gota (Metotrexate) |
| 13 | Mujer | 51 | Hipertensión | Alopecia areata | Corticoides orales, corticoides intralesionales, ciclosporina | Baricitinib 4mg/día | Respuesta parcial transitoria | Respuesta parcial | Metotrexate 15mg/semana (oral) | 11 | Ninguna | Sin respuesta y efectos adversos | Fallo primario, cambio a ruxolitinib 20mg/12h monoterapia | Transaminitis y aumento del volumen corpuscular medio (Metotrexate) |
| 14 | Mujer | 65 | Osteoporosis | Alopecia areata | Corticoides orales, ciclosporina, metotrexate | Baricitinib 4mg/día | Ninguna | Sin respuesta | Metotrexate 15mg/semana (oral) | 6 | Ninguna | Efectos adversos | Fallo primario, cambio a ruxolitinib 20mg/12h monoterapia | Linfopenia y infección por virus herpes simplex (Baricitinib) |
| 15 | Mujer | 44 | Ninguna | Alopecia areata | Corticoides orales, metotrexate, corticoides intralesionales, ciclosporina | Baricitinib 4mg/día | Ninguna | Sin respuesta | Metotrexate 10mg/semana (oral) | 5 | Ninguna | Sin respuesta | Fallo primario, cambio a ruxolitinib 20mg/12h monoterapia | Artralgia (Metotrexate) |
| 16 | Hombre | 21 | Tabaquismo, asma | Dermatitisatópica | Corticoides orales, ciclosporina, dupilumab | Upadacitinib 30mg/día | Respuesta completa | No controlado con inmunosupresores clásicos | Prednisona 30mg/día en pauta descendente (oral) | 0,5 | Respuesta completa | Respuesta completa | No suspendido | Ninguno |
| 17 | Hombre | 39 | Glaucoma y cataratas | Dermatitisatópica | Antibióticos orales, corticoides orales, metotrexate, micofenolato, ciclosporina, azatioprina, dupilumab | Upadacitinib 15mg/día | No valorable | No controlado con tratamiento biológico | Dupilumab 300mg/14 días | 32(en curso) | Respuesta completa | No suspendida | No suspendido | Ninguno |
| 18 | Mujer | 54 | Alergia ambiental, asma, artritis reumatoide, sarcoidosis pulmonar | Dermatitisatópica | Corticoides orales, ciclosporina | Baricitinib 4mg/día | Ninguna | Sin respuesta | Dupilumab 300mg/14 días | 6 | Respuesta parcial | Falta de mejoría de la respuesta | Mal control artritis, cambio a adalimumab 40mg/14 días | Náuseas (Dupilumab) |
| 19 | Mujer | 54 | Alergia ambiental, asma, artritis reumatoide, sarcoidosis pulmonar | Dermatitisatópica | Corticoides orales, ciclosporina, metotrexate | Baricitinib 4mg/día | No valorable | Sin respuesta | Ciclosporina 100mg/12h | 12 | Respuesta parcial | Falta de mejoría de la respuesta | Mal control artritis, cambio a adalimumab 40mg/14 días | |
| 20 | Woman | 55 | Alergia ambiental, asma, artritis reumatoide, sarcoidosis pulmonar | Dermatitisatópica | Corticoides orales, ciclosporina, metotrexate | Upadacitinib 15mg/día | No valorable | Corticoides orales para controlar artritis | Prednisona 15mg /día en pauta descendente (oral) | 12 | Respuesta completa | Respuesta completa | No suspendido | Aumento de 6kg de peso (Upadacitinib) |
| 21 | Woman | 27 | Alergia ambiental | Dermatitisatópica | Fototerapia, corticoides orales, ciclosporina, metotrexate, azatioprina | Upadacitinib 15mg/día | Respuesta completa | Pérdida de eficacia de JAKi en monoterapia | Dupilumab 300mg/14 días | 6 | Respuesta completa | Preferencia del paciente | Preferencia del paciente | |
| 22 | Woman | 27 | Alergia ambiental | Dermatitisatópica | Fototerapia, corticoides orales, ciclosporina, metotrexate, azatioprina, upadacitinib, dupilumab | Upadacitinib 15mg/día | No valorable | No controlado con tratamiento biológico | Dupilumab 600mg/14 días | 3 | Respuesta completa | Combinación no financiada | Combinación no financiada | Neutropenia (Upadacitinib) |
La duración media del tratamiento combinado fue de 14,8 meses (con 4 pacientes aún en tratamiento combinado hasta la fecha). Se obtuvo una respuesta completa en 8 pacientes diagnosticados de AA y en 3 casos de DA, lo que representa un 61,1%. Sin embargo, en 3 pacientes (17%), todos diagnosticados de AA (casos n.° 13, 14 y 15; tabla 1) no se observó ninguna mejoría significativa tras una duración media de 7 meses de tratamiento combinado con baricitinib y metotrexato a 15mg/semana. En 2 de estos casos, también se observaron EA —linfopenia leve y elevación de transaminasas— que llevaron a la interrupción de ambos tratamientos y al inicio de otro inhibidor de JAK.
Se notificaron un total de 13EA distintos en 10 pacientes diferentes. Dos tercios de estos EA se produjeron en 5 pacientes que tomaban metotrexato 15mg/semana más baricitinib 4mg/día para tratar la alopecia areata. Estos acontecimientos aparecieron tras una media de 9 meses (intervalo: 1-23 meses) de uso de la terapia combinada. Los EA notificados incluyeron intolerancia oral (1), artralgia (1), episodio de gota (1), reactivación de herpes simple bucal (3), dislipidemia (1), linfopenia leve (810 células ×109/l) (1), elevación de transaminasas (alanina aminotransferasa: 87,6U/l; aspartato aminotransferasa: 50,99U/l) (1), y un aumento del volumen corpuscular medio a 106fl (1).
Además, un paciente con DA en tratamiento con baricitinib 4mg/día y dupilumab experimentó náuseas durante varios días tras la primera dosis de dupilumab. Otro paciente, tratado durante 6 meses con upadacitinib 30mg/día y prednisona 10mg, experimentó un aumento de peso de 6kg, lo que obligó a reducir la dosis de los JAKi en un 50%. Un paciente con DA, en tratamiento con upadacitinib 15mg/día y terapia intensificada con dupilumab (caso n.° 22; tabla 1), desarrolló una neutropenia leve (1.030células/109/l); sin embargo, este paciente tenía antecedentes de neutropenia y ya había reducido la dosis de upadacitinib en un 50%. Por último, un receptor de trasplante renal presentó una recidiva de herpes bucal a los 12 meses de tratamiento con baricitinib mientras recibía tratamiento inmunosupresor con tacrolimus y prednisona (casos n.° 7 y 8; tabla 1).
En 7 pacientes que obtuvieron una respuesta completa, se retiró el inmunosupresor clásico. Por el contrario, en 4 casos se suspendieron ambos tratamientos y se sustituyeron por otro inhibidor de la JAK debido al fracaso del tratamiento primario. En tres pacientes con AA que habían recibido baricitinib y metotrexato se cambió el tratamiento a ruxolitinib 20mg/2 veces al día. Además, en 2 pacientes se decidió el cambio de baricitinib 4mg/día a upadacitinib 30mg/día: en uno de ellos, debido a una respuesta estacionaria en un paciente con AA y en el otro, debido a un fracaso secundario del inhibidor de JAK en un paciente con DA (casos n.° 1 y 11; tabla 1).
En función de nuestra experiencia, la combinación de los JAKi con inmunomoduladores sistémicos parece ser una estrategia factible para un porcentaje considerable de pacientes, en particular aquellos que no pueden obtener una respuesta completa en monoterapia o con comorbilidades específicas. Cabe destacar que se observaron efectos secundarios en cerca del 50% de los pacientes, todos ellos clasificados como leves. Solo en 2 pacientes se interrumpió el tratamiento combinado, cambiando a otro JAKi en monoterapia, no debido a la gravedad de los EA sino a que se disponía de una alternativa factible. Cabe destacar que durante el seguimiento no se notificaron EA de especial interés, como tromboembolia venosa, embolia pulmonar, eventos adversos cardiovasculares importantes, neoplasias, infecciones graves o cáncer de piel no melanoma.
Aunque este tratamiento combinado introduce nuevos abordajes para el manejo de enfermedades inflamatorias dermatológicas complejas, la validación de nuestras observaciones requiere más estudios prospectivos con cohortes de mayor amplitud y seguimiento.
Declaración de la IA generativa y las tecnologías asistidas por IA en el proceso de escrituraDurante la preparación de este trabajo los autores utilizaron ChatGPT para optimizar el recuento de palabras del artículo y la ortografía. Tras utilizar esta herramienta, los autores revisaron y editaron el contenido según la necesidad y asumen toda la responsabilidad por el contenido de la publicación.
Conflicto de interesesClara Muntaner-Virgili declara haber recibido apoyo para la asistencia a reuniones por parte de Lilly y Sanofi.
Clara Torrecilla-Vall-llossera declara haber recibido apoyo para la asistencia a congresos por parte de Lilly, Sanofi y LEO Pharma.
Montserrat Bonfill-Orti declara haber recibido honorarios como ponente por parte de Lilly, Abbvie, LEO Pharma y Sanofi.
Ignasi Figueras-Nart declara haber recibido honorarios como ponente y asesor por parte de Lilly, Abbvie y Sanofi.