La utilización clínica habitual de los fármacos biológicos en el tratamiento de la psoriasis es en segunda línea, es decir, tras el uso previo de un fármaco clásico. Sin embargo, en casos particulares –particularidades del paciente o criterio médico– se realiza la indicación en primera línea. No existen estudios sobre las características demográficas, clínicas y de seguridad de los pacientes que reciben fármaco biológico en primera línea. Como objetivo primario se pretende determinar dichas características de acuerdo con la iniciación de la terapia biológica en primera o segunda línea.
Material y métodoSe realizó un estudio descriptivo, multicéntrico, de 181 pacientes que iniciaron tratamiento biológico como primer fármaco sistémico para control de su psoriasis moderada-grave, y que forman parte del Registro Español de Acontecimientos Adversos Asociados con Medicamentos Biológicos en Dermatología, entre enero de 2008 y noviembre de 2016.
ResultadosLos pacientes de ambos grupos son muy similares, si bien se evidencia que el grupo que recibe el biológico en primera línea presenta una edad más avanzada, sin que se justifique por gravedad de la enfermedad (PASI) ni por el tiempo de evolución de esta desde el diagnóstico. En este grupo de pacientes es más frecuente la presencia de hipertensión, diabetes y hepatopatía. No hemos encontrado diferencias en motivos de suspensión ni seguridad entre ambos grupos.
ConclusionesNo se han encontrado diferencias relevantes entre los 2 grupos, lo cual refuerza la seguridad de los fármacos biológicos en este contexto.
Biologic drugs are usually prescribed as second-line treatment for psoriasis, that is, after the patient has first been treated with a conventional psoriasis drug. There are, however, cases where, depending on the characteristics of the patient or the judgement of the physician, biologics may be chosen as first-line therapy. No studies to date have analyzed the demographics or clinical characteristics of patients in this setting or the safety profile of the agents used. The main aim of this study was to characterize these aspects of first-line biologic therapy and compare them to those observed for patients receiving biologics as second-line therapy.
Material and methodWe conducted an observational study of 181 patients treated in various centers with a systemic biologic drug as first-line treatment for moderate to severe psoriasis between January 2008 and November 2016. All the patients were registered in the Spanish Registry of Adverse Events Associated with Biologic Drugs in Dermatology.
ResultsThe characteristics of the first- and second-line groups were very similar, although the patients receiving a biologic as first-line treatment for their psoriasis were older. No differences were observed for disease severity (assessed using the PASI) or time to diagnosis. Hypertension, diabetes, and liver disease were all more common in the first-line group. There were no differences between the groups in terms of reasons for drug withdrawal or occurrence of adverse effects.
ConclusionsNo major differences were found between patients with psoriasis receiving biologic drugs as first- or second-line therapy, a finding that provides further evidence of the safety of biologic therapy in patients with psoriasis.
La psoriasis es una enfermedad crónica que afecta al 2,3% de la población española1. El porcentaje de pacientes que presentan formas graves se desconoce, aunque se estima en un 20,3% para la psoriasis y un 25,7% para la artritis psoriásica2. Un porcentaje de estos pacientes se encuentra infratratado3 y en nuestro país se estima que solo el 6,8% recibe terapia sistémica4.
Los fármacos biológicos autorizados para su uso son: etanercept, infliximab, adalimumab, ustekinumab, secukinumab e ixekizumab. Habitualmente, según ficha técnica, su indicación es en segunda línea, es decir, en pacientes que no han respondido a otras terapias. Sin embargo, en situaciones clínicas particulares o bajo criterio médico se utilizan en primera línea.
Por ello, nos planteamos como objetivo principal de este estudio caracterizar los perfiles demográficos, clínicos y de seguridad de los pacientes que han recibido tratamiento biológico en primea línea (naive) en comparación con los que lo recibieron en segunda línea, a partir del Registro Español de Acontecimientos Adversos Asociados con Medicamentos Biológicos en Dermatología (BIOBADADERM), que incluye como cohorte prospectiva desde 2008 a los pacientes con psoriasis moderada-grave que están recibiendo terapia sistémica, fármacos biológicos y no biológicos. Toda la información sobre la cohorte está en la página web (https://biobadaderm.fundacionpielsana.es/).
Material y métodoDiseño del estudio. Población de estudio y grupos de comparaciónEn este estudio se han incluido los pacientes de BIOBADADERM desde enero de 2008 hasta noviembre de 2016. A partir de esta población se han constituido 2 cohortes: a) naive: pacientes que reciben un biológico en primera línea (etanercept, infliximab, adalimumab, ustekinumab y secukinumab; ixekizumab no se incluyó por no estar aprobado al cierre temporal), y b) clásica: pacientes con tratamiento sistémico clásico previo (acitretina, ciclosporina, metotrexato; no se incluyó apremilast por no estar aprobado en ese momento). La fototerapia no se consideró como tratamiento sistémico. De todos ellos se disponía de datos como: sexo, edad, duración de la enfermedad, PASI basal, tipo de psoriasis, comorbilidades asociadas, tratamientos utilizados, motivos de suspensión, tiempo de seguimiento y acontecimientos adversos (AA).
Análisis estadísticoLos datos demográficos y descriptivos se expresan como números absolutos y porcentajes en las variables categóricas, y como medias y desviaciones estándar (DE) en las cuantitativas continuas. Se realizó un análisis descriptivo entre las variables de cada grupo utilizando la prueba de chi-cuadrado y la t de Student. Hemos representado gráficamente las incidencias acumuladas de los motivos de suspensión: ineficacia, AA y remisión, como estimación de la probabilidad de suspensión del tratamiento. Cada uno de los motivos se ha considerado que representa un riesgo competitivo para los otros. También se han estimado las tasas de incidencia de los AA por cada 1.000 personas-año, con su intervalo de confianza del 95% (IC 95%). Posteriormente se han comparado las tasas en cada grupo mediante la razón de tasas de incidencia, con su correspondiente IC 95%.
ResultadosEsta serie comprende 915 pacientes en tratamiento con un fármaco biológico: 181 pacientes recibieron un biológico como primera línea y 734 tras haber fracasado un fármaco clásico.
El grupo de pacientes naive incluye un 39% de mujeres, con una puntuación media de PASI de 15 (DE 9,9) y una duración media de la enfermedad antes del inicio del biológico de 18 años (DE 13), sin diferencias con la población clásica. La edad media de inicio del biológico en la cohorte naive es significativamente más alta (54 años, DE 15) que en la clásica (p<0,01).
En la tabla 1 se detallan los aspectos clínicos de los pacientes, como el tipo clínico de psoriasis o la presencia de artritis psoriásica, que no evidencian diferencias significativas, y comorbilidades asociadas donde sí que existe una mayor prevalencia estadísticamente significativa para el grupo naive, de hipertensión arterial, diabetes, hepatopatía crónica, hepatitis C y VIH.
Descripción de los pacientes
| Tratamiento biológico en primera línea (naive) | Tratamiento biológico en segunda línea | p | |
|---|---|---|---|
| Datos demográficos | |||
| Pacientes, n (%) | 181 (100) | 734 (100) | |
| Mujeres, n (%) | 71 (39) | 277 (38) | 0,72 |
| Edad en años, media (DE) | 54 (15) | 50 (14) | <0,01 |
| Duración enfermedad al inicio del tratamiento en años, media (DE) | 18 (13) | 19 (12) | 0,33 |
| PASI, media (DE) | 15 (9,9) | 15,1 (9,1) | 0,91 |
| Diagnóstico, n (%) | |||
| Psoriasis en placas | 172 (95) | 703 (96) | 0,66 |
| Psoriasis en gotas | 9 (5) | 30 (4) | 0,54 |
| Eritrodermia | 3 (2) | 22 (3) | 0,45 |
| Psoriasis pustulosa | 1 (1) | 12 (2) | 0,48 |
| Psoriasis palmoplantar | 3 (2) | 8 (1) | 0,46 |
| Psoriasis anular | 0 (0) | 5 (1) | 0,59 |
| Artritis psoriásica | 26 (14) | 151 (21) | 0,06 |
| Comorbilidades, n (%) | |||
| Cardiopatía isquémica | 7 (4) | 12 (2) | 0,17 |
| Insuficiencia cardiaca | 2 (1) | 4 (1) | 0,49 |
| Hipertensión arterial | 56 (31) | 124 (17) | <0,01 |
| Diabetes | 41 (23) | 73 (10) | <0,01 |
| Hipercolesterolemia | 50 (28) | 167 (23) | 0,37 |
| Cáncer en los últimos 5 años | 2 (1) | 12 (2) | 0,83 |
| Hepatopatía crónica | 22 (12) | 40 (5) | <0,01 |
| Insuficiencia renal crónica | 5 (3) | 11 (1) | 0,51 |
| EPOC | 6 (3) | 16 (2) | 0,56 |
| Hepatitis B | 7 (4) | 26 (4) | 0,97 |
| Hepatitis C | 11 (6) | 13 (2) | 0,01 |
| VIH | 0 (0) | 5 (1) | <0,01 |
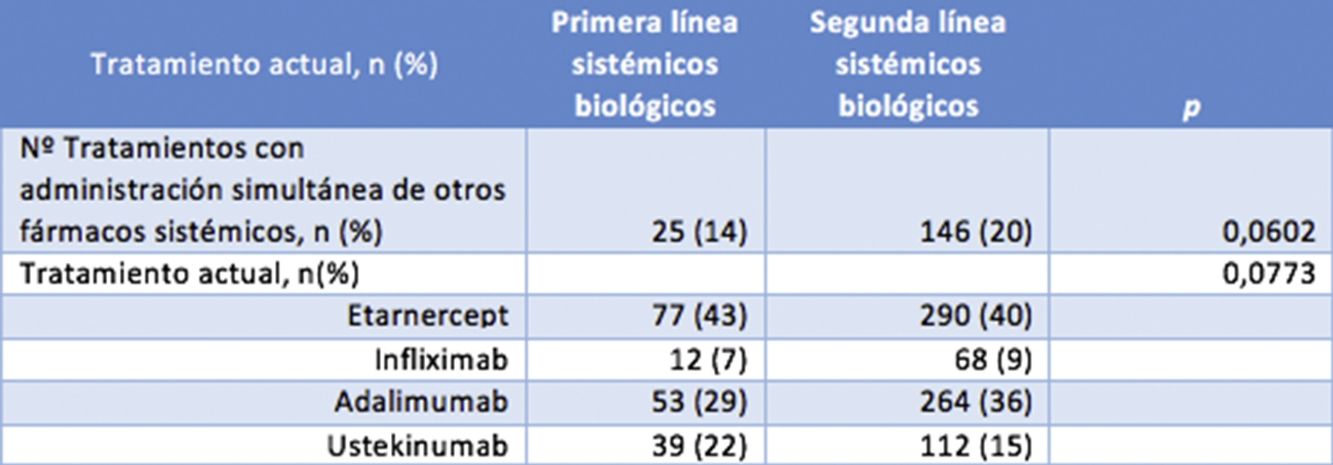
Los fármacos que recibieron los 2 grupos de pacientes se muestran en la tabla 2, así como el porcentaje en el que se asoció un tratamiento sistémico. En ninguno de los casos se observaron diferencias estadísticamente significativas entre los 2 grupos.
Descripción de los tratamientos
| Tratamiento actual | Biológico en primera línea | Biológico en segunda línea | p |
|---|---|---|---|
| Tratamientos con administración simultánea de otros fármacos sistémicos, n (%) | 25 (14) | 146 (20) | 0,06 |
| Tratamiento actual, n (%) | 0,08 | ||
| Etanercept | 77 (43) | 290 (40) | |
| Infliximab | 12 (7) | 68 (9) | |
| Adalimumab | 53 (29) | 264 (36) | |
| Ustekinumab | 39 (22) | 112 (15) |
La media del tiempo de seguimiento de los tratamientos biológicos en el grupo naive se situó en 2,58 años, sin diferencia con la cohorte clásica (2,38 años) (p=0,41).
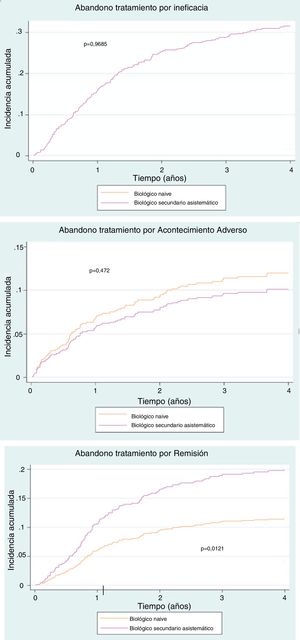
De los 181 pacientes naive, un 68,5% habían suspendido el tratamiento en algún momento del estudio. Los motivos del abandono se recogen en la tabla 3. No se encontraron diferencias significativas entre ambas cohortes (p=0,19). Sin embargo, hay una mayor incidencia acumulada de abandono de tratamiento por remisión en la cohorte clásica (p=0,01) (fig. 1 a-c).
Motivos de suspensión del tratamiento
| Motivo | Tratamiento biológico en primera línea (naive) | Tratamiento biológico en segunda línea | p |
|---|---|---|---|
| Causas de retirada, n (%) | 124 (100) | 550 (100) | 0,19 |
| Ineficacia o pérdida de efectividad | 51 (41) | 217 (39) | |
| Acontecimiento adverso | 21 (17) | 75 (14) | |
| Embarazo o deseo gestacional | 4 (3) | 13 (2) | |
| Pérdida de seguimiento | 9 (7) | 38 (7) | |
| Remisión | 17 (14) | 130 (24) | |
| Otros | 22 (18) | 77 (14) |
Los pacientes naive presentaron un total de 310 AA (467 pacientes-año), de los que 278 fueron leves, 30 graves y 2 mortales (adenocarcinoma de páncreas y tumor carcinoide del ciego). La tasa global de AA (por 1.000 pacientes-año) de la cohorte naive fue de 763,5 (IC 95% 593,6-741,7), sin diferencias significativas con la clásica (tasa de incidencia 1,12; IC 95% 0,99-1,27; p=0,084) (tabla 4).
Descripción de los acontecimientos adversos (AA)
| Tratamiento biológico en primera línea (naive) | Tratamiento biológico en segunda línea | |||
|---|---|---|---|---|
| Frecuencia, n (pacientes-año) | ||||
| Todos los AA | 310 (467) | 1.052 (1.772) | ||
| AA graves | 30 (467) | 88 (1.772) | ||
| AA no graves | 278 (467) | 963 (1.772) | ||
| AA mortales | 2 (467) | 1 (1.772) | ||
| Tasa de incidencia (IC 95%) | p | |||
| Tasa bruta (por 1.000 personas-año) (IC 95%) | ||||
| Todos los AA | 763,5 (593,6-741,7) | 593,6 (558,8-630,6) | 1,12 (0,99-1,27) | 0,08 |
| AA graves | 64,2 (44,9-91,8) | 49,7 (40,3-61,2) | 1,29 (0,85-1,96) | 0,22 |
| AA no graves | 595,0 (529,1-669,3) | 543,4 (510,1-578,8) | 1,10 (0,96-1,25) | 0,18 |
| AA mortales | 4,3 (1,1-17,1) | 0,6 (0,1-4,0) | 7,59 (0,69-83,69) | 0,09 |
La mayoría de los datos publicados respecto a eficacia y seguridad de los fármacos biológicos en psoriasis hacen referencia a su uso como segunda línea de tratamiento en pacientes con psoriasis moderada-grave. No obstante, las guías del grupo de psoriasis de la Academia Española de Dermatología recogen además su indicación en otras situaciones (tabla 5)5. Por ello, disponer de una cohorte de pacientes naive a biológicos es de interés para evaluar dichos aspectos.
Recomendaciones: criterios de elegibilidad para el tratamiento biológico
| A. Tratamiento sistémico (convencional o biológico): está indicado en pacientes con psoriasis moderada/grave, es decir, que cumplan alguna de las siguientes condiciones: No controlable con tratamiento tópico Con formas extensas (BSA≥5-10%), PASI≥10 Empeoramiento rápido Compromiso de áreas visibles Limitación funcional (palmoplantar, genital) Con percepción de gravedad subjetiva (DLQI>10) Eritrodermia o psoriasis pustulosa extensa Asociada a artropatía psoriásica |
| B. Tratamiento biológico: según las fichas técnicas, actualmente están indicados en el tratamiento de pacientes con psoriasis moderada/grave que no han respondido, tienen contraindicación o presentan intolerancia, efectos adversos o probable toxicidad —aguda o por dosis acumulada— a los tratamientos sistémicos clásicos, incluyendo acitretina, metotrexato, ciclosporina, fototerapia o foto(quimio)terapia, o a otros tratamientos biológicos, y se incluyen en esta definición: Pacientes en quienes no se consigue un control eficaz con los agentes sistémicos disponibles, solos o en combinación Pacientes que presentan recaídas rápidas (en menos de 3 meses) después de suspender cualquier tipo de tratamiento Pacientes que requieren dosis altas de tratamiento sistémico clásico (con riesgo de aparición de efectos adversos por toxicidad aguda o acumulada en un porcentaje significativo de pacientes) Pacientes con intolerancia a algún tratamiento sistémico (aparición de toxicidad o efectos adversos a dosis eficaces) o riesgo elevado (por la dosis o la duración del tratamiento, susceptibilidad individual, factores de riesgo individual: edad, sexo, comorbilidades o posibles interacciones medicamentosas) de toxicidad acumulativa con metotrexato, ciclosporina, acitretina o foto(quimio)terapia, incluso en ausencia de alteraciones analíticas Pacientes que por razones laborales, de horario, desplazamiento o disponibilidad no sean susceptibles de recibir tratamiento con foto(quimio)terapia |
Fuente: Puig et al.5.
En este estudio se incluyeron 915 pacientes en tratamiento biológico incluidos en BIOBADADERM, de los que 181 (19,78%) eran pacientes naive.
Aunque el perfil de pacientes entre ambas cohortes es muy parecido, los naive reciben tratamiento a una edad más avanzada (54 vs. 50 años; p=0,003), sin que se justifique por el grado de afectación (PASI naive 15 vs. PASI clásica 15,1; p=0,91) ni por el tiempo de evolución desde el diagnóstico (naive 18 vs. clásica 19; p=0,33). A pesar de la precaución inicial con respecto al uso de biológicos en mayores, en un estudio previo del grupo ya se había confirmado la tendencia creciente a utilizarlos6. Además, llama la atención que en ambos grupos los pacientes tengan que esperar una media de 18 años para recibir un tratamiento sistémico (biológico o sistémico), aunque se desconoce si estos datos son similares en otras series.
En ocasiones, es la presencia de comorbilidades la que dificulta la indicación de un fármaco clásico. De hecho, en este estudio se aprecia que los pacientes naive presentan más hipertensión arterial (31 vs. 17%; p<0,01), diabetes (23 vs. 10%; p<0,01), hepatopatía crónica (12 vs. 5%; p<0,01) y hepatitis C (6 vs. 2%; p=0,015). También es significativa la diferencia respecto a la presencia previa de VIH (2 vs. 1%; p<0,01), si bien no podemos asegurar que fueran esas las causas directas del uso del biológico inicial.
La distribución de fármacos biológicos empleados es similar. En ambos grupos, el más usado fue etanercept, seguido de adalimumab, ustekinumab e infliximab, similar a otras series publicadas7–9. Por lo tanto, no parece que el prescriptor aplique criterios distintos al hacer la elección del fármaco en primera o segunda línea.
El porcentaje de casos que asociaban un sistémico fue similar (14 vs. 20%; p=0,08). No había tampoco diferencias respecto al tiempo medio de seguimiento (2,58 vs. 2,41 años; p=0,41). Por lo tanto, los datos evidencian que los pacientes fueron manejados bajo los mismos criterios clínicos.
Las causas de retirada del fármaco de ambas cohortes fueron similares en cuanto a porcentajes globales (p=0,19). Sin embargo, en la incidencia acumulada se aprecia una menor suspensión por remisión significativa en la cohorte naive respecto a la clásica (p=0,01). Este hecho no se justifica por diferencias ni en la gravedad ni en el manejo clínico, por lo que de no existir algún factor de confusión, plantearía la posibilidad de la existencia de un comportamiento de control de la enfermedad distinto al utilizarlos en primera o segunda línea.
La tasa bruta global (1.000 personas-año) de AA de la cohorte naive fue ligeramente superior a la clásica, pero sin diferencias significativas (p=0,08). Tampoco se observaron diferencias entre las 2 cohortes al analizar separadamente las tasas de AA. En total, se registraron 3 casos de AA mortal (2 en la cohorte naive y uno en la clásica) (tabla 4). No parece que el momento de indicación de un biológico modifique sus efectos adversos y se les podría asignar un grado de seguridad similar.
Sin duda, el uso de un biológico en primera línea de tratamiento sistémico plantea cuestiones interesantes: ¿la indicación del biológico en primera línea modifica la evolución de la enfermedad?, ¿se conseguiría un blanqueamiento más rápido e intenso?, ¿se controlarían las potenciales comorbilidades asociadas a la enfermedad, especialmente la degeneración osteoarticular cuando asocia artritis?, ¿se mantendrían los mismos datos de seguridad cuando se utiliza en primera o segunda línea?
Estas cuestiones conducen a plantearse las siguientes hipótesis: a) la intervención terapéutica precoz en psoriasis podría modificar la evolución natural de la enfermedad y el manejo terapéutico, y b) ¿habría diferencias si empezamos con un fármaco químico respecto a empezar directamente con un biológico? Se han publicado al respecto datos en artritis reumatoide que apoyan la idea de que su uso en primera línea modifica la actividad inflamatoria y la gravedad10–12, pero hasta ahora no disponemos de datos en psoriasis. En cualquier caso, el escenario clínico no es comparable, ya que la artritis reumatoide puede tener un curso degenerativo crónico, que no es propio de la psoriasis, aunque sí de la artritis psoriásica.
En la práctica clínica es habitual que el paciente psoriásico cambie de un fármaco a otro, bien por falta de respuesta, bien por eventos adversos o comorbilidades que aconsejen modificarlo. Por otra parte, su utilización durante largo tiempo demuestra que estos fármacos son seguros13 y, teniendo en cuenta además que los biológicos alcanzan objetivos terapéuticos óptimos en mayor porcentaje que los clásicos, ¿por qué no iniciar entonces el tratamiento con un biológico?
Razones de indicación y económicas aparte, para abordar esta cuestión se debería disponer de más datos respecto a eficacia y seguridad del uso de biológicos en primera línea.
Una de las fortalezas del estudio presentado es que recoge datos de una cohorte importante de pacientes naive a fármacos biológicos (181), en seguimiento continuo y homogéneo según la práctica clínica habitual en 13 centros diferentes. Por otro lado, la limitación principal es que la indicación por paciente no es aleatoria, sino por criterios de cada prescriptor, pudiendo verse influidos por características como la edad, las comorbilidades, la disponibilidad del fármaco en cada centro, la experiencia y otros desconocidos, que pudieran generar factores de confusión.
Otra limitación es que los datos para medir la eficacia son pobres, ya que solo se dispone de medidas indirectas, como el motivo de suspensión o la duración de los tratamientos.
ConclusionesEn general, los pacientes de los 2 grupos son muy similares, si bien la proporción de comorbilidades y la edad de inicio son superiores en los pacientes naive. Una posible explicación sería que el fármaco biológico se elige para evitar efectos adversos o interacciones con dichas comorbilidades.
El hecho de no haber encontrado diferencias en términos de motivos de suspensión y seguridad entre ambos grupos refuerza la seguridad de los fármacos biológicos en este contexto.
Agradecemos a Novartis la financiación de este estudio.
Conflicto de interesesDr. G. Carretero Hernández ha colaborado como consultor, ponente y/o investigador de ensayos clínicos patrocinados por laboratorios AbbVie, Janssen-Cilag, Pfizer, MSD, Celgene, Novartis, Almirall S. A. y Leo-Pharma. Dr. C. Ferrándiz ha colaborado como consultor y/o ponente y/o participante en ensayos clínicos promovidos por Laboratorios Abbvie, Janssen Pharmaceuticals Inc., Pfizer, Celgene, Lilly y Almirall S. A., y ha recibido becas de Laboratorios Abbvie. Dra. R. Rivera Díaz ha participado como consultora para Abbvie Laboratories, Janssen Pharmaceuticals Inc., MSD y Pfizer-Wyeth. Dr. E. Daudén Tello ha colaborado como consultor para Abbvie Laboratories, Amgen, Astellas, Celgene, Centocor Ortho Biotech Inc., Galderma, Glaxo, Jansen-Cilag, Leo-Pharma, MSD, Novartis y Pfizer Inc., ha recibido honorarios de Abbott Laboratories, Amgen, Celgene, Janssen-Cilag Pty Ltd., Leo-Pharma, MSD, Novartis y Pfizer Inc., ha participado como ponente para Abbvie Laboratories, Janssen Pharmaceuticals Inc., MSD y Pfizer Inc., y ha recibido becas de Abbvie Laboratories, Janssen Pharmaceuticals Inc. y Pfizer Inc. Dr. P. de la Cueva-Dobao ha colaborado como consultor para Janssen-Cilag, Abbvie, MSD, Pfizer y Leo-Pharma. Dr. E. Herrera-Ceballos ha colaborado como consultor y ponente para Abbvie Laboratories, Janssen Pharmaceuticals Inc. y Pfizer-Wyeth. Dr. I. Belinchón Romero ha colaborado como consultor para Pfizer-Wyeth, Janssen Pharmaceuticals Inc., MSD, Almirall S. A., Lilly y Leo-Pharma, y como ponente para Abbvie, Pfizer-Wyeth, Janssen Pharmaceuticals Inc., Novartis y MSD. Dr. J.L. López-Estebaranz ha colaborado como consultor para Abbott Laboratories, Janssen Pharmaceuticals Inc., MSD y Pfizer-Wyeth y como ponente para Abbvie Laboratories, Janssen Pharmaceuticals Inc., MSD y Pfizer-Wyeth. Dra. M. Alsina Gibert ha colaborado como consultora para Abbvie Laboratories y Merck/Schering-Plough. Dr. J.L. Sánchez-Carazo ha colaborado como consultor para Abbvie Laboratories, Janssen Pharmaceuticals Inc., MSD y Pfizer-Wyeth. Dra. M. Ferrán Farrés ha colaborado como consultora para MSD, Pfizer, Abbvie y Janssen, como ponente para MSD, Abbvie y Janssen, y como investigadora para MSD, Abbvie, Pfizer y Janssen. Dr. J.M. Carrascosa Carrillo ha colaborado como consultor y ponente para Abbvie Laboratories, Janssen Pharmaceuticals Inc., MSD, Pfizer-Wyeth, Novartis y Celgene. Dra. M. Llamas Velasco ha recibido ayuda económica para participar en congresos por parte de Abbvie, Janssen y Novartis, y ha colaborado como ponente de Abbvie y Novartis. Dra. D. Ruiz Genao ha recibido ayuda económica para participar en congresos por parte de Pfizer, Abbvie, Janssen y Novartis, y ha colaborado como ponente para Abbvie, Pzifer, Janssen y Novartis. Dr. I. García-Doval ha recibido ayuda económica para participar en congresos por parte de Merck/Schering-Plough, Pfizer y Janssen. El resto de los autores declara no tener ningún conflicto de intereses.