El propranolol, un betabloqueante no selectivo, sigue siendo la primera línea de tratamiento para el hemangioma infantil problemático. Sin embargo, aunque poco frecuente, un subgrupo de pacientes experimenta efectos secundarios indeseables, lo que despierta el interés sobre otros betabloqueantes selectivos. Presentamos una amplia serie de casos de 46 lactantes tratados con éxito con atenolol, un bloqueante selectivo beta-1.
Propranolol, a non-selective beta-blocker, remains the first line of treatment for problematic infantile hemangioma. However, although rarely, a subset of patients experience undesirable side effects, raising interest in other selective beta-blockers. We present a large case series of 46 infants treated successfully with oral atenolol, a selective beta-1 blocker.
El hemangioma infantil (HI) es el tumor benigno más común en la infancia1,2. Hasta la fecha, el principal tratamiento para el HI es el propranolol oral, un betabloqueante no selectivo2. Sin embargo, una minoría de los pacientes sometidos a este tratamiento experimenta efectos secundarios indeseables, lo que limita su empleo3–5. El presente informe describe una experiencia multicéntrica con atenolol oral, un bloqueante selectivo beta-1, en 46 pacientes con HI, demostrando su eficacia y efectos secundarios.
Materiales y métodosSe incluyeron 46 lactantes, tratados entre agosto del 2016 y marzo del 2018, procedentes de 2 institutos nacionales de salud del niño, en Lima, Perú. Todos los HI necesitaron tratamiento por riesgo funcional, desfiguración cosmética y falta de respuesta a los tratamientos previos o aparición de efectos secundarios al propranolol. Este estudio no fue evaluado por un comité de revisión ética. Los padres de los pacientes recibieron información acerca de los efectos y los eventos adversos del tratamiento y dieron su consentimiento antes de iniciar este. Todos los pacientes que iniciaban el tratamiento con atenolol necesitaron una exploración física, un electrocardiograma basal y una evaluación por parte del cardiólogo pediátrico. En cada visita de seguimiento se registraba la frecuencia cardiaca y la presión sanguínea.
Se indicó a todos los pacientes el tratamiento con atenolol oral 1mg/kg en dosis diaria en un entorno ambulatorio. La dosificación del atenolol se ajustó según la ganancia de peso en cada visita mensual y, si se observaba una respuesta inadecuada, se aumentaba la dosis hasta un máximo de 3mg/kg. Se llevaron a cabo controles con documentación fotográfica al inicio, a las 2 semanas y mensualmente hasta finalizar el tratamiento (figs. 1 y 2).
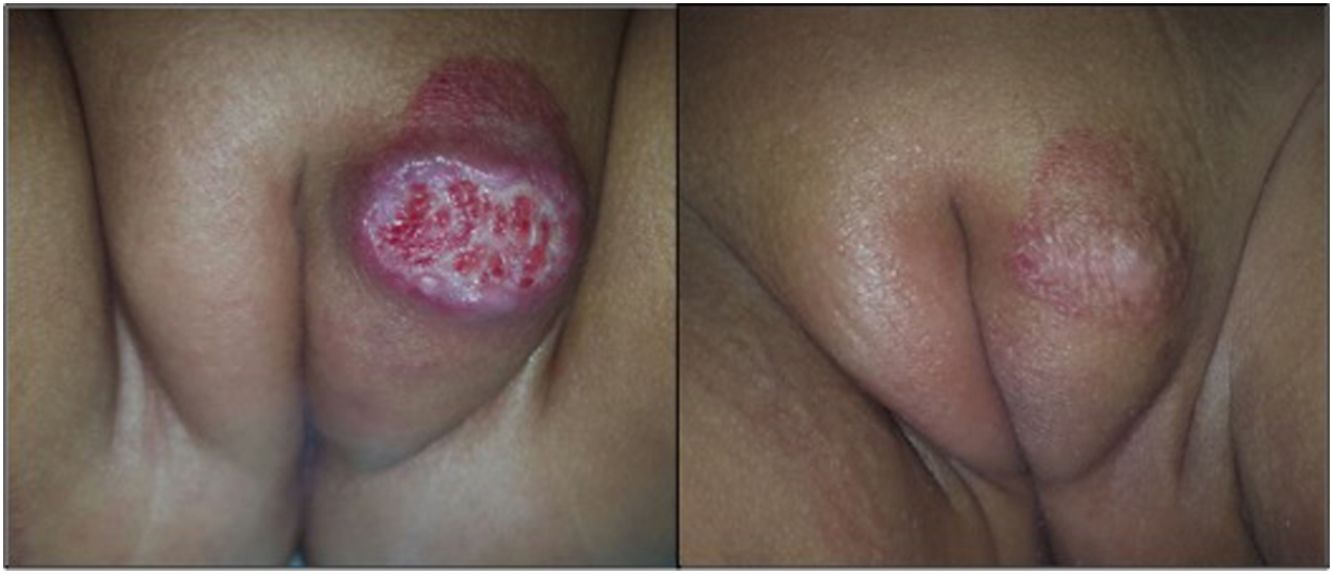
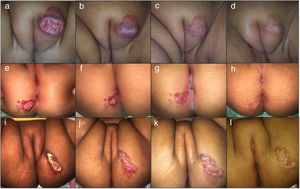
Fotografías clínicas de una niña de 7 meses de edad con un HI mixto focal ulcerado del labio mayor y de 2 niñas de 4 meses de edad con HI superficial focal ulcerado de las nalgas, todos ellos tratados con atenolol oral. Se observan los cambios en el color, el tamaño y la cicatrización de las heridas al inicio del tratamiento (a, e, i), a las 2 semana (b, f, j), a los 4 meses (c, g, k) y a los 6 meses (d, h, l).
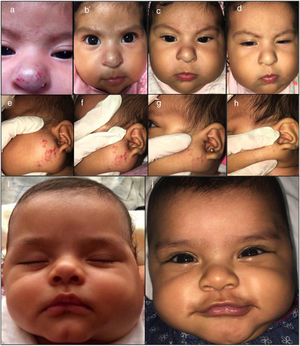
Fotografías clínicas de una niña de 2 meses de edad con un HI mixto nasal y de una niña de 4 meses de edad con un HI mixto parotídeo, tratadas con atenolol oral. Se muestran los cambios en el tamaño al inicio del tratamiento (a, e, i), en el mes 1 (b, f), a los 2 meses (c, g) y a los 4 meses (d, h, j).
La involución clínica se evaluó mediante fotografías clínicas en centros ambulatorios en los que se valoró el cambio de color, el ablandamiento a la palpación y la reducción del tamaño. El resultado del tratamiento se clasificó como involución completa (presencia de telangiectasias o tejido fibroadiposo residual), regresión parcial y no respuesta. En cada visita se registraron los efectos secundarios.
ResultadosEl estudio se llevó a cabo sobre 46 lactantes, de los cuales 35 (76,1%) eran niñas y 11 (23,9%) niños, que presentaban un total de 55 HI. El 61,8% de los HI se localizaron en la zona de la cabeza y el cuello; el 16,4% en las extremidades, el 14,5% en los genitales y el 7,3% en el tronco. Por el tipo de HI, el 60% fueron superficiales, el 32,7% mixtos y el 7,3% profundos. De todos los HI, el 12,7% mostraban ulceración. Cuatro pacientes en nuestra series se habían sometido a un tratamiento con propranolol, que se suspendió como consecuencia de los efectos secundarios. La edad media de inicio del tratamiento con atenolol fue de 4,35 meses (rango de edad entre 1 y 34 meses).
El tratamiento duró un promedio de 6,4 meses (rango 4-17 meses). Todos los pacientes respondieron observándose una involución completa en el 61,8% de los pacientes y una remisión parcial en el 38,2%. Los HI ulcerados presentaron un cierre completo de la herida en un tiempo medio de 16,4 días (fig. 1). No se observó recurrencia tras la interrupción del tratamiento. El 23,9% de los pacientes mostraron efectos secundarios moderados. El principal efecto secundario notificado se redujo a una diarrea transitoria leve. Únicamente un paciente presentó alteración moderada del sueño al inicio del tratamiento, con resolución espontánea. No se informó de efectos adversos como hipoglucemia, broncoespasmo, bradicardia o hipotensión.
DiscusiónDesde la aprobación de la FDA, el propranolol, un bloqueante lipofílico betaadrenérgico no selectivo, continúa siendo el tratamiento fundamental del HI1,2. Sin embargo, en algunas ocasiones el propranolol puede presentar efectos secundarios no deseados y de ahí el interés mostrado últimamente por alternativas terapéuticas con una eficacia similar3,4. El atenolol es un bloqueante selectivo beta-1 hidrofílico cuyo mecanismo de acción sobre el HI aún es desconocido4,5. Sin embargo, en comparación con el propranolol, se han observado varias ventajas. Primero, al evitar los receptores beta-2, se elude la hiperreactividad bronquial y la hipoglucemia. Segundo, sus propiedades hidrofílicas restringen el paso a la barrera hematoencefálica y, consecuentemente, reducen las alteraciones del sueño6. El atenolol también se administra una vez al día, por lo que proporciona una mejor adherencia al tratamiento4–8.
Previamente, el único estudio aleatorizado comparativo atenolol vs. propranolol demostró eficacias similares con menores efectos secundarios relacionados con el broncoespasmo4. Estudios posteriores han mantenido una consistencia similar con estos resultados5,7,8. En nuestra serie de casos, logramos demostrar excelentes resultados con atenolol al tiempo que no se observaron efectos secundarios adversos. Otro resultado interesante es la rapidez de la respuesta al atenolol en los 7 HI ulcerados. Aunque se trata de un subgrupo pequeño de nuestros HI tratados, comparativamente un estudio previo mostró una media de 8 semanas para la curación completa de la herida9. Adicionalmente, se prescribió a todos nuestros hemangiomas ulcerados sulfato de cinc al 1% (15ml en 50ml de agua) como curas tópicas 2 veces al día, hasta alcanzar la epitelización completa.
ConclusiónPresentamos una serie de casos no aleatorizados sin cegamiento la evaluación de 46 pacientes con HI tratados exitosamente con atenolol oral. Nuestros hallazgos se basan en observaciones clínicas. Teniendo en cuenta estas limitaciones, se ha probado que el atenolol oral es una alternativa eficaz y segura para el tratamiento de los HI problemáticos.
Proponemos el atenolol como una primera línea de tratamiento. Aunque nuestro estudio tiene sus limitaciones, sirve para proporcionar evidencia clínica adicional para futuros estudios comparativos formales dirigidos a evaluar la eficacia del atenolol frente al propranolol para confirmar nuestros hallazgos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos a los padres de nuestros pacientes su cooperación, apoyo y el habernos concedido su consentimiento para la publicación de las imágenes clínicas en este manuscrito.