La dermatomiositis (DM) cursa con diversas manifestaciones cutáneas, algunas de las cuales están asociadas a neoplasias internas. Hasta la fecha, se han reportado informes de casos individuales de DM vesículo-ampollosa en la literatura inglesa1-6. Describimos aquí cinco casos de DM vesículo-ampollosa en pacientes con neoplasias internas.
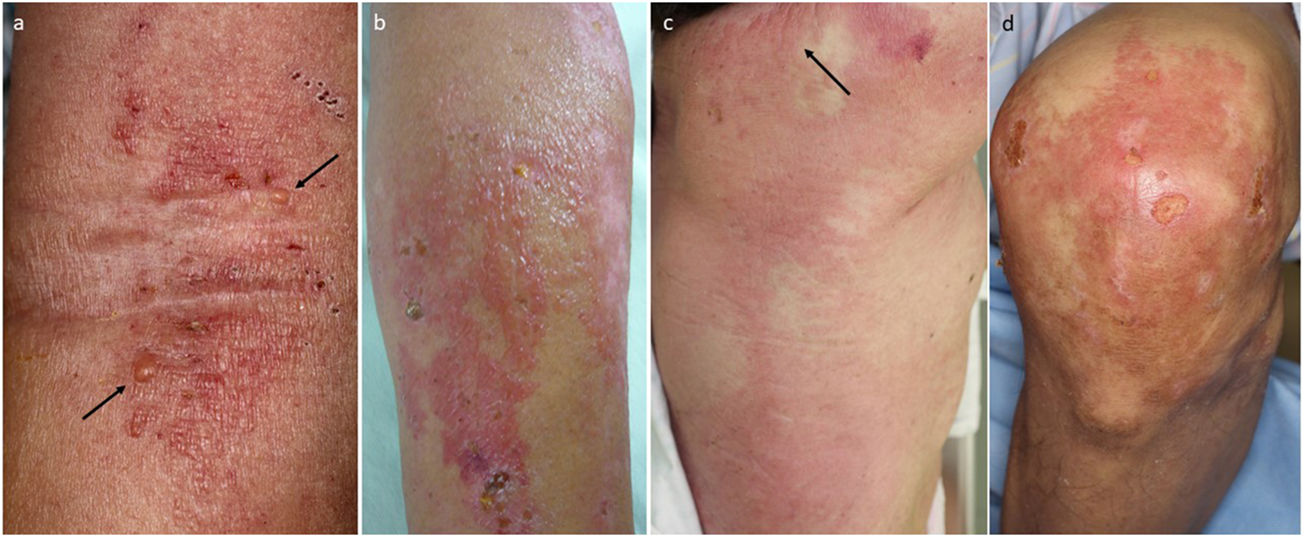
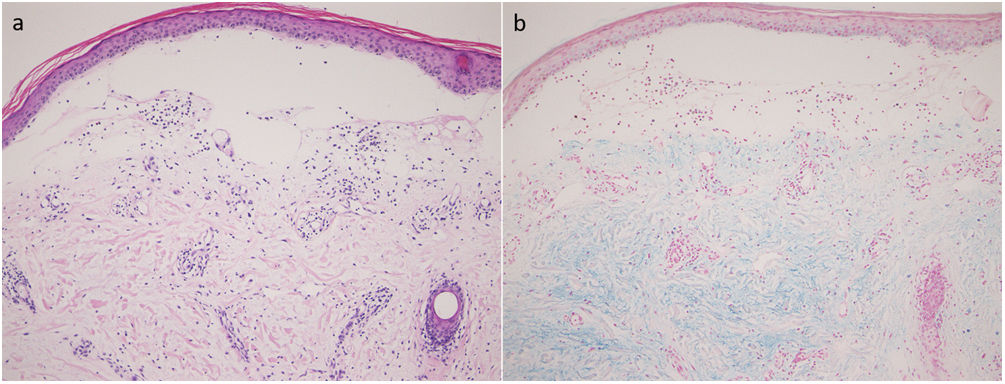
El presente estudio incluyó cinco pacientes con DM, que desarrollaron vesículas y/o ampollas durante su curso. El diagnóstico de DM se basó en los criterios diagnósticos propuestos por Bohan et al.7. El diagnóstico de DM clínicamente amiopática se realizó sobre la base de los criterios de clasificación propuestos por Sontheimer8. Los pacientes fueron cuatro varones y una mujer, con un rango de edad de 68 a 76años (edad media: 71,6años). La localización de la lesión ampollosa fue la siguiente: codo (n=2), parte superior del brazo (n=1), rodilla (n=1), tronco (n=1) y hombro (n=1) (fig. 1). Se realizó biopsia de la lesión ampollosa en cuatro casos (casos1 a4), que reveló edema subepidérmico marcado con depósito de mucina en la dermis superior (fig. 2). Los hallazgos de inmunofluorescencia directa fueron negativos en la zona de membrana basal en todos los casos. Otros signos cutáneos observados fueron pápulas de Gottron (n=4), poiquilodermia (n=3), eritema maligno (n=2), eritema facial de tipo dermatitis seborreica (n=1) y eritema flagelado (n=1). Tres casos (casos1, 3 y5) estuvieron acompañados de miositis, y un caso (caso4) fue diagnosticado de DM clínicamente amiopática. En un solo caso (caso1), se detectaron autoanticuerpos específicos de miositis, es decir, anticuerpos anti-TIF-1γ. No se observó enfermedad pulmonar intersticial (EPI) en ninguno de los casos. Se observaron neoplasias en todos los casos: cáncer de pulmón (n=3), cáncer de esófago (n=1) y cáncer de ovario (n=1). Tres casos (casos2, 4 y5) fueron tratados con quimioterapia. En el caso1 se diagnosticó cáncer de esófago tras el alta de nuestro hospital, no siendo clara la situación médica detallada del paciente. En el caso3 existieron muchas lesiones metastásicas en el momento del diagnóstico de cáncer de ovario, no pudiendo tratarse a la paciente con quimioterapia debido a su mala situación general. Tres casos (casos1, 3 y4) fueron tratados con prednisolona oral. El paciente del caso1 tuvo disfagia progresiva y severa, siendo tratado con metilprednisolona (1.000mg/diarios durante tres días consecutivos), terapia de inmunoglobulina intravenosa en tres tiempos, prednisolona y metotrexato. Sin embargo, la función deglutoria no se recuperó totalmente y el paciente desarrolló neumonía por aspiración repetidamente. Tres pacientes (casos3 a5) murieron debido a las neoplasias transcurridos 6meses, 1año y 2años del diagnóstico de DM, respectivamente. Se desconoció el pronóstico de los dos casos restantes (casos1 y2). En todos los casos, las lesiones ampollosas aparecieron paralelamente al inicio o el incremento de la actividad de DM, que fue diagnosticada más o menos al mismo tiempo de descubrirse el cáncer o el desarrollo de metástasis (tabla 1).
Cinco pacientes con presentación de dermatomiositis vesículo-ampollosa
| Caso | Edad | Sexo | Sitio de la lesión ampollosa | Otras lesiones cutáneas | Enfermedad pulmonar intersticial | Neoplasia | Miositis | CK (U/l)45-163 | ANA | Tratamiento |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 74 | M | Codo | Pápulas de Gottron, poiquilodermia, dermatitis seborreica, sangrado en pliegue ungueal | − | Esófago | + | 8.028 | 320 (homogéneo) | mPSL, PSL, IVIG, MTX |
| 2 | 68 | M | Parte superior del brazo | Pápulas de Gottron, poiquilodermia | − | Pulmón | Sin datos | 462 | 160 (homogéneo y moteado) | Quimioterapia |
| 3 | 76 | F | Tronco | Pápulas de Gottron, eritema maligno | − | Ovario | + | 264 | 80 (homogéneo) | PSL |
| 4 | 72 | M | Codo, hombro | Eritema flagelado, eritema maligno | − | Pulmón | − | 139 | < 40 | PSL, Quimioterapia |
| 5 | 68 | M | Rodilla | Pápulas de Gottron, poiquilodermia | − | Pulmón | + | 2.966 | < 160 | Quimioterapia |
CK: creatincinasa; IVIG: inmunoglobulina intravenosa; mPSL: metilprednisolona; MTX: metotrexato; PSL: prednisolona.
La formación de vesículas en la DM es relativamente rara, aunque está altamente asociada a la neoplasia interna. Todos nuestros pacientes tenían cánceres sólidos, es decir, cáncer de pulmón (n=3), cáncer de esófago (n=1) y cáncer de ovario (n=1). Se excluyó la erupción ampollosa inducida por fármacos. De acuerdo con el informe de Kubo et al.1, se revisaron 19 casos de DM vesículo-ampollosa, de los cuales 6 casos fueron varones y 13 casos fueron mujeres. Se observó neoplasia interna en 10 casos: en ovario (n=4), cuello uterino (n=2), estómago (n=1), trompa uterina (n=1), glándula mamaria (n=1) y pulmón (n=1). Tras su informe, recopilamos 17 casos de DM vesículo-bullosa, incluyendo aquellos con cáncer de mama (n=3), cáncer nasofaríngeo (n=2), cáncer de ovario (n=1), cáncer de pulmón (n=1), linfoma maligno (n=1), cáncer de colon (n=1), cáncer de estómago (n=1) y cáncer de tiroides (n=1). Sin embargo, no existió neoplasia en 6 casos, y se observó EPI en 4 casos. La incidencia de neoplasia interna fue muy superior en los pacientes con DM vesículo-ampollosa, en comparación con aquellos sin lesiones ampollosas1.
Se examinaron los anticuerpos específicos de miositis en muy pocos de nuestros casos, dado que el examen de dichos anticuerpos ha estado disponible muy recientemente. Los anticuerpos anti-TIF-1γ se examinaron en un caso (caso1), que reflejó títulos positivos. La prevalencia del cáncer en los pacientes con positividad anti-TIF-1γ varía entre el 38 y el 80%9. Un informe reciente sugiere que el cambio inusual de los antígenos tumorales puede desencadenar una respuesta autoinmune mediante inmunidad de reacción cruzada, causando daño muscular10. Sin embargo, se desconoce el mecanismo de inducción de la formación vesicular asociado a antígenos tumorales.
En conclusión, en una DM la lesión vesículo-ampollosa es un signo cutáneo paraneoplásico de neoplasia interna, y no de EPI. Los facultativos deberán tener en cuenta la DM vesículo-ampollosa.
Conflicto de interesesLos autores declaran la ausencia de conflicto de intereses.