La micosis fungoide foliculotropa es una variante de mal pronóstico y presentación clínica variada. Se ha planteado que la estadificación TNMB usada para esta neoplasia no es útil. En una propuesta reciente basada en aspectos clínicos e histológicos, se clasifica en enfermedad temprana y avanzada, encontrando diferencias pronósticas entre las 2categorías. El objetivo de este estudio fue comparar la supervivencia de estos 2 grupos en nuestra población.
Materiales y métodosSe realizó un estudio observacional retrospectivo de serie de casos donde se evaluó la evolución clínica de los pacientes con micosis fungoide foliculotropa tratados en el Instituto Nacional de Cancerología entre el 2008 y el 2020, realizando un análisis comparativo de supervivencia entre aquellos que tienen enfermedad temprana y enfermedad avanzada.
ResultadosSe incluyó a un total de 21 pacientes, 11 de los cuales presentaban enfermedad temprana y 10 enfermedad avanzada. Se identificaron 7 decesos, todos ellos en los pacientes con enfermedad avanzada. La supervivencia global de la población total a 5 años fue del 62%, mientras que para la población con enfermedad avanzada fue del 40%. No hubo diferencias en la supervivencia según la estadificación TNMB.
ConclusiónLa estadificación TNMB no es útil para los pacientes con una micosis fungoide foliculotropa. Por el contrario, la nueva clasificación clínico-patológica parece brindar información pronóstica fiable y permite tomar medidas terapéuticas acordes.
Folliculotropic mycosis fungoides is a variant that has poor prognosis and a variable clinical presentation. Concerns have been expressed that the current TNMB staging of this tumor may not be useful. A recently developed classification system based on clinical and histologic variables classifies this tumor as early or advanced, a distinction found to correlate with prognosis. The aim of this study was to compare survival in FMF in Colombia between patients with early versus advanced tumors.
Material and methodsRetrospective, observational study of clinical course and outcomes in patients with FMF treated at the National Cancer Institute of Colombia between 2008 and 2020. Survival was compared between early and advanced disease.
ResultsTwenty-one patients (11 with early FMF and 10 with advanced FMF) were studied. Seven patients, all with advanced disease, died. Survival at 5 years was 62% overall and 40% for patients with advanced FMF. No differences were observed when survival was analyzed according to TNMB stage.
ConclusionsTNMB staging is not useful in FMF. The new classification system based on clinicopathologic features appears to provide reliable information for assessing prognosis and guiding treatment decisions.
La micosis fungoide (MF) es el linfoma cutáneo primario más frecuente, correspondiendo a un 50% de los linfomas cutáneos1,2 y al 81,8% de los linfomas cutáneos manejados en el Instituto Nacional de Cancerología (INC) en el 20193, con una incidencia de 5,7 casos por millón de habitantes2,4,5. La MF tiene múltiples variantes clínicas, clínico-patológicas e histopatológicas: la foliculotropa (MFF) es una variante clinicopatológica reconocida por la Organización Mundial de la Salud, siendo entre el 5-10% de las MF y el 2,8% en nuestra población2,6-8.
La MFF es una enfermedad que afecta en una mayor proporción a los hombres y cuyo inicio está entre la quinta y sexta década de la vida7,9,10. Su presentación clínica es diversa, caracterizándose inicialmente por su compromiso folicular y presentándose como áreas alopécicas, pápulas foliculares, lesiones similares a una queratosis pilar, milia, lesiones acneiformes, con quistes y comedones, y facies leonina, aunque también puede presentarse como una MF clásica9,10. La MFF se caracteriza por un infiltrado foliculotropo, predominantemente CD4+, con o sin epidermotropismo y, en algunas ocasiones, mucinosis folicular4,7,9,10.
El pronóstico de la MFF, clásicamente, se describe como el de la MF en estadio tumoral, con una supervivencia a 5 años que varía entre el 68 y el 75%1,2,11, además de tener una respuesta menor a las terapias dirigidas a la piel y un peor pronóstico que la MF. Por ello, se ha planteado que su estatificación por el sistema Tumor Node Metastasis Blood Staging system (TNMB) actual no es útil1,10-12 y se ha propuesto una estatificación diferente2,13. Hodak et al. propusieron la clasificación de MFF en enfermedad temprana o avanzada14. En la primera incluía los parches, la alopecia, las lesiones acneiformes, similares a la queratosis pilaris o milia, y las placas no infiltradas. En la enfermedad avanzada se incluye a los pacientes con unas placas clínicamente infiltradas, asociando la densidad del infiltrado perifolicular a la placa avanzada, y esta última a un peor pronóstico. Posteriormente, van Santen et al. refinaron esta clasificación teniendo como eje el infiltrado linfoide perifolicular. Así, la placa temprana se caracterizaba por un infiltrado perifolicular e intrafolicular escaso, con células pequeñas, y en cambio, la placa avanzada un infiltrado difuso o confluente, compuesto por unas células de tamaño mediano o grande. Los autores encontraron diferencias en su supervivencia, siendo a 10 años del 80% para la enfermedad temprana y del 25% para la avanzada12.
En este estudio se describen las características clínicas e histológicas de la MFF en una muestra de pacientes, verificando si existe MFF en ambos estadios, temprano y tardío, a través de un seguimiento retrospectivo de los casos del INC como fue descrito por van Santen et al. Además, se realizó un análisis de supervivencia según el tipo de MFF.
MétodosSe realizó un estudio observacional retrospectivo tipo serie de casos, siguiendo la metodología STROBE, donde se describen la supervivencia, las características clínicas y de respuesta al tratamiento de la totalidad de pacientes tratados del INC en el periodo comprendido entre enero del 2008 y junio del 2020, diagnosticados de MFF por la existencia histológica de un infiltrado del epitelio folicular por linfocitos atípicos. Fueron excluidos aquellos pacientes con una transformación a célula grande al momento de la biopsia de diagnóstico o con la presencia de otras neoplasias hematolinfoides o sólidas, o aquellos con una información clínico-patológica incompleta.
La fuente primaria de información para las características clínicas, de tratamiento y respuesta recogidas para el estudio fue obtenida de los registros clínicos en SAP® bajo los códigos CIE-10 C840 (micosis fungoide) y registrada en la plataforma RedCap® (Research Electronic Data Capture). Tras la confirmación del diagnóstico, las laminillas histológicas de los casos seleccionados fueron valoradas por el Servicio de Anatomía Patología con el fin de establecer el tipo de lesión (parche, placa temprana, placa avanzada y tumor) y el grado de foliculotropismo presente en la muestra.
Esta investigación cumplió con los lineamientos establecidos por la declaración de Helsinki y las pautas éticas para la investigación biomédica preparadas por el Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS) y con los parámetros establecidos por la normativa nacional. Adicionalmente, fue aprobado por el comité de ética en investigaciones institucional y fue vigilado por un equipo de monitorización independiente que verificó la validez de la información registrada en RedCap.
Las variables clínicas, histopatológicas, de tratamiento y de respuesta clínica se presentan en tablas y se describen mediante medidas de frecuencia absoluta y relativa en el caso de las variables cualitativas, y medidas de tendencia central y dispersión para las variables cuantitativas. Se desagregaron algunas variables de interés mediante la función de tablas dinámicas de SPSS Vr. 19 (IBM Corp., Armonk, NY, EE. UU.). El tiempo de supervivencia global (SG) y supervivencia libre de enfermedad se describe de forma gráfica y con funciones de tiempo al evento, estimadas mediante el método de Kaplan-Meier. La SG se definió como el tiempo trascurrido en meses entre la fecha del diagnóstico y la fecha del último contacto y la supervivencia libre de enfermedad como el tiempo transcurrido desde la fecha de respuesta completa hasta la fecha en que se presenta recaída local o sistémica. Se comparó la SG entre los 2grupos poblacionales, aquellos con una enfermedad temprana y aquellos con una enfermedad avanzada. La confirmación del estado vital de cada paciente se realizó trimestralmente, con un periodo máximo de observación de 36 meses o hasta el fallecimiento del último paciente. Las definiciones de respuesta clínica cutánea fueron basaron en aquellas publicadas por Olsen et al.15
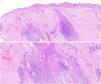
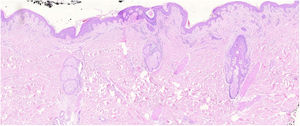
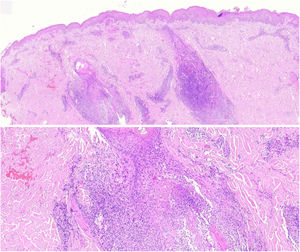
Los cortes histopatológicos en los que se dio el diagnóstico de MFF fueron evaluados por 2dermatopatólogos (SM y XR) cegados para los datos clínicos y de seguimiento. Los parámetros histológicos evaluados fueron basados en los estudios de Santen et al.12,16,17 y son los siguientes: subtipo histológico (1. enfermedad temprana o parche; 2. placa temprana; 3. placa avanzada; 4. tumor); extensión del infiltrado neoplásico (1. escaso; 2. prominente perifolicular y perivascular confinado al área perifolicular; 3. confluente perifolicular e interfolicular; 4. completo difuso); porcentaje de células atípicas en el infiltrado (< 10%; 11%-25%; > 25%); grado de foliculotropismo (leve, moderado y extensor); epidermotropismo (ausente o presente); siringotropismo (ausente o presente); mucinosis folicular (ausente o presente); infiltrado eosinófilo (ausente o presente); expresión de Ki-67 (menor del 10% o mayor al 10%), además de incluir la presencia de otros hallazgos microscópicos como la transformación a célula grande o el fenotipo CD8. Las placas fueron evaluadas en hematoxilina eosina y con marcadores de inmunohistoquímica (se presenta un ejemplo de placa temprana [fig. 1] y de avanzada [fig. 2]).
Placa temprana. Se observa un infiltrado linfoide atípico escaso perifolicular, con mucinosis folicular prominente, epidermotropismo con disposición lineal de los linfocitos en banda en la unión dermoepidérmica, llamando la atención el fondo fibrótico y con poiquiloderma, además de algunos queratinocitos apoptóticos y melanófagos.
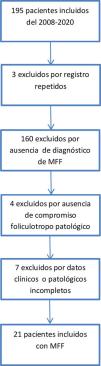
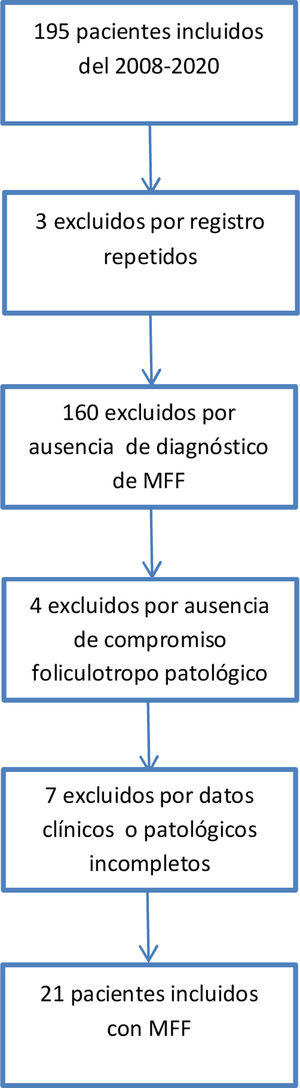
El proceso de selección de pacientes se describe en la figura 3. El 10,9% de las MF atendidas entre el 2008 y el 2020 fueron foliculotropas. Las características clínicas demográficas se describen en la tabla 1. El puntaje mSWAT15 solo se encontraba registrado en 10 historias clínicas, se obtuvo una mediana de 138,5 (12-300). La población final de estudio fue constituida por 21 pacientes tras la revisión de su historia clínica y la evaluación de las laminillas histopatológicas que confirmaron el diagnóstico de MFF. Las características patológicas se encuentran en la tabla 2. El 95,2% de los pacientes recibieron al menos una terapia tópica, el 66,7% recibió al menos una terapia sistémica y el 57,1% combinó terapias dirigidas a la piel con terapias sistémicas. La combinación más frecuente incluía el uso de interferón con PUVA, usada en 7 pacientes (33,3%), seguida de combinaciones que incluían el uso de fotoféresis con esteroide tópico en 4 pacientes (19%).
Características clínicas
| Variable | Resultado |
|---|---|
| Edad (media) | 50,9 años (9,7-85,9) |
| Edad al inicio de síntomas (media) | 45,7 años (7-85) |
| Sexo, n (%) | |
| Masculino | 16 (76,2) |
| Femenino | 5 (23,8) |
| Tumor, n (%) | |
| T1 | 5 (23,9) |
| T2 | 7 (33,3) |
| T3 | 4 (19) |
| T4 | 5 (23,8) |
| Ganglios, n (%) | |
| N0 | 19 (90,5) |
| N1 | 0 |
| N2 | 2 (9,5) |
| Metástasis, n (%) | |
| M0 | 21 (100) |
| Sangre, n (%) | |
| B0 | 20 (95,2) |
| B1 | 0 |
| B2 | 1 (4,8) |
| Estadio, n (%) | |
| IA | 5 (23,8) |
| IB | 7 (33,3) |
| IIB | 4 (19) |
| IIIA | 4 (19) |
| IVB | 1 (4,8) |
| Prurito, n (%) | |
| No | 4 (19) |
| Si | 13 (61,9) |
| Sin dato | 314,3) |
| Clínicaa, n (%) | |
| Máculas | 2 (9,5) |
| Parches | 3 (14,3) |
| Placas | 14 (66,7) |
| Pápulas foliculares | 6 (28,6) |
| Quistes/comedones | 0 (0) |
| Alopecia | 6 (28,6) |
| Tumor | 5 (23,8) |
| Eritrodermia | 5 (23,8) |
| Localizacióna, n (%) | |
| Cabeza y cuello | 15 (71,4) |
| Tronco | 14 (66,7) |
| Extremidades superiores | 14 (66,7) |
| Extremidades inferiores | 15 (71,4) |
| Glúteos | 9 (42,9) |
a Los pacientes pueden tener más de una manifestación y localización clínica.
Características histopatológicas
| Variable | Resultado |
|---|---|
| Subtipo histopatológico, n (%) | |
| Enfermedad temprana | 1 (4,8) |
| Placa temprana | 10 (47,6) |
| Placa avanzada | 7 (33,3) |
| Tumor | 3 (14,2) |
| Extensión del infiltrado neoplásico, n (%) | |
| Escaso | 3 (14,3) |
| Prominente perifolicular y perivascular confinado al área perifolicular | 9 (42,9) |
| Confluente perifolicular e interfolicular | 8 (38,1) |
| Completo difuso | 1 (4,8) |
| Porcentaje de células atípicas en el infiltrado, n (%) | |
| Menos del 10% | 3 (14,3) |
| 11%-25% | 6 (28,6) |
| Más del 25% | 12 (57,1) |
| Foliculotropismo, n (%) | n (%) |
| Leve | 3 (14,3) |
| Moderado | 7 (33,3) |
| Extenso | 11 (52,4) |
| Epidermotropismo, n (%) | |
| Ausente | 8 (38,1) |
| Presente | 13 (61,9) |
| Siringotropismo, n (%) | |
| Ausente | 14 (66,7) |
| Presente | 7 (33,3) |
| Mucinosis folicular, n (%) | |
| Ausente | 4 (19,0) |
| Presente | 17 (81,0) |
| Infiltrado eosinófilo, n (%) | |
| Ausente | 14 (66,7) |
| Presente | 7 (33,3) |
| Ki-67, n (%) | |
| Menor al 10% | 6 (28,6) |
| Mayor al 10% | 10 (47,6) |
| Sin dato | 5 (23,8) |
| Otros hallazgos, n (%) | |
| Transformación a célula grande | 2 (9,5) |
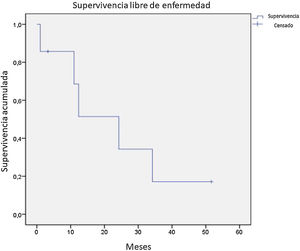
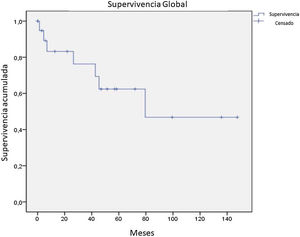
De los 21 pacientes de la serie, 7 obtuvieron una respuesta completa a la terapia recibida, 9 parcial, 1 solo enfermedad estable, 2 progresaron desde el inicio del seguimiento. De los 16 pacientes con una respuesta completa o parcial, 9 presentaron progresión durante el estudio. De los 7 pacientes que obtuvieron respuesta completa, 5 presentaron recaída, obteniendo una mediana de supervivencia libre de enfermedad de 12,4 meses (fig. 4). Tras una mediana de seguimiento de 43,2 meses, se presentaron 7 decesos durante el seguimiento, con una mediana de SG del total de 42,6 meses, y una SG a 5 años del 62% (fig. 5).
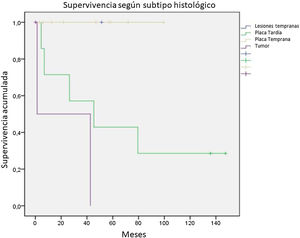
Se evaluó la SG según los grupos definidos, aquellos con una enfermedad temprana, que incluían a pacientes con enfermedad temprana o parches y placa temprana, y aquellos con una enfermedad avanzada, que incluían placa avanzada y tumores. Los 11 pacientes con una enfermedad temprana no presentaron decesos; en cambio, de los 10 pacientes con enfermedad avanzada solo 3 pacientes sobrevivieron al final del seguimiento. Al evaluar únicamente los pacientes con placa avanzada el 28,6% estaba vivo al final del seguimiento y aquellos tumorales solo el 33,3%, como se observa en la figura 6.
Se realizaron tablas de contingencia entre las variables clínicas y patológicas, con los desenlaces respuesta clínica, progresión y SG, que se muestran en la tabla 3.
Respuesta global, progresión y muerte respecto a variables clínicas e histopatológicas
| Variable | RC | RP | EE | Progresióna | Muerte |
|---|---|---|---|---|---|
| Sexo (n) | |||||
| Femenino (5) | 40% | 40% | 0% | 60% | 40% |
| Masculino (16) | 31,3% | 43,8% | 6,3% | 50% | 31,2% |
| Estadio (n) | |||||
| IA (5) | 40% | 20% | 20% | 40% | 20% |
| IB (7) | 28,6% | 57,1% | 0% | 57,1% | 75% |
| IIB (4) | 50% | 25% | 0% | 50% | 42,8% |
| IIIA (4) | 25% | 75% | 0% | 50% | 25% |
| IVB (1) | 0% | 0% | 0% | 100% | 100% |
| Subtipo (n) | |||||
| Enfermedad temprana (1) | 0% | 100% | 0% | 0% | 0% |
| Placa temprana (10) | 50% | 30% | 10% | 40% | 0% |
| Placa avanzada (7) | 28,6% | 42,9% | 0% | 85,7% | 71,4% |
| Tumor (3) | 0% | 66,6% | 0% | 33,3% | 66,6% |
| Infiltrado neoplásico (n) | |||||
| Escaso (3) | 66,6% | 33,3% | 0% | 33,3% | 0% |
| Perifolicular (9) | 33,3% | 44,4% | 11,1% | 44,4% | 22,2% |
| Perifolicular e interfolicular (8) | 25% | 37,5% | 0% | 62,5% | 50% |
| Difuso (1) | 0% | 100% | 0% | 100% | 100% |
| Porcentaje de células atípicas (n) | |||||
| Menor del 10% (3) | 66,6% | 0% | 33,3% | 33,3% | 0% |
| 11-25% (6) | 33,3% | 50% | 0% | 50% | 0% |
| Más del 25% (12) | 25% | 50% | 0% | 58,3% | 58,3% |
| Grado de foliculotropismo (n) | |||||
| Leve (3) | 33,3% | 66,6% | 0% | 33,3% | 0% |
| Moderado (7) | 42,9% | 28,6% | 14,3% | 57,1% | 14,3% |
| Extenso (11) | 27,3% | 45,5% | 0% | 54,5% | 54,5% |
| Epidermotropismo (n) | |||||
| Ausente (8) | 37,5% | 50% | 12,5% | 25% | 37,5% |
| Presente (13) | 30,8% | 38,5% | 0% | 69,2% | 30,7% |
| Siringotropismo (n) | |||||
| Ausente (14) | 21,4% | 50% | 7,1% | 35,7% | 28,5% |
| Presente (7) | 57,1% | 28,6% | 0% | 85,7% | 42,8% |
| Mucinosis folicular (n) | |||||
| Ausente (4) | 50% | 50% | 0% | 0% | 25% |
| Presente (17) | 29,4% | 41,2% | 5,9% | 64,7% | 35,3% |
| Ki-67 (n) | |||||
| Menor del 10% (6) | 33,3% | 50% | 16,6% | 33,3% | 16,6% |
| Mayor del 10% (10) | 30% | 40% | 0% | 70% | 50% |
| Sin dato (5) | 40% | 40% | 0% | 40% | 20% |
RC: respuesta completa; RP: respuesta parcial.
Los pacientes con MFF valorados en el INC se presentan en la quinta década de la vida con una edad media de inicio de 50,9 años y un predominio masculino (relación aproximada H/M=3/1), similar a los descrito en una revisión de la literatura mundial9. En dicha revisión, la edad de inicio se ubica entre los 46 y los 59 años, con una relación H/M entre 2-5/1. Cabe destacar que el tiempo medio transcurrido entre el inicio de los síntomas y el diagnóstico para nuestra población fue de 62,4 meses, mucho mayor que lo descrito de 18-48 meses, probablemente causado por los tiempos de remisión prolongados, al ser un centro de referencia único en el país. Otro aspecto que llama la atención es el aumento en la proporción de casos de MFF respecto a MF en la institución, de 4% en el reporte del 2011 de Rueda et al.6, respecto al 10,9% actual, que se asemeja más al 5-10% referido en la literatura2,7. Aunque puede ser infraestimado por los casos excluidos por datos incompletos, al ser un centro de referencia se observan más casos de los que puedan registrase en la población general.
En nuestro estudio encontramos una clara diferencia en la mortalidad de los pacientes con una enfermedad temprana respecto aquellos con una enfermedad avanzada, con una SG a 5 años del 100% de los pacientes para enfermedad temprana y del 40% para enfermedad avanzada. Hallazgos que se contrastan al valorar la mortalidad por estadios, donde no hubo relación entre la estadificación del paciente y su riesgo de muerte (tabla 3), soportando la idea de la ausencia de beneficio del uso del TNMB en la MFF1,10-12,18, reconociendo la escasa representación en número de pacientes que pudiesen tener algunos estadios. Además, otros factores histológicos, como el infiltrado neoplásico, el porcentaje de células atípicas, el grado de foliculotropismo, el siringotropismo y el Ki-67, a medida que aumentaban en su compromiso también aumentaba en la mortalidad.
Los resultados del presente estudio son similares a los hallados por Santen et al., quienes encontraron diferencias en el pronóstico de los pacientes con placas, las cuales clasificaron en temprana y avanzada, con base en la densidad del infiltrado folicular. Los pacientes con placa temprana presentaron un comportamiento similar al de los pacientes con parches y pápulas, mientras aquellos con placa avanzada se comportaban de forma similar al de los pacientes con nódulos y tumores, con una SG a 5 años del 92% para la enfermedad temprana limitada a la piel respecto al 55% de la enfermedad avanzada limitada a la piel12. Posteriormente, Santen et al.17 confirmaron sus hallazgos al evaluar pacientes con enfermedad en placa, encontrando como datos asociados a un mal pronóstico: una edad mayor 60 años, la ausencia de remisión tras el primer tratamiento, el epidermotropismo interfolicular, un infiltrado de células atípicas mayor del 25%, una expresión de Ki-67% superior al 10% y un tamaño celular mediano a grande, similar a lo encontrando en nuestro estudio. En cambio, la mucinosis folicular se asoció a mejores desenlaces en el estudio de Santen et al. respecto al presente, donde la presencia de mucina en el epitelio folicular tuvo una mayor mortalidad.
La evolución fue similar a la observada por Hodak et al.14, quienes clasificaron la MFF en enfermedad temprana y avanzada, encontrando un mayor infiltrado perifolicular, una profundidad mayor del infiltrado y un mayor número de eosinófilos y plasmocitos en las lesiones avanzadas, además de una diferencia en la supervivencia a 5 años, un 94% para la enfermedad temprana y del 69% para el avanzado. Los pacientes con estadios tempranos que presentaron una progresión de la enfermedad tenían un mayor infiltrado perifolicular. Charli-Joseph et al.18, en el 2021, publicaron la validación de los hallazgos de van Santen et al. en Estados Unidos, dividiendo la MFF en enfermedad temprana o avanzada según los hallazgos clínicos y el compromiso histológico de la enfermedad en placas, obteniendo una SG y una supervivencia específica de la enfermedad (SEE) a 5 años para la cohorte del 89%. El grupo de enfermedad temprana presentó una SG y una SEE a 5 años de 96%, mientras que el grupo de enfermedad avanzada tuvo una SG y SEE para la enfermedad de 70%.
En contraste, Deonizio et al.19, en Brasil, en su cohorte de MFF, no evidenciaron diferencias en la supervivencia entre la enfermedad temprana (estadio IA-IB) y la avanzada (≥ estadio IIB). Posteriormente, Wieser et al.10 encontraron que el estadio que más progresó fue el IB y aquellos con una menor probabilidad de supervivencia fueron los pacientes con estadios IVA y IVB, además de aquellos con una transformación a célula grande y una edad mayor de 65 años. Kalay Yildizhan et al.20 tampoco encontraron diferencias en la SEE entre aquellos con una enfermedad temprana o avanzada, cuya mediana fue de 48 meses, ni en su SG a 5 años del 83%, y a 10 años del 69%, siendo los únicos factores asociados a mortalidad la LDH aumentada y la transformación a célula grande. Los 3estudios clasificaron la enfermedad por TNMB sin tener en cuenta los hallazgos histológicos.
Este estudio tiene limitaciones: por un lado, al ser retrospectivo impide hacer asociaciones estadísticas, por otro, al ser un centro de referencia es probable que presentemos un sesgo de selección, con una sobrestimación de la cantidad real de pacientes con MFF o con casos de mayor severidad. De momento, se confirman los hallazgos de Hodak et al. y de van Santen et al., validando este abordaje pronóstico, permitiendo además un abordaje temprano agresivo de la población de pacientes con placa avanzada.
En conclusión, la MFF es una variante inusual de la MF con una peor supervivencia que la variante clásica, para la que la clasificación TNMB no es de utilidad para estimar el pronóstico. En nuestra población, la clasificación que distingue entre enfermedad temprana y avanzada, basada en los hallazgos clínicos e histológicos, permitió diferenciar 2grupos con un comportamiento claro de la enfermedad, al igual que ya ha sido demostrado en otras poblaciones. Probablemente se deba a que tiene en cuenta la presencia de una mayor carga tumoral, expresada por el mayor infiltrado linfoide atípico observado histológicamente pero que aún no tiene expresión clínica. La mayor progresión y muerte observada en los pacientes con una mayor cantidad de células atípicas en el infiltrado y con un mayor grado de extensión del foliculotropismo, parece apoyar esta hipótesis. Los estudios donde no se encuentran diferencias en la supervivencia basaban su agrupación en el TNMB, más no en la diferencia del infiltrado en la histopatología, probablemente impidiendo la correcta identificación de pacientes con un mayor riesgo.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.