Realizar un análisis coste-efectividad y coste-utilidad de ingenol mebutato en el tratamiento de la queratosis actínica en España.
MétodosSe realizó la adaptación de un modelo de Markov que simuló una cohorte de pacientes (73 años de media) con queratosis actínica en un horizonte temporal de 5 años. Los comparadores fueron diclofenaco 3% e imiquimod 5%. El análisis se desarrolló desde la perspectiva del Sistema Nacional de Salud, incluyendo costes directos sanitarios (PVPIVA con la deducción obligatoria, € 2015). La estimación de recursos se llevó a cabo por un panel de expertos y los costes unitarios se obtuvieron de bases de datos de costes nacionales. La tasa de descuento considerada fue del 3% anual. Se realizaron análisis de sensibilidad determinísticos y probabilísticos.
ResultadosIngenol mebutato fue más eficiente frente a diclofenaco, con 0,192 aclaramientos incrementales en la cara y el cuero cabelludo y 0,129 en el tronco y las extremidades. Los costes totales fueron de 551,50€ y 622,27€ comparados con 849,11€ y 844,93€ en diclofenaco (cara y cuero cabelludo y tronco y extremidades, respectivamente). Es decir, ingenol mebutato es una alternativa de tratamiento dominante frente a diclofenaco 3%. Ingenol mebutato también mostró una mayor eficacia frente a imiquimod 5%, con 0,535 vs. 0,503 aclaramientos ganados, y unos costes totales de 551,50€ vs. 527,89€, siendo la relación coste-efectividad incremental resultante de 728,64€/aclaramiento adicional.
ConclusionesIngenol mebutato resultó ser una estrategia dominante vs. diclofenaco, y eficiente, es decir, presentó mayor efectividad y mayores costes (relación coste-utilidad incremental inferior a 30.000€/AVAC) vs. imiquimod.
To perform a cost-effectiveness and cost-utility analysis of ingenol mebutate in the treatment of actinic keratosis in Spain.
MethodsWe used an adapted Markov model to simulate outcomes in a cohort of patients (mean age, 73 years) with actinic keratosis over a 5-year period. The comparators were diclofenac 3% and imiquimod 5%. The analysis was performed from the perspective of the Spanish National Health System based on direct costs (2015 retail price plus value added tax less the mandatory discount). A panel of experts estimated resources, taking unit costs from national databases. An annual discount rate of 3% was applied. Deterministic and probabilistic sensitivity analyses were performed.
ResultsThe effectiveness of ingenol mebutate—with 0.192 and 0.129 more clearances gained in treatments for face and scalp lesions and trunk and extremity lesions, respectively—was superior to diclofenac's. The total costs of treatment with ingenol mebutate were lower at € 551.50 (face and scalp) and € 622.27 (trunk and extremities) than the respective costs with diclofenac (€ 849.11 and € 844.93). The incremental cost-effectiveness and cost-utility ratios showed that ingenol mebutate was a dominant strategy vs diclofenac. Ingenol mebutate also proved to be more effective than imiquimod, based on 0.535 and 0.503 additional clearances, and total costs of € 551.50 and € 527.89 for the two drugs, respectively. The resulting incremental cost-effectiveness ratio was € 728.64 per clearance gained with ingenol mebutate vs imiquimod.
ConclusionsIngenol mebutate was a dominant treatment option vs diclofenac and was efficient vs imiquimod (i.e., more effective at a higher cost, achieving an incremental cost-utility ratio of<€30000/quality-adjusted life-years).
La queratosis actínica (QA) se manifiesta como lesiones rojas o del color de la piel normal, con grados variables de hiperqueratosis que le confieren un tacto rasposo. Se localizan en zonas fotoexpuestas (cara, cuero cabelludo y extremidades), dado que es la exposición solar el factor más importante en su desarrollo, aunque existen otros factores de riesgo1.
En Europa, la QA afecta al 15% de los hombres y al 6% de las mujeres2, con prevalencias del 34 y el 18% en>70 años (en hombres y mujeres, respectivamente)3. Un estudio epidemiológico desarrollado en España estimó que esta enfermedad afecta a un 23,5% de la población>45 años4.
La QA presenta un riesgo de progresión a carcinoma invasivo del 0,075% por lesión-año, incrementándose hasta un 0,53% por lesión si hay antecedentes de cáncer cutáneo. Extrapolando los datos, un paciente no inmunosuprimido sin historial de cáncer cutáneo, que presente 8 lesiones, tiene un riesgo del 5,8% de desarrollar carcinoma espinocelular en 10 años5.
Debido a su alta prevalencia, la QA genera un considerable gasto. En EE. UU., el cáncer cutáneo se sitúa entre los 5 cánceres de mayor coste6.
Además del potencial carcinogénico de la QA, hay que contemplar la repercusión sobre la calidad de vida de los pacientes, asociada a las enfermedades de la piel7. Las terapias disponibles para la QA abarcan desde procedimientos mínimamente invasivos, tipo criocirugía o farmacológicos, hasta técnicas menos frecuentes, como escisión por afeitado, electrodesecación y curetaje, cirugía con láser y exfoliación química8. Los desarrollos posteriores incluyen el tratamiento del campo de cancerización mediante terapia fotodinámica o tratamientos tópicos, como 5-fluorouracilo (0,5 y 5%), ingenol mebutato (0,015 y 0,05%), diclofenaco (3%) e imiquimod (2,5, 3,75 y 5%), con diversas indicaciones según la zona corporal a tratar. Estos tratamientos pretenden eliminar las lesiones visibles (lo que se denomina aclaramiento) evitando la progresión hacia carcinoma invasivo, y frenar la aparición de nuevas lesiones, aunque son frecuentes las recurrencias entre los pacientes tratados9.
En situaciones de crisis económica asociada a medidas de contención del gasto y ante un arsenal terapéutico variado, resulta interesante disponer de la mayor información posible para realizar una buena selección y asignación de los recursos. En este sentido, la evaluación económica de tecnologías sanitarias o farmacoeconomía, mediante la realización de estudios metodológicamente rigurosos que valoren tanto los costes como los beneficios en salud de diferentes alternativas, deben entenderse como una herramienta útil y complementaria a la toma de decisiones con base en datos puramente clínicos.
El objetivo del presente estudio fue estimar la eficiencia de ingenol mebutato en el tratamiento de pacientes con QA en España.
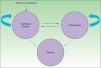
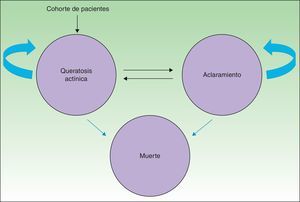
MétodosSe utilizó un modelo de Markov con 3 estados de salud (QA, aclaramiento y muerte) que simuló la evolución de la enfermedad en una cohorte hipotética de pacientes (fig. 1).
La simulación se inicia con toda la cohorte (73 años de edad promedio)4 situada en el estado «QA», en el que los pacientes pueden permanecer o a partir del cual transitan hacia «aclaramiento» o «muerte».
El modelo, mediante la transición permitida entre «aclaramiento» y «QA», recoge la posibilidad de recurrencia y de reaparición de lesiones. La evidencia disponible estima una tasa de recurrencia anual del 20%10, independientemente del tratamiento recibido.
La probabilidad de fallecer se refiere, en el presente análisis, no a la mortalidad asociada a QA, sino a la mortalidad por cualquier causa en población general11.
La inclusión de la muerte como estado de salud se realizó con intención de poder estimar la eficiencia no solo en términos de coste-efectividad, sino también en términos de coste-utilidad, es decir, expresada como coste incremental por cada año de vida ajustado por calidad (AVAC) adicional.
El desarrollo del análisis se realizó con la asesoría de un panel de expertos constituido por 5 dermatólogos de diferentes hospitales del ámbito nacional, autores firmantes del presente trabajo. Siguiendo la metodología Delphi se diseñaron cuestionarios en Word y Excel para validar y recoger información y datos necesarios para la ejecución del modelo, que fueron cumplimentados por cada uno de los expertos, y cuyas respuestas fueron posteriormente confrontadas y discutidas en una reunión presencial, donde se alcanzó un valor consensuado para cada uno de los parámetros.
Alternativas terapéuticasSe incluyeron como comparadores las alternativas farmacológicas actualmente autorizadas para el tratamiento de la QA en la cara y el cuero cabelludo, así como en el tronco y las extremidades: ingenol mebutato, diclofenaco 3% e imiquimod 5%.
Dado que no todas las alternativas disponen de indicación para tratamiento de todas las localizaciones corporales, se plantearon 3 escenarios: uno, comparando ingenol mebutato vs. diclofenaco 3% para el tratamiento de lesiones en la cara y el cuero cabelludo; el segundo, comparando ingenol mebutato frente a diclofenaco 3% en QA de tronco y extremidades; y por último, ingenol mebutato frente a imiquimod 5% en QA localizada en la cara y el cuero cabelludo.
Perspectiva, horizonte temporal y tasa de descuentoLa perspectiva del análisis fue la del Sistema Nacional de Salud, por lo que solo se consideraron recursos y costes directos sanitarios. El horizonte temporal fue de 5 años, tiempo suficiente para identificar y cuantificar la evolución de los pacientes, considerando no solo el tratamiento inicial, sino también las posibles recurrencias a medio plazo. La tasa de descuento anual aplicada fue del 3% a los costes y resultados en salud12.
Resultados en saludLa medida de eficacia de los tratamientos fueron las tasas de aclaramiento total, que en ausencia de estudios de comparación directa (head to head) se obtuvieron mediante técnicas de comparación indirecta (tabla 1), realizadas con el método de Bucher.
Resultados de las comparaciones indirectas (ingenol mebutato vs. diclofenaco 3% e imiquimod 5%)
| ID ensayo clínico | Ingenol mebutato vs. placebo DR (IC 95%) | Diclofenaco vs. placebo DR (IC 95%) | DR indirecta (IC 95%) |
|---|---|---|---|
| Comparación indirecta ingenol mebutato vs. diclofenaco 3% en cara y cuero cabelludo | |||
| PEP005-016 | 34,8 (26,3; 43,3) | ||
| PEP005-025 | 42,0 (33,0;51,0) | ||
| Rivers et al.13, 2002 | 23,1 (7,9; 38,3) | ||
| Stockfleth et al.14, 2011 | 16,6 (6,8; 26,4) | ||
| Wolf et al.15, 2001 | 28,3 (12,4; 44,3) | ||
| Agrupados | 34,8 (29,5; 46,9) | 20,6 (13,2; 27,9) | 17,6 (6,18; 29,01) |
| Comparación indirecta ingenol mebutato vs. diclofenaco 3% en tronco y extremidades | |||
| PEP005-014 | 23,1 (14,5; 31,8) | ||
| PEP005-028 | 37,1 (26,6; 47,7) | ||
| Rivers et al.13, 2002 | 23,1 (7,9; 38,3) | ||
| Stockfleth et al.14, 2011 | 16,6 (6,8; 26,4) | ||
| Wolf et al.15, 2001 | 28,3 (12,4; 44,3) | ||
| Agrupados | 29,6 (20,1; 39,1) | 20,6 (13,2; 27,9) | 9,0 (−3,0; 21,0) |
| Comparación indirecta ingenol mebutato vs. imiquimod 5% en cara y cuero cabelludo | |||
| PEP005-016 | 34,8 (26,3; 43,3) | ||
| PEP005-025 | 42,0 (33,0; 51,0) | ||
| Jorizzo et al.16, 2007 | 39,0 (28,2; 49,8) | ||
| Korman et al.17, 2005 | 41,1 (34,1; 48,2) | ||
| Agrupados | 38,2 (29,5; 46,9) | 40,5 (34,6; 46,4) | −2,3 (−12,8; 8,2) |
| Tratamiento | Eficacia | ||
| Ingenol mebutato vs. diclofenaco 3% (cara y cuero cabelludo) | Ingenol mebutato | Diclofenaco 3% | |
| 42,24% | 24,64% | ||
| Ingenol mebutato vs. diclofenaco 3% (tronco y extremidades) | Ingenol mebutato | Diclofenaco 3% | |
| 34,07% | 25,07% | ||
| Ingenol mebutato vs. imiquimod 5% (cara y cuero cabelludo) | Ingenol mebutato | Imiquimod 5% | |
| 42,24% | 44,54% | ||
DR: diferencia de riesgo; IC: intervalo de confianza.
Se realizó una revisión de la literatura para identificar ensayos clínicos en el tratamiento de la QA que evaluaran la eficacia, en términos de tasa de aclaramiento, de alguna de las alternativas evaluadas. Para los escenarios que compararon ingenol mebutato versus diclofenaco 3% se seleccionaron ensayos clínicos específicos13–15 dependiendo de la zona a tratar (cara y cuero cabelludo o tronco y extremidades); sin embargo, el escenario que evaluó ingenol mebutato frente a imiquimod 5% solo incluyó estudios16,17 de aplicación en cara y cuero cabelludo, dado que la ficha técnica de imiquimod18 no recoge la indicación para tratamiento de lesiones en tronco y extremidades.
El panel de expertos clínicos consultado durante el desarrollo del análisis estimó una adherencia al tratamiento del 90% para ingenol mebutato y del 60% para los otros tratamientos, considerando que la falta de adherencia ocasiona una disminución del 50% de la eficacia del tratamiento correspondiente.
Medida de los resultados obtenidosLa estimación de la relación coste-efectividad incremental (RCEI) y de la relación coste-utilidad incremental (RCUI) se calculó como la diferencia de costes entre ingenol mebutato y el comparador dividido por la diferencia de resultados en salud (aclaramientos o AVAC, respectivamente) de ingenol mebutato vs. la terapia alternativa.
UtilidadesLa estimación de AVAC se realizó multiplicando los años de vida ganados por un factor denominado utilidad que representa la preferencia de los pacientes por unos determinados estados de salud. Los valores de utilidad oscilan entre 0 y 1, donde 1 representa una salud perfecta y el 0 refleja la muerte.
En este análisis se consideró un valor de utilidad de 0,986 para pacientes con QA, y de 1 para pacientes con aclaramiento de las lesiones19.
Consumo de recursos y costes asociadosEn el análisis se consideraron las diferencias de posología en función de la zona a tratar (tabla 2).
Consumo de recursos y costes utilizados en los casos base
| Principio activo | Presentación | PVPIVA | PVPIVA con deducción*/** | Posologías |
|---|---|---|---|---|
| Costes farmacológicos | ||||
| Ingenol mebutato | Picato® 150μg/g gel, 3 tubos unidosis de 0,47g | 105,22€ | 97,33€* | Un tubo/día durante 3 días consecutivos (una vez al año) |
| Picato® 500μg/g gel, 2 tubos unidosis de 0,47g | 109,45€ | 101,24€* | Un tubo/día durante 2 días consecutivos (una vez al año) | |
| Diclofenaco 3% | Solaraze® 30mg/g gel, un tubo de 25g | 30,57€ | 28,28€* | 1g/día durante 90 días consecutivos (una vez al año) |
| Solaraze® 30mg/g gel, un tubo de 60g | 73,37€ | 67,87€* | ||
| Imiquimod 5% | Aldara® (50mg/g crema 24 sobres 250mg) | 125,93 € | 116,49€** | Un sobre/día durante 12 días consecutivos (una vez al año) |
| Recursos | ||||
| Visitas al especialista | Número | Coste unitario | Total visitas | |
| Visita dermatología (primera consulta) | 1 | 57,37€ | 3 (independientemente del tratamiento) | |
| Visita dermatología (consulta sucesiva) | 2 | 31,43€ | ||
La estimación del coste total con cada alternativa incluyó los siguientes gastos: farmacológico y derivados de visitas al dermatólogo (asociadas al manejo de acontecimientos adversos y el seguimiento de la enfermedad). Todos los costes están expresados en euros del año 2015 (tabla 2).
Los costes farmacológicos se calcularon con precio de venta al público20 considerando la deducción establecida en el Real Decreto-ley 8/201021. La identificación y la estimación de los recursos consumidos (número de consultas al dermatólogo durante el periodo de seguimiento) fueron proporcionadas por el panel de expertos (tabla 2), y los costes unitarios de los recursos sanitarios fueron obtenidos de bases de datos de costes sanitarios nacionales22.
Análisis de sensibilidadSe realizaron análisis de sensibilidad (AS) determinísticos y probabilísticos para evaluar la influencia de diferentes parámetros y comprobar la consistencia del mismo y de los resultados.
En el AS determinístico se modificaron la tasa de descuento (0 y 5%), el horizonte temporal (30 años), la adherencia al tratamiento (igualdad en el porcentaje de no adherencia,siendo del 10% para cualquiera de los tratamientos), la eficacia (disminución de un 33,3% en pacientes que no presentan adherencia al tratamiento), las visitas a Urgencias por acontecimientos adversos (un 5% de los pacientes con ingenol mebutato requieren de una visita adicional a Urgencias, un 2% con diclofenaco y un 10% con imiquimod), la administración de tratamiento antibiótico adicional (de los pacientes que necesitan una visita adicional al dermatólogo reciben tratamiento antibiótico un 30% de los tratados con ingenol mebutato, un 5% con diclofenaco y el 100% con imiquimod), y el uso de imiquimod genérico e imiquimod 3,75%, con las consecuentes diferencias en el precio (tabla 3).
Costes utilizados en los análisis de sensibilidad
| Coste farmacológico | |||
|---|---|---|---|
| Principio activo | Presentación | PVPIVA | PVPIVA con deduccióna |
| Ácido fusídico | Ácido fusídico ISDIN® (20mg/g crema 15g) | 2,56€ | 2,56€ |
| Imiquimod 3,75% | Zyclara® 3,75% (37,5mg/g crema 28 sobres 250mg) | 134,47€ | 125,09€ |
| Imiquimod 5% | Imunocare® (50mg/g crema 12 sobres 250mg) | 50,38€ | 46,60€ |
| Mupirocina | Mupirocina ISDIN® (20mg/g pomada 15g) | 3,76€ | 3,76€ |
| Coste asociado a acontecimientos adversos | |||
| Visita a Urgencias | 132,04€ | ||
PVPIVA: precio de venta al público.
El AS probabilístico incluyó 1.000 simulaciones de MonteCarlo, modificando simultáneamente los valores de los parámetros según las funciones de distribución beta, log normal y gamma.
ResultadosAl finalizar los 5 años de la simulación, ingenol mebutato resultó más efectivo que diclofenaco 3%, consiguiendo 0,192 aclaramientos más y 0,011 AVAC adicionales en el tratamiento de lesiones en la cara y el cuero cabelludo, y 0,129 aclaramientos adicionales y 0,007 AVAC ganados en el tratamiento de QA en el tronco y las extremidades (tabla 4).
Resultados de los casos base
| Ingenol mebutato vs. diclofenaco 3% | ||||||
|---|---|---|---|---|---|---|
| Cara y cuero cabelludo | Tronco y extremidades | |||||
| Costes totales | Aclaramientos totales | AVAC totales | Costes totales | Aclaramientos totales | AVAC totales | |
| Ingenol mebutato | 551,50€ | 0,536 | 4,451 | 622,27€ | 0,477 | 4,447 |
| Diclofenaco 3% | 849,11€ | 0,343 | 4,440 | 844,93€ | 0,347 | 4,440 |
| Ingenol mebutato vs. imiquimod 5% | |||||
|---|---|---|---|---|---|
| Costes totales | Aclaramientos totales | AVAC totales | RCEI(€/aclaramiento adicional) | RCUI (€/AVAC ganado) | |
| Ingenol mebutato | 551,50€ | 0,536 | 4,451 | 728,64€/aclaramiento | 10,906€/AVAC |
| Imiquimod 5% | 527,89€ | 0,503 | 4,449 | ||
AVAC: años de vida ajustados por calidad; RCEI: relación coste-efectividad incremental; RCUI: relación coste-utilidad incremental.
El coste total a los 5 años fue inferior con ingenol mebutato que con diclofenaco 3% en el tratamiento de lesiones de cara y cuero cabelludo, donde el coste incremental fue de −297,60€, y en el tratamiento de QA en tronco y extremidades, donde la diferencia de costes (y, por tanto, el ahorro) se estimó en −222,666€.
Ingenol mebutato aportó mayores resultados en salud y en términos de aclaramientos y de AVAC, y resultó ser una alternativa de menor coste en comparación con diclofenaco 3% para tratamiento de QA en cara y cuero cabelludo y en tronco y extremidades.
Comparado con imiquimod 5% para el tratamiento de lesiones en cara y cuero cabelludo, ingenol mebutato presentó una mayor efectividad, con 0,032 y 0,002 aclaramientos y AVAC incrementales, respectivamente. El coste total por paciente fue de 551,50€ con ingenol mebutato y de 527,89€ con imiquimod 5%.
La RCEI y la RCUI resultantes fueron 728,64€/aclaramiento y 10.906€/AVAC adicional con ingenol mebutato frente a imiquimod 5%.
Considerando como aceptable el umbral de 30.000€/AVAC23 utilizado como valor de referencia en la mayoría de las evaluaciones económicas de tecnologías sanitarias realizadas en España24, el tratamiento con ingenol mebutato sería una estrategia eficiente en comparación con diclofenaco 3% y con imiquimod 5%.
Los AS determinísticos confirmaron la consistencia del modelo en los 3 escenarios, ya que ingenol mebutato vs. diclofenaco 3% resultó una opción dominante en todos los AS, independientemente del área corporal a tratar (tabla 5 y S1 del Anexo disponible en la versión electrónica). Los resultados también mostraron que el tratamiento con ingenol mebutato en la cara y el cuero cabelludo podría considerarse una alternativa de tratamiento coste-efectiva frente a imiquimod 5% (considerando como aceptable un umbral de eficiencia de 30.000€/AVAC17) en el 80% de los AS realizados. El valor de RCUI superó los 30.000€/AVAC adicional en 2 situaciones: cuando se consideró una disminución de la eficacia del 33% asociada a la no adherencia, en lugar del 50%, y cuando la estimación del coste de imiquimod 5% se realizó con el precio de imiquimod 5% genérico en lugar de la marca comercial (tabla 6 y S2 del Anexo disponible en la versión electrónica).
Resultados del análisis de sensibilidad determinístico ingenol mebutato vs. diclofenaco 3% (cara y cuero cabelludo y tronco y extremidades)
| Cara y cuero cabelludo | ||||
|---|---|---|---|---|
| Parámetros | Valor CB | Valor AS | RCEI | RCUI |
| CB ingenol mebutato vs. diclofenaco 3% (cara y cuero cabelludo) | Dominante | Dominante | ||
| Visita a Urgencias a causa de AA | 5% tratados con ingenol mebutato y 2% tratados con diclofenaco 3% | Dominante | Dominante | |
| Tratamiento antibiótico | 30% tratados con ingenol mebutato y 5% tratados con diclofenaco 3% | Dominante | Dominante | |
| Eficacia | 42,24% ingenol mebutato y 24,64% con diclofenaco 3% | 33% menos de eficacia | Dominante | Dominante |
| Tasa de descuento en costes y resultados en salud | 3% | 0% 5% | Dominante | Dominante |
| Horizonte temporal | 5 años | 30 años | Dominante | Dominante |
| Adherencia al tratamiento | 10% no adherencia ingenol mebutato 40% no adherencia diclofenaco 3% | 10% no adherencia ambos tratamientos | Dominante | Dominante |
| Tronco y extremidades | ||||
|---|---|---|---|---|
| Resultados | Valor CB | Valor AS | RCEI | RCUI |
| CB ingenol mebutato vs. diclofenaco 3% (tronco y extremidades) | Dominante | Dominante | ||
| Visita a Urgencias a causa de AA | 5% tratados con ingenol mebutato y 2% tratados con diclofenaco 3% | Dominante | Dominante | |
| Tratamiento antibiótico | 30% tratados con ingenol mebutato y 5% tratados con diclofenaco 3% | Dominante | Dominante | |
| Eficacia | 34,07% ingenol mebutato y 25,07% diclofenaco 3% | 33% menos de eficacia | Dominante | Dominante |
| Tasa de descuento en costes y resultados en salud | 3% | 0% 5% | Dominante | Dominante |
| Horizonte temporal | 5 años | 30 años | Dominante | Dominante |
| Adherencia al tratamiento | 10% no adherencia ingenol mebutato 40% no adherencia diclofenaco 3% | 10% no adherencia ambos tratamientos | Dominante | Dominante |
ACE: análisis de coste-efectividad; ACU: análisis de coste-utilidad; AS: análisis de sensibilidad; CB: caso base; RCEI: relación coste-efectividad incremental; RCUI: relación coste-utilidad incremental.
Resultados del análisis de sensibilidad determinístico ingenol mebutato vs. imiquimod 5% (cara y cuero cabelludo)
| Cara y cuero cabelludo | ||||
|---|---|---|---|---|
| Resultados | Valor CB | Valor AS | RCEI | RCUI |
| CB ingenol mebutato vs. imiquimod 5% (cara y cuero cabelludo) | 728,65€/aclaramiento | 10.906 | ||
| Visita a Urgencias a causa de AA | 5% tratados con ingenol mebutato 10% tratados con imiquimod 5% | 148,56€/aclaramiento | 2.224€/AVAC | |
| Tratamiento antibiótico | 30% tratados con ingenol mebutato 100% tratados con imiquimod 5% | 667,43€/aclaramiento | 9.990€/AVAC | |
| Eficacia | 42,24% ingenol mebutato 44,54% imiquimod 5% | 33% menos de eficacia Considerando igual eficacia en ambos tratamientos | 2.567,73€/aclaramiento 222,57€/aclaramiento | 37.428€/AVAC 3.377€/AVAC |
| Precio | Imiquimod 5% (Aldara®) | Considerando el coste farmacológico de Imunocare® y no de Aldara® Considerando el coste farmacológico de Zyclara® y no de Aldara® | 2.786,33€/aclaramiento Dominante | 41.706€/AVAC Dominante |
| Tasa de descuento en costes y resultados en salud | 3% | 0% 5% | 745,61€/aclaramiento (0%) 718,27€/aclaramiento (5%) | 10.475€/AVAC (0%) 11.195€/AVAC (5%) |
| Horizonte temporal | 5 años | 30 años | 1.242,93€/aclaramiento | 7.997€/AVAC |
| Adherencia al tratamiento | 10% no adherencia ingenol mebutato 40% no adherencia diclofenaco 3% | 10% no adherencia ambos tratamientos | Dominante | Dominante |
ACE: análisis coste-efectividad; ACU: análisis coste-utilidad; AS: análisis de sensibilidad; AVAC: año de vida ajustado por calidad; CB: caso base; RCEI: relación coste-efectividad incremental; RCUI: relación coste-utilidad incremental.
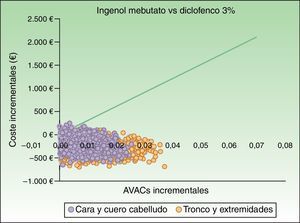
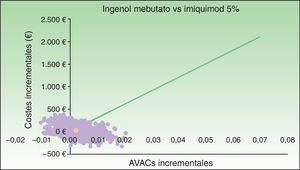
El AS probabilístico se representó gráficamente en un plano de coste-efectividad, en forma de nube de puntos, donde cada punto representa el valor de RCUI de cada una de las 1.000 simulaciones realizadas. En los escenarios que evaluaron ingenol mebutato vs. diclofenaco 3%, el 96% de las simulaciones en cara y cuero cabelludo y el 91% de las de tronco y extremidades presentaron un valor de RCUI inferior al umbral de 30.000€/AVAC adicional17 (fig. 2). En el escenario que comparó ingenol mebutato vs. imiquimod 5%, el 80% de las simulaciones fueron coste-efectivas (fig. 3).
La QA, por su elevada prevalencia en la población, es una enfermedad que ocasiona un gasto considerable a los sistemas sanitarios. De esto deriva la importancia de contar con nuevas alternativas de tratamiento que sean más efectivas y puedan acortar al máximo la duración de la enfermedad y reducir las recaídas, contribuyendo con ello a la sostenibilidad del Sistema Nacional de Salud al reducir los costes asociados al tratamiento y el manejo de los pacientes con QA.
En ocasiones, debido al perfil del paciente que padece mayoritariamente esta enfermedad (personas de avanzada edad), es difícil la elección de la mejor alternativa terapéutica, por lo que un indicador como la RCEI que unifica los costes y los resultados en salud percibidos puede ser trascendental, junto con el tiempo de tratamiento de las alternativas, aspecto importante a tener en cuenta ya que la menor duración del tratamiento va a aumentar la adherencia del paciente a este25, lo que repercutirá directamente en un incremento de la eficacia. A pesar de las respuestas cutáneas predecibles derivadas del uso de las 3 alternativas evaluadas (ingenol mebutato, diclofenaco 3%, imiquimod 5%), se observa que la calidad de vida en pacientes con QA mejora después del tratamiento con ingenol mebutato, ya que la presencia de efectos secundarios no afecta a la calidad de vida o la satisfacción del paciente con el tratamiento26.
La presente investigación tiene una serie de fortalezas, como, por ejemplo, ser el único análisis coste-efectividad sobre la QA en España que evalúa las principales alternativas de tratamiento (a excepción de incluir la terapia fotodinámica) usadas en la actualidad en la práctica clínica en España (validado por el panel de expertos). La única evaluación económica de la QA en España fue publicada recientemente, pero las alternativas de tratamiento evaluadas no son las incluidas en el presente análisis27. Se identificaron 2 evaluaciones económicas realizadas en el contexto escocés28 y finlandés29, comparando ingenol mebutato vs. diclofenaco 3% y vs. imiquimod 5%. Ambos estudios utilizaron la perspectiva del sistema sanitario, y en ambos casos ingenol mebutato fue una alternativa coste-efectiva22 (mayores costes y mayores resultados en salud) y dominante23 (menores costes y mayores resultados en salud) vs. diclofenaco 3%, y coste-efectiva vs. imiquimod 5%23.
Además, para la realización de este estudio se recogieron y agruparon los datos de los diferentes ensayos clínicos aglutinándolos según la zona tratada en los pacientes en función del área donde se localizaban las lesiones, para, de este modo, ser lo más conservadores posible a la hora de obtener las eficacias mediante las comparaciones indirectas entre tratamientos.
Los resultados de los AS realizados modificando los parámetros que podrían comprometer al modelo corroboraron su consistencia puesto que, pese a las numerosas variaciones realizadas, los resultados mostraron que la prescripción de ingenol mebutato vs. diclofenaco 3% es una opción de tratamiento dominante en todos los AS, es decir, implica una mayor eficacia con una disminución del coste incremental y una alternativa coste-efectiva frente a imiquimod 5% en todos los AS realizados, excepto en 2 ya mencionados. Los parámetros que más influyeron en la variación de los resultados fueron la disminución de la eficacia en pacientes no adherentes y la variación del coste farmacológico por el uso de imiquimod genérico, sobrepasando en ambos escenarios el umbral de los 30.000€/AVAC17 de RCUI y los 2.500€/aclaramiento.
Este estudio no está exento de limitaciones que se deben tener en cuenta a la hora de interpretar los resultados. Entre ellas cabe destacar el carácter teórico inherente a cualquier modelización, que puede no alcanzar el objetivo de representar fielmente la realidad de la práctica clínica diaria. Para el presente análisis se optó por emplear un modelo de Markov, que permite recoger la existencia de eventos repetitivos como es el caso de las posibles recurrencias de episodios de QA en un mismo paciente; sin embargo, se han identificado en la literatura otras evaluaciones económicas de intervenciones en esta misma enfermedad que emplearon árboles de decisión que pueden resultar más intuitivos y sencillos de interpretar. La posibilidad de transición al estadio «muerte» puede parecer alejada de la realidad en una enfermedad que no se asocia con un incremento intrínseco de la mortalidad, pero se consideró necesaria para la estimación de una medida final en términos de supervivencia, los AVAC, que permitiera referir el resultado obtenido respecto a un umbral de coste-efectividad. El diseño del modelo y la determinación de los estados de salud contemplados estuvieron, en cualquier caso, condicionados por la disponibilidad de datos clínicos para realizar la simulación prevista.
Otra de las posibles limitaciones es la relacionada con la metodología empleada para la consideración de las variables de eficacia. Debido a la ausencia de ensayos de comparación directa entre las alternativas evaluadas, se recurrió a técnicas de comparación indirecta para obtener las eficacias, existiendo la problemática de que las comparaciones indirectas pueden estar sujetas a un mayor sesgo que las comparaciones directas y pueden sobreestimar la eficacia de las intervenciones30. En cualquier caso, las comparaciones indirectas son una metodología estandarizada y ampliamente reconocida, utilizada cuando no hay evidencia directa o suficiente de los ensayos aleatorizados, y pueden proporcionar información útil y complementaria sobre la eficacia relativa de las intervenciones comparadas, siempre y cuando cuenten con una elevada validez interna, externa y similitud entre los ensayos clínicos31, e igualmente evidencia útil para seleccionar con criterio la mejor opción de tratamiento32. A pesar de esto, sería ideal en un futuro reevaluar este estudio utilizando comparaciones directas.
Otra limitación es la relacionada con la utilización de datos extraídos de la literatura procedente de estudios llevados a cabo en otros países, al no existir trabajos de este tipo realizados específicamente en España. Las utilidades empleadas en el modelo derivaron de un estudio en Reino Unido13 y fueron validadas por el panel de expertos, que consideró que estos datos eran representativos de la población con QA en España, corroborándose así que las utilidades derivadas de los estados de salud (utilizando los valores definidos por el cuestionario EQ-5D) no difieren en la población general entre distintos países europeos33.
A pesar de las limitaciones descritas, el presente estudio de evaluación económica podría ayudar a facilitar la toma de decisiones a la hora de prescribir un determinado tratamiento en la práctica clínica, dado que ingenol mebutato es una terapia dominante que origina menos costes al Sistema Nacional de Salud y más resultados en salud para el paciente en comparación con diclofenaco 3%, y que además, considerando como aceptable un umbral de disponibilidad a pagar de 30.000€/AVAC17, podría considerarse una alternativa de tratamiento coste-efectiva frente a imiquimod 5% en el abordaje de la QA de cara y cuero cabelludo en nuestro país.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesI. Elías, N. Ortega-Joaquín e I. Oyagüez son empleados de PORIB, una consultora especializada en evaluación económica de tecnologías sanitarias, que ha recibido una financiación no condicionada de LEO-Pharma para el desarrollo de este análisis.
A. Miranda, E. Mosquera y C. Gibbons son empleados de LEO-Pharma.
P. de la Cueva, L. J. del Pozo, D. Moreno-Ramírez, A. Boada y M. Aguilar han colaborado como expertos en la validación de los parámetros empleados en el análisis, habiendo recibido por ello una financiación no condicionada de LEO-Pharma, que en ningún momento ha influido en sus opiniones y ni en las conclusiones obtenidas.