La relevancia del ensayo controlado con asignación aleatoria (ECA) para determinar si existe una asociación entre una intervención y un desenlace está determinada por su calidad y rigor científico.
ObjetivoEvaluar la calidad metodológica de los ECA publicados en revistas dermatológicas en español.
MétodosSe realizó una búsqueda manual y sistemática de los ECA publicados en las revistas de Dermatología españolas y latinoamericanas entre 1997 (publicación de los criterios CONSORT) y 2012. Se determinó el riesgo de sesgo de cada ECA, evaluando los siguientes dominios: generación de la secuencia aleatoria, ocultamiento de la asignación, cegamiento de los pacientes/evaluadores de desenlaces, datos faltantes y seguimiento de pacientes. Se identificaron la fuente de financiación de los estudios y el reporte de conflictos de interés.
ResultadosSe identificaron 70 ECA publicadas en 21 revistas. La mayoría de los ECA tuvo un alto riesgo de sesgo, principalmente por falta de reporte de los aspectos metodológicos importantes. Solo 15 estudios declararon fuentes de financiación.
Discusión y conclusionesA pesar del número considerable de revistas existentes en España y Latinoamérica, en los 15 años estudiados se han publicado pocos ECA. La mayoría de los estudios presentó problemas de calidad importantes, al carecer de información metodológica que permitiera evaluar su calidad y a las falencias en el reporte de las fuentes de financiación y de los conflictos de interés de los autores. La investigación clínica experimental dermatológica que se publica en Ibero-Latinoamérica debe mejorar ostensiblemente tanto en su diseño como en su reporte de resultados.
The value of randomized clinical trials (RCTs) undertaken to identify an association between an intervention and an outcome is determined by their quality and scientific rigor.
ObjectiveTo assess the methodological quality of RCTs published in Spanish-language dermatology journals.
MethodsBy way of a systematic manual search, we identified all the RCTs in journals published in Spain and Latin America between 1997 (the year in which the CONSORT statement was published) and 2012. Risk of bias was evaluated for each RCT by assessing the following domains: randomization sequence generation, allocation concealment, blinding of patients and those assessing outcomes, missing data, and patient follow-up. Source of funding and conflict of interest statements, if any, were recorded for each study.
ResultsThe search identified 70 RCTs published in 21 journals. Most of the RCTs had a high risk of bias, primarily because of gaps in the reporting of important methodological aspects. The source of funding was reported in only 15 studies.
Discussion and conclusionsIn spite of the considerable number of Spanish and Latin American journals, few RCTs have been published in the 15 years analyzed. Most of the RCTs published had serious defects in that the authors omitted methodological information essential to any evaluation of the quality of the trial and failed to report sources of funding or possible conflicts of interest for the authors involved. Authors of experimental clinical research in dermatology published in Spain and Latin America need to substantially improve both the design of their trials and the reporting of results.
El ensayo clínico controlado con asignación aleatoria (ECA) es el tipo de diseño metodológico más riguroso e idóneo para determinar si existe una asociación de causa-efecto entre una intervención y un resultado o desenlace a evaluar. Los ECA son la materia prima para la realización de revisiones sistemáticas y metaanálisis. Sin embargo, el valor de estos estudios dependerá de la calidad y la rigurosidad metodológica con la que se hayan realizado.
En el campo de la Dermatología, ha habido un incremento importante en la investigación clínica experimental durante las últimas décadas. No obstante, este auge investigativo no ha sido proporcional al refinamiento metodológico de los estudios. Diferentes estudios reportan que los ECA publicados en Dermatología suelen estar por debajo de los estándares aceptables1-4.
Ante la necesidad de elevar la calidad en el reporte de resultados de ensayos clínicos en el ámbito mundial, se definieron los criterios Consolidated Standards of Reported Trials statement (CONSORT) en 19965. CONSORT es una lista de verificación que pretende mejorar la forma en que los ECA son publicados, pero que de forma indirecta da cuenta del rigor científico con el que se han desarrollado los estudios.
Tras la implementación del CONSORT y el establecimiento de la reglamentación de Buenas Prácticas Clínicas (disponible en: http://www.fda.gov/downloads/Drugs/Guidances/ucm073122.pdf y http://www.mrc.ac.uk/documents/pdf/good-clinical-practice-in-clinical-trials/), era esperable una mejora en la calidad científica y en el formato de publicación de los ECA. No obstante, la evidencia apunta a que se continúan encontrando serios errores en el diseño y el reporte de resultados en los ensayos clínicos publicados a partir de 19976. Esta problemática también se ha observado en los estudios publicados sobre Dermatología en español después de dicho año. En un estudio realizado en España, se encontró que solo 6 (25%) de los 24 ensayos clínicos encontrados en la revista dermatológica de mayor impacto de ese país, Actas Dermo-Sifiliográficas, fueron calificados como de buena calidad3.
Teniendo en cuenta lo anterior, este trabajo busca evaluar la calidad metodológica de la investigación clínica experimental en Dermatología publicada en idioma español, contribuyendo así a facilitar el análisis de sus fortalezas y retos. Los ECA analizados son aquellos identificados en un estudio reciente a través del cual se revisaron manualmente las revistas dermatológicas en español7.
En el presente artículo complementamos dicho trabajo con el análisis de la calidad metodológica de los ECA publicados entre 1997 y 2012 utilizando las recomendaciones de la Colaboración Cochrane para este fin, así como determinando el reporte de conflictos de interés y fuentes de financiación.
Objetivo del estudioEvaluar la calidad metodológica de los ECA publicados en revistas dermatológicas en español entre 1997 y 2012.
Materiales y métodoIdentificación de las revistas, búsqueda manual y electrónicaLa metodología utilizada para la detección de ECA en revistas dermatológicas publicadas en español ya ha sido descrita en una publicación previa7.
Primero se identificaron todas las revistas elegibles en el marco de un proyecto liderado por la Red Cochrane Iberoamericana (Barcelona, España). Siguiendo este protocolo, se realizaron búsquedas en las bases de datos de PubMed, EMBASE, LILACS, SciELO, Periódica, Latindex, Índice Médico Español, Catálogo Nacional de Publicaciones Periódicas en Ciencias de la Salud Españolas (C-17) y en otros catálogos colectivos de publicaciones periódicas en ciencias de la salud de España. Se complementó la búsqueda en el Índice Bibliográfico Español en Ciencias de la Salud (IBECS e IMBIOMED), con búsquedas libres en Google y contactando diferentes asociaciones de Dermatología de cada país participante y diferentes especialistas en la materia.
Cada una de las revistas identificadas se revisó de manera manual con el objetivo de identificar los ECA publicados. La revisión fue retrospectiva y siguiendo las directrices para la búsqueda manual de ensayos clínicos de la Colaboración Cochrane (disponible en http://www.cochrane.es/∼cochrane/?q=es/node/140) desde el año 2012 hasta el año de inicio de publicación de la revista, o hasta donde fuera posible recuperar el texto completo7.
Adicional a la búsqueda manual de ECA, se realizó una búsqueda electrónica en MEDLINE (a través de PubMed), EMBASE, LILACS e IBECS, y a través del Portal de Búsqueda de la Biblioteca Virtual de Salud de Bireme, la Organización Panamericana de la Salud y la Organización Mundial de la Salud.
Extracción de datosSe creó una base de datos para registrar cada ECA identificado y para seguir el progreso de búsqueda manual de cada revista, con el fin de garantizar que los datos se recogieron de forma ordenada y sistemática. Adicionalmente, se determinó qué revistas incluían CONSORT dentro de su normativa de publicación y su indización en MEDLINE o EMBASE.
Análisis de la calidad y riesgos de sesgoPara la revisión del rigor científico y la calidad metodológica, se incluyeron solo los ECA identificados entre 1997 (implementación del CONSORT) y el año 2012. Esta evaluación fue realizada por duplicado; cualquier discrepancia fue resuelta por un tercer evaluador. Se utilizó la herramienta proporcionada por la Colaboración Cochrane para el análisis del riesgo de sesgo (alta/media/baja)8. Este instrumento evalúa aspectos de la metodología de los experimentos clínicos, tales como generación de la secuencia aleatoria, ocultamiento de la asignación de pacientes a los diferentes brazos del estudio, cegamiento de pacientes o evaluadores de los desenlaces, datos faltantes y seguimiento de los pacientes. A cada uno de estos dominios se les asigna un «sí», «no» o «inespecífico/no reportado».
Para que un estudio fuera categorizado como «alto riesgo de sesgo» debía presentar falencias en más de uno de los aspectos metodológicos evaluados, o siempre que presentara falencias en la generación de la secuencia aleatoria. Si la información no se encontraba disponible se catalogaba como de «riesgo inespecífico/no reportado». La revisión de estos aspectos y su respectiva puntuación se registraron en el programa Review Manager versión 5.2 (Copenhagen, The Nordic Cochrane Centre, The Cochrane Collaboration, 2012). Adicionalmente, se determinaron la fuente de financiación de los estudios y el reporte de conflictos de interés de los autores.
Análisis estadísticoSe realizó un análisis descriptivo de la información recogida, evaluando las frecuencias mediante el análisis univariado de las variables. En las variables continuas se calcularon las medidas de resumen apropiadas; en las variables cualitativas, se determinaron las frecuencias absolutas y relativas y sus porcentajes. Se calculó el intervalo de confianza para las proporciones cuando fuera apropiado. Para el almacenamiento de la información, aparte de Review Manager, se utilizó una base de datos de Excel (Microsoft Office®, versión 2010, Redmond, Estados Unidos). Para los análisis estadísticos, se utilizó el programa IBM® SPSS® Statistics versión 19 (New York, Estados Unidos).
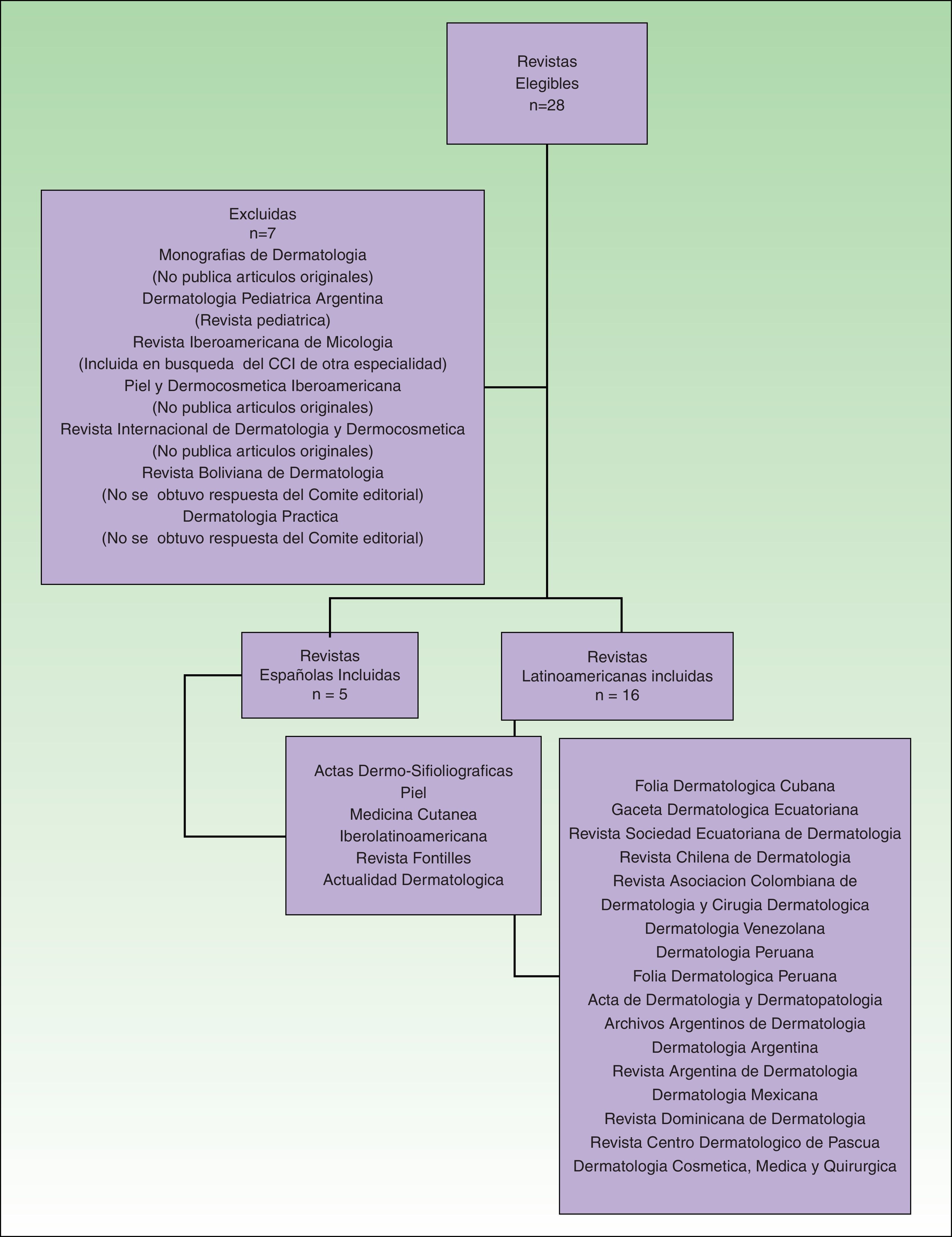
ResultadosDe las 28 revistas que reunieron criterios de elegibilidad, se incluyeron finalmente 21 publicaciones, 5 de España y 16 de diferentes países latinoamericanos. Solo la revista Actas Dermo-Sifiliográficas se encuentra actualmente indexada en MEDLINE y EMBASE, mientras que las revistas Dermatología Revista Mexicana, Argentina de Dermatología, Medicina Cutánea Ibero Latinoamericana y Piel se encuentran indexadas en EMBASE7.
El total de revistas incluidas y excluidas y la respectiva justificación se han descrito previamente en otra publicación (fig. 1)7.
Flujograma de selección de las revistas dermatológicas según criterios de inclusión y exclusión. (Extraído del artículo: Sanclemente G, Pardo H, Sánchez S, Bonfill X. Identificación de ensayos clínicos en revistas dermatológicas publicadas en español. Actas Dermosifiliogr. 2015;106:415-422).
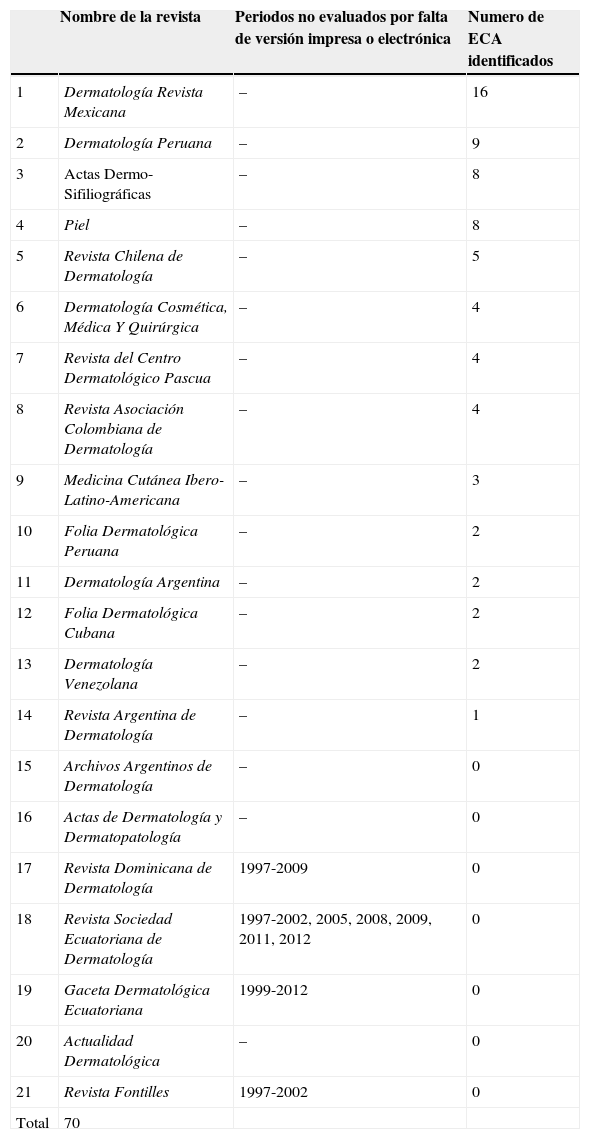
Desde el año 1997 hasta el 2012 se identificaron 70 ECA en las 21 revistas incluidas (tabla 1) (anexo 1). De forma global, el 73% (51) de estos fueron publicados en las 16 revistas latinoamericanas y el 27% (19) en las 5 revistas españolas (tabla 1). Entre las revistas latinoamericanas, las que más ECA publicaron fueron Dermatología Revista Mexicana (16), Dermatología Peruana (9) y Revista Chilena de Dermatología (5) (tabla 1). Entre las revistas españolas, Actas Dermo-Sifiliográficas y Piel fueron las que más publicaron, con 8 ECA cada una (tabla 1).
ECA identificados en las revistas dermatológicas españolas y latinoamericanas
| Nombre de la revista | Periodos no evaluados por falta de versión impresa o electrónica | Numero de ECA identificados | |
|---|---|---|---|
| 1 | Dermatología Revista Mexicana | – | 16 |
| 2 | Dermatología Peruana | – | 9 |
| 3 | Actas Dermo-Sifiliográficas | – | 8 |
| 4 | Piel | – | 8 |
| 5 | Revista Chilena de Dermatología | – | 5 |
| 6 | Dermatología Cosmética, Médica Y Quirúrgica | – | 4 |
| 7 | Revista del Centro Dermatológico Pascua | – | 4 |
| 8 | Revista Asociación Colombiana de Dermatología | – | 4 |
| 9 | Medicina Cutánea Ibero-Latino-Americana | – | 3 |
| 10 | Folia Dermatológica Peruana | – | 2 |
| 11 | Dermatología Argentina | – | 2 |
| 12 | Folia Dermatológica Cubana | – | 2 |
| 13 | Dermatología Venezolana | – | 2 |
| 14 | Revista Argentina de Dermatología | – | 1 |
| 15 | Archivos Argentinos de Dermatología | – | 0 |
| 16 | Actas de Dermatología y Dermatopatología | – | 0 |
| 17 | Revista Dominicana de Dermatología | 1997-2009 | 0 |
| 18 | Revista Sociedad Ecuatoriana de Dermatología | 1997-2002, 2005, 2008, 2009, 2011, 2012 | 0 |
| 19 | Gaceta Dermatológica Ecuatoriana | 1999-2012 | 0 |
| 20 | Actualidad Dermatológica | – | 0 |
| 21 | Revista Fontilles | 1997-2002 | 0 |
| Total | 70 |
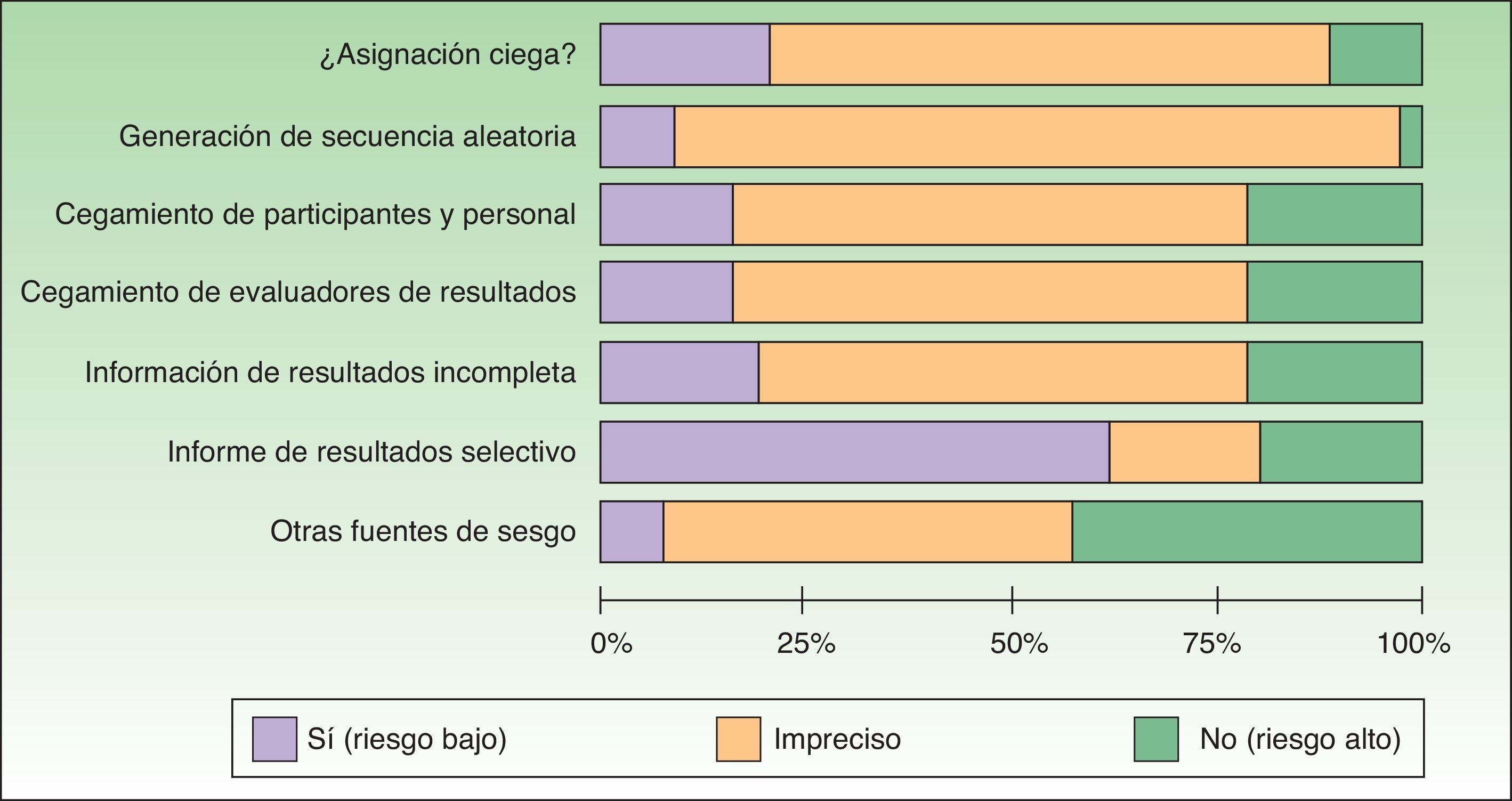
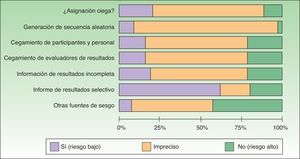
Globalmente, la mayoría de los estudios se clasificaron como de «alto riesgo de sesgo» porque no se reportó en ellos la información necesaria para evaluar la calidad y el rigor metodológico del estudio (tabla 2). Un bajo porcentaje de estudios presentó bajo riesgo de sesgo en los aspectos evaluados (tabla 2) (fig. 2).
Evaluación de diferentes aspectos metodológicos de ECA identificados en las revistas dermatológicas de España y Latinoamericana
| Aspecto metodológico | N (%) | IC del 95% |
|---|---|---|
| Ocultamiento de la asignación | ||
| Inespecífico/no reportado | 48 (68,6) | 57,73%-79,47% |
| Sí | 14 (20) | 10,63%-29,37% |
| No | 8 (11,4) | 3,95%-18,85% |
| Generación de la secuencia | ||
| Inespecífico/no reportado | 62 (88,6) | 81,15%-96,05% |
| Sí | 6 (8,6) | 2,03%-15,17% |
| No | 2 (2,8) | –1,06%-6,66% |
| Cegamiento de participantes/personal | ||
| Inespecífico/no reportado | 44 (62,8) | 51,48%-74,12% |
| Sí | 11 (15,7) | 7,18%-24,22% |
| No | 15 (21,5) | 11,88%-31,12% |
| Cegamiento evaluadores desenlaces | ||
| Inespecífico/no reportado | 44 (62,8) | 51,48%-74,12% |
| Sí | 11 (15,7) | 7,18%-24,22% |
| No | 15 (21,5) | 11,88%-31,12% |
| Información incompleta sobre desenlaces | ||
| Inespecífico/no reportado | 42 (60) | 48,52%-71,48% |
| Sí | 13 (18,5) | 9,4%-27,6% |
| No | 15 (21,5) | 11,88%-31,12% |
| Reporte selectivo de desenlaces | ||
| Inespecífico/no reportado | 12 (17,2) | 8,36%-26,04% |
| No | 44 (62,8) | 51,48%-74,12% |
| Sí | 14 (20) | 10,63%-29,37% |
| Otras fuentes de sesgo | ||
| Inespecífico/no reportado | 35 (50) | 38,29%-61,71% |
| No | 5 (7, 15, 8) | 7,26%-24,34% |
| Sí | 30 (42,9) | 31,31%-54,49% |
| Financiación del estudio | ||
| No se reporta | 55 (78,6) | 68,99%-88,21% |
| Se reporta | 15 (21,4) | 11,79%-31,01% |
| Conflictos de interés | ||
| No se reporta | 65 (92,8) | 86,74%-98,86% |
| Se reporta | 5 (7,2) | 1,14%-13,26% |
IC del 95%: intervalo de confianza del 95%.
Un total de 15 estudios comunicaron fuentes de financiación, de los cuales solo 2 lo hicieron de forma adecuada (Ramirez-Bosca et al. y Pinto et al.) (anexo 1). Los autores de 5 estudios reportaron conflictos de interés, pero solo uno lo hizo siguiendo los estándares aceptados para este fin (Ramirez-Bosca et al.) (anexo 1). De todas las revistas evaluadas, únicamente Actas Dermo-Sifiliográficas se adhiere a los criterios CONSORT en sus instrucciones para autores desde el año 2008, pero en el cuerpo de los artículos no se comunica si se utilizó dicha herramienta como guía para publicar el estudio.
La figura 2 proporciona de manera gráfica un sumario del riesgo de sesgo de los estudios identificados.
DiscusiónEl objetivo de este estudio fue evaluar la calidad metodológica de los ECA publicados en revistas dermatológicas en español entre 1997 y 2012. De acuerdo con nuestros resultados, el riesgo de sesgo de los ensayos clínicos sobre Dermatología publicados en español en el periodo 1997-2012 fue alto, principalmente por la falta de reporte de aspectos metodológicos relevantes. Si bien este hallazgo ya se había descrito en estudios anteriores enfocados en revistas dermatológicas específicas del idioma español9, es la primera vez que se hace este análisis de manera global para todas las revistas dermatológicas que publican ECA en España y Latinoamérica. Estos resultados son similares a otros llevados a cabo con ECA en Dermatología publicados en inglés y con ECA sobre patologías como la dermatitis perioral o la dermatitis atopica4,10,11.
Es por tanto preocupante que se encuentren estas falencias en el análisis de la calidad de los ECA, por corresponder estos a los referentes de «oro» para evaluar la eficacia y la seguridad de una intervención. Esto necesariamente implica que la práctica dermatológica en la actualidad (al menos aquella basada en los estudios evaluados) puede estar fundamentada en información recolectada de manera no sistemática o en experimentos clínicos sin grupos control12. Asimismo, se detecta un desfase en los desenlaces que se evalúan y aquellos que pueden interesar a los pacientes. Por ejemplo, en la actualidad muchos estudios en Dermatología han incorporado la calidad de vida dado el marcado interés que los pacientes tienen en este desenlace en relación con los tratamientos dermatológicos13-15. No obstante, llama la atención que en los 70 ECA evaluados solo uno haya incluido esta variable de resultado.
Entre los aspectos metodológicos menos comunicados se encontraron la generación de la secuencia aleatoria, las fuentes de financiación, la descripción de los conflictos de interés y el ocultamiento de la asignación. Estos resultados son similares a lo encontrado en revistas con o sin inclusión de los criterios CONSORT6,16,17 y realza falencias en el rigor científico con los que se han diseñado y reportado los ECA identificados. En el futuro, la investigación clínica experimental que se publica en España y Latinoamérica en Dermatología debe mejorar ostensiblemente tanto en su diseño como en su reporte de resultados (adopción de los criterios CONSORT).
Se debe tener en cuenta que el punto de partida para que un estudio no sea sesgado es la utilización de un mecanismo que asegure que todos los pacientes tengan la misma probabilidad de pertenecer a un grupo u otro, y de que el ocultamiento de la asignación evite un reclutamiento selectivo de pacientes de acuerdo a sus factores pronósticos (disponible en http://handbook.cochrane.org/). De hecho, se ha demostrado que una inadecuada generación de la secuencia en un ECA podría sobreestimar el efecto de un tratamiento hasta en un 12%18, mientras que la falta de ocultamiento de la secuencia de asignación aleatoria puede incrementar el efecto hasta en un 18%. Adicionalmente, un experimento clínico clasificado como de tipo aleatorizado no garantiza por sí mismo que cumpla con los estándares metodológicos asociados a este tipo de estudios19.
En cuanto a los criterios CONSORT, solo la revista Actas Dermo-Sifiliográficas exige esta herramienta para la publicación de ensayos clínicos. Esto explicaría la mayor calidad metodológica encontrada en los últimos ECA publicados por esta revista. No obstante, se ha encontrado que si bien el uso de esta herramienta ha mejorado el reporte de los ECA, este aún continúa siendo subóptimo en términos de garantizar una mejor calidad de los estudios6.
Es de resaltar que la gran mayoría de estudios carecieran de la descripción de las fuentes de financiación y los conflictos de interés. El reporte de estos es esencial, ya que los resultados se pueden ver afectados por los intereses particulares del investigador o del promotor del estudio (muchas veces, un laboratorio farmacéutico)20-22. Lo anterior es relevante, pues en la literatura dermatológica es frecuente encontrar el reporte selectivo de desenlaces (o «endpoints» en inglés), lo que conduce en la mayoría de los casos a sobreestimar los positivos23. Esta práctica puede estar fomentada por la presencia de conflictos de interés. Por esto, hacia el futuro se hace necesario evaluar minuciosamente estas características en los estudios publicados en las revistas dermatológicas de habla hispana24.
Una de las principales fortalezas de este estudio es la recopilación manual de los ECA de 21 revistas dermatológicas en español, los cuales serán próximamente incluidos en el Registro Central de Ensayos Clínicos Controlados de la Colaboración Cochrane (CENTRAL), por lo que se encontrarán disponibles para futuras revisiones sistemáticas y otros documentos de síntesis. Tal y como se reporta en el artículo sobre la identificación de ensayos asociado a este estudio7, la detección y la recuperación del texto completo de los 70 ECA identificados no hubiese sido posible mediante una búsqueda electrónica, pues únicamente la revista Actas Dermo-Sifiliográficas se encuentra indexada en MEDLINE y solo Dermatología Revista Mexicana, Revista Argentina de Dermatología, Medicina Cutánea Ibero Latinoamericana y Piel se encuentran indexadas en EMBASE7. Otra fortaleza de este trabajo es el análisis por duplicado de la calidad de los ECA y el uso de las herramientas Cochrane, las cuales han sido debidamente validadas y cuentan con reconocimiento mundial. (Disponible en: http://handbook.cochrane.org/chapter_8/8_assessing_risk_of_bias_in_included_studies.htm).
La principal limitación de este estudio radica en la imposibilidad de evaluar la totalidad de volúmenes y los números de 3 de las revistas, específicamente 2 de Ecuador y una de la República Dominicana. No obstante, es probable que su análisis no hubiese cambiado significativamente los resultados de este estudio, pues en los números y los volúmenes revisados de dichas publicaciones no se encontró ningún ECA. Asimismo, dichas publicaciones no han incorporado los criterios CONSORT como requerimiento para los autores. Otra limitación es la variabilidad en los desenlaces y la forma de medirlos en los ECA identificados. Esto conduce a una alta heterogeneidad entre los estudios que impediría resumir cuantitativamente los resultados en un metaanálisis.
En conclusión, el riesgo de sesgo de los ensayos clínicos publicados en revistas dermatológicas en español entre 1997 y 2012 fue alto, principalmente por la insuficiente información proporcionada para evaluar la calidad y el rigor metodológico de los estudios. Asimismo, existen falencias en la descripción y el reporte de las fuentes de financiación y los conflictos de interés de los autores. Se recomienda el reporte exhaustivo de todos los aspectos metodológicos de los estudios, lo que permitirá detectar sus sesgos y falencias. Lo anterior es relevante pues la descripción completa de los estudios facilita, por un lado, el adecuado análisis de la evidencia y, por otro, evita la injusta calificación de un alto riesgo de sesgo atribuido esencialmente a la falta de información proporcionada. De esta manera, se beneficiaría a los pacientes quienes son en última instancia el fundamento de la práctica dermatológica basada en la evidencia y adicionalmente contribuiría a la toma de decisiones en este campo de la medicina. Por último, y como estrategia futura, se planea contactar a los diferentes editores de las revistas dermatológicas revisadas para estandarizar herramientas de identificación prospectiva de los ECA publicados en sus revistas. De esta manera, se facilitará la actualización continua de este trabajo sin necesidad de volver a llevarlo a cabo en un futuro y de manera manual.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónGrupo de Investigación Dermatológica (GRID), Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.
A todos los estudiantes del Máster en Salud Pública de la Universitat Autònoma de Barcelona, por su ayuda en la identificación de las revistas dermatológicas. A Ivan Solá, del Centro Cochrane Iberoamericano, por su asistencia en las búsquedas y la lectura crítica del manuscrito. Adicionalmente, a Elizabeth Dussan y Nelly Pinzón, de la Asociación Colombiana de Dermatología; a Karina Vielma y a la Dra. María Isabel Herane (Sociedad Chilena de Dermatología); al Dr. Alexandro Bonifax (Revista Dermatología Mexicana); al Dr. Roberto Arenas y al Dr. Jorge Ocampo-Candiani (Revista Dermatología Cosmética Médica y Quirúrgica), y al Dr. Edgardo Chouela, por su gestión y su colaboración en la búsqueda y el envío del texto completo de los artículos solicitados.
La Dra. Gloria Sanclemente es candidata a PhD en el Departamento de Pediatría, Obstetricia y Ginecología y Medicina Preventiva de la Universitat Autònoma de Barcelona, España. Este trabajo contó con la colaboración del Grupo de Investigación Dermatológica (GRID) de la Universidad de Antioquia, Medellín, Colombia.
| 1. Alacán PL, Lemus CO, Lima AAS, Moredo RE. Eficacia de podofilina, ácido tricloroacético y criocirugía en el tratamiento de las verrugas genitales externas. Folia Dermatol Cub. 2012;6(3) |
| 2. Alfaro-Orozco LP, Alcalá-Pérez D, Navarrete-Franco G, González- González M, Peralta-Pedrero ML. Efectividad de la solución de Jessner más ácido tricloroacético al 35% vs 5-fluorouracilo al 5% en queratosis actínicas faciales múltiples. Dermatol Rev Mex. 2012;56:38-46 |
| 3. Alfonso-Trujillo I, Acosta D, Álvarez M, Pernas A, Toledo MC, Rodríguez MA. Condiloma acuminado: eficacia terapéutica comparativa entre el ácido tricloroacético solo y el ácido tricloroacético asociado al levamisol. Dermatol Perú. 2009;19: 114-121. |
| 4. Alfonso-Trujillo I, Acosta Medina D, Álvarez Labrada M, Rubén Quesada M, Rodríguez García MA. Condiloma acuminado: eficacia terapéutica comparativa entre la podofilina sola y la podofilina combinada con levamisol. Piel. 2009;24:354-359. |
| 5. Alfonso-Trujillo I, Acosta-Medina D, Álvarez-Labrada M, Gutiérrez AR, Rodríguez-García MA, Collazo-Caballero S.¿Radiocirugía o criocirugía en condiloma acuminado de localización anal? Dermatol Peru. 2008;18:98-105. |
| 6. Alfonso-Trujillo I, Rodríguez García MA, Rosa Gutiérrez A, Acosta Medina D, Navarro Maestre M, Collazo Caballero S. ¿Ácido tricloroacético o criocirugía en el tratamiento del condiloma acuminado? Piel. 2009;24(4):176-180. |
| 7. Alfonso-Trujillo I, Alvarez Labrada M, Gutiérrez Rojas AR, Rodríguez García MA, Collazo Caballero S. Condiloma acuminado: eficacia terapéutica comparativa entre la podofilina y la criocirugía. Dermatol Perú. 2008;18(1):27-34. |
| 8. Alonzo Romero Pareyón L, Navarrete Franco G, Hugo Alarcón H, Izabal M. Tratamiento del herpes zóster con ribavirina oral y tópica vs. placebo. Efecto sobre la incidencia de neuralgia postherpética. Estudio doble ciego. Rev Cent Dermatol Pascua. 2000;9:39-42. |
| 9. Amrouni B, Pereiro M Jr, Iglesias A, Labandeira J, Toribio J. Estudio comparativo en fase iii del clotrimazol y flutrimazol en la vulvovaginitis candidiásica aguda. Actas Dermosifiliogr. 1999;90(S1)72-73. |
| 10. Calderón C, Gutiérrez RM. Imiquimod al 5% en el tratamiento del carcinoma basocelular. Evaluación de la eficacia y tolerabilidad. Dermatol Rev Mex. 2002;46:114-120. |
| 11. Carbajosa Martínez J, Arenas R. Onicomicosis. Evaluación de la utilidad del curetaje quirúrgico en el tratamiento combinado (oral y tópico). Dermatología CMQ. 2008;6(3):157-162. |
| 12. Castillo-Oliva A, Alfonso-Trujillo I, Montecer-Ramosa B, Nodarse-Cuníb H, Pérez-Alonso T, Collazo-Caballero S, et al. Uso de crema de interferón alfa leucocitario humano en condilomas acuminados. Piel. 2009; 24(7):350-353. |
| 13. Catacora-Cama J, Cavero-Guardamino J, Manrique-Silva D, Delgado-González V, Aliaga-Ochoa E. Estudio comparativo de la seguridad y eficacia del furoato de mometasona vs dipropionato de betametasona en psoriasis. Folia Dermatol Per. 2001;12:1-6. |
| 14. Chouela E, Fleischmajer R, Pellerano G, Poggio N, Demarchi M, Mozzone R, et al. Tetraciclinas en el tratamiento de la psoriasis. Dermatol Argentina. 2004;4:307-312. |
| 15. Domínguez Soto L, Hojyo MT, Eljure N, Ranone VA, Garibay Valencia M, Fortuño Cordova V. Estudio comparativo entre 5-fluorouracilo a 0,5% en liposomas y 5-fluorouracilo a 5%, crema en tratamiento de queratosis actínica. Dermatología CMQ. 2010;8:173-183. |
| 16. Dominguez-Gomez J, Daniel-Simón R, Abreu-Daniel A. Eficacia del ácido glicirricínico (Herpigen-Glizygen) y un inmunoestimulador (Viusid) en el tratamiento de verrugas genitales. Folia Dermatol Cub. 2008;2(3). |
| 17. Dressendörfer LM, Jervis C, Palacios S. Eficacia terapéutica con el método de Goeckerman en pacientes con psoriasis en placas. Trabajo realizado en el servicio de Dermatología del Hospital Carlos Andrade Marín (Ecuador), agosto-noviembre de 2001. Rev Argent Dermatol. 2006;87:238-246. |
| 18. Fernández G, Enríguez J. Onicocriptosis: estudio comparativo del periodo posoperatorio de una matricectomía parcial lateral con el de una matricectomía parcial lateral con fenolización. Dermatol Rev Mex. 2006;50:87-93. |
| 19. Ferrándiz C, Bielsa I, Ribera M, Fuente MJ, Carrascosa JM. Terapia de refuerzo en pacientes con psoriasis tratada con calcipotriol. Actas Dermosifiliogr. 1998;89:626-630. |
| 20. Fonseca Capdevila E. Eficacia de eberconazol crema al 1% frente a clotrimazol crema al 1% en pacientes con micosis cutáneas. Piel. 2004;19:480-484. |
| 21. Fonseca Capdevila E, López Bran E, Fernández Vozmediano JM, Torre Fraga C de la;, Querol Nasarre I, Moreno Giménez JC. Prevención de secuelas cicatriciales de la extirpación de lesiones cutáneas benignas: estudio multicéntrico, prospectivo, abierto y controlado que compara un gel de silicona y láminas de silicona en 131 pacientes con nevos melanocíticos. Piel. 2007;22(9):421-426. |
| 22. Fonseca E, del Pozo J, Márquez M, Herrero E, Fillat O, Torres J, rt al. Evaluación de la eficacia y seguridad del sertaconazol en crema en aplicación única diaria en el tratamiento de las dermatofitosis. Piel. 1997;12 183-188. |
| 23. Gajardo Julio G, Valenzuela Gabriel R. Eficacia de la tretinoína tópica en fotoenvejecimiento cutáneo: estudio doble ciego randomizado. Rev Chil Dermatol. 2002;18:111-116. |
| 24. Galarza Manyari C. Eficacia y seguridad del tratamiento tópico con capsaicina 0,075 por ciento vs. capsaicina 0,050 por ciento en el tratamiento de la neuralgia postherpética. Hospital Nacional Dos de Mayo. Marzo 2003-febrero 2004. Dermatol Peru. 2005;15:108-112. |
| 25. Gaxiola-Álvarez E, Jurado Santa-Cruz F, Domínguez-Gómez MA, Peralta-Pedrero ML. Tratamiento de la alopecia areata en placas con capsaicina en ungüento al 0,075%. Rev Cent Dermatol Pascua. 2012;21:91-98. |
| 26. Guerra-Tàpia A, Díaz-Castella JM, Balañá-Vilanova M, Borràs-Múrcia C. Estudio para valorar la repercusión de una intervención informativa en la expectativa, el cumplimiento y la satisfacción de los pacientes con onicomicosis tratados con terbinafina. Estudio TERESA. Piel. 2005;20:211-218. |
| 27. Guerrero Robinson A, Medina Raquel K, Kahn Mariana Ch, Guerrero Javiera M. Utilidad y seguridad del 17-alfa-estradiol 0, 025 por ciento versus minoxidil 2 por ciento en el tratamiento de la alopecia androgénica. Rev Chil Dermatol. 2009;25(1):21-25. |
| 28. Herrán P, Ponce R, Tirado A. Eficacia y seguridad del 2-octil cianoacrilato versus sutura simple de heridas quirúrgicas en piel con inflamación crónica. Dermatol Rev Mex. 2011;55:185-187. |
| 29. Hinostroza-da-Conceicao D, Beirana-Palencia A. Tratamiento del molusco contagioso con hidróxido de potasio al 15% en solución acuosa. Dermatol Peru. 2004;14:185-191. |
| 30. Honeyman J. Isotretinoína oral en dosis bajas en el tratamiento del acné moderado. Dermatología Argentina. 1998;4:338-344. |
| 31. Jiménez RN, Aguirre AC, Ponce HS, Velasco AF. Mini injerto autólogo de piel e ingestión de 8-metoxipsoraleno en pacientes con vitiligo vulgar estable. Dermatol Rev Mex. 2002;46:260-267. |
| 32. Lapadula MM, Stengel FM, Maskin M, González P, Kaczvinsky Jr J, Soto R J, Get al. Estudio clínico para evaluar el efecto de dos cremas humectantes con protector solar en la piel de pacientes que utilizan tretinoína 0,025% para el tratamiento del fotodaño. Med Cutan Ibero Lat. 2008;36(5):232-239. |
| 33. Lizárraga García C, Rodríguez Acar M. Impacto de la adherencia en la efectividad de candidina intralesional vs ácido salicílico tópico al 27% en el tratamiento de las verrugas vulgares. Rev Cent Dermatol Pascua. 2009;18:5-18. |
| 34. López E, Álvarez M, Agorio C, Avendaño M, Bonasse J, Chavarría A, et al. Tratamiento comparativo entre ivermectina vía oral y permetrina tópica en la escabiosis. Rev Chil Dermatol. 2003;19:27-32. |
| 35. Loyo ME, Zapata G, Santana G. Molusco contagioso: evaluación de diversas modalidades terapéuticas. Dermatología Venezolana. 2003;41(2):25-28. |
| 36. Lugo-Villeda L, Leon-Dorantes G, Blancas González F. Thuja occidentalis homeopática vs- placebo en verrugas vulgares. Dermatol Rev Mex. 2001;45:14-18. |
| 37. Llergo Valdez RJ, Enríquez Merino J. Eficacia y tolerabilidad del polidocanol al 1% en el tratamiento con escleroterapia de várices grado i y ii, empleando compresión en el tercio proximal afectado. Rev Cent Dermatol Pascua. 2008;17:79-83. |
| 38. Maguiña C, Gotuzzo E, Álvarez H. Nuevos esquemas terapéuticos en el loxoscelismo Cutáneo en Lima, Perú. Folia Dermatológica Peruana. 1997;2:1-11. |
| 39. Martín Ezquerra G, Sánchez Regaña M, Umbert Millet P. Tratamiento de psoriasis en placas estable con un preparado que contiene furfuril sorbitol. Med Cután Ibero Lat. 2006;34: 155-158. |
| 40. Martínez-Abundis E, González-Ortiz M, Reynoso-von Drateln C, Pascoe- González S, de la Rosa-Zamboni D. Efecto de una mezcla de champú y anticonceptivos orales sobre el folículo piloso en mujeres sanas. Dermatol Rev Mex. 2004;48:77-81. |
| 41. Martorell-Calatayud A, Requena C, Nagore E, Sanmartín O, Serra-Guillén C, Botella-Estrada R, et al. Ensayo clínico: la infiltración intralesional con metotrexato de forma neoadyuvante en la cirugía del queratoacantoma permite obtener mejores resultados estéticos y funcionales. Actas Dermosifiliogr. 2011;102:605-615. |
| 42. Méndez-Velarde FA, Salceda-Pérez MA, Borjón-Moya C, Azpeitia- de la O CM, Vázquez-Coronado DP, Ore-Colio L. Efecto de una crema hidratante para prevenir las estrías del embarazo. Dermatol Rev Mex. 2010;54:273-278. |
| 43. Morales-Toquero A, Ocampo-Candiani J, Gómez-Flores M, González -González SE, Eguia-Rodríguez R, Méndez-Olvera NP, et al. Evaluación clínica e histológica de imiquimod a 5% en crema vs. 5-fluorouracilo a 5% en ungüento en pacientes con queratosis actínicas en la cara. Dermatología Rev Mex. 2010;54:326-331. |
| 44. Otero V, Bitar R, Rodríguez G. Tratamiento de la miliaria. Estudio comparativo sobre el uso de azitromicina. Rev Asoc Colomb Dermatol Cirug Dermatol. 2000;8:249-254. |
| 45. Pinto C, Hasson A, González S, Montoya J, Droppelmann, Inostroza ME, et al. Efecto de la terapia fotodinámica con metil aminolevulinato (MAL) comparada con luz roja en el tratamiento del acné inflamatorio leve a moderado. Rev Chilena Dermatol. 2011;27:177-187. |
| 46. Prada S, Salazar M, Muñoz A, Álvarez L. Tratamiento de úlceras venosas con factores de crecimiento derivados de plaquetas autólogas. Rev Asoc Colomb Dermatol Cirug Dermatol. 2000;8:122-128. |
| 47. Queiroz-Telles F, Ribeiro-Santos L, Santamaria J-R, Nishino L, Rocoo N-DO, Milanez V, Bastos C. Tratamiento da onicomicose dermatofitica con itraconazol: comparaçao entre dos esquemas terapéuticos. Med Cutan Ibero Lat. 1997;25:137-142. |
| 48. Ramírez-Bosca A, Zapater P, Betlloch I, Albero F, Martínez A, Díaz-Alperi J, et al. Extracto de polypodium leucotomos en dermatitis atópica. Ensayo multicéntrico aleatorizado, doble ciego y controlado con placebo. Actas Dermosifiliogr. 2012;103:599-607. |
| 49. Regis Roggero A, Pancorbo Mendoza J, Lanchipa Yokota P, Regis Roggero RM, Aguero M. Tratamiento y reinfestación por escabiosis humana: estudio comparativo entre permetrina al 5 por ciento vs benzoato de bencilo al 25 por ciento. Dermatol Peru. 2003;13:30-33. |
| 50. Ríos Yuil JM, Ríos Castro M. Respuesta clínica a las distintas modalidades terapéuticas antifúngicas en pacientes hospitalizados con onicomicosis. Dermatología Venezolana. 2011;49:25-29. |
| 51. Rodas Espinoza AF, Enríquez-M J, Alcalá-P D, Peralta-P ML. Efectividad de la bleomicina intralesional para el tratamiento de pacientes con cicatrices queloides. Estudio comparativo con dexametasona. Dermatol Rev Mex. 2011;55:119-126. |
| 52. Rodríguez C, Sánchez L, Minaya G, Vasquez J, Reymer D, Macher C. Tratamiento de las verrugas vulgares en niños con la hemolinfa del insecto Epicauta sp. Dermatol Peru. 2000;10:94-96. |
| 53. Rodríguez de Rivera-Campillo ME, López-López J, Chimenos-Küstner E. Tratamiento del síndrome de boca ardiente con clonacepam tópico. Piel. 2011;26:263-268. |
| 54. Rodríguez M, Medina-Hernández E. Estudio doble ciego, comparativo, sobre la eficacia y seguridad del crotamitón versus benzoato de bencilo en el tratamiento de la rosácea con demodicidosis. Dermatol Rev Mex. 2003;47(3):126-130. |
| 55. Rodríguez M. Efectividad de dos pastas de aplicación oral (amlexanox al 5% y clobetasol propionato 0,5%) en el tratamiento de úlceras aftosas recurrentes menores. Estudio clínico controlado, asignado aleatoriamente, enmascarado multicéntrico. Rev Asoc Colomb Dermatol Cirug Dermatol. 2004;12:78. |
| 56. Romero G, García M, Vera E, Martínez C, Cortina P, Sánchez P, et al. Resultados preliminares de DERMATEL: estudio aleatorizado prospectivo comparando modalidades de teledermatología síncrona y asíncrona Actas Dermosifiliogr. 2006;97:630-636. |
| 57. Rosón E, García Doval I, Flórez A, Cruce M. Estudio comparativo del tratamiento de la psoriasis en placas con baño de PUVA y UVB de banda estrecha 311nm. Actas Dermosifiliogr. 2005;96:371-375. |
| 58. Sáez M, Guimerà F, García M, Dorta S, Escoda M, Sánchez R, et al. Cloruro de aluminio hexahidratado en el tratamiento de las pustulosis palmoplantares Estudio preliminar. Actas Dermosifiliogr. 2000;91:416-469. |
| 59. Salomone C, Cárdenas C, Nicklas C, Pérez M-L. La consejería oral y escrita es un instrumento útil para mejorar la adherencia al tratamiento a corto plazo en sujetos con acné vulgar: ensayo clínico randomizado simple ciego. Rev Chil Dermatol. 2009;25(4):339-343. |
| 60. Sánchez M, Iglesias M, Umbert P. Tratamiento de la psoriasis en placas con propiltiouracilo tópico. Actas Dermosifiliogr.2001;92(4):174-176. |
| 61. Sánchez Domínguez MC. Estudio comparativo de la eficacia y seguridad del ácido pirúvico vs. crioterapia en el tratamiento de verrugas plantares. Dermatol Rev Mex. 2003;47:219-231. |
| 62. Tirado Sánchez A, Ponce Olivera RM. Eficacia y tolerabilidad del ß-lipohidroxiácido en barra dermolimpiadora en el manejo del acné comedónico leve a moderado. Dermatología CMQ. 2009;7(2):102-104. |
| 63. Tirado-Sánchez A, Ponce-Olivera RM, Montes de Oca-Sánchez G, León-Dorantes G. Calidad de vida y síntomas psicológicos en pacientes con acné severo tratados con isotretinoína. Dermatol Rev Mex. 2006;50:121-126. |
| 64. Valbuena MC, Gamboa LA. Comparación de la eficacia del trimetroprim-sulfametoxazol con el clorhidrato de tetraciclina en el tratamiento de acné nódulo-quístico. Rev Asoc Colomb Dermatol Cirug Dermatol. 1999;7:165-171. |
| 65. Valverde-López J, Lescano-Alva R. Eficacia comparativa de esquemas terapéuticos con cotrimoxazol en pediculosis capitis. Dermatol Peru. 2007;17:21-24. |
| 66. Vázquez González D, Fierro-Arias L, Arellano-Mendoza I, Tirado-Sánchez A, Peniche-Castellanos A. Estudio comparativo entre el uso de apósito hidrocoloide vs. uso de tie-over para valorar el porcentaje de integración de los injertos cutáneos de espesor total. Dermatol Rev Mex. 2011;55:175-179. |
| 67. Vences Carranza M, Rodríguez-Acar M. Efecto acaricida del azufre octaédrico, tintura de yodo con ácido salicílico y benzoato de bencilo en el tratamiento de la demodicidosis. Dermatol Rev Mex. 2004;48:121-126. |
| 68. Vicuña-Ríos D, Tincopa-Montoya L, Valverde-López J, Rojas-Plasencia P, Tincopa-Wong O. Eficacia de las cremas de ciclopirox 1% y ketoconazol 2% en el tratamiento de la dermatitis seborreica facial leve a moderada. Dermatol Perú. 2005;15:25-29. |
| 69. Vidal-Flores A, Enríquez-Merino J. Matricectomía parcial quirúrgica vs. matricectomía parcial con electrofulguración en el tratamiento de la onicocriptosis. Dermatol Rev Mex. 2006;50:54-59. |
| 70. Villaseñor Ovies P, Rebollo Domínguez N, Fernández Martínez R, Arenas Guzmán R, Magaña C, Soto Navarro M. Comparación entre bifonazol y ketoconazol en el tratamiento de tinea pedis: resultados de un ensayo clínico. Dermatología CMQ. 2012;10:168-171. |