El melanoma mucoso es un subtipo infrecuente de melanoma que difiere del melanoma cutáneo en su biología, clínica y manejo. El diagnóstico suele realizarse de forma tardía debido a su localización en zonas de difícil acceso a la exploración física y a la falta de signos específicos y tempranos. La cirugía es el tratamiento de elección en caso de enfermedad localizada. El papel de la biopsia selectiva de ganglio centinela y de la linfadenectomía permanece todavía incierta. La radioterapia se puede emplear como tratamiento adyuvante con el fin de controlar localmente la enfermedad. Existe un mayor porcentaje de mutaciones en c-KIT que en otros tipos de melanoma, lo que ha llevado a avances significativos en el tratamiento de la enfermedad metastásica con imatinib.
Mucosal melanoma is a rare melanoma subtype that differs from the cutaneous form of the tumor in its biology, clinical manifestations, and management. Diagnosis is usually late due to a lack of early or specific signs and the location of lesions in areas that are difficult to access on physical examination. Surgical excision is the treatment of choice for localized disease. The value of sentinel lymph node biopsy and lymphadenectomy is still unclear. Radiotherapy can be used as adjuvant therapy for the control of local disease. c-KIT mutations are more common than in other types of melanoma and this has led to significant advances in the use of imatinib for the treatment of metastatic mucosal melanoma.
El melanoma mucoso se desarrolla a partir de los melanocitos de las mucosas. Existen melanocitos en todas las superficies mucosas, donde no participan en la fotoprotección, sino que cumplen funciones inmunológicas, antibacterianas, fagocíticas y de presentación de antígenos y producción de citocinas1. Aunque todos los melanocitos tienen el mismo origen embriológico, el microambiente en su destino final difiere en distintos lugares del organismo. Los melanocitos se sitúan en diferentes clases de tejidos y están rodeados por diferentes tipos de células, por lo que difieren en moléculas de adhesión o vías de señalización (pathways) que afectan a su crecimiento y mantenimiento, y consecuentemente al desarrollo del melanoma2.
Debido a su rareza, los conocimientos sobre la patogenia son insuficientes y no hay protocolos establecidos para su estadificación o tratamiento.
EpidemiologíaEl melanoma mucoso representa el 1% de todos los melanomas y su incidencia permanece estable, en contraste con el melanoma cutáneo, cuya incidencia va en aumento3–5. Aparecen por orden de frecuencia en la cabeza y el cuello, en la mucosa ano-rectal y en la mucosa vulvo-vaginal.
En comparación con el melanoma cutáneo el melanoma mucoso suele aparecer en edades más avanzadas, con una edad media al diagnóstico de 70 años6, aunque el melanoma de cavidad oral aparece en sujetos más jóvenes7. Al contrario que el melanoma cutáneo, el melanoma mucoso es más frecuente en mujeres que en hombres, con una ratio de 1,85 a 13. Este predominio del sexo femenino es debido a la frecuencia del melanoma vulvo-vaginal, que es el tipo más común que afecta a las mujeres8. En hombres el subtipo más frecuente es el de la cabeza y el cuello.
Existe una mayor proporción de melanoma mucoso sobre el total de melanomas en sujetos de raza negra, asiáticos e hispanos9. Hasta el 9% de todos los melanomas diagnosticados en negros o asiáticos son melanomas mucosos en comparación con el 1% en blancos8. A pesar de esto la incidencia absoluta de melanoma mucoso es mayor en blancos.
EtiopatogeniaDebido a su rareza se conoce poco sobre la patogenia, y hasta el momento no se han identificado factores de riesgo implicados. La asociación existente entre la exposición a radiación ultravioleta y el melanoma cutáneo no está presente en el melanoma mucoso. No se ha establecido tampoco asociación con el virus del papiloma humano, los herpes virus ni el poliomavirus2. Se ha sugerido que el formaldehído puede ser un factor de riesgo para el melanoma nasosinusal10,11, y que el melanoma oral puede estar precedido por un fenómeno de melanosis oral12, y aunque el tabaco puede inducir la aparición de lesiones pigmentadas en la mucosa oral no existen pruebas suficientes para considerar el tabaco como un carcinógeno en relación con el melanoma mucoso.
Existen distintos tipos de mutaciones en los diferentes tipos de melanoma. Los melanomas cutáneos presentan frecuentemente mutaciones oncogénicas en BRAF, mientras que esta mutación se encuentra raramente en el melanoma mucoso13. En este se ha encontrado una mayor proporción de mutaciones y/o incremento en el número de copias de KIT (receptor tirosín cinasa), que varían entre el 15,6 y el 39% según las series14,15. Beadling et al. encuentran mutaciones en el 15,6% y aumento de copias en el 26,3%15. En este mismo estudio encuentran además que estos porcentajes varían en función de la localización del melanoma mucoso, siendo más frecuente en el melanoma vulvo-vaginal (44,4%) con respecto al de la cabeza y el cuello (8,3%). En otro estudio similar encuentran mutaciones de KIT en el 35% de los melanomas vulvares, el 9% de los ano-rectales, el 7% de los de cavidad nasal y el 20% de pene, sin encontrar mutaciones en los melanomas vaginales16. Además reportan frecuencias de mutaciones del 10% en NRAS y del 6% en BRAF de los melanomas mucosos estudiados. En un estudio europeo encuentran mutaciones en KIT en el 30% de los melanomas genitales, mientras que no encuentran en los sinusales y anales17. Otras alteraciones evidenciadas en los melanomas mucosos son la presencia de una mayor frecuencia de amplificaciones focales y pérdidas de loci (amplificaciones en CDK4 y pérdidas del locus CDKN2A), así como aberraciones cromosómicas distintas de los melanomas localizados en piel con daño solar crónico18. Todas las series publicadas contienen un número limitado de casos, por lo que serían necesarios más estudios para ver si estas tendencias son significativas. Sin embargo, estas diferencias en las mutaciones genéticas entre los distintos tipos de melanoma indican que probablemente representen entidades biológicas diferentes, además de su diferencia clínica.
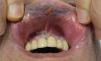
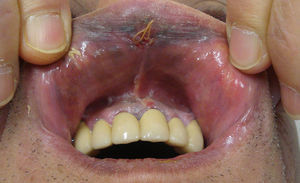
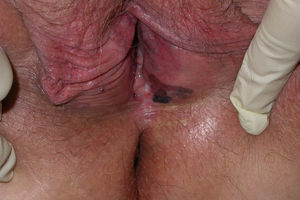
Características clínicas y diagnósticoEl melanoma mucoso es difícil de diagnosticar por su localización en áreas de complicado acceso a la exploración y por adoptar una clínica muy variada (figs. 1 y 2). Frecuentemente son diagnosticados durante largo tiempo de otros procesos y cuando se diagnostica mediante biopsia suele encontrarse en estadios avanzados. Se ha estimado que el 20% de los melanomas mucosos son multifocales19 comparado con el 5% de los cutáneos, y que aproximadamente el 40% son amelanóticos20 en comparación con el 10% de los melanomas cutáneos (tabla 1).
Comparación entre melanoma mucoso y cutáneo
| Melanoma mucoso | Melanoma cutáneo | |
|---|---|---|
| Incidencia | 2,2 por millón de personas/año | 153,5 por millón de personas/año |
| Tendencia incidencia | Estable | En aumento |
| Mujeres:varones | 1,85:1 | 0,72:1 |
| Grupos demográficosNegrosBlancosHispanos | 2 por millón4 por millón4% de todos los melanomas | 22 por millón347 por millón86% de todos los melanomas |
| Influencia geográfica | No existen diferencias | Mayor incidencia en países del sur y con costas |
| Factores de riesgo | Desconocidos | Radiación ultravioleta |
| Edad media al diagnóstico (años) | 70 | 44 |
| ClínicaMultifocalAmelanótico | 20%40% | 5%10% |
| Afectación ganglionar al diagnóstico | Cabeza y cuello 21%Ano-rectal 61%Vulvo-vaginal 23% | 9% |
| Supervivencia a los 5 años | 25% | 83% |
| Sistema de estadificación | No existe un sistema validado y aceptado | AJCC |
| Mutaciones genéticas más frecuentes | c-KIT | BRAF |
| Tratamiento de la enfermedad local | Cirugía±radioterapia | Cirugía |
| Indicación de ganglio centinela | No | Breslow mayor de 1mm |
| Linfadenectomía | Solo si adenopatías sintomáticas | Si N+ |
| Tratamiento sistémico | Imatinib | Vemurafenib |
AJCC: American Joint Committee on Cancer.
En caso de pigmentación oral focal se debe realizar el diagnóstico diferencial con la mácula melanótica y la melanosis del fumador fundamentalmente. La mácula melanótica es una lesión pequeña, bien delimitada, de color marrón-negro, homogénea, que suele localizarse en los labios y las encías. La melanosis del fumador aparece en el 25-31% de los fumadores en forma de múltiples máculas marrones que coalescen y que suelen localizarse en la superficie labial de la encía mandibular. Puede desaparecer tras meses de abandono tabáquico. Existen otras causas de pigmentación de la mucosa oral que suelen dar pigmentaciones más difusas y que en determinados casos también tendremos que tener en cuenta (pigmentación fisiológica, postinflamatoria, por cuerpo extraño, farmacológica u hormonal)21.
En caso de pigmentación genital focal se debe realizar el diagnóstico diferencial con la mácula melanótica genital, que clínicamente se presenta como una lesión pequeña, homogénea y estable en el tiempo. En el caso de presentar características atípicas o cambios en el tiempo debería realizarse una biopsia para descartar el diagnóstico de melanoma. En caso de pigmentación difusa o con múltiples lentigos debemos pensar en que se trate de una manifestación de una enfermedad sistémica (lentiginosis o endocrinopatías)22.
En la dermatoscopia del melanoma mucoso se observa un patrón multicomponente en el 75% de los casos y homogéneo en el 25% restante. Los algoritmos de diagnóstico dermatoscópico que se utilizan para el melanoma cutáneo son válidos también para el melanoma mucoso, con alta sensibilidad y especificidad23. La combinación de áreas de color azul, gris y blanco son indicadores de melanoma mucoso24.
En el diagnóstico del melanoma mucoso es crucial excluir la posibilidad de que se trate de una metástasis de un melanoma cutáneo u ocular, incluso de un melanoma regresado2. Si no existe historia previa de melanoma se debe realizar un examen físico cutáneo y oftalmológico. La presencia de melanoma in situ es importante para distinguir la forma primaria de la metastásica25.
Los melanomas cutáneos presentan afectación ganglionar locorregional en el 9% de los casos en el momento del diagnóstico. Esta afectación ganglionar en el momento del diagnóstico es más frecuente en el melanoma mucoso, ya que está presente en el 21% de los melanomas mucosos de la cabeza y el cuello, en el 61% de los ano-rectales y en el 23% de los vulvo-vaginales7.
EstadificaciónNo existe un sistema de estadificación universal para todos los tipos de melanoma mucoso. Se utilizan distintos sistemas de estadificación según la localización anatómica utilizando la de otros tipos de tumor en la misma localización.
Existe sin embargo un sistema de estadificación que se puede utilizar en todos los casos (estadificación simplificada de Ballantyne26):
Estadio I: enfermedad localizada.
Estadio II: afectación ganglionar regional.
Estadio III: enfermedad metastásica a distancia.
Debido a su rareza no se han realizado ensayos clínicos controlados, por lo que la práctica clínica se basa en series de casos y análisis retrospectivos.
En el caso de que la enfermedad esté localizada en el momento del diagnóstico el manejo debe de ir encaminado a un control locorregional de la enfermedad mediante cirugía y/o radioterapia. El tratamiento de primera elección es siempre la cirugía con márgenes libres. En casos en los que la extirpación no sea completa, o esta no sea factible, el tratamiento de elección es la radioterapia, ya sea adyuvante o paliativa. El control local de la enfermedad es complicado debido a su delicada localización anatómica y a su naturaleza multifocal. Se considera un defecto del campo donde pueden aparecer múltiples lesiones primarias, que pueden estar presentes en el momento del diagnóstico o pueden desarrollarse durante el seguimiento19. Esta naturaleza multifocal parece más frecuente en el melanoma de vulva, uretra masculina y cabeza y cuello27–29. Sugiere un desorden compartido de los melanocitos de las mucosas y comporta un reto a la hora de obtener un control quirúrgico local.
El manejo agresivo locorregional mediante cirugía y radioterapia tiene como objetivo el control local de la enfermedad, por lo que es necesario siempre sopesar el balance riesgo-beneficio y analizar cada caso por separado. El papel de la biopsia selectiva del ganglio centinela y de la linfadenectomía electiva no está todavía claro.
Melanoma mucoso de cabeza y cuelloLa afectación de la región naso-sinusal es más frecuente que la de la región oral (59-80% y 16-41% respectivamente)29,30. La mayoría de los pacientes (80%) presentan enfermedad localizada en el momento del diagnóstico gracias al desarrollo de síntomas tempranos como epistaxis, obstrucción nasal, cambios en la visión o molestias orales. La afectación ganglionar en el momento del diagnóstico es más frecuente en los de la región oral que en los de la naso-sinusal (25 versus 6%)29. Los tumores con invasión vascular histológica, grosor mayor de 5mm y un estadio más avanzado al diagnóstico se han asociado con un peor pronóstico29. El pronóstico general es malo, con una supervivencia del 26% a los 2 años y del 8% a los 5 años30.
Se utiliza el sistema de estadificación de la AJCC31, el cual, reflejando el mal pronóstico de la enfermedad, considera directamente estadio iii a la enfermedad localizada. La enfermedad avanzada es considerada estadio iv con varios subtipos (A, B y C) según el grado de afectación local, la existencia de extensión ganglionar o a distancia (tablas 2 y 3).
Clasificación TNM del melanoma mucoso de cabeza y cuello
| Tumor primario (T) |
| T3: enfermedad mucosa |
| T4a: enfermedad moderadamente avanzada; tumor que afecta a tejidos blandos profundos, cartílago, hueso o piel suprayacente |
| T4b: enfermedad muy avanzada; tumor que afecta al cerebro, duramadre, pares craneales bajos (ix, x, xi, xii), espacio masticador, arteria carótida, espacio prevertebral o estructuras mediastínicas |
| Ganglios regionales (N) |
| NX: ganglios linfáticos no evaluables |
| N0: sin metástasis en ganglios linfáticos regionales |
| N1: metástasis en ganglios linfáticos regionales |
| Metástasis a distancia (M) |
| M0: sin metástasis a distancia |
| M1: metástasis a distancia |
Fuente: AJCC cancer staging manual, 7th ed. (2010).
El manejo en los estadios iii y ivA es fundamentalmente quirúrgico, preferentemente endoscópico en los casos en que sea posible, con el objetivo de minimizar la morbilidad. La resección completa con márgenes negativos es difícil de alcanzar debido al crecimiento lentiginoso, a la enfermedad multifocal y a las dificultades anatómicas. A pesar de realizar cirugías agresivas las tasas de recurrencia permanecen altas (29-79%)29. En caso de recurrencia local es necesario realizar una reestadificación antes de repetir la resección, ya que la recurrencia local se asocia a metástasis a distancia32.
El papel de la biopsia del ganglio centinela no está claro33, de la misma manera que no hay datos suficientes que apoyen el tratamiento adyuvante con interferón-alfa 2b para mejorar la supervivencia en caso de que este sea positivo. La linfadenectomía se recomienda solo en caso de adenopatías clínicamente aparentes. No existen diferencias en la supervivencia de pacientes con y sin afectación ganglionar dada la temprana y alta tasa de diseminación hematógena, a pesar de un manejo agresivo de los ganglios34. La radioterapia se ha utilizado como tratamiento adyuvante tras la resección quirúrgica, pero su beneficio no está claro y no mejora la supervivencia35–37; se puede utilizar para mejorar el control local de la enfermedad.
Melanoma mucoso ano-rectalSe divide de manera igualitaria en canal anal, recto y sitios intermedios38. La incidencia es mayor en mujeres, pero esto puede ser debido a un factor de confusión debido a una mayor frecuencia de evaluación perineal durante las exploraciones ginecológicas5. Los síntomas más frecuentes son sangrado, dolor y prolapso. Habitualmente son lesiones polipoides con o sin pigmentación. Suelen diagnosticarse inicialmente de hemorroides, pólipos o adenocarcinoma.
En el momento del diagnóstico el 60% de los pacientes presentan afectación ganglionar y el 20% metástasis a distancia7. El pronóstico es malo, con una supervivencia a los 5 años del 20% en caso de enfermedad locorregional resecable y del 0% en enfermedad avanzada39.
Para su estadificación se utiliza el sistema simplificado de Ballantyne26. La presencia de invasión perineural en la histología ha sido identificada como un predictor de mortalidad independiente6.
El manejo de la enfermedad localizada es quirúrgico. Se prefiere realizar cirugías con márgenes amplios pero conservadoras, ya que cirugías más agresivas conllevan mayor morbilidad sin mejorar el pronóstico39–41. Ni la técnica del ganglio centinela ni la linfadenectomía mejoran el pronóstico, y las metástasis ganglionares no se asocian con mayor recurrencia o peor pronóstico40. Solo se deberían resecar las adenopatías sintomáticas. La radioterapia adyuvante puede mejorar el control local de la enfermedad pero no mejora el pronóstico.
Melanoma mucoso vulvo-vaginalLa mayoría de los casos se localizan en la vulva y una minoría en la vagina (menos del 5%). El pronóstico del melanoma vulvar es mejor que el del melanoma vaginal (supervivencia a los 5 años del 50 y 19% respectivamente) y afecta a pacientes mayores (60-80 años versus 50-70 años)42–44. El melanoma de vulva es la segunda malignidad más frecuente en esta localización tras el carcinoma epidermoide, y aparece más frecuentemente en el área clitoriana y en los labios mayores. Se puede presentar en forma de sangrado, masa, picor o disuria. Pueden ser amelanóticos y presentar lesiones satélite.
Para el melanoma vaginal se utiliza el sistema de estadificación simplificada de Ballantyne26. Para el melanoma vulvar existe un sistema de estadificación específico de la AJCC31 que es el mejor predictor de supervivencia.
El manejo locorregional es quirúrgico, con márgenes amplios pero evitando cirugías agresivas, ya que no aumentan la supervivencia45,46. El papel de la técnica del ganglio centinela no está claro, y la resección ganglionar solo está indicada si existen adenopatías sintomáticas.
Localizaciones menos frecuentesSe han publicado un número limitado de casos de melanoma mucoso en otras localizaciones menos frecuentes como la uretra masculina, la vejiga, el esófago y otras partes del intestino47–51.
Tratamiento adyuvanteSe desconoce la actividad del interferón-alfa para las formas de melanoma mucoso, ya que su biología es distinta y se ha excluido de los ensayos clínicos debido a su alta resistencia a terapias sistémicas. Esta exclusión también se mantiene en los recientes ensayos clínicos que comparan como tratamiento adyuvante altas dosis de interferón-alfa con ipilimumab e ipilimumab con placebo.
La radioterapia se ha utilizado como tratamiento adyuvante tras la resección quirúrgica para mejorar el control local de la enfermedad, aunque su beneficio no está claro, ya que no se ha demostrado que mejore la supervivencia36–38.
Tratamiento sistémico para el melanoma mucoso avanzadoEl tratamiento quimioterápico estándar con dacarbazina utilizado en el melanoma cutáneo con limitada eficacia parece tener una eficacia menor en el melanoma mucoso52. Existen otras series cortas de instituciones únicas que utilizan un régimen más agresivo de bioquimioterapia (cisplatino, vinblastina, dacarbazina, interferón-alfa 2b e interleucina-2) en pacientes con varios subtipos de melanoma mucoso reportando bajas tasas de respuesta, tanto completa como parcial53–55. Estas pequeñas series sugieren respuestas similares a las del melanoma cutáneo.
Existe un ensayo clínico aleatorizado en fase ii que compara observación versus interferón-alfa 2b versus quimioterapia (temozolamida y cisplatino) en pacientes con melanoma mucoso extirpado. En los resultados destaca un aumento en la supervivencia global y en la supervivencia libre de enfermedad en el brazo de la quimioterapia56.
El ipilimumab fue el primer agente en demostrar un beneficio en la supervivencia global en pacientes con melanoma cutáneo avanzado en un ensayo en fase iii57. Hasta el momento la información disponible sobre el tratamiento con ipilimumab en melanoma mucoso es insuficiente.
Gracias a los nuevos conocimientos sobre anormalidades genéticas en distintos tipos de melanoma ha sido posible desarrollar nuevos agentes dirigidos contra dianas terapéuticas. En el caso del melanoma mucoso inhibidores de pequeñas moléculas de c-KIT, como el imatinib, han demostrado actividad en pacientes con mutaciones y/o amplificaciones de c-KIT58. En un estudio donde tratan a 13 pacientes con melanoma mucoso y aberraciones en c-KIT observan respuesta en 3 pacientes, uno con una respuesta completa duradera (mutación y amplificación), uno con una respuesta parcial duradera (mutación sin amplificación) y otro con una respuesta parcial transitoria (mutación y amplificación)59. Hay que tener en cuenta que no todas las mutaciones en c-KIT son oncogénicas. Los tumores con mutaciones que afectan a los exones 11 y 13 son particularmente sensibles a la inhibición de c-KIT. En otro estudio en fase ii donde tratan a 43 pacientes con mutaciones en c-KIT se observó una tasa de respuesta del 23%60. En este estudio se incluyeron 11 pacientes con melanoma mucoso, pero no se realizó un análisis por subgrupos en cuanto a respuesta clínica. Se está llevando a cabo también un estudio con dasatinib en pacientes con distintos tipos de melanoma con mutaciones en c-KIT.
Se ha observado el desarrollo de resistencias tempranas en pacientes que inicialmente responden a inhibidores de c-KIT. Aunque el mecanismo de resistencia no está claro, parece que podrían aparecer nuevas mutaciones distintas. En este sentido existe un caso publicado de un paciente que desarrolló una mutación en NRAS que previamente no presentaba61, y otro caso describe el desarrollo de una sobreexpresión de mTOR con buena respuesta a everolimus62. Son necesarios más estudios para conocer estos mecanismos de escape y sus potenciales dianas para nuevos tratamientos o combinaciones. Actualmente se está realizando un ensayo clínico con nilotinib en pacientes que han desarrollado resistencia o intolerancia (NCT00788775).
En aquellos pacientes con melanoma mucoso y con mutaciones en BRAF parece que no existen diferencias respecto al resto de melanomas en cuanto a la respuesta al tratamiento con vemurafenib, por lo que este tratamiento estaría indicado en este grupo de pacientes63.
Debería considerarse la realización de un estudio de mutaciones en KIT y en BRAF en pacientes con melanoma mucoso avanzado. En caso de detectarse una de estas mutaciones habría que considerar su inclusión en ensayos clínicos con agentes inhibidores de KIT (imatinib, sorafenib, dasatinib, sunitinid o nilotinib) o de BRAF (vemurafenib). En el caso de que estos pacientes desarrollen mutaciones se debería valorar la realización de nuevos estudios moleculares. En caso de no encontrarse ninguna mutación podría ser de utilidad el tratamiento con ipilimumab5.
ConclusionesEl melanoma mucoso es una entidad clínica y biológicamente distinta del melanoma cutáneo. Su diagnóstico suele ser tardío y su pronóstico malo. El tratamiento quirúrgico con márgenes libres suele ser difícil debido a la localización anatómica y a la multifocalidad.
La cirugía es el tratamiento de elección en caso de enfermedad localizada, con el fin de obtener márgenes libres, pero sin realizar amplias extirpaciones. El papel de la biopsia selectiva del ganglio centinela y de la linfadenectomía electiva permanece todavía incierta. La radioterapia se puede emplear como tratamiento adyuvante con el fin de controlar localmente la enfermedad. No se ha demostrado hasta la fecha que el pronóstico de la enfermedad mejore con una cirugía radical, con la técnica del ganglio centinela, con la realización de una linfadenectomía ni con la radioterapia.
El descubrimiento de la mutación en c-KIT ha llevado a grandes avances en el tratamiento de la enfermedad, aunque todavía quedan por esclarecer los mecanismos de resistencia a estos fármacos y sus posibles dianas terapéuticas. Son por tanto todavía necesarios más estudios para mejorar el pronóstico de estos pacientes.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.