INTRODUCCION
Cada vez que en una reunión del Grupo Español de Dermatopatología se ha planteado el problema de los criterios para el diagnóstico histopatológico de nevo melanocítico displásico la reacción habitual ha sido decir que era un problema demasiado complejo y que la discusión se iba a alargar durante horas sin llegar a ningún acuerdo. Sin embargo, nevo displásico es un diagnóstico que se hace a diario en la mayoría de los laboratorios de Anatomía Patológica de España y del mundo, por lo que cabe suponer que los que lo hacen se basarán en unos criterios, igual que los tienen para diagnosticar liquen plano o carcinoma basocelular.
Por otro lado, si en las reuniones no se discuten y se delimitan esos criterios cabe suponer que los dermatopatólogos se basan en los criterios publicados en los actuales libros de dermatopatología. Por ello, con el fin de intentar saber cuáles son esos criterios, hemos acudido a esos textos.
MATERIAL Y MÉTODOS
Nuestro trabajo ha consistido en reproducir y resumir con la mayor fidelidad posible, tanto en los conceptos como en la traducción, las descripciones histopatológicas de los textos que pasamos a enumerar. En algunos casos en que las descripciones originales son algo desordenadas hemos procurado ponerlas en orden sin cambiar sus palabras ni su sentido.
Los textos resumidos son los siguientes:
-- Los dos primeros artículos de Clark y su grupo en los que definieron el síndrome B-K1 y el síndrome del nevo displásico2.
-- El libro de Maize y Ackerman sobre lesiones pigmentadas de la piel, de 19873.
-- El capítulo sobre nevo displásico y melanoma de la primera edición del libro de Farmer & Hood4.
-- Los capítulos referentes a neoplasias melanocíticas de los seis últimos libros de dermatopatología publicados entre 1996 y 20005-10.
-- El libro, de reciente aparición, sobre proliferaciones melanocíticas de Crowson et al11.
Estos once textos comprenden:
El punto de partida del concepto de nevo displásico1-2.
-- Su primera descripción coherente3.
-- Los textos donde los autores de libros de dermatopatología de mayor difusión mundial resumen su concepto del tema.
Hemos incluido el capítulo correspondiente de la primera edición del Farmer & Hodd porque sus dos primeros autores son Clark y Elder4, los primeros firmantes de las dos descripciones princeps1, 2; así podemos saber cómo ha evolucionado su concepto y sus criterios entre 1978 y 1990. Por otro lado, en tres de los siete últimos libros enumerados alguno de los autores de los respectivos capítulos son destacados discípulos, colaboradores y continuadores de las ideas de Clark: Elder7, Barnhill8 y Mihm11.
El resumen de los criterios histopatológicos para el diagnóstico de nevo displásico de cada uno de los capítulos y libros mencionados va precedido por la clasificación que sus autores hacen de las neoplasias melanocíticas. De este modo intentamos saber cuál es la idea de sus autores en cuanto a la naturaleza de ese proceso; es decir, si lo consideran una mera variedad de nevo melanocítico, un melanoma de baja malignidad o una entidad sui generis.
Tanto la clasificación como los criterios histopatológicos de nevo displásico de cada autor o autores son comentados por separado y finalmente hacemos una recapitulación del problema enumerando las coincidencias y discrepancias entre ellos y aportamos nuestra personal visión del tema.
RESULTADOS
La descripción princeps de Clark et al1
La descripción histopatológica del lunar B-K1
La histología es necesaria para diagnosticar los lunares B-K.
Microscópicamente se ve un nevo melanocítico com-puesto.
Su componente intraepidérmico es similar al de los nevos melanocíticos ordinarios y su componente dérmico es uniformemente celular, limitado a la dermis papilar y no muestra neurotización.
Algunos de los lunares grandes mostrarían los cambios microscópicos característicos del síndrome del lunar B-K.
Esos cambios se superponen a un nevo melanocítico compuesto e incluyen:
-- Hiperplasia melanocítica atípica.
-- Cambios mesenquimales en dermis superficial.
-- Infiltrado linfocitario.
Hiperplasia melanocítica atípica (o displasia melanocítica) significa:
-- Melanocitos individuales o pequeños nidos de melanocitos que tienen alguno de los caracteres estructurales de los melanocitos malignos, pero cuyo potencial de desarrollo hacia un melanoma es oscuro; puede permanecer indolente, regresar completamente o progresar a la malignidad.
-- Los melanocitos atípicos pueden estar aislados en la zona basilar de la epidermis o disponerse en nidos irregulares, elipsoides, de eje mayor paralelo a la interfase dermoepidérmica.
También pueden verse en la parte más superficial de la dermis papilar.
-- Los melanocitos atípicos individuales son grandes y relativamente pálidos. Pueden observarse figuras de mitosis. Son frecuentemente fusiformes, pero pueden ser grandes y epitelioides.
El citoplasma es abundante y lleno de finos gránulos de melanina «pulverulenta».
En las zonas donde hay melanocitos atípicos, hay cambios dérmicos y un infiltrado de linfocitos y macrófagos.
-- La dermis papilar está ensanchada porque hay fibroplasia delicada y neoformación vascular.
La histología dérmica es virtualmente indistinguible de la de las zonas de regresión de los melanomas.
Ocasionalmente se ve un lunar B-K sin componente intradérmico: lunar B-K de novo.
Comentario
Como muy bien dicen los autores, «la histología es necesaria para diagnosticar los lunares B-K». En patología tumoral el diagnóstico se basa en la histopatología. La clínica sólo manda, a efectos de diagnóstico, para determinados hechos circunstanciales como, por ejemplo, la edad de aparición de la lesión (congénita o adquirida, etc.) o el número de lesiones (lentiginosis frente a mácula melanótica, etc.). Por eso no puede hablarse nada acerca de ningún otro aspecto del nevo displásico sin que previamente haya un consenso sobre cuáles son los criterios mínimos imprescindibles para su diagnóstico histopatológico.
Los autores consideran que el lunar B-K es un nevo melanocítico compuesto con algunas características añadidas: hiperplasia melanocítica atípica y cambios de la dermis superficial, incluida una reacción linfocitaria.
Los melanocitos atípicos, aislados o en nidos, tienen «alguno de los caracteres estructurales de los melanocitos malignos» (frase de difícil comprensión, pues mezcla citología y estructura).
Estas lesiones, como todos los nevos melanocíticos, pueden permanecer inalterables, regresar o malignizarse (los autores olvidan que otra de las evoluciones habituales de los nevos melanocíticos es la de madurar [envejecer]).
Los autores introdujeron en este artículo una palabra que, creemos, no había aparecido hasta entonces en la literatura dermatopatológica en lengua inglesa: la palabra basilar. Se trata de un sinónimo de basal; esta palabra aparece repetida reiteradamente en los artículos del grupo a lo largo de los años para recalcar la situación siempre en la basal, nunca suprabasal, de los melanocitos epidérmicos (aislados o en nidos) del nevo displásico, hecho esencial para diferenciarlo de un melanoma. No se trata, parecen querer decir, de un melanoma incipiente, sino de un nevo melanocítico compuesto con mayor propensión a malignizarse que otros nevos melanocíticos compuestos. Y esa tendencia biológica se trasluce en su estructura histológica, principalmente porque sus nidos son «irregulares, elipsoides, de eje mayor paralelo a la interfase dermoepidérmica».
Los melanocitos atípicos son grandes, pálidos, frecuentemente fusiformes y también epitelioides*, conteniendo melanina pulverulenta. En dermis papilar, coincidiendo con los melanocitos atípicos, hay reacción inflamatoria y toda la dermis papilar muestra fibroplasia y neoformación vascular.
* No nos gusta el término «epitelioide» porque es rara la entidad tumoral o inflamatoria donde no se hayan descrito células «epitelioides», lo cual quita cualquier especificidad al término como consecuencia de su abuso. Si lo usamos debemos entender que hablamos de células con citoplasma amplio de límites bien visibles, ya que ésa es la característica diferencial de la mayor parte, aunque no de todas, las células epiteliales.
Aunque los autores empiezan definiendo al lunar B-K como un nevo compuesto, finalmente dicen que a veces es juntural; y añaden que ése sería el lunar B-K de novo, como dando a entender que el lunar B-K compuesto es un nevo melanocítico «común» que de pronto empieza a hacer «tonterías».
Resulta muy difícil, por no decir imposible, hacerse una idea de cómo es, histológicamente, el lunar B-K leyendo la descripción de los autores, ya que se trata de un nevo melanocítico compuesto «con un componente epidérmico similar al de los nevos melanocíticos ordinarios» y un componente dérmico uniformente celular. ¿Cómo encuadrar en este fondo los cambios microscópicos característicos del lunar B-K? Cuando el más viejo de nosotros leyó este artículo, hace ya bastantes años, no fue capaz de enterarse de casi nada, por no decir de nada.
La descripción princeps de Elder et al2
La descripción histopatológica del nevo displásico2
-- Hemos identificado una segunda clase de nevo displásico que de forma habitual clasificamos histológicamente como displasia melanocítica letiginosa.
-- Hay proliferación basal irregular de melanocitos hipercromáticos, pleomorfos, que muestran un artefacto de retracción citoplasmática prominente. Los melanocitos hiperplásicos se disponen habitualmente en los márgenes de crestas epidérmicas alargadas.
Los aspectos histológicos comunes a todos los nevos displásicos fueron pleomorfismo e hipercromatismo nuclear en unas pocas o muchas células de cada lesión. Las mitosis no eran frecuentes.
Crecimiento desordenado de los melanocitos intraepidérmicos con dos variantes:
-- Displasia melanocítica lentiginosa (es la más común; se halla en todas las lesiones displásicas). Hiperplasia de melanocitos intraepidérmicos irregularmente orientados, basalmente situados. Aunque algunas células se agrupaban en nidos pequeños, las clásicas tecas aisladas del nevo juntural no estaban presentes.
Por regla general los melanocitos displásicos se disponían en la periferia de las crestas alargadas. Ese alargamiento de las crestas con hiperplasia melanocítica basal es similar a la que se observa en el lentigo simple y por eso llamamos lentiginosa a esta imagen histológica.
-- Displasia epitelioide. Nidos bastante bien definidos de células grandes con abundante citoplasma pálido con melanina pulverulenta. Los nidos tendían a la confluencia y a la extensión lateral, con una disposición horizontal, uniendo lateralmente crestas adyacentes.
Aunque esta citología se asemeja a la clásica del melanoma de extensión superficial, no había diseminación intraepidérmica de células pagetoides y las mitosis eran infrecuentes.
En todas las lesiones displásicas había un componente névico intradérmico. Las células névicas dérmicas eran de los tipos o epitelioide o pequeño, y la mayoría de las lesiones sólo mostraban ligera evidencia de neurotización (maduración).
Caracteres histológicos de los nevos displásicos (sacados de la tabla 3 del artículo)
-- Características comunes: hipercromatismo y pleomorfismo nuclear; respuesta inflamatoria linfocitaria con fibroplasia.
-- Displasia de células epitelioides: células epitelioides con pigmento pulverulento. Los nucleo-los pueden ser prominentes. Fusión lateral y pleomorfismo de los nidos. Pequeñas células névicas hipercromáticas en la dermis papilar.
-- Displasia melanocítica lentiginosa: prominente artefacto de retracción citoplasmático; crecimiento melanocítico basal (no en nidos) irregular. Frecuentemente juntural (no componente dérmico).
Comentario
A los 2 años de describir el lunar B-K, Elder et al, entre éstos Green y Clark, coautores del primer artículo1, comunicaron que en algunos pacientes con melanoma no familiar podían verse lunares similares a aquéllos2. Al estudiarlos histológicamente encontraron que, además de la displasia descrita en el lunar B-K, había otro patrón al que llamaron displasia lentiginosa, mientras que el anterior era denominado displasia epitelioide.
Este segundo patrón, el lentiginoso, no sólo es más frecuente que el epitelioide, sino que está presente en todas las lesiones displásicas. Es decir, que la displasia epitelioide estar á siempre mezclada con la lentiginosa.
La displasia lentiginosa se caracteriza por:
-- Crestas epidérmicas alargadas (como el lentigo simple, de ahí el nombre de displasia lentiginosa).
-- En los márgenes (periferia) de estas crestas hay una proliferación basal, irregularmente orientada, de melanocitos.
-- Entre unos pocos y muchos de estos melanocitos muestran hipercromatismo y pleomorfismo nuclear y prominente retracción de sus citoplasmas.
-- Aunque los melanocitos basales están habitualmente aislados, pueden formar nidos pequeños, pero nunca «las clásicas tecas aisladas del nevo juntural».
Resulta difícil comprender cómo unos melanocitos hiperplásicos (es decir, abundantes, casi codo con codo) pueden disponerse «irregularmente orientados» a lo largo de la capa basal, que, por definición, tiene una sola capa de células.
La displasia epitelioide es similar a la descrita en el lunar B-K1.
En cuanto al componente intradérmico, en este artículo no queda tan claro como en el anterior1 que el nevo displásico es (salvo excepciones) un nevo compuesto. Ni en la descripción en el texto de la displasia lentiginosa ni en la parte correspondiente de la tabla 3 del artículo se habla de ello. Sí se habla del componente intradérmico en la displasia epitelioide donde se dice que «en todas las lesiones displásicas había un componente névico intradérmico» y que había «pequeñas células névicas hipercromáticas en la dermis papilar» (tabla 3 del trabajo de Elder et al2). En el texto se dice que las células névicas intradérmicas eran o epitelioides (o de tipo A y, por tanto, de núcleos no hipercromáticos) o pequeñas (o de tipo B y, por tanto, linfocitoides o de núcleos hipercromáticos).
Pero, sobre todo, no se explica en ningún momento cuál era la relación entre ese componente intradérmico y la displasia melanocítica del componente epidérmico del nevo.
Si pretendemos resumir estos dos primeros artículos del grupo de Clark1, 2, en los que se describe la histopatología del nevo melanocítico displásico tendremos que se trata de un nevo melanocítico compuesto cuyo componente epidérmico o es una proliferación melanocítica lentiginosa en la que de algunos a muchos de esos melanocitos están irregularmente orientados y tienen núcleos hipercromáticos y pleomórficos y citoplasmas retraídos, o muestra, además de lo anterior, nidos junturales horizontales de melanocitos con amplio citoplasma pálido con melanina pulverulenta; también estos melanocitos pueden mostrar (pocos o muchos de ellos) hipercromatismo y pleomorfismo nuclear. En todos los casos hay en la dermis superficial reacción inflamatoria linfocitaria y fibroplasia.
El más viejo de entre nosotros cuando leyó este segundo artículo tampoco pudo hacerse una idea coherente de cuál era la histopatología del nevo displásico.
El libro de Maize y Ackerman3
Clasificación
Lesiones pigmentadas de la piel
1. Hiperpigmentación circunscrita sin aparente pro- liferación de melanocitos:
-- Efélide.
-- Mancha café con leche.
-- Máculas melanóticas del síndrome de Albright.
-- Nevo de Becker.
-- Hiperpigmentaciones postinflamatorias localizadas.
-- Cloasma.
-- Urticaria pigmentosa.
-- Amiloidosis maculosa.
-- Lentigo solar.
-- Acantoma de células grandes.
-- Queratosis liquenoide.
-- Queratosis seborreica reticulada.
-- Anomalía pigmentaria reticular de las flexuras.
2. Proliferaciones benignas de melanocitos:
-- Lentigo simple.
-- Nevo juntural.
-- Nevo compuesto.
-- Nevo intradérmico.
-- Nevo de células en balón.
-- Nevos melanocíticos congénitos.
-- Mancha mongólica.
-- Nevo de Ota y Nevo de Ito.
-- Nevo azul.
-- Nevo combinado.
-- Melanopatía diseminada con melanocitos gigantes.
3. Melanoma maligno.
4. Simuladores histopatológicos de melanoma ma-ligno:
-- Nevos melanocíticos recurrentes tras extirpación incompleta.
-- Nevo de Spitz.
-- Nevo con halo.
-- Nevo congénito del recién nacido.
-- Nevos melanocíticos de los genitales, especialmente en jóvenes.
-- El nevo displásico y el síndrome del nevo displásico.
5. Simuladores clínicos no melanocíticos de proliferaciones de melanocitos.
(Una larga serie de neoplasias no melanocíticas pigmentadas.)
La histopatología del nevo displásico según Maize y Ackerman
La presentación más frecuente de un nevo displásico es la de un nevo melanocítico compuesto.
El requisito crucial para el diagnóstico de un nevo displásico de tipo compuesto es que el componente intraepidérmico del nevo se extienda más allá del componente intradérmico, es decir, que en los «hombros» de la lesión haya un nevo juntural de anchura variable (desde menos de 1 mm a varios mm).
Los melanocitos tienen núcleos ovalados, pequeños, no atípicos, y citoplasma abundante, pálido, con melanina pulverulenta.
Se agrupan en nidos de diferente tamaño y forma y no son equidistantes, sino que se disponen al azar, unos agrupados, otros alejados, unos pequeños, otros mayores, y algunos alineados horizontalmente, otros verticalmente, algunos en las bases de la finas crestas alargadas, otros en las zonas suprapapilares y otros en las caras laterales de las crestas.
Melanocitos solitarios similares se ven entre los nidos.
Virtualmente todos los melanocitos (solitarios o en nidos) se sitúan en la unión dermoepidérmica.
En la dermis, especialmente en los «hombros», puede haber:
-- Fibroplasia laminar.
-- Fibroplasia concéntrica.
-- Infiltrados linfocitarios de densidad variable.
-- Melanófagos.
-- Telangiectasias.
Estos cinco hallazgos son inespecíficos.
El sine qua non del nevo displásico compuesto es la extensión de los nidos de melanocitos y de los melanocitos aislados a la epidermis de los «hombros».
Un nevo displásico puede ser totalmente juntural, en cuyo caso es similar al hombro de un nevo displásico compuesto.
Algunos nevos displásicos pueden tener unos pocos núcleos atípicos dentro de la porción epidérmica, incluso dérmica, de la lesión e infrecuentemente la mayoría de los melanocitos y células névicas pueden tener núcleos atípicos. Tales nevos displásicos con muchos núcleos atípicos se diferencian del melanoma por los criterios usuales, esencialmente por los criterios arquitecturales más que por los citológicos.
Comentarios
A la clasificación
Aunque a la vista de las clasificaciones que se irán sucediendo en esta revisión hayamos tenido la tentación de hacer largos y prolijos comentarios sobre las mismas y sobre lo adecuado o inadecuado de incluir tal o cual entidad en éste o en aquel grupo, resistiremos la tentación por no salirnos del objetivo único de esta, ya de por sí larga, revisión: el nevo displásico.
Maize y Ackerman lo incluyen en el apartado de simuladores histopatológicos de melanomas malignos, junto al nevo persistente, al nevo de Spitz, etc., todos ellos nevos melanocíticos en los que diversas circunstancias de edad, localización o de evolución natural o artificial les confieren caracteres histológicos fuera de lo habitual o común que pueden llevarnos a confundirlos con melanomas.
Sin embargo, tras la descripción histopatológica del nevo displásico, Maize y Ackerman llegan a la conclusión de que se trata de una de las formas más frecuentes de nevo melanocítico: «En nuestra experiencia, la mayor parte de los nevos melanocíticos de tipo compuesto ligeramente cupuliformes, confinados a la epidermis y a la dermis papilar, son nevos displásicos».
Y terminan diciendo: «En conclusión, Clark et al han llamado la atención sobre uno de los muchos tipos de nevos melanocíticos, concretamente los nevos displásicos. Esos peculiares nevos melanocíticos pueden ser generalmente reconocidos clínica e histológicamente mediante criterios repetibles y fidedignos. Clínicamente tienden a ser grandes cuando se han desarrollado plenamente, y tienden a ser elevados en su zona central, más oscura, y más claros en su porción periférica, más plana y de límites mal definidos. Algunas veces las lesiones muestran diversos tonos abigarrados de marrón, en cuyo caso suelen diagnosticarse de melanomas. Histológicamente los tipos compuestos de nevo displásico se caracterizan por la extensión del componente intraepidérmico del nevo, en los «hombros», más allá del componente intradérmico del mismo. Algunos melanomas se desarrollan en nevos displásicos, pero la mayor parte de los melanomas aparecen de novo. Los nevos displásicos son sumamente frecuentes y totalmente benignos. Los pacientes con muchos nevos displásicos y con historia personal o familiar de melanoma parecen tener un mayor riesgo de desarrollar melanomas y, por tanto, deben ser controlados cuidadosamente con el fin de descubrir una posible evolución a melanoma cuando éste es aún pequeño, plano y curable.»
Es decir, que una vez conocidas sus características histopatológicas, los nevos llamados displásicos resultan ser frecuentísimos y fácilmente reconocibles.
A la histopatología
Cuando el más viejo de nosotros leyó el capítulo sobre nevo displásico del libro de Maize y Ackerman3 notó que se hacía la claridad en la parte de su cerebro que llevaba 9 años intentando descifrar lo que era el nevo displásico. Por eso desde entonces, tanto en público como en privado, viene diciendo que, aunque el nevo displásico fue inicialmente descrito por Clark et al1 y por Elder et al2, fueron Maize y Ackerman3 los primeros que hicieron una descripción comprensible del mismo. Tanto es así que a partir de entonces en todas las descripciones del nevo displásico, como iremos viendo, se incorpora el concepto de «hombro» (shoulder) de Maize y Ackerman3.
Maize y Ackerman describieron el nevo displásico como un nevo melanocítico compuesto cuyo componente intraepidérmico se extiende más allá (alrededor) del componente intradérmico. En esos «hombros» los melanocitos se disponen bien de forma aislada bien en nidos; estos últimos son de forma y tamaño variables, no equidistantes, unos horizontales y otros verticales, y se sitúan en cualquier parte del límite dermoepidérmico. Están formados por melanocitos de núcleo pequeño, ovalado, no atípico, y citoplasma abundante, pálido, con melanina pulverulenta. En la dermis superficial subyacente puede haber fibroplastia, inflamación linfohistiocitaria y telangiectasias; estas alteraciones dérmicas son, en todo caso, hallazgos inespecíficos3
Cuando vemos un nevo melanocítico juntural con las caracteríticas descritas en el hombro del nevo melanocítico compuesto se trata de un nevo displásico juntural3 (lo que Clark et al llamaron lunar B-K de novo1).
Según Maize y Ackerman un nevo displásico puede tener además de todo lo anterior una cantidad mayor o menor de núcleos atípicos. Estos casos se diferenciarían de un melanoma por sus características estructurales, no por las citológicas3.
Maize y Ackerman3 sólo hablan de lo que Elder et al llamaron displasia epitelioide, pero nunca de algo parecido a lo que estos últimos autores llamaron displasia lentiginosa, que, según ellos, era la más frecuentemente vista en el nevo displásico, hasta considerarla obligatoria2.
Las ideas de Clark y Elder, 12 años después4
Clasificación
En esta primera edición del libro de Farmer y Hood los tumores melanocíticos se tratan en dos capítulos sucesivos: el primero, por Imber y Mihm, se titula «Tumores melanocíticos benignos»12, y el segundo, por Clark, Elder y Guerry, «Nevo displásico y melanoma maligno»4, por lo que la siguiente clasificación está sacada del conjunto de ambos capítulos.
Tumores melanocíticos benignos:
-- Nevos melanocíticos adquiridos.
-- Nevos melanocíticos congénitos.
-- Nevo de células fusiformes y epitelioides (nevo de Spitz).
-- Nevo pigmentado de células fusiformes.
-- Melanocitosis dérmicas.
-- Lesiones nevomelanocíticas misceláneas:
* Lentigo simple.
* Lentigo solar.
* Melanoacantoma.
* Mancha café con leche.
El nevo displásico: crecimiento disregulado.
Melanoma.
Formas raras e infrecuentes de melanoma.
El nevo displásico: crecimiento disregulado
Tanto este título como todos los párrafos que lo siguen son traducción literal del capítulo de Clark, Elder y Guerry dysplastic nevi and malignant melanoma en el libro de Farmer & Hood4.
«La marca de fábrica de un nevo displásico es el desarrollo de un nuevo período de proliferación celular inapropiada, caracterizada por el desarrollo de asimetría de la forma.»
«Es dentro de esta zona de proliferación celular asimétrica donde aparecen algunos melanocitos atípicos. Cuando aparecen aplicamos el término de displasia melanocítica. No disponemos de métodos para hacer decisiones precisas acerca de la presencia o ausencia de un síndrome del nevo displásico ni para dividir el síndrome en varios subgrupos.»
«Hasta que haya pruebas que suplementen las observaciones clínicas e histológicas es probable que la confusión rodee la naturaleza del nevo displásico y del síndrome del nevo displásico.»
«Hasta que esos estudios se hayan realizado debemos confiar en la histología y el empleo acrítico del término "síndrome del nevo displásico" debe evitarse.»
Lesión histológica
«El patrón histológico de displasia melanocítica más característico y más frecuentemente encontrado se ve en la periferia de un nevo melanocítico (juntural, compuesto o intradérmico) que no es en sí mismo displásico.»
«Las alteraciones se ven habitualmente en una zona limitada de la periferia, un hombro ectópico de displasia.»
«Esta combinación de hechos, restos de un nevo banal con áreas periféricas de displasia, sugiere que la lesión no era en su inicio displásica.»
«Otras lesiones, vistas con menor frecuencia, pueden mostrar la histología de la displasia, que ahora describimos, sólo en la epidermis o como displasia dermoepidérmica, sin evidencia de un nevo ordinario precursor. Esto podría ser una displasia desde el comienzo.»
«Puede simular el momento más inicial de una neoplasia melanocítica mostrando una proliferación melanocítica basilar similar a la de un lentigo. Así se puede ver un nevo juntural, compuesto o intradérmico con un área de proliferación melanocítica basilar extendiéndose a partir de una zona limitada de su margen... También se puede ver una forma más profusa de crecimiento melanocítico en la región basilar, asociada con la elongación de las crestas. Aquí la capa basal está formada por melanocitos, no por queratinocitos. Esos melanocitos son mayores que los normales y pueden mostrar un curioso puenting* entre crestas próximas. Con menor frecuencia, el crecimiento melanocítico puede manifestarse por un incremento de melanocitos epitelioides, grandes, aislados o en pequeños nidos. Estos dos patrones defectuosos de crecimiento melanocítico pueden presentarse de forma aislada o mezclados entre sí.»
* Nos hemos tomado la libertad de traducir bridging por «puenting», un deporte de moda.
«La atipia citológica de un nevo displásico es, en nuestra opinión, relativamente ligera. Raramente se ve una atipia marcada o llamativa y las mitosis son muy infrecuentes. Cuando se hallan los hechos anteriores debe pensarse seriamente en melanoma y debe hacerse una cuidadosa evaluación del tamaño, del patrón de crecimiento y de las respuestas epitelial y linfocítica de la lesión.»
Requerimientos para el diagnóstico histológico de nevo displásico
«Hemos insistido en que el diagnóstico histológico de displasia melanocítica del tipo visto en el síndrome del nevo displásico incluye un patrón anormal de crecimiento melanocítico y atipia nuclear melanocítica. Otros hallazgos histológicos se ven habitualmente en el nevo displásico, pero el patrón de crecimiento anormal y la atipia nuclear de los melanocitos son imperativas.
Comentarios
A la clasificación
Al titularse el capítulo de Imber y Mihm «Tumores melanocíticos benignos»12 y no incluirse en el mismo el nevo displásico nos hace pensar que los autores no lo consideran una lesión benigna, pese a lo cual lo siguen llamando nevo, término equivalente a tumor melanocítico benigno. Tampoco Clark et al lo incluyen entre los melanomas, luego no es maligno. ¿Cuál es entonces la naturaleza pronóstica de una lesión llamada nevo (benigna) y displásico (premaligna)?
A la histopatología
El primer párrafo de los transcritos es, en nuestra opinión, incomprensible. De la lectura de párrafos posteriores parece deducirse que se están refiriendo a los «hombros» como «período de proliferación celular inapropiada». Más difícil es entender lo de «asimetría de la forma», ya que, muy frecuentemente, los nevos displásicos son simétricos al tener ambos «hombros» longitudes aproximadas.
Las afirmaciones de los párrafos 3, 4 y 5 son realmente deprimentes; en un momento en que las revistas y reuniones de dermatopatología de todo el mundo bullen con artículos y comunicaciones sobre el nevo displásico y el síndrome del nevo displásico (el artículo Clark et al de 19781 es el quinto más citado de toda la bibliografía dermatológica mundial13), los «padres de la criatura» confiesan no saber qué fue lo que concibieron. Sin embargo, parece como si al dejar el síndrome y centrarse sólo en la histopatología del nevo displásico los autores abandonasen el pesimismo. Parece que el «hombro» los reconforta, pues dicen que es ahí donde se encuentra «el patrón histológico de displasia melanocítica más característico». De todas maneras resulta difícil imaginar el hombro de un nevo displásico juntural.
Tras describir las dos formas de displasia melanocítica, lentiginosa y epitelioide, concluyen que se trata de dos «patrones defectuosos» de crecimiento melanocítico. Imber y Mihm se expresan de forma similar en su capítulo: «Dicho de manera sencilla, una proliferación melanocítica juntural emigra sincrónicamente a través de la unión dermoepidérmica y establece un componente dérmico de dimensión lateral igual a la del componente epidérmico original. La presencia del llamado hombro de hiperplasia melanocítica juntural, lateral a la masa central de una lesión compuesta por lo demás benigna, refleja un desarrollo aberrante. Tal asimetría histológica aparente puede reflejar bien una emigración asincrónica de la población melanocítica juntural a la dermis papilar, bien la reanudación de una proliferación melanocítica juntural en lo que ha-bía sido hasta entonces una lesión de evolución normal12».
En primer lugar, sólo los ejércitos en formación emigran sincrónicamente. Casi todos los nevos melanocíticos tienen la superficie más o menos convexa porque la porción central es la más antigua y, por tanto, en los nevos compuestos es la que tiene mayor componente intradérmico, mientras que en los extremos a menudo terminan en un nido juntural. ¿Por qué es «aberrante» o defectuosa la presencia del halo periférico? Eso es lo que caracteriza al nevo moteado (nevus spilus) y se encuentra en muchos nevos congénitos. En este tema los autores han partido de un axioma no demostrado.
En cuanto a la atipia citológica del nevo displásico, si en el párrafo segundo decían los autores que en la zona «asimétrica» había «algún melanocito atípico», más adelante dicen que «la atipia citológica del nevo displásico es... relativamente ligera. Raramente se ve una atipia marcada...»
Finalmente, los autores recalcan que sólo «el patrón de crecimiento anormal (suponemos que se refieren al «hombro») y la atipia nuclear de los melanocitos son imperativas», dando a entender que todo lo demás, incluidas las alteraciones dérmicas, no lo son. De todas formas dicen los autores que en los «hombros» aparece «algún melanocito atípico» y que esta atipia es «relativamente ligera»; raramente es «marcada o llamativa».
Podemos concluir, por tanto, que para Clark et al el mínimo común denominador de nevo displásico es un nevo melanocítico con «hombros» en los que hay algunos melanocitos ligeramente atípicos. A ello se pueden añadir otros cambios «no imperativos».
El libro de McKee5
Clasificación
Enumeración de los epígrafes del capítulo 13 del libro de McKee titulado Melanocytic nevi and malignant melanoma:
-- Efélides.
-- Lentigo simple.
-- Lentigo senil.
-- Nevo de Becker.
-- Hipomelanosis idiopática en gotas.
-- Nevos melanocíticos.
-- Nevo penetrante profundo.
-- Nevo recurrente.
-- Nevo congénito.
-- Nevo de Spitz y variantes.
-- Nevo de Reed.
-- Nevo con halo.
-- Nevo de Meyerson.
-- Nevo displásico.
-- Melanocitosis dérmicas.
-- Melanoma maligno.
La descripción histopatológica5
El nevo displásico, bien sea familiar o esporádico, muestra los mismos caracteres histológicos.
Se considera generalmente que los nevos displásicos muestran cambios proliferativos, tanto epidérmicos como melanocíticos, y estos últimos son displasias que no llegan a ser la de un melanoma in situ.
Pueden ser junturales o compuestos.
En los compuestos, el componente epidérmico se extiende frecuentemente más allá del borde lateral de las células névicas dérmicas. Esto se denomina, a veces, el fenómeno del hombro.
El nevo displásico se caracteriza por hiperplasia melanocítica lentiginosa.
La epidermis, generalmente de grosor normal, aunque a veces puede ser ligeramente acantósica, muestra una marcada elongación lentiginosa de las crestas.
Los melanocitos displásicos se caracterizan por:
-- Tamaño nuclear aumentado.
-- Irregular membrana nuclear.
-- Nucleolos prominentes.
-- Pleomorfismo nuclear y citoplásmico.
-- Hipercromatismo variable.
Se distribuyen al azar en la capa basal.
Células epitelioides, con núcleos vesiculosos, nucleo-los prominentes y melanina pulverulenta pueden ser evidentes.
Los melanocitos pueden estar aislados o en nidos.
Los melanocitos muestran un artefacto de fijación característico.
En cada nevo hay, característicamente, una mezcla de melanocitos normales o displásicos.
Sus nidos son irregulares, en forma y en distribución y no están confinados a los vértices de las crestas, como suele ocurrir en los nevos adquiridos comunes.
Se ve frecuentemente fusión de nidos adyacentes. Mitosis infrecuentes.
La dermis papilar muestra a menudo:
-- Respuesta eosinófila periepidérmica.
-- Respuesta fibroblástica laminar.
-- Linfocitos y melanófagos en parches.
-- Acentuación de la vascularización.
El componente dérmico (parece que se refiere a la zona central donde el nevo es de tipo intradérmico o compuesto) si está presente está formado por melanocitos pequeños pigmentados que pueden ser ligeramente atípicos (variabilidad de tamaño y forma del núcleo e hipercromatismo focal). A veces no maduran en profundidad.
Comentarios
A la clasificación
De la estructura del capítulo no puede deducirse ninguna clasificación, ya que el autor usa el mismo tipo de letra para enunciar las 16 entidades entre las que no establece ningún orden ni jerarquía. Lo único que tal vez cabría deducir del orden en que aparece cada entidad es que el nevo diplásico está muy alejado de los «nevos melanocíticos», con entidades interpuestas como el nevo congénito y el nevo de Spitz que parecen romper cualquier tipo de relación expositiva entre ellas. Por otro lado, el nevo displásico está cerca del melanoma maligno, pero parece una proximidad engañosa, ya que se interpone entre ambos algo tan escasamente relacionado con ellos como las melanocitosis dérmicas. Podemos concluir, por tanto, que de la estructura del capítulo no puede deducirse ninguna idea del autor acerca de las relaciones entre las distintas variedades de proliferaciones melanocíticas. Más cuando incluye en un capítulo titulado Melanocytic nevi and malignant melanoma las efélides, el lentigo senil, el nevo de Becker y la hipomelanosis idiopática en gotas que no tienen nada que ver ni con los nevos melanocíticos ni con los melanomas.
A la histopatología
«La epidermis, generalmente de grosor normal, aunque a veces puede ser ligeramente acantósica, muestra una marcada elongación lentiginosa de las crestas». (Las crestas son parte de la epidermis, por tanto una epidermis con «marcada elongación de las crestas» es una epidermis marcadamente acantósica y no «de grosor normal».
Los melanocitos displásicos «se distribuyen al azar en la capa basal» y muestran «pleomorfismo nuclear y citoplásmico» (el concepto de pleomorfismo como criterio de la malignidad nunca puede ser citoplásmico, ya que el comportamiento maligno de una célula depende de su núcleo [su ADN] no de su citoplasma).
El autor no aclara si la hiperplasia melanocítica lentiginosa se produce en todo el nevo compuesto o sólo en los hombros.
Si las «células epitelioides... pueden ser evidentes» cabe deducir que predomina otro tipo celular, pero no explica cuál es. Únicamente aclara que «hay, característicamente, una mezcla de melanocitos normales o displásicos» (¿debemos entender que todos los displásicos tienen carácter epitelioide?).
Los nidos son irregulares en forma y en distribución, se fusionan con frecuencia y «no están confinados a los vértices de las crestas».
En dermis hay, a menudo, «respuesta eosinófila periepidérmica» (es difícil imaginar una «respuesta» que rodee la epidermis), respuesta fibroblástica laminar, inflamación y neovascularización.
La parte intradérmica del nevo compuesto es algo atípica también.
La descripción histopatológica de McKee es, en nuestra opinión, cualquier cosa menos clara. Por poner un ejemplo, cuando parece que va a explicarnos cómo es la displasia melanocítica lentiginosa comienza diciendo que la epidermis es generalmente de grosor normal, y dentro de la descripción de la citología mezcla, sin ninguna explicación, lo que parecen caracteres de la displasia llamada lentiginosa con la llamada displasia epitelioide.
El libro de Weedon6
Clasificación
Lentigos, nevos y melanomas
1. Lesiones con proliferación melanocítica basal:
-- Lentigo simple.
-- Mancha melánica labial.
-- Lentigo solar.
-- Nevo lentiginoso.
-- Nevo moteado.
-- Lentigo del PUVA.
2. Nevos melanocíticos:
-- Nevo juntural.
-- Nevo compuesto.
-- Nevo intradérmico.
-- Nevo de Meyerson.
-- Nevo penetrante profundo.
-- Nevo con células en balón.
-- Nevo con halo.
-- Nevo en escarapela.
-- Nevo centrado por el conducto ecrino.
-- Nevo recurrente.
-- Nevo de Spitz.
-- Nevo fusocelular pigmentado.
-- Nevo congénito.
3. Lesiones melanocíticas dérmicas.
4. Lesiones melanocíticas atípicas:
-- Nevo displásico (atípico)
-- Nevo displásico lentiginoso de los viejos.
5. Lesiones melanocíticas malignas.
Descripción histopatológica
1. Hiperplasia lentiginosa intraepidérmica:
-- Proliferación de melanocitos aislados (también en nidos) a lo largo de la capa basal.
-- Los nidos, igual en los lados que en los extremos de las crestas. También hay nidos «puente».
-- Distribución irregular del componente juntural (desorden de los nidos junturales).
-- Células comúnmente con artefacto de retracción con escaso citoplasma y patrón fusiforme.
-- En algunas lesiones, células cuboideas (epitelioides) con pigmento pulverulento.
2. Atipia citológica ocasional:
-- Presencia ocasional de células con núcleos hipercromáticos agrandados, algunas veces con nucleolos prominentes.
-- Los núcleos son iguales o mayores que los de los queranocitos suprayacentes.
-- La atipia va de ligera a marcada (no hay un consenso universal).
-- También se ve atipia en nevos no displásicos.
3. Respuesta del estroma:
-- Fibroplasia laminar y concéntrica.
-- Infiltrado linfocitario superficial en parches.
-- Neoformación vascular, a veces.
Los nevos displásicos son generalmente nevos compuestos con actividad juntural y lentiginosa periférica y atipia citológica ocasional en el componente epidérmico.
Ackerman y otros ponen el énfasis en la arquitectura más que en la citología para definir el nevo displásico (atípico). Ellos hacen hincapié en la importancia del «fenómeno del hombro» para hacer el diagnóstico.
Comentarios
A la clasificación
Parece que el autor divide las proliferaciones melanocíticas en benignas, atípicas y malignas. En tal caso, el nevo displásico es una proliferación ni benigna ni maligna, atípica, y además la coloca junto a los melanomas. El problema está en que si el nevo displásico es atípico ello se debe a que todas las demás lesiones melanocíticas enumeradas más arriba eran típicas, pero es una lista tan variopinta que más bien parecen ellas las atípicas.
A la histopatología
Los nevos displásicos son generalmente nevos compuestos con periferia juntural y lentiginosa, con atipia citológica ocasional.
Los melanocitos aislados o en nidos están todos en la capa basal. Los nidos en cualquier parte de las crestas se disponen desordenadamente y forman puentes.
La citología predominante es fusiforme, con escaso citoplasma y artefacto de retracción (¿retracción del núcleo o del citoplasma?). Sólo a veces hay células «epitelioides».
La atipia citológica es ocasional y puede ser entre ligera y marcada. También se ve atipia citológica ocasional en los nevos no displásicos.
En el estroma hay fibroplasia, inflamación y a veces neoangiogénesis.
Tras leer a Weedon nos preguntamos: si en el nevo displásico la atipia citológica es ocasional, también tiene atipia citológica, menos ocasional, el nevo penetrante profundo y el nevo de Spitz. Suponemos que lo que hace atípico al nevo displásico en su arquitectura, los «hombros» y la irregularidad de sus nidos. Pues el carácter lentiginoso, admitido en el lentigo simple de donde ha tomado el nombre, también se ve en el frecuente nevo lentiginoso que el autor ha colocado tan lejos del melanoma. Por otro lado, todos los nevos moteados y muchos nevos congénitos tienen «hombros». Entonces nos quedamos sólo con la forma, tamaño y distribución de los nidos junturales como lo único que caracteriza al nevo displásico, pues las alteraciones dérmicas, como luego veremos, son frecuentes en los nevos junturales.
De nuevo Elder, 19 años después7
Clasificación
Lesiones pigmentadas benignas y melanoma maligno
1. Melanocitosis dérmicas.
2. Nevo azul.
3. Efélide. Mácula melanótica.
4. Lentigos.
5. Nevos melanocíticos:
-- Comunes*.
-- Con células en balón.
-- Acro.
-- Genital.
-- De Spitz.
-- Fusocelular pigmentado.
-- Congénito.
-- Penetrante profundo.
-- Displásico.
-- Con halo.
6. Melanoma maligno.
Descripción histopatológica
Nevo con desorden arquitectural y atipia melanocítica
1. Desorden arquitectural:
-- Proliferación lentiginosa de células névicas:
* Crestas alargadas.
* Aumento del número de melanocitos.
* Nidos horizontales que forman «puentes».
-- Juntural:
Melanocitos frecuentemente fusiformes, pero pueden ser grandes y epitelioides con abundante citoplasma con melanina pulverulenta.
-- Compuesto (pápula central de nevo «común» y hombros junturales).
-- Infiltrado inflamatorio ligero a moderado en zona juntural.
-- No melanocitos suprabasales.
2. Atipia melanocítica:
-- Para hacer el diagnóstico se requiere encontrar atipia nuclear (núcleos grandes, irregulares e hipecromáticos) en algunos melanocitos.
-- La atipia afecta únicamente a una minoría de las células de la lesión (random** cytologic atypia).
-- Hay lesiones límite entre nevo displásico y melanoma incipiente.
* Common: común, vulgar, corriente, ordinario.
** Random: ocasional, impensado, fortuito.
Comentarios
A la clasificación
Clasifican las proliferaciones melanocíticas en dos grupos: lesiones pigmentadas benignas y melanomas malignos (lesiones pigmentadas benignas es un mal término, pues debería incluir la queratosis seborreica, el acantoma de células grandes y todas las proliferaciones anexiales pigmentadas, además de los histiocitomas).
Dividen las «lesiones benignas» en cinco grupos; el último está formado por los nevos melanocíticos, cuyas variantes son enumeradas y ordenadas de forma bastante anárquica. No parece lógico tratar en nivel de igualdad al nevo con células en balón una rarísima anomalía citológica de algún nevo melanocítico congénito o adquirido, con el nevo de Spitz y sobre todo con el nevo congénito, infinitamente más frecuente e importante. Por tanto, no podemos concluir nada acerca de la situación asignada al nevo displásico.
Únicamente parece claro que es considerado como una variedad de nevo melanocítico e incluido, por tanto, dentro de las lesiones benignas pigmentadas. Esto contrasta con el capítulo del Farmer & Hood4 en el que Elder, junto con Clark, incluía el nevo displásico en el capítulo del melanoma. En la discusión volveremos sobre este capítulo en el que Elder parece desmarcarse de sus primeras ideas sobre el carácter premaligno del nevo displásico.
A la histopatología
Los autores parten de la definición de la Conferencia de Consenso de 1992: «Nevo con desorden arquitectural y atipia melanocítica»14 ¿Qué es desorden arquitectural? Al parecer eso significa que:
-- Las crestas son alargadas.
-- Los nidos son horizontales.
-- Hay «hombros».
-- Hay reacción inflamatoria.
Pues éstos son los únicos datos arquitecturales de que hablan en su exposición. Y nos preguntamos: ¿es un desorden el que un nevo melanocítico tenga hombros, nidos horizontales, crestas alargadas y reacción inflamatoria?
Los melanocitos son a menudo fusiformes y, con menor frecuencia, epitelioides.
Para diagnosticar nevo displásico tiene que haber atipia nuclear de algunos melanocitos. Esta atipia es ocasional, inesperada o fortuita. En esto, Elder no ha cambiado su criterio de 1990.
Podemos resumir diciendo que Elder y Elenitsas consideran al nevo displásico como un peculiar nevo melanocítico (benigno) con alguna atipia nuclear ocasional. Si una vez extirpado se plantease alguna duda de si se trata de una lesión límite entre nevo displásico y melanoma incipiente, ello no tendría ninguna consecuencia práctica, pues la les ión ha sido completamente extirpada.
Libro de Barnhill8
Clasificación
Tumores de melanocitos
1. Lesiones pigmentadas circunscritas formadas por melanocitos basilares:
-- Lentigo solar.
2. Léntigos y nevos melanocíticos adquiridos:
-- Lentigo simple.
-- Máculas melanóticas y lentigos mucocutáneos.
-- Nevos melanocíticos adquiridos comunes:
Variantes de los nevos melanocíticos:
* NM de la piel acra.
* N con células en balón.
* N con halo.
* N juntural lentiginoso y nevo celular lentiginoso.
* N neural.
* N moteado (nevus spilus).
* NM recurrente.
* NM atípico de la región genital.
3. Nevo de Spitz y sus variantes.
4. Tumor fusocelular pigmentado.
5. Tumor fusocelular pigmentado con desorden arquitectural y atipia citológica.
6. Melanocitosis dérmicas, nevos azules y afecciones relacionadas.
7. Nevos melanocíticos con heterogeneidad fenotípica.
-- N combinado.
-- N invertido tipo A y nevo melanocítico con componente focal atípico de células epitelioides.
-- N penetrante profundo.
-- N fusocelular plexiforme.
8. Proliferaciones melanocíticas con desorden arquitectural y atipia citolótica (displasia melanocítica y nevo displásico).
9. Melanoma maligno.
Descripción histopatológica
El 80% son compuestos (la mayoría de ellos relativamente planos).
El 20% son junturales.
Muchos son lentiginosos:
-- Crestas epidérmicas alargadas.
-- A menudo en maza.
-- Con hiperplasia melanocítica.
-- Con hiperpigmentación epidérmica.
La gran mayoría de los nevos displásicos compuestos tienen:
-- Extensión lateral.
-- Mala delimitación del componente epidérmico.
-- Disminuye la celularidad intraepidérmica gradualmente, sin una clara demarcación.
Caracteres arquitecturales:
-- Proliferación melanocítica lentiginosa*.
-- Variación de tamaño, forma y localización de los nidos junturales con puenting y confluencia*.
-- No hay nidos en los extremos de las crestas.
-- Dishesión de los nidos junturales.
-- Extensión lateral (fenómeno del hombro) del componente juntural.
* Caracteres imprescindibles para el diagnóstico.
Caracteres citológicos:
-- Patrón fusocelular (con importante artefacto de retracción del citoplasma).
-- Patrón epitelioide.
-- Atipia nuclear discontinua*:
* Núcleos grandes, pleomórficos, hipercromáticos, con nucleolos prominentes.
* Nucleolos prominentes.
-- Citoplasma prominente, pálido y pulverulento.
-- Gránulos gruesos de melanina.
Respuesta del huésped:
-- Infiltrado linfocitario.
-- Fibroplasia:
* Patrón eosinofílico concéntrico.
* Patrón laminar.
-- Vascularización prominente.
* Caracteres imprescindibles para el diagnóstico.
Comentarios
A la clasificación
Se trata de una peculiar clasificación que merecería un largo comentario fuera del ámbito de esta revisión.
Para Barnhill el nevo displásico no es una variante de nevo melanocítico, sino que parece ser una lesión benigna (la llama nevo), pero por su situación en la clasificación parece ser la que está más cerca del melanoma.
A la histopatología
Es el único autor que da cifras de la frecuencia del nevo displásico juntural (20%) y compuesto (80%). Añade que el componente dérmico del segundo es relativamente plano.
El nevo displásico lentiginoso tiene crestas alargadas, a menudo en maza, y hay hiperpigmentación epidérmica.
Los hombros del nevo displásico compuesto están mal delimitados y disminuyen gradualmente (todos los nevos junturales disminuyen gradualmente).
Criterios mayores (imprescindibles):
-- Proliferación melanocítica lentiginosa.
-- Variación en forma, tamaño y localización de los nidos (con «puenting» y confluencia).
-- Atipia nuclear «discontinua».
En los caracteres citológicos coexisten un patrón fusocelular con retracción del citoplasma y un patrón epitelioide (sin que nos diga cuál de ellos predomina, ni si coexisten, o se hallan por separado en algunos casos (¿cuántos?).
Los demás caracteres estructurales (situación de los nidos en las crestas, hombros, patrón celular [lentiginoso o epitelioide] y la respuesta dérmica) son opcionales, no imprescindibles para el diagnóstico.
Con todo lo anterior resulta difícil hacerse una idea de cómo es un nevo displásico; ¿un nevo melanocítico con epidermis lentiginosa (crestas largas y numerosos melanocitos individuales en la basal) y nidos variables y desordenados (aunque casi nunca en los extremos de las crestas, luego hay un orden dentro del desorden) y atipia nuclear discontinua?
Maize, 12 años después9
Clasificación
Neoplasias de melanocitos
-- Lentigo simple y nevo lentiginoso.
-- Nevos adquiridos: juntural, compuesto e intradérmico.
-- Reacciones en halo en los nevos melanocíticos.
-- Nevos melanocíticos congénitos.
-- Nevo de Spitz.
-- Nevo de Ota, nevo fusocerúleo cigomático, nevo de Ito, mancha mongólica.
-- Nevos azules.
-- Nevos combinados.
-- Nevo recurrente (persistente).
-- Melanoma.
-- Melanoma metastásico.
Descripción histopatológica
Algunos nevos junturales anchos, especialmente en el tronco, pueden tener características del llamado nevo displásico o nevo de Clark como:
-- «Puenting».
-- Fibroplasia concéntrica o laminar.
-- Infiltrados linfocitarios de moderada densidad.
Muchos nevos compuestos, especialmente en tronco y extremidades proximales, son compuestos (epidermis y dermis papilar).
A menudo tienen nidos junturales de melanocitos con abundante citoplasma pálido. Estos nidos se ex-tienden lateralmente más allá del componente dérmico.
Crestas adyacentes parecen «puenteadas» por nidos de melanocitos horizontales con núcleo ovoide o fusiforme.
En la periferia de estos nevos compuestos se encuentra también:
-- Ligera ectasia vascular.
-- Infiltrado linfocitario de ligero a moderado.
-- Fibrosis horizontal (fibroplasia laminar) de la dermis papilar.
-- A veces, melanocitos iguales a los junturales se pueden ver en dermis superficial en zonas de fibroplasia.
Sólo excepcionalmente:
-- Los melanocitos son marcadamente atípicos de acuerdo con criterios citopatológicos estándar.
-- Hay un infiltrado linfocitario denso.
El nevo compuesto atípico con displasia melanocítica ha provocado gran controversia.
Parece claro que hallazgos tales como:
-- Extensión de los nidos junturales más allá del componente dérmico.
-- «Puenting».
-- Fibroplasia concéntrica o laminar.
-- Infiltrados linfocitarios de moderada densidad.
-- Ligera variabilidad en el tamaño y forma de los núcleos melanocíticos junturales.
no son prueba de que un nevo melanocítico esté a punto de convertirse en un melanoma.
Comentarios
A la clasificación
Es la única clasificación en que no aparece el nevo displásico porque los autores lo consideran como una simple variante de nevo juntural o nevo compuesto.
A la histopatología
Las características histológicas de la variante displásica del nevo compuesto son:
-- Hombro.
-- «Puenting».
-- Melanocitos con abundante citoplasma pálido.
-- Fibroplasia.
-- Reacción inflamatoria.
-- Atipia melanocítica ocasional.
Los nevos displásicos junturales son iguales, pero, naturalmente, sin «hombros» al carecer, por definición, del componente dérmico central. Los autores se niegan a establecer una relación especial entre nevo displásico y melanoma.
La segunda edición del Farmer & Hodd10
Clasificación
Tumores melanocíticos
-- Tumores melanocíticos benignos.
-- Otros tumores que contienen melanocitos.
-- Nevo displásico.
-- Melanomas.
Descripción histopatológica
Criterios mayores
-- Patrón de proliferación melanocítica afectando a la unión dermoepidérmica.
-- Presencia de atipia melanocítica
Criterios menores
-- Fibroplasia.
-- Neovascularización.
-- Infiltrado linfohistiocitario.
Hechos diferenciales a favor de nevo melanocítico displásico
1. Con carácter absoluto (yes or no):
-- Proliferación melanocítica lentiginosa.
-- Extensión radial de melanocitos epidérmicos alrededor del componente dérmico (3 cres-tas o más).
-- Formación desordenada de nidos junturales.
-- Atipia melanocítica epidérmica (from none to marked).
-- «Puenting» de crestas y nidos.
-- Neovascularización.
-- Infiltrado linfohistiocitario.
2. Con carácter relativo (variable or usually):
-- Nidos en caras laterales de las crestas.
-- Melanina pulverulenta en los melanocitos.
-- Componente dérmico no neurotizado.
Comentarios
A la clasificación
No incluye al nevo displásico entre los tumores melanocíticos benignos. Tampoco entre los me-lanomas, pero más cerca de éstos que de los primeros.
A la histopatología
Se trata de una descripción muy escueta y esquemática en la que establecen con carácter absoluto la presencia de:
-- Proliferación juntural lentiginosa.
-- Nidos desordenados.
-- Hombro.
-- «Puenting».
-- Atipia melanocítica (entre ninguna y marcada).
-- Neovascularización.
-- Infiltrado inflamatorio.
Llama la atención que no describan ninguna peculiaridad citológica del nevo displásico (pese a lo cual hablan de melanina pulverulenta como un carácter variable) ni se entretienen en describir la atipia melanocítica. Aceptan que ésta puede estar ausente para hacer el diagnóstico.
De todo ello podemos deducir que estos autores dan más importancia a la arquitectura que a la citología.
El libro monográfico de Crowson, Magro y Mihm11
Clasificación
-- Pecas y lentigos.
-- Nevos adquiridos no displásicos.
-- Melanocitosis dérmicas.
-- Nevo de Spitz.
-- Nevo combinado, nevo penetrante profundamente y nevo fusocelular pigmentado.
-- Nevo melanocítico recurrente.
-- Nevo congénito.
-- Nevo melanocítico displásico.
-- Melanoma maligno.
Descripción histopatológica
-- La histología del nevo displásico es tan reproducible que su diagnóstico puede hacerse normalmente con la lupa.
-- La citología (para conocer el grado de atipia) sólo puede ser adecuadamente estudiada con el objetivo x40 o con mayor aumento.
Criterios diagnósticos
1. Criterios mayores (imprescindibles para hacer el diagnóstico):
a) Proliferación basilar asimétrica de nevo melanocitos a lo largo de la unión dermoepidérmica por fuera de los límites de un componente dérmico preexistente.
b) Las células tienen:
-- Una citomorfología característica.
-- Un patrón de crecimiento intraepidérmico específico.
c) Hay dos subtipos:
-- Displasia melanocítica lentiginosa:
* Células aisladas dispuestas al azar se localizan a lo largo de y entre crestas alargadas y formando nidos de tamaño variable. Los bordes citoplásmicos pueden ser espiculados.
* Muestran núcleos hipercromáticos («en mancha de tinta»), de tamaño variable, igual o mayor que el de los queratinocitos vecinos.
-- Displasia melanocítica de células epitelioides:
* Melanocitos epitelioide solos o agrupados en nidos junturales de tamaño variable en la unión dermoepidérmica.
* Núcleo oval o redondeado con cromatina abierta, delicada.
* Citoplasma redondeado, desde acrómico a lleno de granos groseros de melanina.
d) Las células son displásicas porque hay:
-- Variabilidad de célula a célula.
-- Nucleolación conspicua.
-- Membrana nuclear gruesa.
-- Sus núcleos son mayores que los de los queratinocitos vecinos.
2. Criterios menores (que no siempre están presentes):
-- Fibrosis eosinófila concéntrica.
-- Fibroplasia laminar.
-- Infiltrado linfocítico superficial, más intenso donde hay más atipia citológica.
-- Vasos prominentes, neoformados o preexistentes.
-- Fusión de crestas por crecimiento confluente entre nidos de melanocitos adyacentes.
El diagnóstico de nevo displásico se hace cuando se encuentran todos los criterios mayores y dos de los menores.
Comentarios
A la clasificación
Es la primera vez que vemos clasificar los nevos melanocíticos en no displásicos y displásicos. Esto, lejos de separar el nevo displásico del «común», lo que hace, creemos, es relacionarlos íntimamente, ya que la definición de uno dependerá de la del otro.
A la histopatología
El diagnóstico se hace con la lupa, es decir, se basa en la arquitectura. Y ¿cuál es esa arquitectura diagnóstica? Los «hombros» (asimétricos).
Los autores describen de nuevo, como Elder et al2, con toda claridad los dos subtipos de displasia melanocítica: lentiginosa y epitelioide.
Los caracteres mayores para el diagnóstico son:
-- Hombros.
-- Displasia melanocítica lentiginosa o epitelioide.
-- Atipia celular.
Para el diagnóstico exigen todas ellas y, además, dos de los cuatro siguientes criterios menores:
-- Fibroplasia.
-- Inflamación.
-- Vasos prominentes.
-- «Puenting».
Llama la atención su afirmación de que el grado de atipia «sólo puede ser adecuadamente estudiado con objetivo x40 o con mayor aumento». Si se mirasen así todas la neoplasias benignas tiene atipias, incluso los nevos intradérmicos más maduros.
DISCUSION
De la lectura de todo lo anterior podemos deducir que existe práctica unanimidad en una serie de características del nevo displásico que pasamos a enumerar:
1. Cuando un nevo displásico es compuesto (la mayor parte de las veces) se trata de:
-- Un nevo compuesto o intradérmico rodeado por un «hombro» (halo) juntural.
-- En este halo («hombro») juntural hay nidos junturales y melanocitos junturales aislados.
-- Los nidos son de forma y tamaño variables (llama la atención que a menudo son elipsoides y horizontales, haciendo «puenting») y de distribución desordenada.
-- Los nevocitos basales (tanto de los nidos como los aislados) son, a menudo, fusiformes y epitelioides, con amplio citoplasma claro con melanina pulverulenta.
-- La dermis superficial subyacente a esos «hombros» muestra a menudo fibroplasia, infiltrado linfochistiocitario y aumento de la vascularización.
2. Un nevo displásico juntural consiste en un «hombro sin cabeza».
3. Un nevo displásico no es un melanoma in situ. Éste muestra proliferación suprabasal de melanocitos y atipia nuclear de todos ellos.
Junto a esta coincidencia casi unánime hay discordancia, o al menos falta de claridad, en dos características:
-- La displasia lentiginosa.
-- La atipia celular.
La displasia melanocítica lentiginosa
La displasia melanocítica lentiginosa fue descrita por Elder et al2 y la denominaron así por su similitud estructural con el lentigo simple. Es decir, porque la epidermis tenía finas crestas alargadas flanqueadas por numerosos melanocitos basales. Estos melanocitos mostraban un prominente artefacto de retracción citoplásmica. Había, como en la displasia epitelioide, pleomorfismo e hipercromatismo nuclear «en unas pocas o en muchas células». Esta displasia lentiginosa la encontraron en todos los nevos displásicos de forma que la displasia epitelioide que habían descrito Clark et al1 nunca era pura, sino que se entremezclaba siempre con la lentiginosa.
Sin embargo, cuando Maize y Ackerman3 describieron la arquitectura del nevo displásico, con sus famosos «hombros» en los que se sitúa la displasia, la descripción de ésta se ajusta a la displasia epitelioide de Clark et al1 sin citar en ningún momento nada que recuerde a la displasia lentiginosa de Elder et al2. Lo mismo ocurre en la descripción del nevo de Clark por Maize et al9. Pero si repasamos las descripciones de los demás autores5-8, 10, 11 vemos que sólo Crowson11 et al reproducen la dicotomía de Elder et al2 al describir separadamente la displasia lentiginosa y epitelioide. Todos los demás habla sólo de la primera, pero cuando luego se refieren a nidos y células mezclan ambos tipos de displasia5-8, 10.
La atipia celular
La atipia celular, el pleomorfismo e hipercromatismo nuclear de los melanocitos (atipia nuclear) son términos que se repiten en casi todas las descripciones del nevo displásico, pero con tal serie de matices que uno acaba por dudar de su existencia. En cada uno de nuestros resúmenes de las descripciones del nevo displásico por los diversos autores hemos resaltado en negrita lo referente al grado de atipia del nevo displásico:
-- «Melanocitos individuales o pequeños nidos de melanocitos que tienen alguno de los caracteres estructurales de los melanocitos malignos, pero cuyo potencial de desarrollo hacia un melanoma es oscuro.»1
-- «Los aspectos histológicos comunes a todos los nevos displásicos fueron pleomorfismo e hipercromatismo nuclear en unas pocas o muchas células de cada lesión. Las mitosis no eran frecuentes2.»
-- «Algunos nevos displásicos pueden tener unos pocos núcleos atípicos dentro de la porción epidérmica, incluso dérmica, de la lesión e infrecuentemente la mayoría de los melanocitos y células névicas pueden tener núcleos atípicos. Tales nevos displásicos con muchos núcleos atípicos se diferencian del melanoma por los criterios usuales, esencialmente por los criterios arquitecturales más que por los citológicos3.»
-- «Es dentro de esta zona de proliferación celular asimétrica donde aparecen algunos melanocitos atípicos. Cuando aparecen aplicamos el término de displasia melanocítica4.»
-- «La atipia citológica de un nevo displásico es, en nuestra opinión, relativamente ligera. Raramente se ve una atipia marcada o llamativa, y las mitosis son muy infrecuentes4.»
-- «Los melanocitos displásicos [...] se distribuyen al azar en la capa basal5.»
-- «Presencia ocasional de células con núcleos hipercromáticos agrandados, algunas veces con nucleolos prominentes6.»
-- «Para hacer el diagnóstico se requiere encontrar atipia nuclear (núcleos grandes, irregulares e hipercromáticos) en algunos melanocitos7.»
-- «La atipia afecta únicamente a una minoría de las células de la lesión (random cytologic atypia)7.»
-- «Atipia nuclear discontinua..., núcleos grandes, pleomórficos, hipercromáticos, con nucleolos prominentes8.»
-- «Sólo excepcionalmente los melanocitos son marcadamente atípicos de acuerdo con criterios citopatológicos estándar.»
-- «Atipia melanocítica epidérmica (from none to marked)10.»
-- «La citología (para conocer el grado de atipia) sólo puede ser adecuadamente estudiada con el objetivo x40 o con mayor aumento11.»
Es decir, que el nevo displásico es una neoplasia melanocítica benigna que ocasionalmente puede tener algún melanocito ligeramente atípico. Entonces, ¿por qué no llamamos displásico al nevo de Spitz o al nevo penetrante profundo?
El nevo lentiginoso
Cuando Elder et al en 1980 describieron la displasia melanocítica lentiginosa2, el concepto histológico de lentigo simple era bastante confuso. Por ejemplo, la confusión entre lentigo simple y lentigo solar llegaba hasta el extremo de que en las ediciones del libro de Lever y Schaumurg-Lever de 197515 y 198316 la ilustración de la histopatología del lentigo solar se hace con una microfotografía del más típico lentigo simple que pueda imaginarse; y en la primera edición del McKee17 el lentigo simple se ilustra con un fragmento de epidermis sin apenas melanocitos y que probablemente corresponde a un acantoma de células grandes.
En esos mismos libros15-17 y en el de Pikus y Mehregan18, la histopatología de nevo juntural se ilustraba con microfotografías de x200 a x400, donde apenas cabían de uno a tres nidos junturales, grandes, perfectamente redondeados. Esta variedad de nevo juntural es, en nuestra experiencia, bastante infrecuente. La que hallamos con mayor frecuencia es la llamada (impropiamente) lentigo nevoide y (más propiamente) nevo lentiginoso6. Anteriormente, Pikus y Mehregan lo denominaron nevus incipiens18 y luego Maize y Ackerman le dieron la humorística denominación de «jéntigo»3. Parece que muchos nevos junturales no son más que lentigos simples que siguen evolucionando hacia nevo juntural, nevo compuesto y nevo intradérmico3, 4. Sin embargo, como luego veremos, no todos los nevos junturales se desarrollan a partir de un lentigo simple.
La siguiente descripción histológica de lentigo simple es compartida hoy día por la mayor parte de los autores: una epidermis con finas crestas digitiformes en cuya capa basal hay numerosos melanocitos aislados. Estas crestas están hiperpigmentadas. La melanina puede abundar en todas las capas epidérmicas, incluida la capa córnea. En la dermis superficial subyacente hay melanófagos y un ligero a moderado infiltrado linfohistiocitario. A lo anterior, varios autores3, 9, 11, 17 añaden la presencia de fibroplasia concéntrica.
Según Maize et al9 si se hacen cortes seriados de un lentigo simple casi siempre aparece algún nido juntural y, a veces, nidos intradérmicos. Según Weedon6 en el nevo lentiginoso hay un borde lentiginoso y un centro de nevo juntural o de nevo compuesto, es decir, que en algunos casos se trataría de un nevo melanocítico compuesto con un halo juntural y otro más externo, lentiginoso; y todo ello con reacción inflamatoria y, a menudo, con fibroplasia, es decir, un nevo displásico.
Según Elder y Elenitsas «estas lesiones que combinan características de lentigo simple y de nevo juntural son extraordinariamente frecuentes (exceedingly common) y se las puede denominar "nevos junturales lentiginosos". Lesiones con estas características que miden clínicamente más de 5 mm y de 4 a 5 mm en los cortes histológicos a menudo son nevos displásicos.»
Según Barnhill «es un problema frecuente tener que diferenciar un lentigo simple de un nevo melanocítico típico o de un nevo displásico. El nevo melanocítico se distingue por la presencia de nidos junturales8». Es curioso que el autor termina así el párrafo sin explicarnos cómo podremos distinguir el lentigo simple del nevo displásico.
Para Crowson et al «algunas lesiones (de lentigo simple) muestran fibrosis concéntrica eosinofílica alrededor de los extremos de las crestas y de las crestas fusionadas, lo cual es una característica arquitectural típicamente asociada con el nevo displásico11».
En nuestra experiencia una de las formas más frecuentes de nevo juntural es una variedad de nevo lentiginoso al que llamamos «superlentiginoso» porque tiene unas larguísimas crestas digitiformes. Son lesiones de más diámetro que un lentigo simple, con abundantes nidos junturales, en general pequeños, en cualquier zona de las crestas y una llamativa fibroplastia concéntrica. Algunos muestran además, nidos intradérmicos en su porción central. Creemos que, muy probablemente, fue a casos como éstos a los que Elder et al2 denominaron nevos con displasia lentiginosa.
Otra de las formas más frecuentes de nevo juntural, en nuestra experiencia, es el nevo displásico juntural tal como lo describieron Clark et al1 y Maize y Ackerman3, es decir, la variante epitelioide.
El tercer tipo de nevo juntural, en frecuencia, sería el clásicamente ilustrado en los libros, con hermosos nidos redondeados (por lo que proponemos llamarle «clásico»), y aún tenemos una cuarta y una quinta forma de nevo melanocítico juntural, las de los nevos de Reed y de Spitz.
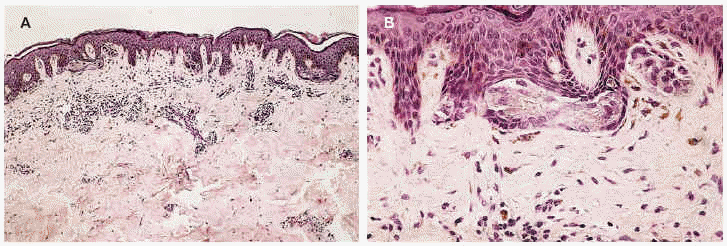
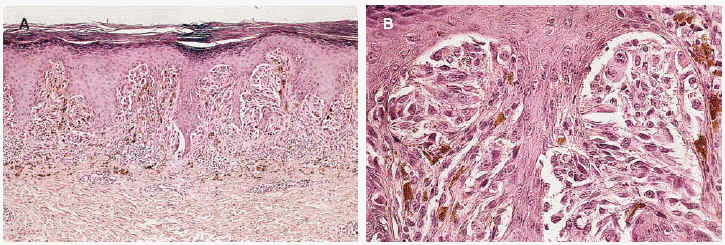
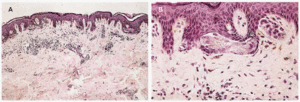
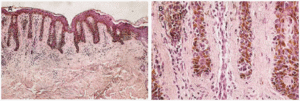
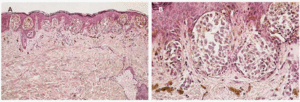
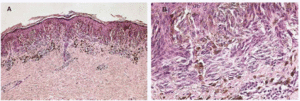
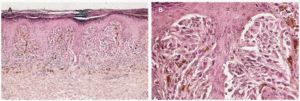
Si comparamos todos estos tipos de nevo melanocítico juntural, ¿seremos capaces de llamar a uno displásico y a los demás no? Creemos que se trata, simplemente, de diversas variedades de nevo melanocítico juntural a las que podemos llamar: de Clark (fig. 1), lentiginosa (fig. 2), clásica (fig. 3), de Reed (fig. 4) y de Spitz (fig. 5).
Fig. 1.--Nevo melanocítico juntural tipo Clark. Nidos desiguales y «colgando» de la epidermis, unos pequeños y otros grandes y horizontales uniendo crestas contiguas (puenting). La dermis superficial muestra un moderado infiltrado linfohistiocitario, con el consiguiente aumento de la vascularización, y una fibroplasia laminar, que se aprecia muy bien en B, con numerosos fibrocitos y finos haces colágenos dispuestos paralelamente al nido horizontal; éste está formado por melanocitos de amplísimo citoplasma (hematoxilina-eosina. A: x100; B: x400).
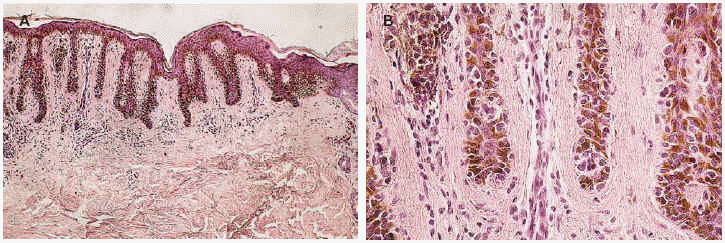
Fig. 2.--Nevo melanocítico juntural lentiginoso. Destaca la gran longitud de las finas crestas (nevo «superlentiginoso») flanqueadas por numerosísimos melanocitos basales. En dermis papilar y subpapilar hay una inflamación moderada. En B llama la atención la fibroplasia concéntrica (finísimos haces colágenos rodean, en múltiples capas concéntricas, las crestas lentiginosas). En todas éstas se aprecia algún pequeño nido juntural (hematoxilina-eosina. A: x100; B: x400)
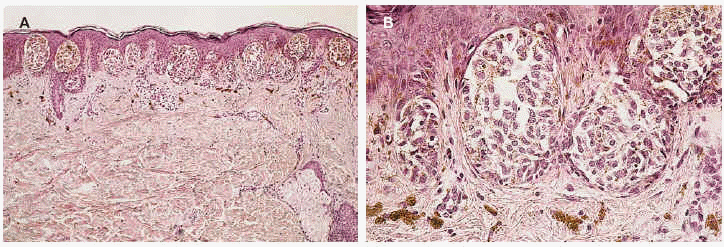
Fig. 3.--Nevo melanocítico juntural de tipo clásico. Grandes nidos junturales redondeados. No se aprecia fibroplasia, pero sí son abundantes los melanófagos (hematoxilina-eosina. A: x100; B: x400).
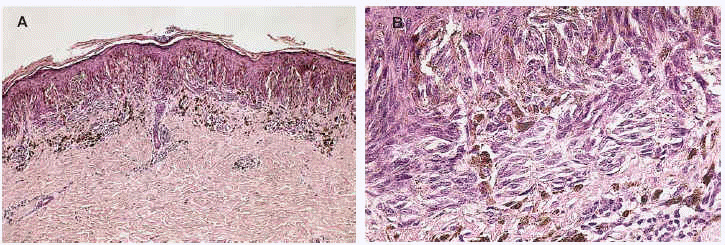
Fig. 4.--Nevo melanocítico juntural tipo Reed (también llamado nevo fusocelular pigmentado). Grandes nidos, unos de eje mayor vertical (A) y otros horizontales (B) formados por melanocitos fusiformes sin citoplasma eosinófilo. Hay una banda dérmica inflamatoria superficial rica en melanófagos. La epidermis es ligeramente acantósica (hematoxilina-eosina. A: x100; B: x400).
Fig. 5.--Nevo melanocítico juntural tipo Spitz. Destaca una epidermis de patrón liquenoide: acantosis irregular, hipergranulosis en V e hiperqueratosis compacta. Los nidos junturales son de forma y tamaño variados (en general grandes y verticales) y confluyen. Sus células, con amplio citoplasma eosinófilo, facetado, contienen algunos núcleos muy atípicos. Banda inflamatoria superficial con melanófago (hematoxilina-eosina. A: x100; B: x400.)
¿Sería importante ahora la búsqueda de algún núcleo hipercromático con el objetivo x40 o superior? No lo creemos. Para atipias, las de muchos nevos de Spitz o las del nevo penetrante profundo, y nadie los llama por esto atípicos* ni displásicos.
* Simón Huarte propuso, sin éxito, en 1968 llamar nevo atípico de Spitz al tumor que entonces solía denominarse melanoma juvenil20.
En todo nevo juntural hay aumento de la vascularización (como en las cercanías de todo proceso proliferativo), reacción inflamatoria y en muchos fibroplasia19.
En cuanto a la existencia de un halo juntural o lentiginoso en torno al componente dérmico, es un hecho obligatorio en los nevos moteados y se halla en muchos nevos melanocíticos congénitos.
En conclusión, consideramos que antes de 1978 se había establecido un estándar erróneo de nevo melanocítico juntural al que hemos llamado clásico, que resulta ser bastante infrecuente. Partiendo de este axioma erróneo, y sin establecer un grupo control de pacientes sin melanoma familiar1 y sin melanoma espo-rádico2, se consideraron diferentes, displásicos, a los demás nevos melanocíticos junturales y compuestos que luego se ha visto que son exceedingly common7.
De la misma forma que se ha demostrado la existencia de dos formas, no sólo distintas, sino contrapuestas, de nevo melanocítico adquirido intradérmico (sin contar con el nevo de Spitz intradérmico ni con el nevo penetrante profundo), el nevo de Unna y el nevo de Miescher21, 23, también hay distintas variedades (hasta cinco al menos) de nevo melanocítico juntural. ¿Es alguna de ellas peor que las otras? Probablemente lo que no parece muy conveniente es tener muchos de estos lunares pasados los 30 años, del mismo modo que tampoco es bueno tener nevos congénitos muy grandes al nacer, ya que en ambos casos se dispone de una gran superficie epidérmica donde hay melanocitos epidérmicos en proliferación constante y las posibilidades de un error en la misma siempre será mayor que si se tienen pocos lunares o si éstos ya no tienen componente juntural (proliferativo).
Reproducimos a continuación lo que Elder, uno de los padres del nevo displásico, escribió 17 años después7:
«Los nevos displásicos se presentan frecuentemente como lesiones solitarias y son muy comunes, encontrándose en el 5% al 20% de diferentes poblaciones, según los criterios empleados.»
«La mayoría de los nevos displásicos son clínicamente estables, es decir, no son «activos» en el sentido de crecimiento continuo.»
«Una lesión en el límite puede ser un nevo displásico o un melanoma de extensión superficial incipiente, todavía in situ o microinvasor. Puesto que tales melanomas tempranos son curables tras escisión simple, esa distinción no conlleva peligro de muerte siempre que la lesión esté totalmente extirpada.»
El riesgo de melanoma «se establece mejor (que por el estudio histológico del nevo) por la evaluación clínica de la historia del paciente y de su fenotipo cutáneo. El número total de nevos y el número de nevos grandes, la piel clara, y numerosas pecas, son todos ellos factores de riesgo para el desarrollo de mela-nomas.»
«Aunque los melanomas en pacientes con nevo displásico pueden originarse en ellos, la mayoría surgen de novo.»
«La mayoría de los nevos displásicos son clínicamente estables y nunca evolucionan a melanoma.»
Es decir, que como antes decíamos, tener muchos nevos junturales, como es el caso de los llamados nevos displásicos y de los nevos congénitos, es como llevar muchos números para el sorteo de Navidad: aumenta la posibilidad de «premio», pero nada más.
Si el llamado nevo displásico es un nevo, es decir, una lesión benigna, y además se extirpa por completo, ¿de qué hay que temer? Que se sepa, de nada. Otra cosa sería si se demostrase, como en el síndrome de Muir-Torre, que la presencia de una inocente neoplasia benigna en la piel puede ser el marcador de una tendencia personal y familiar al cáncer de colon o de las vías urinarias24. Pero algo así nadie ha demostrado que ocurra con el nevo de Clark. Entonces, ¿conviene seguir usando el adjetivo displásico para una lesión benigna? Algunos seguimos usando en los informes el término epitelioma, en lugar de carcinoma para no asustar a los pacientes con los habituales carcinomas cutáneos poco agresivos; entonces, ¿por qué usar un término que implica peligro en la denominación de una lesión totalmente benigna?
En el caso concreto del llamado nevo displásico tenemos las denominaciones alternativas de nevo lentiginoso y de nevo de Clark para sus dos variantes estructurales y citológicas: la lentiginosa y la epitelioide.
Respuestas correctas a las preguntas correspondientes a la Revisión de Formación Médica Continuada del número 4, abril 2002.
1c 6d 11b
2d 7c 12c
3c 8d 13a
4c 9c 14a
5a 10b 15b