Los linfomas cutáneos primarios (LCP) constituyen un grupo heterogéneo de neoplasias linfoides que se originan primariamente en la piel. La mayoría (75%) son linfomas de células T y solo un 20-25% se originan a partir de los linfocitos B. Es importante diferenciar los LCP de sus equivalentes ganglionares, dado que presentan características clínicas, histopatológicas, inmunofenotípicas y de biología molecular diferentes con un pronóstico en la mayoría de los casos más indolente y tratamientos diferentes.
Existen múltiples opciones terapéuticas en el manejo de los LCP. La elección del tratamiento debe basarse principalmente en el estadio clínico del paciente, pero deben considerarse también otros factores, como la accesibilidad a los tratamientos, la edad y el estado general del paciente o el coste-beneficio. Además es importante el abordaje multidisciplinar de estos pacientes, formando un equipo experto entre dermatólogos, hematooncólogos y radioterapeutas que conozcan bien esta infrecuente patología. En los últimos años asistimos a la aparición de múltiples terapias nuevas, especialmente para el tratamiento de los estadios avanzados o de pacientes refractarios a tratamientos previos. El motivo de este artículo es revisar todas las alternativas terapéuticas a nuestro alcance.
Primary cutaneous lymphomas (PCLs) are a heterogeneous group of lymphoid tumors that originate primarily in the skin. Most PCLs (75%) are T-cell lymphomas and only 20% to 25% involve B cells. It is important to differentiate between cutaneous lymphomas and lymph node tumors given the differences in their molecular biology and clinical, histopathologic, and immunophenotypic features. Moreover, PCLs generally follow a more indolent course and require different treatments.
Many treatment options are available for managing PLC's. The choice should be based primarily on the clinical stage of disease but must also take into consideration other factors, such as the patient's age and general health, the availability and accessibility of the treatment, and the cost-benefit ratio. It will be important to use a multidisciplinary approach, involving a team of expert dermatologists, hematologist-oncologists, and radiotherapists who are familiar with this rare disease. Recent years have seen the emergence of many new therapies, particularly for advanced stages of the disease and for patients whose tumors have proven refractory to treatment. The objective of this article is to review all the treatment options available to us.
Los linfomas cutáneos primarios (LCP) constituyen un grupo heterogéneo de neoplasias linfoides que se originan primariamente en la piel1. La mayoría (75%) derivan de los linfocitos T (linfomas cutáneos primarios de células T [LCCT]) y entre un 20-25% se originan a partir de las células B (linfomas cutáneos primarios de células B [LCCB]). La micosis fungoide (MF) y el síndrome de Sézary (SS) son las entidades más frecuentes. Es importante diferenciar los LCP de sus equivalentes ganglionares, dado que presentan unas características clínicas, histopatológicas, inmunofenotípicas y de biología molecular diferentes y, lo que es más importante, un pronóstico en la mayoría de los casos más indolente y con tratamiento diferente.
Es necesario conocer bien las últimas clasificaciones como las de la EORTC/WHO1 (tabla 1) y la WHO (2008)2,3 para hacer un diagnóstico correcto, fundamental a la hora del tratamiento. Los LCP son enfermedades con escasa incidencia4 y la mayor parte de los pacientes tienen un supervivencia prolongada. Por ello resulta muy difícil evaluar el impacto de un tratamiento determinado sobre la evolución de la enfermedad y prácticamente no existen estudios casos-control. Estos factores, entre otros, hacen que los niveles de evidencia sean bajos: la situación ideal sería que todo paciente con un LCP fuera incluido en un estudio clínico.
Clasificación de los linfomas cutáneos primarios, EORTC/WHO (2005)
| Linfomas cutáneos de células T |
| Micosis fungoides y variantes |
| MF foliculotropa |
| Reticulosis pagetoide |
| Piel laxa granulomatosa |
| Síndrome de Sézary |
| Síndromes linfoproliferativos CD30+ |
| Papulosis linfomatoide |
| Linfoma anaplásico CD30+ |
| Leucemia/linfoma T del adulto |
| Linfoma T subcutáneo «paniculitis-like» |
| Linfoma NK/T extranodal «nasal-type» |
| Linfoma T periférico no especificado |
| Linfoma CD8+ epidermotrópico |
| Linfoma cutáneo de células T γδ |
| Linfoma CD4 pleomórfico de célula pequeña/mediana |
| Linfomas cutáneos de células B |
| LCCB de la zona marginal |
| LCCB centrofolicular |
| LCCB difuso de célula grande «leg-type» |
| LCCB difuso de célula grande «otros» |
| LCCB de célula grande intravascular |
| Neoplasias de precursores hematológicos |
| CD4+ CD56+ neoplasia hematodérmica |
EORTC: European Organization for Research and Treatment of Cancer; LCCB: linfomas cutáneos primarios de células B; MF: micosis fungoide; WHO: World Health Organization.
Existen múltiples opciones terapéuticas5,6 en el manejo de los LCP. La elección del tratamiento debe basarse principalmente en el estadio clínico del paciente, pero deben considerarse también otros factores, como la accesibilidad a los tratamientos, la edad y el estado general del paciente o el coste-beneficio. No existen datos que demuestren una eficacia superior del tratamiento sistémico (más agresivo) frente al tratamiento local dirigido a las lesiones cutáneas, en los estadios iniciales de la enfermedad. Por lo tanto es recomendable una actitud conservadora.
Podemos clasificar la terapia en 2 grandes grupos:
- 1.
Tratamientos dirigidos a la piel, cuya acción se desarrolla exclusivamente sobre la población neoplásica localizada a nivel cutáneo. Así, los efectos adversos observados suelen ser de menor intensidad que aquellos secundarios a los tratamientos sistémicos. Este tipo de terapia constituye en la práctica la única recomendada como primera línea en las fases precoces de la MF. En estadios avanzados sigue constituyendo una alternativa importante, formando parte de las terapias de combinación. En este apartado se incluyen:
- -
Corticoides tópicos.
- -
Agentes alquilantes: mostaza nitrogenada (mecloretamina) y carmustina tópicas.
- -
Fototerapia–ultravioleta-B (UVB) de banda estrecha, psoralenos+ultravioleta-A (PUVA) y otros.
- -
Radioterapia (convencional y baño de electrones).
- -
- 2.
Tratamientos sistémicos entre los que se encuentran los modificadores de la respuesta biológica (retinoides, citoquinas, inmunotoxinas y vacunas, anticuerpos monoclonales, inhibidores de histonas deacetilasas…), la quimioterapia (mono o poliquimioterapia clásica, nuevos quimioterápicos) y el trasplante alogénico de células precursoras.
Son capaces de inducir apoptosis sobre la mayor parte de los linfocitos neoplásicos del tegumento cutáneo y disminuir el número de células de Langerhans, lo que interfiere con la estimulación de las células neoplásicas. Aunque han sido usados durante años, no existe mucha bibliografía acerca de su manejo7,8. Zackheim et al.8 aportan su experiencia en 79 pacientes con MF en parches o placas. Utilizaron corticoides de mediana y elevada potencia (clases I-III), en ocasiones en cura oclusiva. En pacientes en estadio T1, el 63% presentó remisión completa (RC) y el 31% remisión parcial (RP), mientras que en T2 el 25% alcanzó RC y el 57% RP. Como efectos secundarios observaron supresión suprarrenal en 10 pacientes, irritación cutánea en 2 y atrofia cutánea con estrías en un paciente. Los autores concluyen que es un tratamiento bien tolerado y efectivo para estadios muy iniciales.
Agentes alquilantesLos agentes alquilantes son fármacos que actúan sobre diferentes mecanismos y funciones del ADN, produciendo finalmente la muerte celular.
Mecloretamina tópica (mostaza nitrogenada)Aunque su mecanismo de acción exacto es desconocido, cuando se administra sistémicamente actúa como un agente alquilante con efecto antimitótico, pero su actividad tópica parece mediada por mecanismos inmunes o por interacción con las células de Langerhans. Habitualmente se utiliza9-15 en solución acuosa (10-20mg/100ml) o en ungüento (10-20mg/100g vaselina). Actualmente se está realizando un estudio16 multicéntrico, aleatorizado y doble ciego comparando la seguridad y eficacia de 2 compuestos de mostaza nitrogenada manufacturados (0,02% en propilenglicol versus 0,02% en vaselina) en pacientes con MF estadio IA-IIA refractarios a corticoides tópicos. Los resultados preliminares han demostrado similar eficacia (tasa de respuesta global [RG] sobre un 70%) y buen perfil de seguridad (no se ha visto absorción sistémica) para ambos preparados. En la pauta clínica habitual inicialmente se aplica a diario hasta obtener el aclaramiento de las lesiones (entre 3-6 meses con la solución y 6-12 meses con el ungüento), continuando después con una pauta de mantenimiento intermitente. Se suele recomendar la aplicación sobre toda la superficie corporal, evitándose áreas intertriginosas, pero la necesidad de tratar áreas no afectadas no está muy clara. La respuesta varía entre un 50-75% en T1 a un 25-50% en T2. Produce dermatitis de contacto (alérgica o irritativa) especialmente usando la solución acuosa (30% frente a<5% con el ungüento), urticaria y reacciones anafilácticas. Su uso prolongado incrementa el riesgo de cáncer de piel no melanoma, sobre todo si los pacientes han sido previamente tratados con PUVA o baño de electrones. No parece producir depresión de la médula ósea ni otros efectos sistémicos. La eficacia parece similar para los 2 compuestos, solución y ungüento, aunque no se han hecho estudios prospectivos (a excepción del comentado previamente16). En los últimos años la disponibilidad de la mecloretamina en las farmacias hospitalarias es mínima, por lo que, a pesar de su eficacia, lamentablemente está cayendo en desuso
CarmustinaAgente alquilante que induce muerte celular por inhibición de la síntesis de ADN. Se utiliza17–20 en solución alcohólica (2mg/ml) o en ungüento. Debe aplicarse diariamente sobre piel lesionada y el tiempo de aclaramiento de las lesiones es similar al de la mecloretamina. La tasa de respuesta varía de un 86% en T1 a un 48% en T2. La mayoría de los pacientes presentan eritema, en ocasiones seguido de telangiectasias persistentes, y aproximadamente en el 3-5% aparece leucopenia leve por mielosupresión. Puede utilizarse como alternativa en los pacientes alérgicos a la mostaza nitrogenada, aunque su disponibilidad también es mínima.
FototerapiaFototerapia–ultravioleta-B (UVB) de banda estrecha (311-312nm)Varios estudios21–26 han demostrado su utilidad en estadios iniciales de MF (tasas de RC alrededor del 75%, con una duración media de respuesta de 51 meses). Incrementa el riesgo de cáncer de piel y solo es efectiva en MF con lesiones iniciales, poco o nada infiltradas, por su limitada penetración. Sería especialmente útil en pacientes que no toleraran los psoralenos o con piel muy clara o lesiones muy incipientes27.
Psoralenos más ultravioleta- (320-400nm)Es el tratamiento clásico en estadios iniciales20,29–34. Habitualmente se comienza con 2-3 sesiones semanales, reduciendo la frecuencia según la respuesta. No existe consenso35 sobre si es necesario mantener una pauta de mantenimiento una vez lograda la respuesta completa. En un estudio28 con 82 pacientes con MF en placas superficiales y/o placas palpables, se lograron RC en el 65% y RP en el 30%, con una duración media de 43 meses. En el 10% de los pacientes se objetivó daño actínico crónico, con aparición de epiteliomas en 6 pacientes: 3 con epiteliomas basocelulares y 3 con espinocelulares. Aunque existen estudios que muestran un incremento estadístico de carcinogénesis, incluido el melanoma, creemos que en la práctica este riesgo es más teórico que real, al menos en este grupo de pacientes. En cuanto a la duración del intervalo libre de lesiones, estudios más recientes27,35 lo relacionan con una mayor dosis acumulada de PUVA y un tiempo de tratamiento más prolongado. Aunque pueden existir recaídas tardías, entre el 30 y el 50% de los pacientes en estadios IA, IB y IIA pueden mantenerse en RC durante periodos de hasta 10 años. Las tasas libres de enfermedad para pacientes en estadio IA a los 5 y 10 años fueron 56 y 30%, respectivamente. Para aquellos pacientes en estadios IB/IIA, esta cifras fueron 74 y 50%. Sin embargo, la supervivencia global no varió significativamente entre aquellos que recayeron y los que no.
Otras modalidades de fototerapia- -
La fotoféresis extracorpórea36–39. Es una modificación del PUVA en la que tras la ingestión del psoraleno se exponen células mononucleadas circulantes del paciente a UVA. Su handicap principal es el alto coste de la técnica y que además no presenta una mayor eficacia que otros tratamientos. Las mejores respuestas se obtienen en pacientes con SS que presenten recuentos de CD8 normales y con un tiempo de evolución corto, sin tratamientos agresivos previos.
- -
La hipericina, un nuevo derivado vegetal fotodinámico, induce la apoptosis de linfocitos T utilizando luz visible o UVA. Si se confirman los resultados40 podría tener más interés que otras formas de fototerapia, ya que la luz visible no aumenta el riesgo de cáncer de piel.
- -
La utilización de la terapia fotodinámica41 con derivados del ácido 5- aminolevulínico (5-ALA) puede ser especialmente útil en pacientes con pocas lesiones o con lesiones en cuero cabelludo.
- -
Se ha utilizado también el láser excimer monocromático que emite a una longitud de onda de 308nm, aprobado por la Federal Drug Administration (FDA) para psoriasis y vitíligo. Passeron et al42,43 han realizado un ensayo clínico en el que han obtenido buena respuesta en lesiones muy incipientes, por lo que sería un tratamiento a considerar en zonas no accesibles habitualmente con fototerapia.
Sin embargo, sobre el uso de estas modalidades hay escasa experiencia y poca evidencia disponible respecto al tratamiento con otras opciones terapéuticas.
RadioterapiaConvencional (ortovoltaje)Se utiliza44 para placas muy infiltradas o tumores localizados de MF resistentes a otros tratamientos y especialmente para el tratamiento de LCCB (zona marginal y centrofolicular), en estos casos como primera opción junto a la extirpación quirúrgica45,46. Si se utilizan dosis inferiores a 30Gy hay una mayor tasa de recaídas. La radioterapia local se ha utilizado también en casos de MF «unilesional» con extraordinarios resultados47.
Irradiación corporal total con electrones (baño de electrones)Es un tratamiento de elección en pacientes con MF con placas infiltradas o pequeños tumores generalizados. El esquema más utilizado48 es 6 MeV (megaelectronvoltio) aplicados 4 días por semana con un total de 3.600 cGy en 10 semanas. Puede aplicarse repetidamente si se utilizan dosis reducidas. Los efectos secundarios incluyen eritema generalizado, edema, descamación y exudación, reagudización aparente de las lesiones preexistentes, pérdida total de los anejos cutáneos, melanoniquia transversa y, más raramente, vesiculación. La alopecia generalmente es reversible si la dosis total suministrada no ha excedido los 2.500 cGy. A más largo plazo, los pacientes pueden desarrollar edema, hiperpigmentación, telangiectasias y xerosis cutánea persistente y esterilidad en los varones48–50.
Para prolongar el periodo libre de enfermedad algunos autores preconizan el uso posterior de un tratamiento de mantenimiento, ya sea con mostazas o PUVA48,49,51,52. Las recomendaciones de la EORTC respecto a la irradiación corporal total con electrones (TSEB) en la MF fueron publicadas en 200253. Así, no se recomienda para LCCT eritrodérmico (T3) por el riesgo de descamación grave y porque las tasas de respuesta completa son mayores en estadios iniciales (T1=90%, T2=70%) que en estadios avanzados donde el efecto es meramente paliativo.
Se sabe que el porcentaje de RC depende del estadio de la enfermedad, de la dosis alcanzada y de la energía de los electrones51. De forma global, se obtiene RC en el 96% de los pacientes IA, IB y IIA, en el 36% de aquellos IIB y en el 60% (o menor) de los pacientes en estadio III. Las tasas de RC se relacionan también con la dosis total (32-36Gy) y la energía de los electrones (4-6 MeV)52,53.
Tratamientos sistémicosModificadores de la respuesta biológicaRetinoidesSe ha utilizado isotretinoína y etretinato en el tratamiento de la MF con eficacia similar. Su utilidad como monoterapia es escasa, pues se ha visto que en lesiones clínicamente curadas en apariencia persistían células atípicas en la histología. Se han combinado con PUVA e interferón alfa (IFN-α): asociados a PUVA parecen disminuir las dosis de UVA y con IFN-α parecen aumentar la respuesta al interferón en estadios iniciales, pero no en los avanzados, aunque no existen estudios aleatorizados que comparen IFN-α frente a IFN-α asociado a retinoides54.
El bexaroteno es un nuevo retinoide -rexinoide- cuyo exacto mecanismo de acción es desconocido, pero que in vitro inhibe el crecimiento de los linfocitos tumorales y estimula también el fenómeno de apoptosis55. El bexaroteno activa selectivamente los receptores RXR (un tipo de receptor nuclear activado por el ácido retinoico), actuando como regulador de los procesos de diferenciación y proliferación celular. En el año 2002 la FDA aprobó su uso, tanto tópico al 1% en gel (no comercializado por el momento en nuestro país, puede obtenerse como medicación extranjera), como sistémico a una dosis óptima de 300mg/m2/día. Durante el tratamiento los pacientes deben seguir un riguroso control analítico de los niveles de triglicéridos y hormonas tiroideas principalmente. El bexaroteno produce hipertrigliceridemia, a veces importante, por lo que hay que instaurar tratamiento preventivo la semana previa al inicio del tratamiento con estatinas o fenofibrato, pero no con gemfibrozilo ya que eleva los niveles de bexaroteno en sangre, probablemente por inhibición del citocromo P450. El hipotiroidismo es otro efecto secundario frecuente que se controla con la administración de hormona tiroidea. El bexaroteno puede combinarse con otros tratamientos como PUVA o IFN-α y también se utiliza como mantenimiento tras terapias más agresivas en estadios avanzados. Como el resto de los retinoides exige medidas anticonceptivas por el riesgo de malformaciones56–61.
Interferón alfaSe utiliza como monoterapia en dosis subcutáneas (también se puede utilizar intramuscular o intralesional) de 3-20 millones U diarias, 3 días por semana, con buena respuesta (dosis-dependiente) especialmente en estadios iniciales (tasa de RG alrededor del 70%) o en combinación con otras terapias como PUVA (parece la asociación más eficaz), retinoides o análogos de las purinas (fludarabina) con beneficio aparente (faltan estudios que los comparen con IFN-α solo). Sus efectos secundarios incluyen síndrome seudogripal, alteraciones gastrointestinales, depresión de la médula ósea y elevación de transaminasas. En pacientes con buena respuesta y riesgo de recaída se puede utilizar durante años con dosis de mantenimiento, con riesgo de desarrollar enfermedades autoinmunes como diabetes mellitus, tiroiditis o anemia hemolítica62–64.
InmunotoxinasEl denileukindiftitox (DAB389-interleucina 2 [IL-2]) es la primera citotoxina de fusión aprobada por la FDA para el tratamiento de los LCCT65,66. Actúa como una citotoxina específica para células que presentan el receptor de la IL-2. Se obtiene mediante la fusión de genes del receptor de IL-2 humana con las secuencias citotóxicas de la toxina diftérica para Escherichia coli. Se une al receptor de la IL-2 (CD25) de los linfocitos T, inhibiendo la síntesis de proteínas. Se utiliza por vía intravenosa a dosis de 9 o 18mg/kg/día en ciclos de 5 días cada 3 semanas, y se ha visto que es especialmente eficaz en MF en estadio IIB (tasa de respuesta del 38%). El 60-70% de los pacientes presentaron un síndrome seudogripal transitorio, similar al que aparece con el IFN-α, habiéndose descrito otros efectos secundarios como urticaria, anafilaxia o «vascular leak syndrome». Algunos desarrollaron anticuerpos anti-DAB389 o anti-IL-2 en el primer ciclo, pero sin correlación con la toxicidad ni la respuesta. En estudios recientes67,68 se ha visto que su eficacia aumenta con el uso concomitante con bexaroteno oral, especialmente en pacientes con expresión baja o nula del receptor de la IL-2, permitiendo el uso de dosis menores de ambos tratamientos. Se ha utilizado también en otros LCCT no MF, en monoterapia69 o en combinación con radioterapia70.
Anticuerpos monoclonalesAlemtuzumabEs un anticuerpo monoclonal humanizado dirigido contra la glucoproteína CD52 expresada en la superficie de linfocitos T y B, células NK y, en menor grado, en monocitos y macrófagos. Su mecanismo de acción, no del todo conocido, es llevado a cabo por lisis celular directa mediada por complemento y también por citotoxicidad dependiente de anticuerpos y apoptosis. En 2003 se demostró su utilidad en el tratamiento de 22 pacientes con MF/SS pretratados, la mayoría de ellos en estadios avanzados (86%≥estadio III y 36% con síntomas B) y en mal estado general. La tasa de RG obtenidas fue del 55% (32% RC) y la duración media de las mismas fue de 12 meses71. Recientemente han sido reproducidos estos buenos resultados72. Las citopenias inducidas por alemtuzumab son la complicación potencialmente más grave observada. Aunque pueden desarrollarse distintos grados de anemia y/o trombopenia, por mecanismos no bien conocidos, la linfopenia (T y B) es universal en todos los pacientes, predisponiéndolos73 a infecciones graves por microorganismos oportunistas (sobre todo citomegalovirus y Pneumocystis jirovecii). Alemtuzumab parece74,75 especialmente útil en el control del prurito incoercible de las formas eritrodérmicas (SS).
ZanolimumabEs otro anticuerpo monoclonal dirigido contra el receptor CD4 expresado en linfocitos T y macrófagos. Interfiere en la activación de células T al impedir la interacción de CD4 con moléculas de clase II del complejo mayor de histocompatibilidad y además, produce lisis celular por citotoxicidad mediada por anticuerpos y no por complemento como alemtuzumab76,77. Zanolimumab ha demostrado su eficacia en 2 estudios multicéntricos fase II78 sobre 47 pacientes con LCCT intensamente pretratados, persistentes y refractarios (38 MF y 9 SS). Los brazos de utilización de dosis altas de zanolimumab (560mg/semana para estadios precoces [MF, estadios IB-IIA] y 980mg/semana para estadios avanzados [MF, estadios IIB-IVB y SS]) alcanzaron una tasa de RG del 56% con una espectacular duración media de la misma de 81 semanas (especialmente en las MF). Zanolimumab presenta, globalmente, un perfil de seguridad aceptable con moderados efectos secundarios como dermatitis, eccemas o infecciones limitadas a la piel y al tracto respiratorio superior pese a la profunda depleción de células CD4 que produce su uso. No se observaron diferencias en la incidencia de infecciones entre los distintos grupos de dosis. Pese a observarse un descenso más acentuado de las células CD4 en los grupos de dosis altas (560-980 vs 280mg/semana) sorprendentemente, no se observaron diferencias en la recuperación de las mismas una vez finalizado el tratamiento. Basado en estos hallazgos actualmente está siendo llevado a cabo un estudio pivotal, en fase III.
RituximabEs un anticuerpo monoclonal anti-CD20 quimérico (humano-murino) utilizado principalmente como tratamiento del linfoma B no Hodgkin sistémico como monoterapia o en terapia combinada. Se ha descrito el uso eficaz por vía intralesional en pacientes con LCCB (zona marginal y centrofolicular) en varios estudios45,46,79,80. Sería especialmente útil en pacientes con lesiones múltiples o con gran tendencia a la recidiva, así como en zonas donde queramos evitar las secuelas antiestéticas de cirugía y/o radioterapia. También se utiliza en combinación con CHOP para el LCCB leg-type.
Inhibidores de histonas desacetilasasLas histonas son proteínas presentes en grandes cantidades en el núcleo celular que, junto con otras proteínas «no histónicas» y el ADN, forman la cromatina de las células eucariotas. En los últimos años se han desarrollado varias moléculas81,82, encuadradas dentro del grupo farmacológico de los inhibidores de las histonas desacetilasas (IHDAC) debido a que distintas observaciones experimentales muestran que en la mayoría de los cánceres hay hipoacetilación de las histonas. Cuatro IHDAC han sido estudiados en el tratamiento de LCCT: vorinostat, romidepsin, panobinostat y belinostat.
VorinostatEstá autorizado83 por la FDA para el tratamiento de las manifestaciones cutáneas de pacientes con LCCT que se han mostrado persistentes, progresivas o recurrentes tras al menos 2 tratamientos sistémicos, pero no se ha comercializado en Europa. Esta indicación fue establecida tras un estudio84 en fase II sobre 74 pacientes con MF/SS, la mayoría de ellos en estadios avanzados (≥IIB: 61 pacientes, SS: 30 pacientes, y/o con enfermedad tumoral: 22 pacientes). Todos ellos habían sido tratados intensamente (96% con bexaroteno, 63% con IFN-α, 61% con quimioterapia, 36% con fotoféresis y 31% con denileukindiftitox). La dosis administrada fue de 400mg/día, vía oral, y se ajustó o suspendió según la toxicidad o los efectos secundarios observados. Globalmente alcanzaron respuesta al tratamiento el 29,7% de todos los pacientes y el 29,5% de los pacientes en estadios avanzados (IIB o superior). También alcanzaron respuesta el 33,3% de pacientes con SS. Vorinostat fue generalmente bien tolerado y los efectos adversos observados más frecuentemente fueron gastrointestinales (náuseas, diarrea), constitucionales (astenia, anorexia y pérdida de peso) y citopenias (trombocitopenia y anemia). No se observó neutropenia. Menos del 15% de los pacientes requirieron una reducción de la dosis de vorinostat y el 11% de ellos presentaron efectos adversos graves, fundamentalmente fenómenos tromboembólicos. Solamente fue observada prolongación en el QT en 3 pacientes.
Estudios recientes están utilizándolo en tratamiento combinado con otras terapias: bexaroteno85 o IFN-α86.
RomidepsinEs un nuevo y potente IHDAC que ha sido utilizado en pacientes con LCCT y linfomas T periféricos. Varios estudios87–90 han demostrado su utilidad: RG obtenida en el 41% de los pacientes (7% de respuestas completas, 33% respuestas parciales), 14,9 meses de mediana de duración de respuesta y 8,3 meses de mediana de tiempo a la progresión. Los efectos adversos más frecuentemente encontrados fueron náuseas, astenia y vómitos. Solo se observaron efectos adversos ≥grado 3 en el 33% de los pacientes. Los efectos adversos graves más frecuentes fueron progresión de la enfermedad (6%), fiebre (3%), sepsis (2%), síndrome de lisis tumoral (2%) e hipotensión (2%). Seis pacientes fallecieron, uno de ellos posiblemente en relación con el tratamiento. Solamente se observó alargamiento del QT en el 2% de los pacientes (fueron excluidos del estudio pacientes con «anormalidades cardíacas significativas» y/o en tratamiento con prolongadores del QT o fármacos inhibidores del citocromo P3A4).
PanobinostatEs un nuevo IHDAC que no solo produce acetilación en las histonas sino también inducción de p21, parada del ciclo celular, apoptosis y acetilación de HSP90 (pan-IHDAC). Su utilidad y perfil de seguridad han sido mostrados recientemente en un estudio91 en fase II realizado en 40 pacientes con LCCT refractarios al menos a 2 tratamientos previos (la media fue de 5 tratamientos/paciente): se administraron 20mg/día de panobinostat oralmente los días 1, 3 y 5 de cada semana hasta progresión de la enfermedad o intolerancia, con pobre respuesta: en pacientes tratados anteriormente con bexaroteno (grupo 1: 25 pacientes) se obtuvieron 3 RP y 4 estabilizaciones de la enfermedad, así como progresión en otros 3 pacientes. Otros 30 pacientes no fueron evaluables por escaso seguimiento en el momento de la publicación. Los efectos adversos observados más frecuentemente fueron: diarrea, trombocitopenia, fatiga, astenia, hipertrigliceridemia, alteraciones en el gusto, náuseas y prurito (15% de todos los pacientes). No se observaron alargamientos significativos en el QT.
BelinostatEs también un pan-IHDAC que ha sido probado en un estudio92 en fase II que incluyó 29 pacientes (15 MF, 7 SS, 5 no MF/SS y 2 no categorizados). Se administraron 1000mg/m2 en una infusión intravenosa de 30 min desde el 1 al 5 de cada ciclo, cada 3 semanas. Diecisiete pacientes estabilizaron su enfermedad con una duración superior a los 127 días y se obtuvieron 2 RP y 2 RC con una duración mediana de la respuesta de 273 días. Es importante destacar que el tiempo para la obtención de respuesta fue muy corto: 16 días (extremos 14-35 días) con mejoría importante del prurito. No se observó toxicidad hematológica grado 4 en ningún caso ni prolongación del QT de grado 3. Se observaron 4 efectos adversos de grado 3-4: prurito, eritema, edema e íleo adinámico.
OtrosBortezomibFármaco indicado en el tratamiento de primera línea en pacientes con mieloma múltiple no candidatos a trasplante de progenitores hematopoyéticos y en pacientes en recaída tras un tratamiento previo. El Grupo del Instituto Hematológico de la Universidad de Bolonia ha obtenido en un estudio93 en fase II sobre 12 pacientes (10 MF avanzadas y 2 linfomas T periféricos con participación cutánea aislada), una tasa de RG del 67% que incluyó 2 RC (17%) y 6 RP (50%). Las MF obtuvieron una RC (10%) y los linfomas T periféricos también una RC (50%). La duración de la RC en el paciente con MF fue superior al año tras la finalización del tratamiento y en la del linfoma T periférico se observó la recaída 10 meses después. Bortezomib se utilizó siguiendo el mismo esquema que el usado en mieloma múltiple: 1,3mg/m2, intravenoso, los días 1, 4, 8 y 11 de cada ciclo de 21 días hasta un total de 6 ciclos. Los efectos adversos observados con más frecuencia fueron neutropenia (2 pacientes/17%, grado 3 WHO), trombopenia (2 pacientes/17%, grado 3 WHO) y neuropatía sensorial (2 pacientes/17%, grado 3 WHO). No hubo infecciones durante el tratamiento y no se produjeron muertes asociadas al mismo. La base racional de utilización de bortezomib94 es su capacidad de inhibir el factor nuclear κB (NF-κB), constitutivamente activado en líneas celulares de LCCT, e inducir apoptosis. NF-κB es un factor transcripcional implicado en la generación de respuestas inflamatorias, regulación del ciclo celular y protección frente a la apoptosis.
LenalidomidaSus efectos antitumorales son atribuibles a varios mecanismos de acción: inhibe la producción de mediadores proinflamatorios por los monocitos (TNF-α, IL-1, IL-6, IL-12), facilita la producción de IL-2 e IFN-( por linfocitos T, y potencia la actividad citotóxica de estas citocinas y de células NK. Se ha realizado un estudio95 en fase II que ha usado lenalidomida a dosis de 10-25mg/día, durante 21 días en ciclos de 28 días, en 25 pacientes con LCCT ampliamente pretratados (media de 6 regímenes previos). Siete pacientes obtuvieron una RP tras recibir una media de 9 ciclos de tratamiento. Los efectos adversos observados con más frecuencia fueron anemia, descamación, prurito y edema de extremidades inferiores. En el grupo de alta dosis se observó neutropenia intensa en 2 pacientes y en uno se suspendió el tratamiento por disartria.
QuimioterapiaLa quimioterapia en el tratamiento de los LCCT debe reservarse para los estadios avanzados de la enfermedad, ya que en los estadios iniciales no presenta mayor eficacia que los tratamientos conservadores. Prácticamente todos los agentes quimioterápicos utilizados para linfomas sistémicos se han aplicado en los LCCT avanzados: agentes alquilantes, metotrexato (MTX), cisplatino, etopóxido, bleomicina, vinblastina, ciclofosfamida… No está claro que ninguno sea superior y generalmente las respuestas son de corta duración. La combinación más efectiva, y por tanto la más utilizada, es ciclofosfamida, vincristina y prednisona con (CHOP) o sin doxorrubicina (CVP), pero no existen estudios aleatorizados que demuestren un aumento de la supervivencia con ninguna pauta.
MetotrexatoEs de primera elección en los LCCT CD30+96, especialmente en pacientes con múltiples lesiones (en lesiones solitarias la radioterapia sería mejor alternativa). En algunos casos se requieren dosis altas semanales para conseguir la RC, con mayor riesgo de efectos secundarios.
Recientemente 2 quimioterápicos han demostrado especial utilidad como monoterapia:
GemcitabinaEs un antimetabolito pirimidínico indicado en tumores sólidos clásicamente resistentes a tratamientos convencionales como cáncer de pulmón, ovario, páncreas y vejiga urinaria. Su utilidad en linfomas cutáneos ha sido probada en 2 estudios. El primero97 de ellos se trata de una serie de 32 pacientes (la mayoría con MF) y obtiene unas tasas de RC del 22% (7 pacientes/32) y de RP del 53% (17 pacientes/32). Desafortunadamente utiliza criterios estándar para la evaluación de la respuesta como si se tratara de formas comunes de linfomas no hodgkinianos y no específicamente de linfomas cutáneos (SWAT). El 73% de las MF (26 pacientes) obtuvieron algún tipo de respuesta: el 23% RC y el 50% RP. No respondió el único paciente incluido con SS. La duración mediana de la RC fue de 10 meses (extremos 4–22 meses). La gemcitabina se administró en perfusión intravenosa a dosis de 1.200mg/m2 durante 30 min, en ciclos de 28 días (total de 6 ciclos), los días 1, 8 y 15 de cada ciclo. Los efectos adversos observados con mayor frecuencia fueron las citopenias. La hepatotoxicidad reversible fue el efecto adverso no hematológico más frecuentemente observado (13 pacientes, 40%). No se produjo ninguna muerte atribuida al medicamento. El segundo estudio98 es una serie de 33 pacientes, la mayoría MF intensamente tratadas (mediana de 5 esquemas de tratamientos previos) (31 pacientes) y 2 pacientes con linfoma anaplásico T CD30+. La dosis de gemcitabina fue menor que la del trabajo precedente (1.000mg/m2) pero su esquema de administración y número de ciclos administrados fue el mismo. La evaluación de la respuesta se realizó sobre variables que incluyeron el área cutánea afecta, tamaño de los ganglios linfáticos y citometría de flujo de sangre periférica. Se obtuvo respuesta en el 68% de los pacientes (2 RC). La mielosupresión fue el efecto adverso más frecuentemente observado (grado 3 en 8 pacientes/33) y característicamente fueron diagnosticados 2 síndromes hemolíticos urémicos en sendos pacientes afectos de SS. Otros efectos adversos fueron: elevación de las transaminasas hepáticas, mucositis, letargia, fiebre, hiperpigmentación, erupción maculopapular relacionada con la infusión y varios eventos cardiovasculares. Otro estudio multicéntrico más reciente99 muestra resultados en cuanto a respuesta superponibles a los comentados con anterioridad, pero con un perfil significativamente más tóxico.
Doxorrubicina liposomal pegiladaTiene indicación autorizada para el tratamiento del cáncer de ovario avanzado, mieloma múltiple en recaída tras trasplante de progenitores hematopoyéticos y en el sarcoma de Kaposi asociado con sida. La utilidad de la doxorrubicina liposomal pegilada (DOX-PEG) también ha sido demostrada en el tratamiento de pacientes con LCCT en estudios observacionales y retrospectivos. Recientemente un estudio prospectivo y multicéntrico100 ha analizado su uso sobre 25 pacientes afectos de MF y/o SS en estadios ≥II refractarios al menos a 2 líneas de tratamiento previo y en pacientes con LCCT de células grandes CD30+. La DOX-PEG fue utilizada cada 4 semanas a dosis de 40mg/m2/día administrada por vía intravenosa hasta 8 ciclos. Se obtuvo una tasa de RG objetiva del 56% (14 pacientes/25, 5 RC y 9 RP). En 10 pacientes con SS se observó un alto grado de respuesta (60%, 6 pacientes/10) incluyendo una RC. También se observó un importante grado de respuesta en LCCT que habían sufrido transformación, con un 50% de repuestas que incluyeron una RC. En general se observaron más efectos adversos que en los estudios precedentes, con 4 episodios de infecciones graves y algún evento cardíaco. DOX-PEG ha mostrado también una gran actividad en 5 LCCB (uno de la zona marginal y 4 linfomas difusos de células grandes «leg-type») en un estudio piloto italiano101 en fase II (dosis de 20mg/m2 cada 3 o 4 semanas) obteniendo una impresionante tasa de RC prolongada en 4 de ellos (80%). También han sido comunicados recientemente102 excelentes resultados con DOX-PEG asociada a bleomicina, vinblastina y dacarbacina (esquema CBVD) en 37 pacientes con LCP avanzados tanto de estirpe T (19 pacientes) como B (18 pacientes) obteniendo una tasa de RC del 88,8% y del 100% respectivamente. En el grupo de los LCCT se administraron entre 4 y 6 ciclos de CBVD y en los LCCB entre 2 y 6 (se añadió rituximab al esquema: R-CBVD). Su perfil de seguridad fue muy aceptable. En 3 pacientes (2 LCCT y un LCCB) se realizaron con posterioridad sendos trasplantes alogénicos de progenitores hematopoyéticos.
Otros quimioterápicosForodesinaEs un análogo de las purinas, inhibidor de la purina-nucleósido-fosforilasa. En enero de 2010 acabó el reclutamiento para un estudio pivotal, fase II, sobre pacientes con MF/SS con enfermedad refractaria en estadios ≥IB. Los resultados preliminares de este estudio multicéntrico han sido comunicados recientemente103. La tasa de respuesta global oscila alrededor de un 30%. Los efectos adversos más frecuentemente observados fueron náuseas, cansancio, edemas, disnea y cálculos urinarios.
PralatrexatoLa citotoxicidad inducida por pralatrexato (PTX) puede ser 10 veces superior a la del MTX y capaz de vencer resistencias tumorales adquiridas. PTX ha mostrado104,105 actividad en linfomas T avanzados y se presenta como un fármaco prometedor para tratamientos de mantenimiento en LCCT.
Trasplante de células precursorasEl trasplante autólogo de células precursoras consigue altas tasas de respuesta pero con recaídas inmediatas (tiempo medio hasta la recaída<100 días), por lo que solo resulta útil en algunos pacientes para mejorar su calidad de vida o como medida para ganar tiempo antes de pasar a otras terapias106,107.
El trasplante alogénico de células precursoras ha conseguido108,109 RC de larga duración, aunque con una elevada mortalidad (20%) debida principalmente a la enfermedad injerto contra huésped. Precisamente su eficacia se relaciona con esta reacción, en lo que se llama la reacción injerto contra linfoma110 en la que los linfocitos del donante «atacan» a los linfocitos tumorales del receptor, consiguiendo eliminarlos. Actualmente se trabaja con protocolos que utilizan regímenes no mieloablativos pero citorreductores previos al trasplante, en un intento de mejorar la respuesta y reducir las complicaciones. Un estudio reciente111 apoya el papel de este tratamiento en la MF tumoral (IIB) y el SS. Los porcentajes de supervivencia son significativamente superiores en pacientes en segunda RC, RP o progresión con 3 o menos líneas de terapia sistémica previa, por lo que es conveniente no demorar este tratamiento en el curso de la enfermedad. Posiblemente a corto plazo sea el único tratamiento «curativo» de la enfermedad.
ConclusionesEn la actualidad la meta en el tratamiento de los LCP es evitar la progresión a estadios más avanzados de la enfermedad, ya que por el momento no hay un tratamiento curativo. No existen estudios comparativos entre los distintos tratamientos sistémicos en pacientes con LCP avanzados, por lo que el tratamiento en estos pacientes no está en absoluto protocolizado. Hay todavía mucha controversia112,113 en el manejo de esta patología, por lo que se recomienda una actitud conservadora («start low and go slow»). Se resumen en las tablas 2–8 las recomendaciones de consenso EORTC20,46 de tratamiento así como de estadiaje. Las recomendaciones EORTC de tratamiento para los LCCT20 deberían revisarse a la luz de las nuevas terapias emergentes.
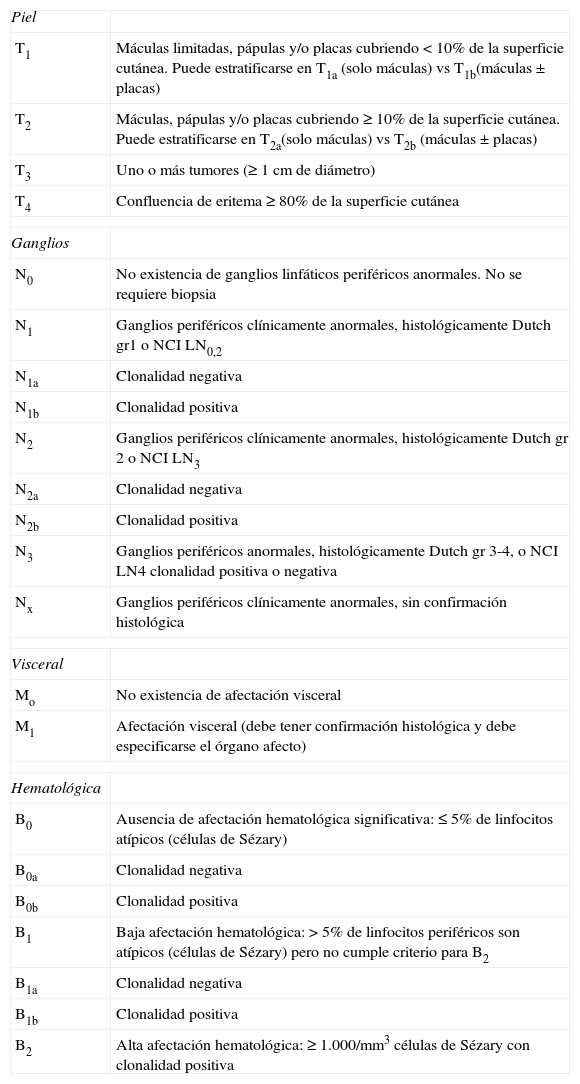
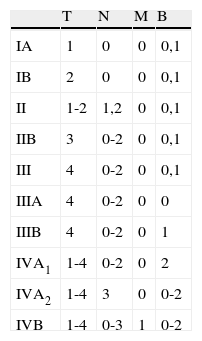
Estadiaje TNMB para la MF/SS
| Piel | |
| T1 | Máculas limitadas, pápulas y/o placas cubriendo <10% de la superficie cutánea. Puede estratificarse en T1a (solo máculas) vs T1b(máculas±placas) |
| T2 | Máculas, pápulas y/o placas cubriendo ≥10% de la superficie cutánea. Puede estratificarse en T2a(solo máculas) vs T2b (máculas±placas) |
| T3 | Uno o más tumores (≥1cm de diámetro) |
| T4 | Confluencia de eritema ≥80% de la superficie cutánea |
| Ganglios | |
| N0 | No existencia de ganglios linfáticos periféricos anormales. No se requiere biopsia |
| N1 | Ganglios periféricos clínicamente anormales, histológicamente Dutch gr1 o NCI LN0,2 |
| N1a | Clonalidad negativa |
| N1b | Clonalidad positiva |
| N2 | Ganglios periféricos clínicamente anormales, histológicamente Dutch gr 2 o NCI LN3 |
| N2a | Clonalidad negativa |
| N2b | Clonalidad positiva |
| N3 | Ganglios periféricos anormales, histológicamente Dutch gr 3-4, o NCI LN4 clonalidad positiva o negativa |
| Nx | Ganglios periféricos clínicamente anormales, sin confirmación histológica |
| Visceral | |
| Mo | No existencia de afectación visceral |
| M1 | Afectación visceral (debe tener confirmación histológica y debe especificarse el órgano afecto) |
| Hematológica | |
| B0 | Ausencia de afectación hematológica significativa: ≤5% de linfocitos atípicos (células de Sézary) |
| B0a | Clonalidad negativa |
| B0b | Clonalidad positiva |
| B1 | Baja afectación hematológica: >5% de linfocitos periféricos son atípicos (células de Sézary) pero no cumple criterio para B2 |
| B1a | Clonalidad negativa |
| B1b | Clonalidad positiva |
| B2 | Alta afectación hematológica: ≥1.000/mm3 células de Sézary con clonalidad positiva |
En sangre, las células de Sézary se definen como linfocitos de núcleo cerebriforme, hiperconvoluto. Si no es posible utilizar la determinación de células de Sézary para establecer el nivel tumoral B2, entonces puede utilizarse uno de los siguientes criterios modificados de la ISCL junto con un reordenamiento clonal positivo del TCR: 1) expansión CD4+ o CD3+ con un cociente CD4/CD8 de 10 o más; 2) expansión de CD4+ con inmunofenotipo anormal incluyendo pérdida de CD7 o CD26.
La clonalidad de células T se define por medio del análisis por PCR o southern blot del gen del receptor de células T.
Dutch: criterios establecidos por el Grupo Holandés de Linfomas Cutáneos; ISCL: Internacional Society of Cutaneous Lymphoma (Sociedad Internacional de Linfomas cutáneos); TCR: receptor de linfocito T.
Clasificación TNM para los linfomas no MF/no SS
| TT1: lesión cutánea únicaT1a: lesión única<5cm de diámetroT1b: lesión única>5cm diámetroT2: lesiones cutáneas múltiples en una zona del cuerpo o en 2 zonas contiguasT2a: todas las lesiones localizadas en un área <15cm de diámetroT2b: todas las lesiones localizadas en un área >15cm y<30cm de diámetroT2c: todas las lesiones localizadas en un área >30cm de diámetroT3: afectación cutánea generalizadaT3a: lesiones múltiples afectando 2 zonas del cuerpo no contiguasT3b: lesiones múltiples afectando más de 3 zonas del cuerpo |
| NN0: afectación ganglionar clínica o histológicaN1: afectación de una región ganglionar periférica a la que drene la zona de la lesión cutáneaN2: afectación de 2 o más regiones ganglionares periféricas o cualquier región ganglionar que no drene la zona de la lesión cutáneaN3: afectación de ganglios no periféricos |
| MM0: no evidencia de enfermedad extracutáneas no ganglionarM1: afectación extracutánea no ganglionar |
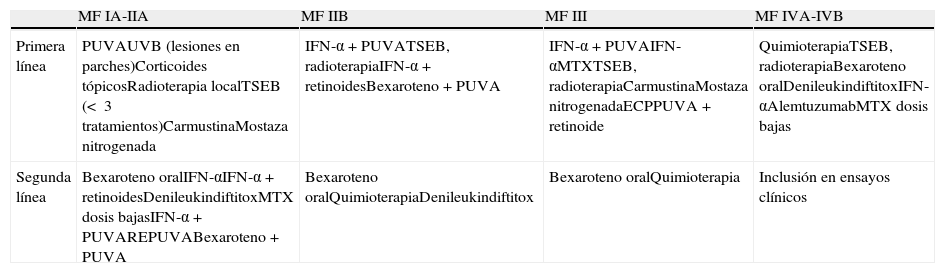
Recomendaciones EORTC para el tratamiento de MF
| MF IA-IIA | MF IIB | MF III | MF IVA-IVB | |
| Primera línea | PUVAUVB (lesiones en parches)Corticoides tópicosRadioterapia localTSEB (< 3 tratamientos)CarmustinaMostaza nitrogenada | IFN-α+PUVATSEB, radioterapiaIFN-α+retinoidesBexaroteno+PUVA | IFN-α+PUVAIFN-αMTXTSEB, radioterapiaCarmustinaMostaza nitrogenadaECPPUVA+retinoide | QuimioterapiaTSEB, radioterapiaBexaroteno oralDenileukindiftitoxIFN-αAlemtuzumabMTX dosis bajas |
| Segunda línea | Bexaroteno oralIFN-αIFN-α+retinoidesDenileukindiftitoxMTX dosis bajasIFN-α+PUVAREPUVABexaroteno+PUVA | Bexaroteno oralQuimioterapiaDenileukindiftitox | Bexaroteno oralQuimioterapia | Inclusión en ensayos clínicos |
ECP: fotoféresis extracorpórea; IFN-α: interferón alfa; MTX: metotrexato; PUVA: psoralenos+ ultravioleta A; TSEB: irradiación corporal total con electrones; UVB: ultravioleta B.
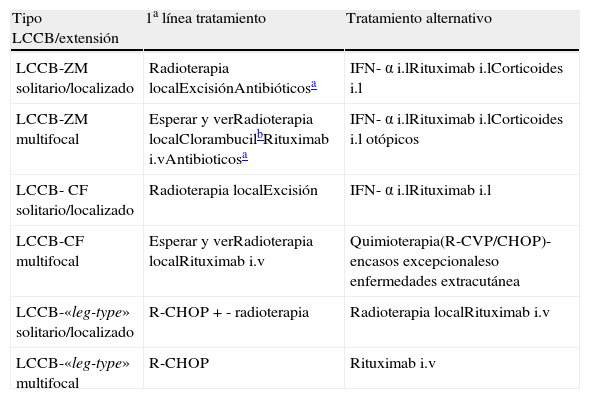
Recomendaciones EORTC para el tratamiento de LCCB
| Tipo LCCB/extensión | 1a línea tratamiento | Tratamiento alternativo |
| LCCB-ZM solitario/localizado | Radioterapia localExcisiónAntibióticosa | IFN- α i.lRituximab i.lCorticoides i.l |
| LCCB-ZM multifocal | Esperar y verRadioterapia localClorambucilbRituximab i.vAntibioticosa | IFN- α i.lRituximab i.lCorticoides i.l otópicos |
| LCCB- CF solitario/localizado | Radioterapia localExcisión | IFN- α i.lRituximab i.l |
| LCCB-CF multifocal | Esperar y verRadioterapia localRituximab i.v | Quimioterapia(R-CVP/CHOP)- encasos excepcionaleso enfermedades extracutánea |
| LCCB-«leg-type» solitario/localizado | R-CHOP+- radioterapia | Radioterapia localRituximab i.v |
| LCCB-«leg-type» multifocal | R-CHOP | Rituximab i.v |
CHOP: ciclofosfamida, vincristina, prednisona y doxorrubicina; CVP: ciclofosfamida, vincristina y prednisona; IFN-α: interferón alfa; i.l: intralesional; i.v: intravenoso.
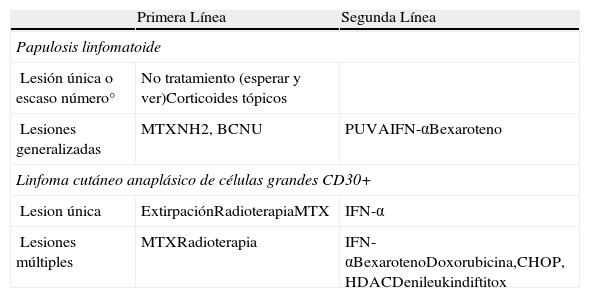
Tratamiento LCCT CD30+
| Primera Línea | Segunda Línea | |
| Papulosis linfomatoide | ||
| Lesión única o escaso número° | No tratamiento (esperar y ver)Corticoides tópicos | |
| Lesiones generalizadas | MTXNH2, BCNU | PUVAIFN-αBexaroteno |
| Linfoma cutáneo anaplásico de células grandes CD30+ | ||
| Lesion única | ExtirpaciónRadioterapiaMTX | IFN-α |
| Lesiones múltiples | MTXRadioterapia | IFN-αBexarotenoDoxorubicina,CHOP, HDACDenileukindiftitox |
BCNU: carmustina; CHOP:- ciclofosfamida, vincristina, prednisona y doxorrubicina; HDAC: Inhibidores de histonas desacetilasas; IFN-α: interferon alfa; MTX: metotrexato; NH2: mostaza nitrogenada; PUVA: psoralenos+ ultravioleta A.
Los autores declaran no tener ningún conflicto de intereses.