A pesar de la gran cantidad de productos disponibles producidos por la industria farmacéutica, hoy en día la formulación magistral sigue teniendo un papel muy importante en el tratamiento de las afecciones dermatológicas. Desde los inicios de la Dermatología se ha usado, siendo muy útil en el tratamiento de enfermedades para las que no se disponía de preparados farmacéuticos específicos; sin embargo, a medida que fueron apareciendo nuevos productos comercializados se puso en duda la utilidad de la formulación, cuestionando su seguridad, estabilidad y efectividad. Esto contrasta con la tendencia actual de recuperar la formulación, haciendo que vuelva a ocupar su lugar en la práctica dermatológica habitual. En el presente artículo revisamos las patologías en las que se usa con más frecuencia la formulación, sus utilidades e inconvenientes, la legislación actual al respecto en nuestro ámbito, aportando las últimas novedades descritas en cuanto a vehículos y principios activos disponibles.
Compounding continues to play a key role in the treatment of skin conditions, despite the abundance of products made by the pharmaceutical industry. Right from the earliest days of dermatology, compounding proved very useful in the treatment of diseases for which no specific drugs were available. However, as new products came onto the market, this usefulness was called into question, and doubts over safety, stability, and effectiveness were raised. Today, compounding is regaining the place it once held in routine dermatological practice. We review the advantages and disadvantages of compounding, the most common indications, current legislation in our setting, and the latest developments in active ingredients and vehicles.
Durante unos años existió, en determinados ambientes profesionales y ante la industrialización a gran escala del medicamento, la duda sobre si la formulación tenía aún razón de existir. Es más, en algunos casos se cometió el error de asociar formulación con praxis antigua de la Medicina.
No cabe duda de que el desarrollo industrial de los medicamentos ha contribuido a una medicina más universalizada y ha permitido un desarrollo considerable de la investigación y de las mejoras en la prestación farmacológica. Sin embargo, la industrialización provoca también un cierto grado de «despersonalización» del medicamento que pasa a ser concebido y desarrollado con un criterio «estadístico», que se ajusta al estándar de la patología, pero no a las características personales de cada paciente. En el medicamento industrial es el paciente el que «se adapta» al medicamento (dosis fijas y formas farmacéuticas limitadas), frente al medicamento personalizado donde es el medicamento el que «se adapta» al grado de patología y características personales del paciente1.
Las dos últimas décadas han puesto claramente de manifiesto que, si bien el medicamento industrial llega a casi todos los ámbitos de la terapéutica, en cada uno de estos ámbitos no resuelve todas las situaciones terapéuticas personalizadas en cuanto a dosis, formas farmacéuticas, vehículos o adaptación del medicamento a la clínica concreta del paciente. Es aquí donde el medicamento personalizado muestra su valor en la terapéutica actual: como una herramienta para complementar u optimizar el medicamento industrial. Así lo reconocen las modernas farmacopeas como la estadounidense (USP), que en el encabezamiento de su monografía 795, dedicada a la formulación, afirma: «La formulación (compounding) es fundamental en la farmacia práctica y es imprescindible para un adecuado sistema de protección de la salud»2. Esta cualidad de ser imprescindible se refiere a que, sin el medicamento personalizado, muchas problemáticas particulares de adecuada administración de fármacos quedarían por resolver.
Esta utilidad del medicamento personalizado no ha sido puesta en entredicho en muchos países europeos como Alemania u Holanda, donde sigue representando un 3-4% con respecto al volumen total de medicamentos dispensados en la farmacia. En el ámbito de la Dermatología la proporción es superior. Otros países que en su momento adoptaron criterios muy restrictivos con respecto a la formulación, como Francia o Estados Unidos, rectificaron luego su posición para dar cabida al medicamento personalizado.
Utilidades de la formulación y su calidadEste planteamiento personalizador de la formulación y complementario al medicamento industrial viene refrendado por 2 documentos de gran interés publicados en el último año 2 dos importantes instituciones:
- 1.
El Consejo de Europa que publica su resolución CM/ResAP (2011), de 1 de enero de 2011 sobre las exigencias relativas a la garantía de calidad y de inocuidad de los medicamentos preparados en las farmacias para las necesidades especiales de los pacientes3.
- 2.
El Consejo General de Colegios de Farmacéuticos de España, que en noviembre de 2010 publica el documento La formulación magistral: una opción de futuro en España, que es la primera reevaluación sobre la actividad realizada en los últimos 25 años1.
En el preámbulo del documento del Consejo de Europa se exponen unos criterios sobre el valor añadido de la formulación y su utilidad terapéutica, que se recogen en la tabla 1.
Criterios del documento del Consejo de Europa3
| - Los medicamentos fabricados por la industria no siempre están autorizados o disponibles para cubrir las necesidades especiales de cada paciente |
| - La preparación de medicamentos en las farmacias, que puede ser necesaria como consecuencia de la situación personal y cuadro médico del paciente, sobre todo en ausencia de determinados productos, es indispensable para satisfacer las necesidades especiales de los pacientes individuales en Europa |
| - Hay que considerar el valor añadido que deben tener las preparaciones en farmacia con respecto a los productos comercializados |
| - Los medicamentos preparados en farmacia es necesario que cumplan con criterios apropiados y específicos de calidad, seguridad y valor añadido |
El documento del Consejo General de Colegios de Farmacéuticos reevalúa el sentido y orientación de la formulación en las líneas antes expuestas. Tiene un gran interés, entre otros aspectos por ser el primer documento actual que especifica con claridad las utilidades terapéuticas reconocidas de la formulación. Estas utilidades se resumen en la tabla 2, y aunque están hechas con una visión general, luego veremos que tienen una gran aplicación en la formulación dermatológica.
Utilidades reconocidas de la formulación. Consejo General de Colegios de Farmacéuticos1
| 1. Cubrir lagunas terapéuticas |
| 1.1. Formas farmacéuticas no comercializadas (vía oral y vía tópica): es la situación de un gran número de fármacos, que afectan a población infantil y adolescente, para los que hay que recurrir a elaborar soluciones y suspensiones. |
| 1.2. Dosificaciones diferentes a las comercializadas. |
| 1.3. Enfermedades raras. |
| 2. Situaciones de desabastecimiento y retirada de fármacos |
| Es el caso del 5-fluorouracilo tópico, de primera elección todavía, y retirado del mercado, o situaciones de desabastecimiento que han afectado a pilocarpina oral, sulfona oral o clorfeniramina inyectable, entre otros. La formulación permite un acceso más rápido al fármaco que otras vías7. |
| 3. Facilitar la administración del fármaco al paciente |
| - Modificar caracteres organolépticos que faciliten la administración |
| - Preparados con escaso tiempo de estabilidad (por ejemplo, permanganato potásico y eosina) |
| - Asociación de varios principios activos en una misma forma farmacéutica, como en patologías superpuestas |
| - Optimizar la cantidad de tratamiento con respecto a la duración del mismo y a la extensión del proceso a tratar |
| - Desarrollo de formulaciónes para grupos reducidos de pacientes, subindicaciones terapéuticas o “áreas huérfanas en terapéutica”, para quienes la industria farmacéutica no desarrolla productos |
| 4. Eliminar o sustituir excipientes (alergias, interacciones, poca tolerancia). |
| 5. Individualizar la composición del tratamiento. Este sería el núcleo de la formulación en Dermatología y existen tres pasos a seguir: |
| 5.1. Graduar dosificación de principios activos |
| El rango de dosificación es propio de cada principio activo. En unos casos es muy amplio, como el ácido retinoico (0,01-0,3%), y en otros más ajustado como la triamcinolona acetónido (0,05-0,2%) |
| 5.2. Asociar otros principios activos si corresponde |
| Son muchas las asociaciones descritas de utilidad terapéutica y con sinergia entre principios activos, habiendo estudios que avalan dichas asociaciones |
| 5.3. Seleccionar el vehículo adecuado |
| 6. Reducir el riesgo de posibles reacciones adversas |
| 7. Atender un gran número de situaciones, como son los pacientes ingresados (nutrición parenteral, terapias paliativas en enfermos terminales, medicamentos adaptados para dificultades de la deglución, mezclas para tratamientos endovenosos), los tratamientos con citostáticos o con radiofármacos, y las preparaciones en ensayos clínicos |
Además de su utilidad terapéutica, un aspecto fundamental en la formulación, hoy en día, es que sea un medicamento elaborado con los criterios de seguridad, eficacia y calidad exigibles a todos los medicamentos. Ello queda fundamentado por una parte por la Ley de Garantías y Uso Racional del Medicamento (Ley 29/2006)4, que en su artículo 42 sobre formulaciones determina que solo podrán utilizarse en formulación principios activos con acción e indicación reconocidas en España. A su vez la calidad en la elaboración queda regulada por el Real Decreto 175/2001 sobre «Normas de correcta elaboración y control de calidad en formulación magistral y preparados oficinales»5 que es vigente en nuestro país desde enero de 2004 y que regula las condiciones de locales, instalaciones, personal, procedimientos normalizados de trabajo, utillajes, registros y documentación de materia prima, documentación pertinente para cada elaboración, etc. y cuya aplicación es regulada por los servicios de inspección de cada una de las comunidades autónomas.
Ventajas e inconvenientes en la formulación dermatológicaSi la finalidad principal de la formulación dermatológica es aportar recursos para personalizar mejor las terapias y resolver problemáticas en la administración de fármacos, un repaso a las utilidades vistas de la formulación nos permite tener una perspectiva exacta de sus ventajas en la terapéutica cotidiana6 (tabla 2).
A pesar de que el recurso de la formulación permite resolver u optimizar muchas situaciones de administración de fármacos, y estar sujeto todo el proceso de suministro de materia prima y elaboración a procesos de calidad, pueden darse dificultades o inconvenientes en su aplicación (tabla 3).
Inconvenientes de la formulación
| • Diferencias en texturas y presentaciones |
| - Errores en la elaboración, que pueden ser objeto de sanción en aplicación del RD 175/2001 |
| - Más frecuente con el uso de términos ambiguos como emulsión O/W, ya que distintas farmacias pueden utilizar diferentes bases y procedimientos de elaboración sin que existan errores en la preparación |
| • Mayor probabilidad de interacciones (precipitaciones, cambios de coloración u otros) |
| - No se dará en el caso de formulaciones estandarizadas y bien descritas |
| • Información menos exhaustiva |
| - Las especialidades farmacéuticas disponen de prospectos normalizados y validados. En las formulaciones con adaptaciones de dosis o cambio de vehículos de principios activos ya registrados la información no diferirá en gran manera |
| - En las formulaciones tópicas, en especial asociaciones, la información es muy inferior. Debemos entregar al paciente una hoja informativa con posología, forma de aplicación y conservación de la formulación |
| • Fecha de caducidad y tiempo de uso recomendado |
| - Gran número de formulaciones vía oral sí disponen de una fecha de caducidad precisa que responde a unos estudios de estabilidad concretos |
| - En las formulaciones tópicas se recurre a tiempos de uso recomendado en función de los principios activos, tipos de vehículos y envases empleados |
| • Disparidad de precios entre farmacias |
Cuando hablamos de novedades en terapéutica estamos acostumbramos a referirnos a la incorporación de nuevos principios activos, pero el concepto de novedad en formulación es más amplio, ya que se refiere a todo aquello que nos proporcione más recursos al prescribir. El periodo 1995-2005ha sido fecundo por la incorporación de nuevos vehículos, resultado por un lado de nuevas prestaciones de la industria química y por otro de la satisfacción de demandas terapéuticas concretas8. A continuación se describen las principales novedades de interés en cuanto a vehículos.
Novedades en emulsionesHa sido importante la incorporación de un nuevo tipo de emulsionantes, los glucídicos y similares, que permiten la realización de emulsiones O/W glucídicas, las cuales tienen una mínima capacidad irritativa, son biodegradables y contribuyen a la acción hidratante del vehículo.
Este tipo de emulsiones se ha mostrado útil en tratamientos faciales de patologías sensibles (rosácea, dermatitis seborreica, dermatitis perioral, etc.) y también en tratamientos corporales de pieles muy sensibles o intolerantes.
Permiten la vehiculización de corticoides, antibióticos, inhibidores de la calcineurina y otros. Un aspecto práctico a tener en cuenta es que no permiten la asociación de un número excesivo de principios activos, como sí lo hacen otro tipo de emulsiones.
Otra incorporación importante es la de los crema-geles. Estos son un tipo de emulsiones O/W producidos por unos emulsionantes especiales que poseen una larga estructura polimérica que permite una orientación tridimensional de la fase externa acuosa, de manera similar a como hace un gelificante hidrófilo. Da como resultado un vehículo poco graso, muy agradable cosméticamente y que transmite frescor. De aplicación, pues, en patologías faciales que requieran estas características.
Tienen la misma particularidad que las anteriores de permitir asociar solo un número limitado de principios activos.
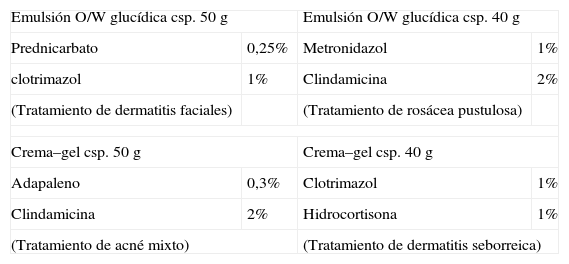
Algunas formulaciones ejemplo de emulsiones O/W glucídicas y crema-geles se recogen en la tabla 4.
Formulaciones con emulsiones glucídicas y crema-gel
| Emulsión O/W glucídica csp. 50g | Emulsión O/W glucídica csp. 40g | ||
| Prednicarbato | 0,25% | Metronidazol | 1% |
| clotrimazol | 1% | Clindamicina | 2% |
| (Tratamiento de dermatitis faciales) | (Tratamiento de rosácea pustulosa) | ||
| Crema–gel csp. 50g | Crema–gel csp. 40g | ||
| Adapaleno | 0,3% | Clotrimazol | 1% |
| Clindamicina | 2% | Hidrocortisona | 1% |
| (Tratamiento de acné mixto) | (Tratamiento de dermatitis seborreica) | ||
Si bien las emulsiones O/W son las más empleadas, por su utilidad y buena aceptación por los pacientes las emulsiones W/O tienen un valor singular al permitir formar un film externo, continuo y protector, que tiene especial interés en patologías secas. Este interés por las emulsiones W/O se desvanecía, en parte, pues hasta hace unos 20 años los conocimientos químicos no permitían elaborar una emulsión W/O con un contenido graso inferior a un 50%. Este tipo de emulsiones W/O, con un 50% de contenido graso, sigue siendo de interés para tratar lesiones corporales en patologías secas como psoriasis o eczemas crónicos. Sin embargo, hoy podemos también:
- 1.
Disponer de emulsiones W/O con un 25% de contenido graso, lo cual nos puede permitir tratar lesiones faciales en pacientes con patologías secas y/o en ambientes fríos.
- 2.
Disponer de emulsiones W/O con un 10% de contenido graso, lo cual permite formar emulsiones W/O fluidas (leches corporales) que pueden aplicarse según la sintomatología o datos clínicos de las patologías dermatológicas a tratar.
Ejemplos de estas emulsiones se describen en la tabla 5.
Novedades en otros vehículos- •
Es de particular interés la incorporación de lacas ungueales. Las lacas son estructuras poliméricas que están incorporadas en una base de solventes potentes que permiten la solubilización de concentraciones importantes de principios activos y un componente volátil, normalmente alcohólico. Al evaporarse esta permite la formación de una película oclusiva con una alta concentración de principio activo, que por aplicación sucesiva va a crear un gradiente de concentración del principio activo en el tejido ungueal, permitiendo que se alcancen concentraciones significativas en el lecho y la matriz. Este fundamento, aplicado en el desarrollo de lacas antimicóticas industriales, ha sido trasladado a otras áreas como la psoriasis (con buenos resultados), la onicomicosis o el liquen plano ungueal, entre otras.
- •
Una buena utilidad han demostrado también los aceites capilares. Se trata de bases oleosas formadas por aceites convencionales con la incorporación de otros lípidos de buena calidad cosmética y siliconas volátiles que permiten que, al aplicar el producto, su aspecto y sustantividad oleosa desaparezca en pocos minutos. Ello es de utilidad en dermatitis seborreica y psoriasis capilares de extensión reducida (evita aplicar emulsiones en el cuero cabelludo). Tienen como limitación que, por cuestiones de solubilidad, no pueden incorporarse libremente todos los principios activos.
- •
También hay que mencionar el interés de los aceites óticos, que permiten tratar mejor que las emulsiones una zona corporal de difícil accesibilidad, y los aceites corporales9. Algunos ejemplos de estos vehículos se exponen en la tabla 6.
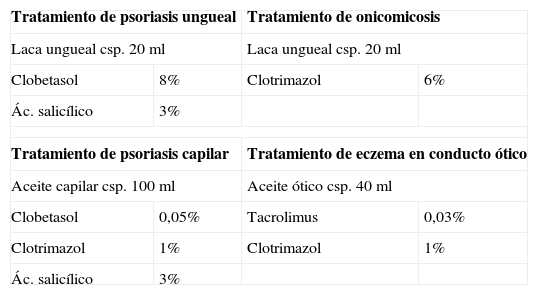
Tabla 6.Formulaciones con lacas y aceites
Tratamiento de psoriasis ungueal Tratamiento de onicomicosis Laca ungueal csp. 20ml Laca ungueal csp. 20ml Clobetasol 8% Clotrimazol 6% Ác. salicílico 3% Tratamiento de psoriasis capilar Tratamiento de eczema en conducto ótico Aceite capilar csp. 100ml Aceite ótico csp. 40ml Clobetasol 0,05% Tacrolimus 0,03% Clotrimazol 1% Clotrimazol 1% Ác. salicílico 3%
El tratamiento tópico sigue siendo un pilar básico en el tratamiento de la psoriasis, ya que hasta el 70% de los pacientes con psoriasis leve-moderada reciben esta modalidad de terapia como única opción10. El 30% restante, que corresponde a casos graves, reciben además terapia sistémica. De hecho, hay estudios que confirman el papel adicional que tienen diversos tratamientos tópicos (corticoides, análogos de la vitamina D, tazaroteno) a la hora de favorecer un blanqueo más rápido o bien necesitando una dosis inferior de la terapia sistémica. A pesar ello, un 40% de los pacientes refieren una escasa adherencia al tratamiento tópico11. Con el fin de optimizarlo al máximo hemos de ofrecer a los pacientes no solo principios activos eficaces y seguros, sino además cómodos y fáciles de aplicar; para ello el empleo de vehículos apropiados para cada área anatómica es crucial. De hecho, el mejor vehículo es aquel que es más probable que el paciente utilice. La formulación magistral (FM) aporta ventajas adicionales en el tratamiento tanto tópico como sistémico de la psoriasis, como por ejemplo al permitir el empleo de tópicos personalizados según el tipo de psoriasis y el área anatómica a tratar, administrando las cantidades requeridas para ello y evitando la automedicación. Además podemos asociar principios activos principales y secundarios (emolientes, hidratantes) haciendo más práctico el tratamiento y a su vez aumentando la adherencia al mismo. En terapia sistémica se dosifica la dosis según peso del paciente, haciendo un fármaco personalizado y para el número de días que consideremos12.
A pesar de que en FM se emplean principios activos ya disponibles en el mercado, su principal ventaja y aportación más relevante es la de poder ofertar al dermatólogo una forma de prescripción más libre, ya que permite no solo modificar las concentraciones de los activos, sino también los vehículos, aumentando así nuestras posibilidades terapéuticas.
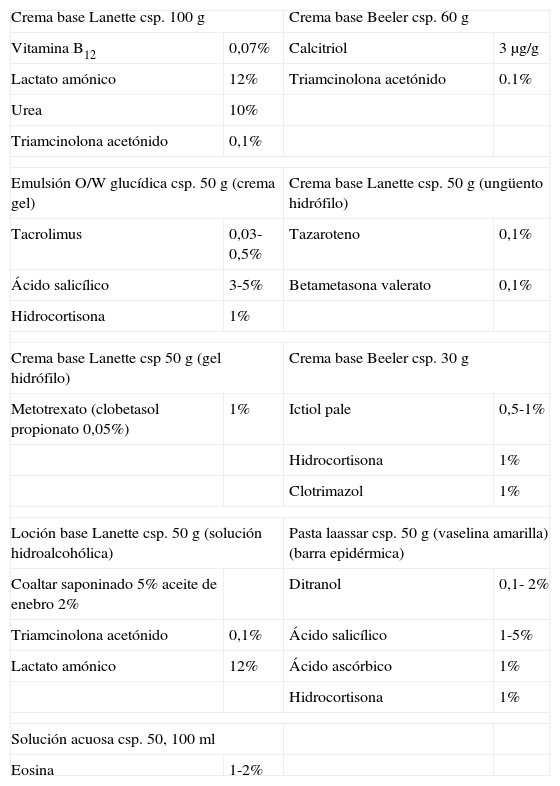
En las tablas 7 y 8 se recogen las aportaciones más relevantes de la FM en los últimos años en el tratamiento de la psoriasis.
Formulaciones en la psoriasis en placas
| Crema base Lanette csp. 100g | Crema base Beeler csp. 60g | ||
| Vitamina B12 | 0,07% | Calcitriol | 3μg/g |
| Lactato amónico | 12% | Triamcinolona acetónido | 0.1% |
| Urea | 10% | ||
| Triamcinolona acetónido | 0,1% | ||
| Emulsión O/W glucídica csp. 50g (crema gel) | Crema base Lanette csp. 50g (ungüento hidrófilo) | ||
| Tacrolimus | 0,03-0,5% | Tazaroteno | 0,1% |
| Ácido salicílico | 3-5% | Betametasona valerato | 0,1% |
| Hidrocortisona | 1% | ||
| Crema base Lanette csp 50g (gel hidrófilo) | Crema base Beeler csp. 30g | ||
| Metotrexato (clobetasol propionato 0,05%) | 1% | Ictiol pale | 0,5-1% |
| Hidrocortisona | 1% | ||
| Clotrimazol | 1% | ||
| Loción base Lanette csp. 50g (solución hidroalcohólica) | Pasta laassar csp. 50g (vaselina amarilla) (barra epidérmica) | ||
| Coaltar saponinado 5% aceite de enebro 2% | Ditranol | 0,1- 2% | |
| Triamcinolona acetónido | 0,1% | Ácido salicílico | 1-5% |
| Lactato amónico | 12% | Ácido ascórbico | 1% |
| Hidrocortisona | 1% | ||
| Solución acuosa csp. 50, 100ml | |||
| Eosina | 1-2% | ||
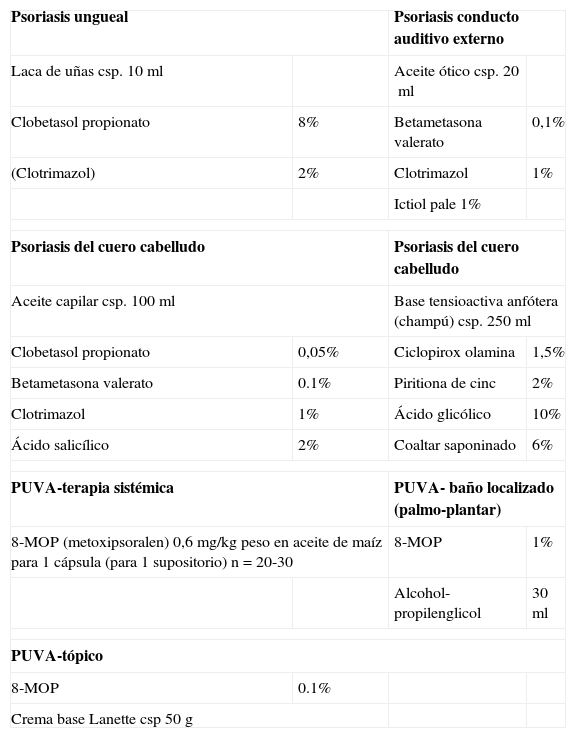
Otras formulaciones para la psoriasis
| Psoriasis ungueal | Psoriasis conducto auditivo externo | ||
| Laca de uñas csp. 10ml | Aceite ótico csp. 20ml | ||
| Clobetasol propionato | 8% | Betametasona valerato | 0,1% |
| (Clotrimazol) | 2% | Clotrimazol | 1% |
| Ictiol pale 1% | |||
| Psoriasis del cuero cabelludo | Psoriasis del cuero cabelludo | ||
| Aceite capilar csp. 100ml | Base tensioactiva anfótera (champú) csp. 250ml | ||
| Clobetasol propionato | 0,05% | Ciclopirox olamina | 1,5% |
| Betametasona valerato | 0.1% | Piritiona de cinc | 2% |
| Clotrimazol | 1% | Ácido glicólico | 10% |
| Ácido salicílico | 2% | Coaltar saponinado | 6% |
| PUVA-terapia sistémica | PUVA- baño localizado (palmo-plantar) | ||
| 8-MOP (metoxipsoralen) 0,6mg/kg peso en aceite de maíz para 1 cápsula (para 1 supositorio) n=20-30 | 8-MOP | 1% | |
| Alcohol-propilenglicol | 30ml | ||
| PUVA-tópico | |||
| 8-MOP | 0.1% | ||
| Crema base Lanette csp 50g | |||
El empleo de hidratantes, humectantes y emolientes forma parte esencial del tratamiento tópico de la psoriasis y, aunque considerados como principios activos secundarios, sus efectos beneficiosos en monoterapia se han atribuido a su capacidad para restablecer la hidratación y la función de barrera acuosa de la placa psoriásica, al tiempo que permiten un control con menor aplicación de dermocorticoides13. En este sentido la FM permite la asociación de hidratantes-emolientes junto a otros principios activos, lo que favorece la cumplimentación terapéutica. Dentro de las hidratantes utilizadas destaca el empleo de lactato amónico al 12% por su reconocida capacidad de mitigar la atrofia inducida por corticoides tópicos14. Su asociación a urea es sinérgica y recomendable.
Entre los principios activos principales que figuran en las fórmulas destaca el uso de la vitamina B12 en la psoriasis en placas, que cuenta con estudios que avalan su eficacia en dicha indicación15,16, además de ser un principio activo muy seguro, ideal como terapia de mantenimiento y que permite combinaciones con otros de mayor potencia (por ejemplo corticoides en fase de brote). La concentración a la que puede emplearse es al 0,07%, ya que a mayores concentraciones (0,14%) no aumenta su efectividad16. El tacrolimus puede emplearse al 0,03% o al 0,1% en emulsiones glucídicas en caso de psoriasis en áreas de piel sensible17, o bien al 0,3-0,5% en el resto de piel, concentraciones a las que no está comercializado, pero es especialmente útil sobre todo si se trata de placas pruriginosas. Sin embargo, en un estudio comparativo con calcipotriol, este último demostró ser más efectivo que tacrolimus a concentraciones altas en la normalización de los parámetros de diferenciación epidérmica18.
La FM permite cubrir áreas huérfanas de la terapéutica, por ejemplo en los últimos años se han dejado de comercializar fármacos como el ditranol y los alquitranes para su uso en psoriasis en placas por su escasa rentabilidad económica. Hay que considerar que son principios activos con características organolépticas que los hacen poco cosméticos, pero lo cierto es que siguen siendo útiles en determinadas situaciones que no resuelven los tópicos comercializados, y para ello hemos de recurrir a la FM. Con esta finalidad, Zampetti et al. publicaron en 2008 su experiencia a lo largo de 15 años con los tratamientos tópicos empleados en la psoriasis en un total de 666 pacientes, observando que la mayor eficacia correspondió a la combinación de clobetasol propionato 0,05 y solución de eosina al 2% a días alternos con solución de eosina 2% y aceite de cade, una brea clásica19.
Tanto el ditranol como la terapia de Goeckerman, con sus modificaciones, continúan siendo terapias utilizadas, incluso en la psoriasis infantil, más en otros países europeos que en España, y siendo de las terapias cuya remisión es más prolongada20,21. Su empleo requiere una explicación detallada al paciente por parte del dermatólogo con el fin de optimizar al máximo su uso. En los últimos años se ha incorporado el ictiol pale en formulaciones de áreas de piel sensible y cuero cabelludo, al ser un reductor con buena tolerancia y cosmeticidad.
Entre los derivados de la vitamina D se encuentra disponible, para su uso en FM, el calcitriol, cuya eficacia está ampliamente reconocida. Especialmente útil resulta su empleo en la psoriasis invertida y otras áreas de piel sensible (cara y genitales)22. Es una molécula inestable, sensible a la oxidación, por ello se aconseja evitar su asociación a otras moléculas en FM, con excepción de los corticoides tópicos. El interés que aporta su uso en FM es doble, de un lado permite modificar el vehículo, haciéndolo con menor contenido graso y más aceptable para el paciente y, por otro lado, permite la asociación con otros principios activos.
Recientemente se ha incorporado el tazaroteno a la FM, con lo cual también podemos modificar el vehículo en el que se encuentra comercializado. En nuestra experiencia23 la FM en ungüento de tazaroteno 0,1%, es eficaz en el tratamiento de la psoriasis ungueal, de la misma forma que otros autores habían descrito con la forma comercializada en gel.
En el caso de las FM de calcitriol, tazaroteno y tacrolimus, podemos recurrir a la asociación con otros principios activos, principalmente corticoides tópicos de mediana potencia. En este caso la asociación sería sinérgica, pues se potenciaría la eficacia y se reduciría la toxicidad de los fármacos por separado. Es bien conocida la irritación que puede aparecer en las primeras aplicaciones de tacrolimus, tazaroteno o calcitriol, y asociando un corticoide tópico podemos reducirla.
De forma empírica se ha empleado metotrexato (MTX) tópico con diversas concentraciones y vehículos en el tratamiento de la psoriasis vulgar y la pustulosis palmo-plantar, a pesar de carecer de evidencia científica. En 2006 Eskicirak et al. publicaron un ensayo en el que demuestran la eficacia y seguridad de MTX 1% frente a placebo24. Al no haber ninguna presentación comercial con MTX tópico es necesario recurrir a la FM.
La psoriasis ungueal es un desafío terapéutico para muchos pacientes y dermatólogos. Es importante clasificar las lesiones, según afecten el lecho o la matriz, así como medir la intensidad de la afectación con alguno de los índices de gravedad, como el NAPSI o el nail-PGA, entre otros; de esa forma si el NAPSI es inferior a 10, la psoriasis ungueal es leve-moderada y puede responder a tópicos. Entre estos conviene destacar, por su evidencia científica, los derivados de la vitamina D, en particular calcipotriol25 y tacalcitol26, cuya eficacia parece más importante en las alteraciones del lecho ungueal. De otro lado, y con la misma filosofía que ha ocurrido en el tratamiento de las onicomicosis, se han utilizado corticoides tópicos a elevadas concentraciones, como el clobetasol propionato 8% vehiculizado en laca de uñas, vehículo que permite una óptima penetración transungueal. En dos estudios clínicos hemos podido constatar la seguridad de dicha molécula y sus positivos efectos en la psoriasis ungueal, en especial en las manifestaciones debidas a las alteraciones de la matriz27,28. Con la finalidad de actuar tanto en el lecho como en la matriz ungueal, puede combinarse tacalcitol con laca de clobetasol propionato al 8% en FM28. Habida cuenta de la mayor prevalencia de onicomicosis en pacientes con psoriasis ungueal, se recomienda la práctica de cultivos microbiológicos seriados al realizar el tratamiento29,30.
El empleo de fórmulas magistrales es muy habitual en el tratamiento de la psoriasis del cuero cabelludo, aun cuando se han comercializado importantes novedades en los últimos años que han mejorado ostensiblemente el tratamiento de esta forma muchas veces refractaria31. En cualquier caso, no creemos justificado recurrir a viejas fórmulas magistrales de eficacia dudosa y, ante todo, de unas características organolépticas nefastas que hacen imposible su uso, máxime cuando la adherencia al tratamiento exige, de nuestra parte, que aportemos tratamientos cómodos y cosméticos. En el cuero cabelludo el dermatólogo formulador sabe que es importante seleccionar vehículos apropiados (champús, aceites capilares, geles semifluidos, emulsiones fluidas, entre otros), así como recordar la toxicidad de los principios activos seleccionados (a destacar: corticoides potentes y ácido salicílico).
En la actualidad la fototerapia UVB de banda estrecha (UVBBE) ha desbancado a la PUVA-terapia en el tratamiento de la psoriasis en placas moderada-grave, tanto por su eficacia como por su seguridad y comodidad32. Si bien no se recomienda el empleo de productos previos en la piel que puedan alterar la penetración de la fototerapia (ácido salicílico) o que se oxiden por la luz ultravioleta (derivados de la vitamina D), en nuestro departamento realizamos un estudio en el cual pacientes con psoriasis en placas tratados con fototerapia acudían a las sesiones con una aplicación fina de una emulsión O/W ligera de ácido oleico al 5% en las placas (n=24), o bien sin la misma (n=20). Nuestros resultados indicaron que los pacientes tratados previamente con ácido oleico al 5% en FM recibían un número menor de dosis (mJ/cm2) de UVBBE, así como de sesiones. De esta forma se podría optimizar la fototerapia, reduciendo la exposición total a la misma33. Respecto a la PUVA-terapia continúa siendo una forma muy útil de tratar a pacientes con piel tipos iv-vi, así como los casos de psoriasis extensa e infiltrada, linfomas cutáneos, liquen plano y morfea, entre otras dermatosis. Al indicar PUVA, tanto tópico como sistémico, es habitual recurrir a la FM. A destacar el empleo de 8-MOP en cápsula única o supositorio (0,6mg/kg peso) para aumentar la tolerancia digestiva34. A pesar de sus limitaciones logísticas, la PUVA-terapia tópica es un recurso terapéutico útil en eccemas de manos refractarios, psoriasis palmo-plantar y otras dermatosis localizadas o extensas en las que la administración del psoraleno esté contraindicada: cataratas, hepatopatías, etc.
Formulación magistral en el acnéEl acné es una de las patologías más frecuentes de la consulta dermatológica y en la que la FM ha tenido, históricamente, más utilidad. Se ha empleado profusamente tanto para incorporar principios activos no disponibles en nuestro país, cuando la legislación lo permitía, como para asociar principios activos, modificar dosis o vehículos, o adecuar cantidades de producto. Aunque en la actualidad tenemos cada vez más específicos disponibles, la FM sigue teniendo un papel importante en el tratamiento del acné.
El acné puede ser comedoniano, papulopustuloso o mixto. En el acné comedoniano o no inflamatorio se recurre a la formulación cuando queremos prescribir dosis inferiores o superiores a las comercializadas (por ejemplo, isotretinoína al 0,01 o al 1%, adapaleno al 3%35), usar vehículos con mejor tolerancia (emulsiones en lugar de geles hidroalcohólicos) o proporcionar cantidades más adecuadas al tratamiento de zonas extensas, como el escote o la espalda (tabla 9). En el acné inflamatorio o papulopustuloso se recurre poco a la formulación, pues la farmacopea es abundante y cubre las expectativas. Es útil para incorporar nuevos principios activos, como es el caso de la dapsona tópica36, que al 5% ha demostrado ser eficaz en las lesiones inflamatorias tras 2-4 semanas de tratamiento (tabla 10). Donde se formula mucho es en las variedades clínicas del acné, que son las más frecuentes, en las que coexisten comedones, pápulas y pústulas, y es necesario utilizar comedolíticos y antibacterianos. La asociación de principios activos tiene un efecto sinérgico en la eficacia, muchas veces mejora la tolerancia en comparación con los mismos principios activos usados en monoterapia y, por supuesto, mejora el cumplimiento terapéutico con una sola aplicación al día.
Hay que tener en cuenta que no todas las asociaciones a prescribir serán químicamente posibles. Son factibles las siguientes: retinoide/antibiótico; ácido glicólico/antibiótico; peróxido de benzoilo/antibiótico y adapaleno/peróxido de benzoilo. No es recomendable asociar otros como retinoides/peróxido de benzoilo (por oxidación) ni ácido azelaico/antibiótico (por inestabilidad química), aunque recientemente se ha descrito la asociación de ácido azelaico al 5% con eritromicina al 2%, evidenciándose un efecto aditivo mayor respecto a la administración de ambos principios activos por separado y respecto a placebo37. Han demostrado especial eficacia, seguridad y viabilidad: ácido retinoico y clindamicina38 o eritromicina; isotretinoína y eritromicina o clindamicina; ácido glicólico y clindamicina; peróxido de benzoilo y eritromicina o clindamicina39 (tabla 11).
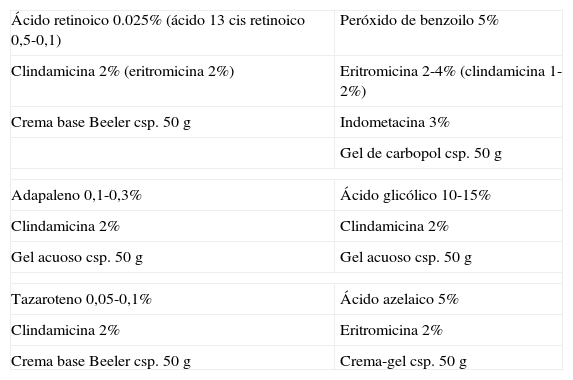
Fórmulas magistrales para el tratamiento del acné mixto
| Ácido retinoico 0.025% (ácido 13 cis retinoico 0,5-0,1) | Peróxido de benzoilo 5% |
| Clindamicina 2% (eritromicina 2%) | Eritromicina 2-4% (clindamicina 1-2%) |
| Crema base Beeler csp. 50g | Indometacina 3% |
| Gel de carbopol csp. 50g | |
| Adapaleno 0,1-0,3% | Ácido glicólico 10-15% |
| Clindamicina 2% | Clindamicina 2% |
| Gel acuoso csp. 50g | Gel acuoso csp. 50g |
| Tazaroteno 0,05-0,1% | Ácido azelaico 5% |
| Clindamicina 2% | Eritromicina 2% |
| Crema base Beeler csp. 50g | Crema-gel csp. 50g |
Es innovadora la asociación de tazaroteno con clindamicina, que parece ser más eficaz que con ácido retinoico. El tazaroteno tiene mayor capacidad despigmentante de la pigmentación postinflamatoria asociada a algunos acnés, y se puede vehiculizar en cremas o crema-geles, menos irritantes que el comercializado40.
En cuanto al tratamiento oral del acné no se recurre a la formulación para los antibióticos orales ni para los contraceptivos, pero sí para la isotretinoína oral cuando se quiere ajustar al máximo la dosis al peso, para evitar tomar varios comprimidos, reducir costes o cuando existen problemas de deglución, pues en esos casos se puede preparar la isotretinoína en suspensión41. Se toman 3ml y se mezclan en un medio lácteo (leche, batido, yogurt, etc.) (tabla 12).
Es muy frecuente en la práctica clínica diaria ver acnés asociados a otras patologías como melasma en mujeres, rosácea, dermatitis seborreica, hirsutismo, atopia, etc. En estas situaciones introduciendo principios activos adecuados a cada patología en un mismo vehículo facilitaremos que se siga el tratamiento (tabla 13).
Formulación en el tratamiento del acné asociado a otras patologías
| Acné+melasma |
| Ácido retinoico 0,025% |
| Clindamicina 2% |
| Hidroquinona 4% |
| Crema base Beeler csp. 50g |
| Acné+hirsutismo |
| Clindamicina 2% |
| Eflornitina 11,5% |
| Crema base Beeler csp. 50g |
| Acné+dermatitis seborreica |
| Eritromicina 2% |
| Clotrimazol 1% |
| Crema base Beeler csp. 50g |
La rosácea es otra de las patologías que se ha beneficiado de la FM, pues la disponibilidad de principios activos y vehículos es escasa en la farmacopea actual. Por ello el clínico formula los tratamientos con mucha frecuencia y, claramente, estos preparados obtienen mejores resultados que los específicos comercializados de que disponemos.
La rosácea se subdivide clínicamente en 4 subtipos: rosácea eritematotelangiectásica, rosácea papulopustulosa, rosácea fimatosa y rosácea ocular.
El tratamiento tópico de la rosácea eritematotelangiectásica o subtipo 1 (tabla 14) es a base de venotónicos (castaño de indias, ruscus, mirtilo, meliloto, etc.), que tienen la intención de reducir el eritema persistente y la tendencia al flushing que caracteriza esta fase de la enfermedad. Pero es de difícil resolución solo con tratamiento tópico, de modo que este suele ser un complemento a otros tratamientos (orales o físicos). Existen numerosos productos comercializados con este fin (aguas termales y múltiples cremas), pero la FM aporta la ventaja de poder añadir metronidazol o antiinflamatorios tópicos (enoxolona, alfa bisabolol) a los venotónicos, con el fin de prevenir el paso a la rosácea papulopustulosa.
Formulación en el tratamiento de la rosácea eritemato-telangiectásica
| Extracto glicólico de meliloto 10% |
| Extracto glicólico de ruscus 10% |
| Metronidazol 1% |
| Gel acuoso csp. 50g |
| Enoxolona 0.5-1% |
| Alfa bisabolol 1% |
| Ácido hialuronico 0.5% |
| Aloe vera 10% |
| Crema pieles sensibles csp. 50g |
| Clonidina clorhidrato 25 microgramos para una cápsula |
| n=90 |
| Metronidazol 1% |
| Enoxolona 0,5-1% |
| Alfa bisabolol 1% |
| Emulsión para pieles sensibles csp. 50g |
La clonidina clorhidrato, no comercializada en nuestro país, a dosis de 25-50 microgramos al día, se utiliza desde hace años como tratamiento oral del flushing. Este agonista alfa adrenérgico se puede emplear de dos formas: para revertir una crisis (tomando 2 cápsulas en ese momento) o bien para prevenir las crisis (tomando 2 cápsulas cada 12 horas continuamente). Los efectos secundarios son poco frecuentes (hipotensión, sequedad de boca, estreñimiento), pero se recomienda la introducción lenta para evitarlos. El uso de la clonidina se basa más en la experiencia clínica que en la existencia de ensayos clínicos que demuestren su eficacia.
El tratamiento tópico de la rosácea papulopustulosa o subtipo 2 (tabla 15) se realiza con antibióticos tópicos, que parecen actuar por su actividad antiinflamatoria. Los más empleados son el metronidazol al 0,75-1%, la eritromicina al 1-2% y la clindamicina al 1-2%. En segunda línea se emplean el ácido azelaico al 10-20% y la sulfacetamida sódica al 10%.
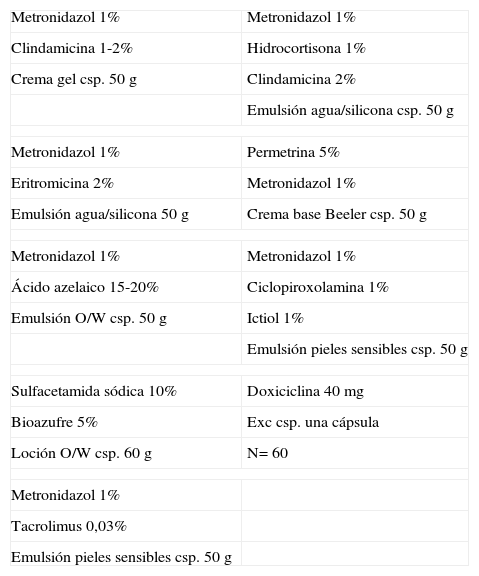
Formulación en la rosácea pápulopustulosa
| Metronidazol 1% | Metronidazol 1% |
| Clindamicina 1-2% | Hidrocortisona 1% |
| Crema gel csp. 50 g | Clindamicina 2% |
| Emulsión agua/silicona csp. 50g | |
| Metronidazol 1% | Permetrina 5% |
| Eritromicina 2% | Metronidazol 1% |
| Emulsión agua/silicona 50g | Crema base Beeler csp. 50g |
| Metronidazol 1% | Metronidazol 1% |
| Ácido azelaico 15-20% | Ciclopiroxolamina 1% |
| Emulsión O/W csp. 50g | Ictiol 1% |
| Emulsión pieles sensibles csp. 50g | |
| Sulfacetamida sódica 10% | Doxiciclina 40mg |
| Bioazufre 5% | Exc csp. una cápsula |
| Loción O/W csp. 60g | N=60 |
| Metronidazol 1% | |
| Tacrolimus 0,03% | |
| Emulsión pieles sensibles csp. 50g | |
La formulación del metronidazol tiene la ventaja de poder aumentar su concentración al 1% (dosis más altas no tienen mayor eficacia), mejorar el vehículo para disminuir los casos de intolerancia y asociarlo a otros antibióticos como la eritromicina o la clindamicina. Aunque no existen estudios que lo ratifiquen, la experiencia clínica demuestra que la asociación de metronidazol con antibióticos tópicos incrementa la respuesta terapéutica en las formas muy pustulosas de rosácea.
En casos de pieles hipersensibles se añadirá algún antiinflamatorio como la enoxolona, el aloe vera o el alfa bisabolol para conseguir tolerarlo.
El ácido azelaico constituye, en nuestra opinión, un tratamiento de segunda línea en la rosácea, aunque algunos estudios le dan una eficacia equivalente a metronidazol42. Se emplea en monoterapia o como complemento a este (por ejemplo ácido azelaico por la mañana y metronidazol por la noche). Se formula poco porque la elaboración es compleja, pero su ventaja radica en la posibilidad de vehiculizarlo en múltiples distintas bases. También es posible asociarlo a metronidazol43.
La sulfacetamida sódica al 10% asociada a bioazufre al 5% se emplea mucho en el mundo anglosajón. Tiene actividad secante y antiinflamatoria. Tiene menor potencia que los anteriores y se emplea para casos más leves o en tratamiento de mantenimiento. En nuestro medio no se comercializa, y por tanto se debe formular.
Cuando la rosácea se asocia a dermatitis seborreica, hecho muy frecuente, tiene mucho interés formular, asociando metronidazol a hidrocortisona (por un corto periodo de tiempo), a un imidazólico (clotrimazol, ketoconazol, ciclopiroxolamina) o a tacrolimus. El tacrolimus, además de actuar contra la dermatitis seborreica, tiene actividad antiinflamatoria y antipruriginosa, por lo que es de utilidad en la rosácea, aunque se han descrito casos de exacerbación.
Los casos con sospecha de democidosis se podrán tratar con permetrina, en monoterapia o asociada a metronidazol.
Las rosáceas moderadas/graves requieren la asociación de antibióticos orales (minociclina, doxiciclina, metronidazol, etc.) que no suelen formularse. Últimamente se ha demostrado que dosis subantibióticas de doxiciclina, de 40mg/día y en liberación retardada, tienen un efecto estabilizador de la enfermedad a largo plazo44, y en caso de prescribirla sí deberá formularse, puesto que esta dosis no está comercializada en nuestro país.
Cuando se indica isotretinoína a dosis bajas, entre 2,5 y 5mg, también se puede recurrir a la formulación para ajustar dosis.
La rosácea fimatosa o subtipo 3 se trata mediante procedimientos físicos (electrocoagulación, láser de CO2, etc.), aunque a menudo se asocian los tratamientos del subtipo 2.
La rosácea ocular o subtipo 4 se beneficia enormemente de la FM, puesto que el metronidazol (0,5-0,75%) se vehiculiza en pomada/colirio/emulsión oftálmica estéril y se aplica directamente en la conjuntiva ocular (tabla 16).
Formulación magistral en los trastornos de la pigmentación cutáneaAunque son numerosísimos los trastornos de la pigmentación, tanto hiperpigmentaciones como hipopigmentaciones, nos referiremos aquí solamente a los que constituyen mayor demanda terapéutica en la consulta dermatológica habitual: el melasma, las lentiginosis solares, la pigmentación postinflamatoria y el vitíligo.
En este campo de la Dermatología tampoco hay muchos específicos de utilidad, por lo que es frecuente formular los tratamientos.
Los agentes despigmentantes disponibles son el ácido retinoico, la hidroquinona y los corticoides tópicos. Ya con menor eficacia disponemos del ácido kójico y el ácido azelaico, que se usan en casos leves, en verano o en tratamiento de mantenimiento.
Pueden emplearse en monoterapia o combinados entre ellos (con mayor eficacia), en diversas dosis y en multitud de posibles vehículos.
La combinación más eficaz es la conocida como la tríada de Kligman, que combina hidroquinona, ácido retinoico y corticoide tópico. Debido a la capacidad irritante de esta combinación han surgido numerosas variantes, con menor dosificación de cada uno de los principios activos (tabla 17).
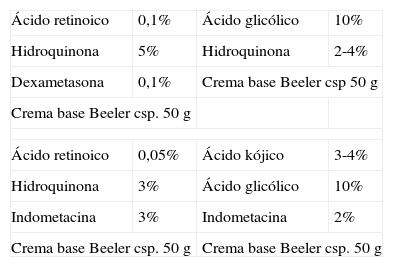
Formulación en el tratamiento del melasma
| Ácido retinoico | 0,1% | Ácido glicólico | 10% |
| Hidroquinona | 5% | Hidroquinona | 2-4% |
| Dexametasona | 0,1% | Crema base Beeler csp 50g | |
| Crema base Beeler csp. 50g | |||
| Ácido retinoico | 0,05% | Ácido kójico | 3-4% |
| Hidroquinona | 3% | Ácido glicólico | 10% |
| Indometacina | 3% | Indometacina | 2% |
| Crema base Beeler csp. 50g | Crema base Beeler csp. 50g | ||
Para hiperpigmentaciones importantes, pero muy localizadas, o para despigmentar las zonas aún no despigmentadas en vitíligos universales puede usarse mequinol al 10 o 20%, que es un éster de la hidroquinona de gran potencia, pero también con alto riesgo de acromias irreversibles (tabla 18).
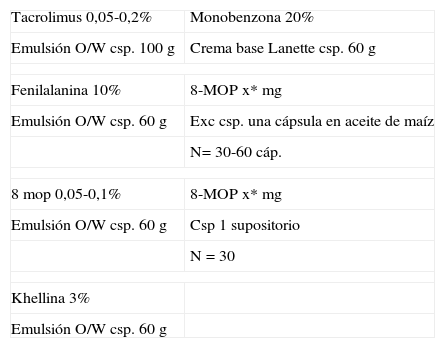
Formulación magistral en el vitíligo
| Tacrolimus 0,05-0,2% | Monobenzona 20% |
| Emulsión O/W csp. 100g | Crema base Lanette csp. 60g |
| Fenilalanina 10% | 8-MOP x* mg |
| Emulsión O/W csp. 60g | Exc csp. una cápsula en aceite de maíz |
| N= 30-60 cáp. | |
| 8 mop 0,05-0,1% | 8-MOP x* mg |
| Emulsión O/W csp. 60g | Csp 1 supositorio |
| N=30 | |
| Khellina 3% | |
| Emulsión O/W csp. 60g | |
*La dosis de 8-MOP se calcula en función del peso, siendo 0,6mg/kg. El poder calcular la dosis exacta ajustada al peso es una ventaja frente a los fármacos comercializados.
De menor eficacia pero útil en períodos estivales o en tratamientos de mantenimiento es la asociación de nicotinamida con ácido ascórbico, descrita recientemente45.
Las placas recientes de vitíligo son tratadas con corticoides tópicos de diversa potencia, de los cuales hay muchísimos comercializados. Si se formulan suele ser para suministrar grandes cantidades en caso de vitíligos extensos. También se utiliza tacrolimus en específico o formulado en diversas concentraciones y con vehículos menos grasos. Una molécula empleada en FM para esta indicación es la khellina al 3%.
Se recurre a la formulación para fototerapia; bien con fenilalanina, 8-MOP tópico, o 8 MOP oral (o en supositorio en caso de molestias digestivas) (tabla 18). También para los casos en los que se desea una despigmentación permanente de las pocas zonas que aún no están afectadas por la enfermedad, tal y como se ha comentado, con monobenzona.
Formulación en la patología de la mucosa oralActualmente disponemos de un número muy reducido de medicamentos adecuados comercializados dirigidos a la aplicación tópica oral. En muchas ocasiones nos vamos a ver obligados a recurrir a la FM.
La mucosa de la cavidad oral corresponde a un epitelio no queratinizado en su mayor parte, lo que la hace muy permeable a las sustancias que vamos a aplicar, pero los vehículos clásicos son de difícil aplicación debido a la continua motilidad bucal y a la humedad constante producida por la saliva, por lo que es recomendable utilizar vehículos adecuados a estas características46.
Vehículos apropiados para mucosa oralExcipiente adhesivo oral. Está constituido por una base grasa (vaselina polietilenada) y gelidificantes hidrófilos. Las moléculas hidrófilas van a facilitar la unión con la mucosa, y la mayoría de principios activos permanecen en la base grasa. Lentamente por capilaridad la saliva va penetrando en el excipiente, hidratándose este y liberando los principios activos. Es el más adecuado de todos. Se aplica en capa fina sobre las lesiones y se recomienda no beber, comer ni hablar durante un mínimo de 30 minutos.
Gel adhesivo oral. Es una alternativa a la aplicación del anterior, de menor adhesividad, mejor sabor y textura (mentolado). Los componentes mayoritarios del mismo son sorbitol, propilenglicol o glicerina, mientras que el gelificante utilizado es la carboximetilcelulosa sódica.
Soluciones orales. Indicadas para la realización de enjuagues en lesiones múltiples, o pulverizadas en spray para lesiones en pilares amigdalinos. En algunos casos son soluciones acuosas, pero también pueden ser soluciones hidroalcohólicas con bajo contenido en etanol para no irritar la mucosa.
Comprimidos bucales. Composición similar a la de los de uso sistémico, pero con un tiempo de disgregación superior por un mayor contenido de agregantes.
Caramelos medicinales. Los llamados lollipops son caramelos en una base sólida de polietilenglicoles que permiten la incorporación de los fármacos correspondientes, y la adición de edulcorantes y saborizantes que tienen especial interés en la población infantil.
Patologías y tratamiento tópico de prescripción magistralAftosisEl tratamiento es principalmente sintomático; aplicaremos fórmulas que contengan la asociación de diferentes principios activos:
- 1.
Antihistamínicos: por su efecto anestésico cuando se aplican tópicamente (difenhidramina, clorfeniramina).
- 2.
Antisépticos: para mantener una buena higiene dental. La clorhexidina digluconato al 0,2% en solución para enjuagues ha demostrado aumentar el tiempo libre de aftosis en pacientes con enfermedad recurrente47, pero el problema es que puede teñir los dientes.
- 3.
Tetraciclinas: por su efecto antiinflamatorio conocido48.
- 4.
Anestésicos tópicos: van a disminuirnos el dolor, pero debemos vigilarlos en pacientes encamados, ya que al suprimir el reflejo de la glotis posibilitan una broncoaspiración (lidocaína 2%).
- 5.
Corticoides tópicos: acortamos la evolución de la enfermedad y disminuimos los síntomas. Es importante conocer los que son liposolubles (triamcinolona acetónido y la mayoría) o hidrosolubles (dexametasona fosfato 0,1%, betametasona fosfato 0,1%) para poder elegir el vehículo adecuado.
- 6.
Protectores de la mucosa gástrica: como el sucralfato y la carbenoxolona. Forman una película aisladora de la saliva (sucralfato 4%)49.
- 7.
Ácido hialurónico: actúa como demulcente, protector de la mucosa oral, inmunomodulador y reparador celular (ácido hialurónico 0,5-1%); esta aplicación ha demostrado ser segura y eficaz tanto en la aftosis recurrente como en la enfermedad de Behçet en varios estudios50,51.
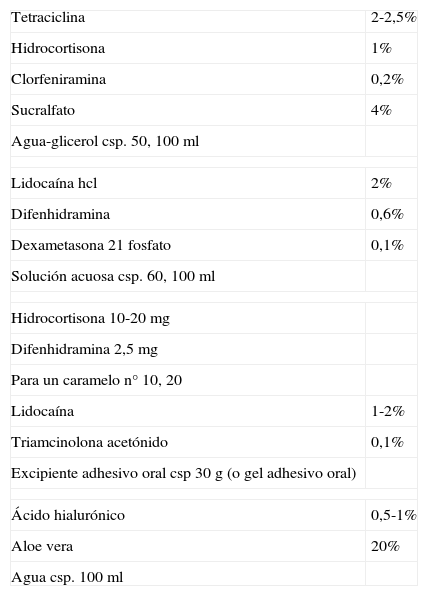
El vehículo a elegir dependerá de la extensión de las lesiones, fármacos que vamos a incluir, preferencias del paciente (el gel adhesivo oral tiene mejor sabor que el excipiente adhesivo oral), y en niños hay que recordar la posibilidad de los caramelos medicinales (tabla 19).
Fórmulas magistrales en aftosis
| Tetraciclina | 2-2,5% |
| Hidrocortisona | 1% |
| Clorfeniramina | 0,2% |
| Sucralfato | 4% |
| Agua-glicerol csp. 50, 100ml | |
| Lidocaína hcl | 2% |
| Difenhidramina | 0,6% |
| Dexametasona 21 fosfato | 0,1% |
| Solución acuosa csp. 60, 100ml | |
| Hidrocortisona 10-20mg | |
| Difenhidramina 2,5mg | |
| Para un caramelo n° 10, 20 | |
| Lidocaína | 1-2% |
| Triamcinolona acetónido | 0,1% |
| Excipiente adhesivo oral csp 30g (o gel adhesivo oral) | |
| Ácido hialurónico | 0,5-1% |
| Aloe vera | 20% |
| Agua csp. 100ml | |
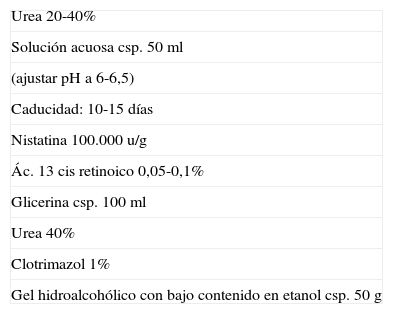
El tratamiento es en primer lugar etiológico, evitándose los posibles factores desencadenantes (fármacos, tabaco, candidiasis, falta de ingesta de alimentos duros, etc.). Se recomienda aumentar la higiene bucal y cepillar la zona afecta con un cepillo impregnado con un queratolítico (ácido retinoico 0,1%, urea 40%) asociado a un antifúngico (clotrimazol o nistatina) por la posible implicación de Candida albicans52. Las soluciones con urea en alta concentración tienen poca estabilidad y pueden desprender amoníaco, por lo que es necesario estabilizar la solución con una ligera acidificación. Hay que tener en cuenta que si a las soluciones de urea se les quiere añadir un antifúngico este no será soluble en agua, lo que es un error de prescripción frecuente. Un recurso es formular un gel con un bajo contenido de alcohol (20%) que puede incorporar el clotrimazol, y en el caso de querer incorporar la nistatina lo mejor es aplicar una solución glicérica (tabla 20).
Liquen plano oralEl liquen plano oral (LPO), al ser un proceso que, en la mayoría de ocasiones va a ser crónico, solo tratamos a aquellos pacientes sintomáticos, con lesiones muy queratósicas o formas erosivas.
Como normas generales deben evitarse traumatismos como el cepillado enérgico de los dientes, evitar alimentos duros, tener una buena higiene dental, no fumar, eliminar rozaduras con las prótesis o con malposición de piezas dentarias.
El tratamiento de primera elección son los corticoides tópicos (potentes o muy potentes) como el propionato de clobetasol al 0,05%, aunque al 0,025% también ha demostrado ser eficaz53 (tabla 21).
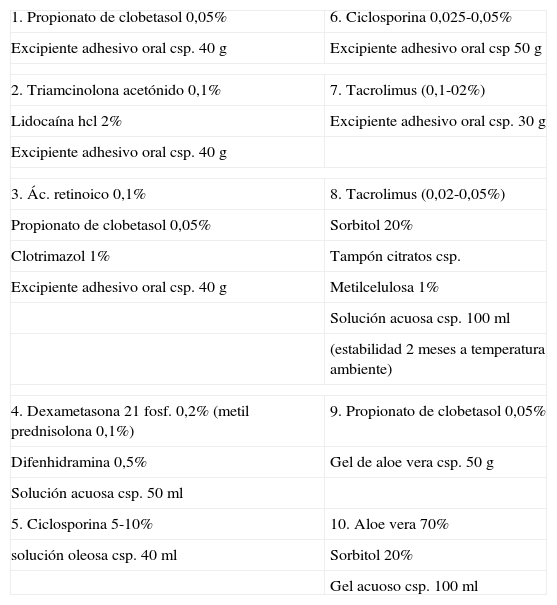
Fórmulas magistrales en el liquen plano oral
| 1. Propionato de clobetasol 0,05% | 6. Ciclosporina 0,025-0,05% |
| Excipiente adhesivo oral csp. 40g | Excipiente adhesivo oral csp 50g |
| 2. Triamcinolona acetónido 0,1% | 7. Tacrolimus (0,1-02%) |
| Lidocaína hcl 2% | Excipiente adhesivo oral csp. 30g |
| Excipiente adhesivo oral csp. 40g | |
| 3. Ác. retinoico 0,1% | 8. Tacrolimus (0,02-0,05%) |
| Propionato de clobetasol 0,05% | Sorbitol 20% |
| Clotrimazol 1% | Tampón citratos csp. |
| Excipiente adhesivo oral csp. 40g | Metilcelulosa 1% |
| Solución acuosa csp. 100ml | |
| (estabilidad 2 meses a temperatura ambiente) | |
| 4. Dexametasona 21 fosf. 0,2% (metil prednisolona 0,1%) | 9. Propionato de clobetasol 0,05% |
| Difenhidramina 0,5% | Gel de aloe vera csp. 50g |
| Solución acuosa csp. 50ml | |
| 5. Ciclosporina 5-10% | 10. Aloe vera 70% |
| solución oleosa csp. 40ml | Sorbitol 20% |
| Gel acuoso csp. 100ml | |
Quedan en una segunda línea los retinoides tópicos (ácido retinoico 0,1% y ácido 13 cis-reticoico 0,1%) y los inhibidores de la calcineurina (sobre todo tacrolimus, ya que disponemos de menos estudios con pimecrolimus).
Los retinoides sobre todo son útiles para las formas queratósicas, restaurando la diferenciación epitelial anormal. El ácido retinoico se debe utilizar a concentraciones altas (0,1%), puesto que si la concentración es más baja tiene menor eficacia. Nosotros combinamos el retinoide con el corticoide tópico, y podemos iniciar el retinoide a una concentración más baja para conseguir mayor tolerancia. No parece haber diferencias de eficacia entre el ácido retinoico y el ácido 13 cis-retinoico aplicados tópicamente para el LPO54.
En varios estudios se ha evidenciado que el tacrolimus tópico puede ser eficaz y seguro, con muy baja absorción sistémica y pocos efectos secundarios locales55. La mejoría se inicia a las dos semanas de la aplicación, controla los síntomas, aclara las lesiones y en general es bien tolerado, pero debemos avisar del ardor que aparece sobre todo en las primeras aplicaciones. En la mayoría de estudios aplican la pomada comercializada directamente; nosotros consideramos que esto disminuye la adherencia, lo que lleva a una menor absorción local y aumenta la ingestión del fármaco, además de que al paciente le resulta desagradable la aplicación de una pomada en la cavidad oral, por lo que recomendamos prescribir tacrolimus en excipiente adhesivo oral o en solución.
La ciclosporina tópica en forma de solución oleosa o en base adhesiva cada vez se prescribe menos por su elevado coste, posible absorción sistémica y posible poder carcinógeno asociado. No se ha demostrado que sea más eficaz que los corticoides tópicos orales56.
El aloe vera se puede también incluir en estas fórmulas magistrales por su efecto antiinflamatorio conocido. Incluso en monoterapia son varios los estudios que evalúan y demuestran la eficacia del aloe vera tópico en el LPO57,58. En nuestra propia experiencia consigue respuestas parciales, y en ocasiones respuestas completas, pero sobre todo nos puede ayudar a reducir el uso de corticoides.
Tratamiento sistémico de prescripción magistralEn pacientes con aftosis recurrente (AR), donde estén contraindicados o no sean eficaces los fármacos ya comercializados (pentoxifilina, colchicina, etc.), podemos ensayar el sulfato de cinc oral, para el que precisamos de la prescripción magistral, siempre avisando al paciente de la posible intolerancia gastrointestinal. El cinc tiene un efecto antiinflamatorio conocido (modula la producción de TNF e IL-6, inhibe la expresión de integrinas mediadoras de la inflamación como el ICAM-1, inhibe la quimiotaxis de los neutrófilos) y son varios los estudios que defienden su eficacia; la mayoría utilizan el sulfato de cinc oral, pero también podemos preescribir el gluconato de cinc por la mejor tolerancia gastrointestinal59,60. La cantidad de cinc elemental varía según la sal: 100mg de gluconato de cinc contienen 15 mEq de cinc elemental y 100mg de sulfato de cinc contienen 22,5 mEq de cinc elemental (tabla 22).
Algunos dermatólogos siguen utilizando el levamisol en ciclos para el tratamiento de la AR (50mg/8h por tres días repitiendo a los 15 días). Es un antihelmíntico con propiedades inmunomoduladoras, y se ha abandonado prácticamente su uso por el riesgo de agranulocitosis, aunque recientes estudios defienden una baja incidencia de este efecto adverso61.
La dapsona es uno de los ejemplos en los que su comercialización en España se ha suspendido en ocasiones, y cuando no disponemos de farmacia hospitalaria para adquirirla podemos realizar su formulación. Tanto en monoterapia como asociada a la colchicina también se puede ensayar en estos pacientes62.
Cabe señalar un estudio donde se demuestra que la doxiciclina a dosis bajas subantimicrobianas (20mg/12h) durante 90 días reduce el número de lesiones en comparación con el placebo63. Parece una terapia potencial en el manejo de la aftosis recurrente, pero requiere ser confirmada con posteriores estudios. La formulación será de gran ayuda para poder dar esta dosis subantimicrobiana al paciente.
Formulación magistral en la patología del cuero cabelludoAunque lo clásico en el cuero cabelludo es prescribir soluciones hidroalcohólicas, es importante conocer nuevos recursos de los que disponemos como vehículos adecuados para esta área cutánea.
Variantes de las soluciones hidroalcohólicas son aquellas en las que incorporamos sobreengrasantes (como el ministrato de isopropilo) para corregir la sequedad excesiva o siliconas volátiles para corregir la sensación de engrasamiento del pelo en aquellas fórmulas con concentraciones altas de propilenglicol. También disponemos de soluciones hidroalcohólicas sin propilenglicol (causante de dermatitis irritativa, picor y sequedad del cuero cabelludo). Los geles semifluidos y los geles compactos permiten aplicaciones más localizadas. También podemos pautar emulsiones O/W fluidas para el cuero cabelludo con irritación, donde debemos evitar el alcohol.
Determinadas patologías como la psoriasis, y en ocasiones la dermatitis seborreica, presentan lesiones hiperqueratósicas que si se tratan con una solución hidroalcohólica causan una mayor sequedad, y si se manejan con emulsiones la aplicación resulta incómoda para los pacientes. En estos casos se pueden beneficiar de la aplicación de aceites capilares; estos van a ayudar a eliminar las escamas y cosméticamente son mucho más agradables que las emulsiones. La composición de esta forma galénica asocia aceites vegetales convencionales con lípidos de alta calidad cosmética y alguna ciclometicona volátil. Tienen como limitación que no permiten la solubilización de ciertos principios activos como la hidrocortisona, el ketoconazol y la urea a altas concentraciones. En la tabla 23 se detallan las compatibilidades46.
Solo nos centraremos en dos de las patologías más frecuentes del cuero cabelludo: la alopecia androgenética (AA) y la alopecia areata (AAR).
Alopecia androgenéticaEl tratamiento de la AA se basa principalmente en el minoxidil tópico y los antiandrógenos orales.
MinoxidilEl minoxidil sigue siendo el referente en el tratamiento tópico de la AA. Se cree que su mecanismo de acción se desarrolla sobre los canales de potasio estimulando el crecimiento del pelo, activando la proliferación celular y la síntesis de ADN del folículo piloso, y sobre el mantenimiento de la red vascular dérmica, entre otras posibles acciones64.
El minoxidil al 2-5% aplicado 1ml dos veces al día sobre el cuero cabelludo seco tiene demostrada su eficacia, con un pico de crecimiento de pelo a las 16 semanas. Como efectos adversos puede aparecer una dermatitis de contacto irritativa y menos frecuentemente alérgica. En ocasiones esta reacción puede ser debida al propilenglicol que suele contener el vehículo. Puede aparecer hipertricosis, sobre todo en mujeres, que suele remitir a los 4 meses de interrumpir el tratamiento. Para evitarlo se debe recomendar lavar las manos tras la aplicación del minoxidil e intentar no tocar la cara con el producto, pero en ocasiones la hipertricosis puede ser resultado de una hipersensibilidad a los bajos niveles de absorción sistémica del minoxidil y no al contacto directo.
El minoxidil tópico al 5% aporta mayor efectividad y rapidez de actuación, con un aumento muy escaso de los efectos secundarios (sobre todo aumenta la irritación, seguramente por la necesidad de incrementar la concentración del propilenglicol). En la mujer solo está aprobado minoxidil tópico al 2%, pero al 5% también se ha evaluado en mujeres y es significativamente más eficaz, aunque aumenta ligeramente la incidencia de hipertricosis facial65,66.
Pese a que disponemos de minoxidil tópico comercializado al 2 y al 5%, la ventaja de la formulación magistral se basa en la prescripción de concentraciones intermedias, en poder vehiculizar el minoxidil con excipientes cosméticamente más adecuados, poder prescribir asociaciones en pacientes que también presenten otras patologías como la dermatitis seborreica o la psoriasis y en realizar vehículos sin propilenglicol en aquellas personas con dermatitis de contacto (tablas 24 y 25). Un nuevo recurso en el caso de dermatitis irritativa es el uso de emulsiones fluidas aplicables en spray, que permiten evitar el vehículo hidroalcohólico, y con ellas podemos formular el minoxidil al 2-3%.
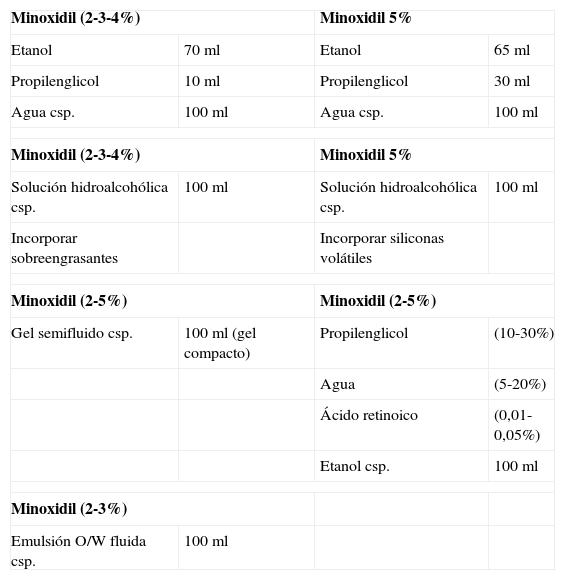
Fórmulas magistrales con minoxidil
| Minoxidil (2-3-4%) | Minoxidil 5% | ||
| Etanol | 70ml | Etanol | 65ml |
| Propilenglicol | 10ml | Propilenglicol | 30ml |
| Agua csp. | 100ml | Agua csp. | 100ml |
| Minoxidil (2-3-4%) | Minoxidil 5% | ||
| Solución hidroalcohólica csp. | 100ml | Solución hidroalcohólica csp. | 100ml |
| Incorporar sobreengrasantes | Incorporar siliconas volátiles | ||
| Minoxidil (2-5%) | Minoxidil (2-5%) | ||
| Gel semifluido csp. | 100ml (gel compacto) | Propilenglicol | (10-30%) |
| Agua | (5-20%) | ||
| Ácido retinoico | (0,01-0,05%) | ||
| Etanol csp. | 100ml | ||
| Minoxidil (2-3%) | |||
| Emulsión O/W fluida csp. | 100ml | ||
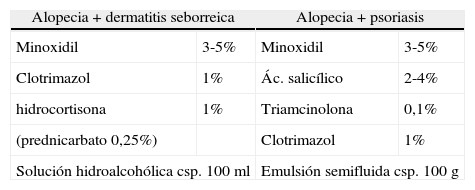
Fórmulas magistrales en patologías asociadas del cuero cabelludo
| Alopecia+dermatitis seborreica | Alopecia+psoriasis | ||
| Minoxidil | 3-5% | Minoxidil | 3-5% |
| Clotrimazol | 1% | Ác. salicílico | 2-4% |
| hidrocortisona | 1% | Triamcinolona | 0,1% |
| (prednicarbato 0,25%) | Clotrimazol | 1% | |
| Solución hidroalcohólica csp. 100ml | Emulsión semifluida csp. 100g | ||
La asociación de retinoides tópicos tiene una acción sinérgica con el minoxidil en el papel del crecimiento del cabello, y además aumenta la absorción percutánea de este. Shin HS et al. han demostrado que la combinación de minoxidil al 5% con tretinoína al 0,01%, aplicado una vez al día, es igual de eficaz que el minoxidil al 5% aplicado 2 veces al día, por lo que la asociación con tretinoína podría eliminar el inconveniente de aplicar la solución 2 veces al día67.
El resto de tratamientos tópicos no tienen una eficacia bien demostrada, aunque existen artículos que defienden la eficacia de hormonas aplicadas tópicamente, pero son estudios anecdóticos y los diferentes autores recomiendan valerato de estradiol al 0,03%68, progesterona al 0,025%, espironolactona 2-5% y canrenona 1-3%. El finasteride tópico al 0,05% no parece incrementar el crecimiento del cabello. Un sorprendente estudio de Blume-Peytavi et la. evalúa la eficacia del tratamiento tópico con latanoprost al 0,1%, en la alopecia androgenética, obteniendo un incremento significativo de la densidad del cabello, aplicándolo dos veces al día durante 24 semanas69. Quizás la formulación magistral nos podrá ayudar en un futuro cercano a su prescripción en el volumen y vehículo adecuado.
FinasterideEl finasteride es un antiandrógeno periférico no esteroideo que inhibe la enzima 5-alfarreductasa tipo ii, bloqueando así la conversión de testosterona libre a dihidrotestosterona (metabolito más activo). Es bien conocida su eficacia en el varón a dosis de 1mg/día, eficacia más controvertida en mujeres. Está aprobado para varones mayores de 18 años, y el pico de eficacia se observa al año de haber iniciado el tratamiento. Trueb demuestra que finasteride es eficaz en AA posmenopáusica, en ausencia de hiperandrogenismo, a dosis de 2,5mg/día (en un número pequeño de pacientes)70, y Iorizzo et al. ensayan en mujeres premenopáusicas asociándolo a un anovulatorio con buenos resultados71. En este último grupo de mujeres hemos de tener en cuenta el riesgo de feminización del feto masculino, por lo que debe usarse con anticoncepción eficaz. La formulación magistral nos podrá facilitar la prescripción de finasteride a dosis de 2,5mg, que parece la más recomendada para mujeres (tabla 26).
El resto de tratamientos orales no son objeto de la formulación magistral.
Alopecia areataLa AAR constituye una consulta dermatológica frecuente. Antes de decidir una opción terapéutica valoraremos la extensión de la enfermedad, la edad del paciente, la repercusión psicológica, los factores de mal pronóstico y los posibles riesgos y beneficios del tratamiento. El curso evolutivo suele ser recurrente con tendencia a remisiones espontáneas y recaídas posteriores, lo que dificulta el conocer con exactitud la verdadera eficacia de los diferentes tratamientos, por lo que no hay una terapia definitiva y satisfactoria para la AAR72.
Tratamientos localesLos tratamientos más eficaces son los corticoides intralesionales y la inmunoterapia de contacto. Los corticoides tópicos, la antralina y el minoxidil son ampliamente utilizados, pero carecemos de ensayos bien controlados que demuestren su eficacia en la AAR73. Comentaremos aquellos tratamientos en los que la formulación magistral va a facilitar la terapéutica de esta patología (tabla 27).
Alopecia areata. Tratamientos tópicos
| Fórmulas magistrales con irritantes | |
| Peróxido de benzoilo 10-20%Gel hidroalcohólico csp 100 ml.Ditranol 1%Ácido salicílico 1-2%Emulsión w/o csp 30 g“terapia de contacto corta” | |
| Fórmulas magistrales: corticoides y minoxidil | |
| Clobetasol 0,05%Solución hidroalcohólica csp. 100ml (gel hidroalcohólico) | Clobetasol 0,05% (betametasona 0,1%)Ác. salicílico 3-4%EtanolLavanda 75mlAgua de rosas 25ml |
| Minoxidil (4-5%)Solución HA csp. 100ml (gel HA) | Minoxidil (4-5%)Clobetasol 0,05% (DMSO 5%)Solución HA csp. 100ml (gel HA) |
| Fórmula magistral con difenciprona | |
| Difenciprona (0,0001-2%)Acetona csp. 50 ccConservar en botella opaca y en neveraSecuencia habitual: 0,0001%, 0,001%, 0,01%, 0,05%, 0,1%, 0,5%, 1%En parche inicial: 2% | |
DMSO: dimetilsulfóxido. Es un incrementador, aumenta la absorción del corticoide. Su adición a la fórmula es opcional; HA: hidroalcohólico/a.
Peróxido de benzoilo. Se ha descrito útil en el tratamiento de placas localizadas de AAR, como irritante, pero faltan estudios clínicos controlados73. Se formula a una concentración mayor a la utilizada en el acné y se puede indicar en la edad pediátrica.
Ditranol (antralina). Hay series de casos no controlados que evalúan la eficacia del ditranol tópico74. Su mecanismo de acción se atribuye a su efecto inmunomodulador y a su capacidad irritativa por contacto. Hay 2 modalidades de contacto: al 0,25-0,5% toda la noche o al 1% en «terapia de contacto corta». Preferimos la modalidad de aplicación de contacto corta porque disminuye los efectos secundarios. Se formula en un vehículo graso como una emulsión de fase externa oleosa, vaselinas e incluso en pasta lassar para localizar el producto en la zona a tratar, y así evitar la irritación perilesional y la pigmentación de los orificios foliculares. Para garantizar la efectividad del ditranol debemos asociar en la fórmula ácido salicílico, que actuará como antioxidante.
Corticoides tópicos. La eficacia de los corticoides potentes es limitada y controvertida, pero se utilizan ampliamente75. Indicados en la alopecia areata focal o multifocal, para algunos autores no son eficaces en monoterapia. Los geles hidroalcohólicos o semifluidos nos ayudarán a focalizar la aplicación. Asociados a minoxidil pueden incrementar su efectividad. Tosti et al. logran respuestas con el propionato de clobetasol al 0,05% en oclusión en pacientes con AAR total/universal76. Puede aparecer foliculitis, sobre todo con las emulsiones y menos con las soluciones y los geles; las telangiectasias y atrofia raramente se desarrollan como efectos secundarios.
Minoxidil. Se ha postulado un posible efecto inmunosupresor del minoxidil, además de los mecanismos de acción ya comentados en este artículo. Se describen respuestas de hasta el 63% en los pacientes tratados con minoxidil tópico al 3%77. Otro estudio también demuestra la mayor eficacia del minoxidil tópico al 5% comparado con el 1%78, pero otros estudios no demuestran esta eficacia. El efecto del minoxidil podría beneficiarse de la asociación con corticoides tópicos, antralina y ácido retinoico.
Análogos de las prostaglandinas. Tanto el latanoprost al 0,005% como el bimatoprost al 0,03% pueden suponer una de las pocas alternativas para el tratamiento de la AAR de pestañas, tal como se describe en dos amplias series de pacientes79,80. Hoy por hoy es difícil conseguir la materia prima, pero podemos modificar el producto comercial para poder localizar mejor su aplicación en el borde palpebral. A una mayor demanda quizás se puedan conseguir, en un futuro, estos análogos de las prostaglandinas para formular un mayor volumen y en un vehículo adecuado.
Inmunoterapia de contacto. La inmunoterapia con difenciprona constituye el tratamiento de elección en adultos, con una afectación mayor al 50% del cuero cabelludo. Consiste en la inducción periódica de una dermatitis alérgica de contacto por la aplicación de un agente sensibilizante potente para provocar un efecto inmunomodulador local. El agente más eficaz y no mutagénico es la difenciprona. Lo formulamos en acetona para que sea más estable frente a la degradación por la radiación UV.
Como agente sensibilizante inicial se prepara una solución de difenciprona al 2% bien en un disolvente orgánico, bien en acetona o en vaselina. Una vez efectuada la sensibilización a las 2 semanas se realiza una batería de soluciones en acetona de diferente concentración y se determina la mínima concentración que desarrolla la respuesta sensibilizante en forma de leve eritema. Podemos no realizar la batería e iniciar las aplicaciones con concentraciones muy bajas (0,0001%) e ir aumentando según la respuesta. El tratamiento se aplica semanalmente, pero también se puede aplicar 2 o 3 veces a la semana, según la respuesta. Varios son los estudios que demuestran su eficacia81; se consiguen tasas de respuesta de un 50 a un 60%, pero las recaídas son frecuentes. Es importante conocer que la respuesta puede iniciarse a los 6 meses de tratamiento, por lo que no se debería suspender el mismo antes de este intervalo.
Fotoquimioterapia (PUVA). Hay varios estudios no controlados que utilizan la PUVA en diferentes modalidades (psoralenos tópicos u orales) con diferentes respuestas; algunos hablan de incluso un 80% de respuesta82, aunque también hay estudios que sugieren que la respuesta es muy baja83. La ventaja de la formulación magistral en el tratamiento oral es la de poder incluir, en cada cápsula, la dosis necesaria para cada paciente (0,6mg/kg, toma previa a la sesión), y en el tratamiento tópico poder realizar una fórmula con psoraleno en solución al 0,0001% (1g/l) y aplicarlo en «turbante»84, o diluyendo una solución hidroalcohólica de 8-MOP al 0,5% en 5 litros de agua o en emulsión al 0,05% para localizar mejor la zona de aplicación. De todos modos, situamos este tratamiento en último lugar por la falta de eficacia demostrada, la alta tasa de recaídas y el incremento del riesgo de malignidades cutáneas.
Tratamientos sistémicosTratamientos como los corticoides sistémicos, ciclosporina, sulfasalazina y MTX están ampliamente comercializados, por lo que no van a ser comentados (tabla 28).
Alopecia areata: tratamientos sistémicos
| Sales de zinc | ||
| Sulfato de zinc 150mg p. una cápsulaN° =100 | Gluconato de zinc200mg p. una cápsula (o para una cápsula gastrorresistente)N° =100 | |
| PUVA-terapia | ||
| 8-MOPX* mg (0,6mg/kg/día)N° 60 | 8-MOP 0,05%Emulsión O/W csp.60g | 8-MOP 0,5%Solución hidroalcohólica csp. 15mlDiluyendo 1ml de esta solución en 5 litros de agua conseguimos una solución de 8-MOP al 0,0001%** |
*La dosis se calcula en función del peso, 0,6mg/kg.
** Se sumerge una toalla de algodón en agua con 0,0001% de 8-MOP (1mg/l), a 37°C. Se elimina el exceso de agua y se envuelve la cabeza del paciente a modo de turbante durante 20 minutos. Seguidamente se expone a los rayos UVA. Se realizan de 3 a 4 sesiones por semana.
Cinc. Se han publicado diferentes estudios en los que tratan a los pacientes afectos de AAR con sales de cinc, obteniendo resultados alentadores. Se usan tanto el gluconato de cinc como el aspartato y el sulfato de cinc. Park et al. sugieren que los suplementos con gluconato de cinc (200mg/día)85 en pacientes con AAR, que tienen niveles séricos de cinc bajos, pueden ser un tratamiento adyuvante. Las dosis que se recomiendan en los artículos son muy superiores a los suplementos vitamínicos comercializados, por lo que sería necesaria su formulación. Hay que tener en cuenta que se deben tomar tras las comidas, y en caso de intolerancia gastrointestinal se pueden preparar en cápsulas gastrorresistentes.
ConclusionesLa FM es un tema que sigue generando debate, pero cada vez queda más claro su importante papel y utilidad en la Dermatología actual. El medicamento personalizado permite cubrir lagunas terapéuticas y facilitar la administración y el cumplimiento de los tratamientos. Es responsabilidad del médico formulador conocer los principios activos, su dosificación, interacciones y propiedades de elaboración, por lo que es importante una buena comunicación con el farmacéutico. La información menos exhaustiva y la falta de prospectos normalizados en la FM son uno de los principales inconvenientes, lo que podría solventarse con la experiencia del dermatólogo formulador y el buen conocimiento de los productos prescritos, dando la máxima información al paciente y estando atentos ante cualquier posible efecto adverso. En un futuro podrían elaborarse prospectos más detallados de las principales formulaciones que se usan habitualmente, y si se consigue su regulación e inclusión en el sistema sanitario público los costes podrían ser menores.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.