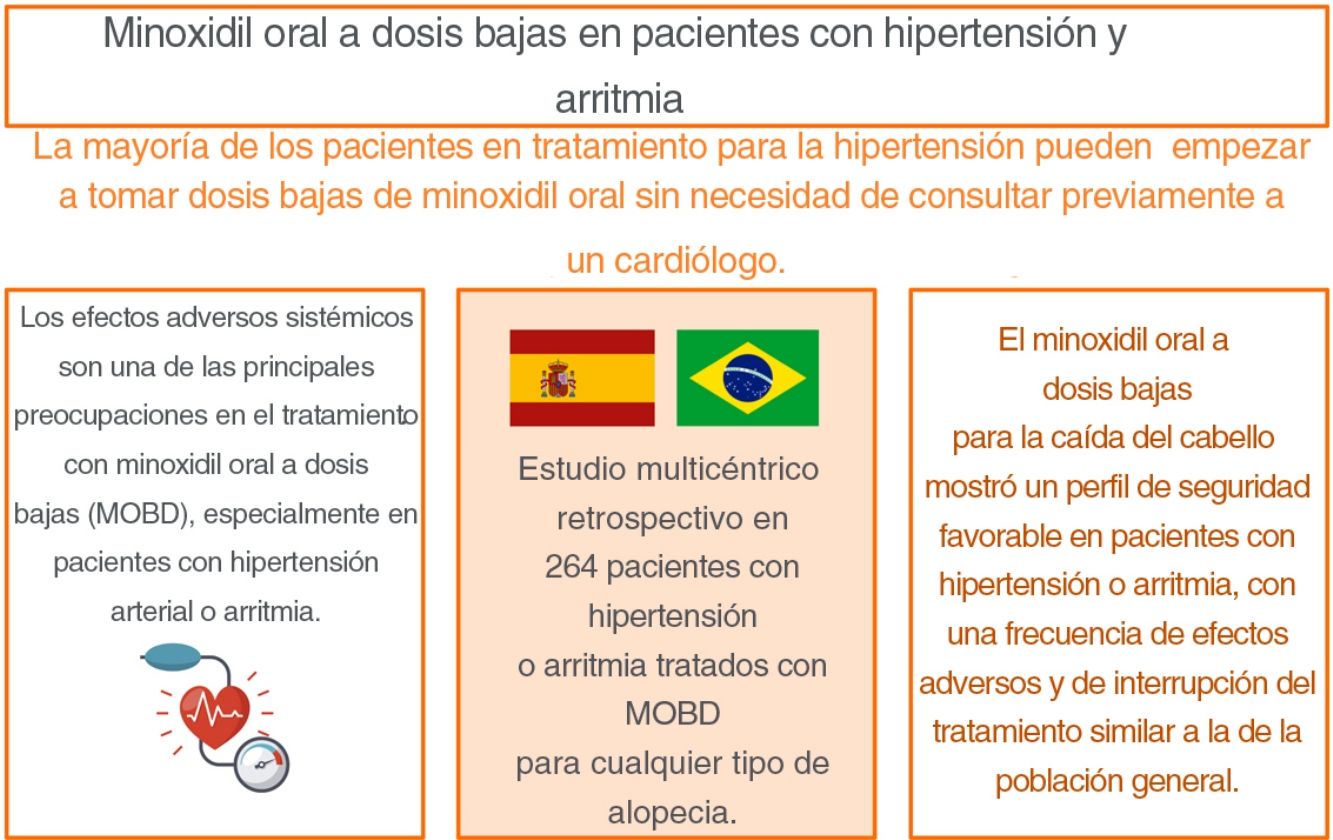
Los efectos adversos sistémicos son una de las principales limitaciones del uso de minoxidil oral a dosis bajas (MODB), especialmente en pacientes con hipertensión arterial o arritmias. El objetivo de este estudio fue evaluar la seguridad de MODB en estos pacientes.
Material y métodoEstudio retrospectivo multicéntrico con pacientes con antecedentes de hipertensión o arritmias tratados con MODB para cualquier tipo de alopecia.
ResultadosSe incluyó un total de 254 pacientes con hipertensión (176 mujeres [69,3%] y 78 hombres [30,7%]) con una edad media de 56,9 años (rango 19 – 82). La dosis de MODB se incrementó gradualmente en 128 pacientes, obteniendo un total de 382 dosis analizadas. Los sujetos estaban tomando de media 1,45 fármacos antihipertensivos (rango 0 – 5). Se detectaron EA sistémicos en 26 casos (6,8%), incluyendo mareo (3,1%), retención de líquidos (2,6%), malestar general (0,8%), taquicardia (0,8%) y cefalea (0,5%), requiriendo suspensión del MODB en seis casos (1,5%). Los pacientes en tratamiento con doxazosina (p < 0,001) o con tres o más antihipertensivos (p = 0,012) presentaron mayor riesgo de suspensión de MODB.
ConclusiónEl tratamiento con MODB mostró un perfil de seguridad favorable en pacientes con hipertensión o arritmias, similar al de la población general.
Systemic adverse effects (AE) are a major concern of low-dose oral minoxidil (LDOM) treatment, especially in patients with arterial hypertension or arrhythmia. The objective of this study was to evaluate the safety of LDOM in patients with hypertension or arrhythmia.
Patients and methodsRetrospective multicenter study of patients with hypertension or arrhythmia treated with LDOM for any type of alopecia.
ResultsA total of 254 patients with hypertension [176 women (69.3%) and 78 men (30.7%)] with a mean age of 56.9 years (range 19–82) were included. From them, the dose of LDOM was titrated in 128 patients, allowing the analysis of 382 doses. Patients were receiving a mean of 1.45 (range 0–5) antihypertensive drugs. Systemic AE were detected in 26 cases (6.8%) and included lightheadedness (3.1%), fluid retention (2.6%), general malaise (0.8%), tachycardia (0.8%) and headache (0.5%), leading to LDOM discontinuation in 6 cases (1.5%). Prior treatment with doxazosin (P<0.001), or with three or more antihypertensive drugs (P=0.012) was associated with a higher risk of discontinuation of LDOM.
ConclusionsLDOM treatment showed a favorable safety profile in patients with hypertension or arrhythmia, similar to general population.
El minoxidil es un vasodilatador arteriolar aprobado en la década de 1970 como tratamiento de la hipertensión refractaria grave, con una dosis estándar que oscilan entre 10 y 40mg diarios (hasta 100mg/día)1. En los últimos años, el minoxidil oral a dosis bajas (MODB) se ha utilizado cada vez con mayor frecuencia en el tratamiento de distintos tipos de alopecia, teniendo el respaldo de numerosos estudios que describen su eficacia y su perfil de seguridad favorable2,3. Uno de los estudios más amplios describió exhaustivamente la frecuencia y cronología de los efectos adversos (EA) del tratamiento con MODB en 1404 pacientes4. La hipertricosis es un EA bien conocido y el más frecuente de MODB y se presentará en aproximadamente el 15% de los pacientes4,5. Aunque son infrecuentes, pueden producirse EA sistémicos que, en una minoría de pacientes, conducen a la interrupción del tratamiento con MODB. La mayoría de los EA sistémicos están relacionados con el efecto cardiovascular y hemodinámico del minoxidil, incluyendo la presencia de mareos (vértigo, hipotensión postural), retención de líquidos (edema de miembros inferiores o facial), taquicardia (palpitaciones), alteraciones del electrocardiograma (principalmente en la onda T), cefalea, insomnio, pesadillas o aumento del apetito1,4,6,7. Estos EA son generalmente bien tolerados y se resuelven tras la interrupción o el ajuste de la dosis del MODB. Se han notificado EA graves con dosis altas de minoxidil oral cuando se utiliza para la hipertensión grave o debido a errores de composición en el tratamiento de la caída del cabello, incluyendo síncope hipotensor, pericarditis, derrame pericárdico o infarto de miocardio1,8.
Los EA sistémicos representan la principal preocupación del tratamiento con MODB en la población general con pérdida de cabello, que en su mayoría son adultos sanos de mediana edad. Teniendo en cuenta que el MODB se utiliza como un tratamiento que está fuera de ficha técnica, estos problemas de seguridad adquieren mayor importancia cuando se prescribe en situaciones especiales, como pacientes con antecedentes personales de hipertensión arterial (HTA) o arritmia. Aún se desconoce si el MODB podría potenciar el efecto hipotensor de otros fármacos antihipertensivos o aumentar el riesgo de EA sistémicos en estos pacientes.
El objetivo de este estudio fue evaluar la seguridad del MODB en el tratamiento de la caída del cabello en pacientes con HTA o arritmia.
MétodosEste estudio de tipo retrospectivo, descriptivo y multicéntrico incluyó pacientes adultos con antecedentes personales de HTA o arritmia que estaban en tratamiento con MODB para la pérdida de cabello de cualquier causa durante al menos un mes; los pacientes se incluyeron a partir de cinco centros de Brasil y España, desde enero de 2018 hasta abril de 2022. La duración mínima del tratamiento de un mes se estableció teniendo en cuenta la cronología de los EA de MODB previamente descrita4. Los datos epidemiológicos, médicos y de seguridad se recogieron de los registros médicos de los pacientes, incluidos los tratamientos previos para la HTA, los EA y la necesidad de retirar o ajustar la dosis de MODB o los tratamientos antihipertensivos. En algunos pacientes, la dosis de MODB se tituló en función de la respuesta y la tolerabilidad, y los parámetros anteriores se analizaron para cada dosis.
El análisis estadístico se realizó con IBM SPSS Statistics (Versión 25.0: IBM Corp., 2017). Las variables continuas se expresaron como media (rango). Se utilizó la regresión logística para identificar las variables asociadas con un mayor riesgo de EA sistémicos, suspensión o ajuste de los tratamientos con MODB o antihipertensivos, que se consideraron estadísticamente significativas si el valor P era<0,05.
ResultadosHipertensiónSe incluyeron 254 pacientes [176 mujeres (69,3%) y 78 hombres (30,7%)] con una edad media de 56,9 años (rango 19-82). De ellos, se tituló la dosis de MODB en varias dosis incrementándolas según la tolerancia en 82 pacientes (32,2%), lo que permitió analizar 382 dosis diferentes. La dosis media de MODB fue de 1,59mg (rango 0,2-10) y la duración media fue de 10,9 meses (1-51). El MODB fue la única terapia sistémica para la caída del cabello en 124 pacientes (48,8%). En los pacientes restantes, el fármaco concomitante más frecuente fue la dutasterida oral. La indicación más frecuente para el tratamiento con MODB fue la alopecia androgenética (68,9%), seguida de la alopecia frontal fibrosante (10,2%), el efluvio telógeno (4,3%), el liquen plano pilar (3,5%), la alopecia fibrosante en patrón de distribución (3,1%), la alopecia areata (2,4%) y otros tipos de alopecia menos frecuentes.
Antes del tratamiento con MODB, los pacientes recibían una media de 1,4 fármacos antihipertensivos (rango 0-5). Sólo 5 pacientes (1,3%) no recibían tratamiento para la HTA. La clase de fármacos más frecuente fueron los antagonistas de los receptores de la angiotensina II (ARA-II) en 190 pacientes (49,7%), seguidos de las tiazidas (28,5%), los betabloqueantes (28%) y otros (tabla 1).
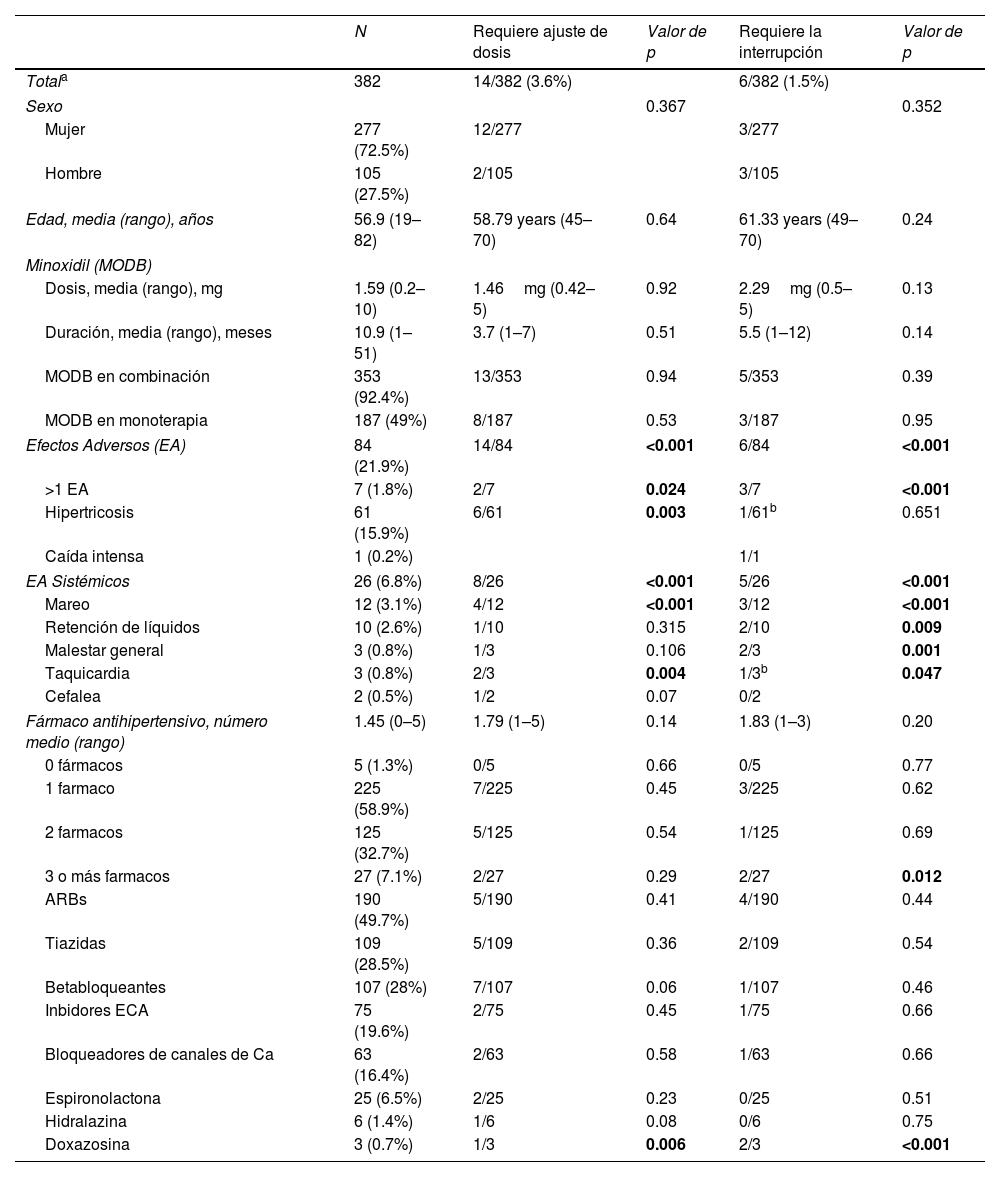
Descripción de la cohorte de pacientes con hipertensión tratados con minoxidil oral a dosis bajas (MODB) y de los subgrupos que requirieron ajuste de dosis y suspensión de MODB
| N | Requiere ajuste de dosis | Valor de p | Requiere la interrupción | Valor de p | |
|---|---|---|---|---|---|
| Totala | 382 | 14/382 (3.6%) | 6/382 (1.5%) | ||
| Sexo | 0.367 | 0.352 | |||
| Mujer | 277 (72.5%) | 12/277 | 3/277 | ||
| Hombre | 105 (27.5%) | 2/105 | 3/105 | ||
| Edad, media (rango), años | 56.9 (19–82) | 58.79 years (45–70) | 0.64 | 61.33 years (49–70) | 0.24 |
| Minoxidil (MODB) | |||||
| Dosis, media (rango), mg | 1.59 (0.2–10) | 1.46mg (0.42–5) | 0.92 | 2.29mg (0.5–5) | 0.13 |
| Duración, media (rango), meses | 10.9 (1–51) | 3.7 (1–7) | 0.51 | 5.5 (1–12) | 0.14 |
| MODB en combinación | 353 (92.4%) | 13/353 | 0.94 | 5/353 | 0.39 |
| MODB en monoterapia | 187 (49%) | 8/187 | 0.53 | 3/187 | 0.95 |
| Efectos Adversos (EA) | 84 (21.9%) | 14/84 | <0.001 | 6/84 | <0.001 |
| >1 EA | 7 (1.8%) | 2/7 | 0.024 | 3/7 | <0.001 |
| Hipertricosis | 61 (15.9%) | 6/61 | 0.003 | 1/61b | 0.651 |
| Caída intensa | 1 (0.2%) | 1/1 | |||
| EA Sistémicos | 26 (6.8%) | 8/26 | <0.001 | 5/26 | <0.001 |
| Mareo | 12 (3.1%) | 4/12 | <0.001 | 3/12 | <0.001 |
| Retención de líquidos | 10 (2.6%) | 1/10 | 0.315 | 2/10 | 0.009 |
| Malestar general | 3 (0.8%) | 1/3 | 0.106 | 2/3 | 0.001 |
| Taquicardia | 3 (0.8%) | 2/3 | 0.004 | 1/3b | 0.047 |
| Cefalea | 2 (0.5%) | 1/2 | 0.07 | 0/2 | |
| Fármaco antihipertensivo, número medio (rango) | 1.45 (0–5) | 1.79 (1–5) | 0.14 | 1.83 (1–3) | 0.20 |
| 0 fármacos | 5 (1.3%) | 0/5 | 0.66 | 0/5 | 0.77 |
| 1 farmaco | 225 (58.9%) | 7/225 | 0.45 | 3/225 | 0.62 |
| 2 farmacos | 125 (32.7%) | 5/125 | 0.54 | 1/125 | 0.69 |
| 3 o más farmacos | 27 (7.1%) | 2/27 | 0.29 | 2/27 | 0.012 |
| ARBs | 190 (49.7%) | 5/190 | 0.41 | 4/190 | 0.44 |
| Tiazidas | 109 (28.5%) | 5/109 | 0.36 | 2/109 | 0.54 |
| Betabloqueantes | 107 (28%) | 7/107 | 0.06 | 1/107 | 0.46 |
| Inbidores ECA | 75 (19.6%) | 2/75 | 0.45 | 1/75 | 0.66 |
| Bloqueadores de canales de Ca | 63 (16.4%) | 2/63 | 0.58 | 1/63 | 0.66 |
| Espironolactona | 25 (6.5%) | 2/25 | 0.23 | 0/25 | 0.51 |
| Hidralazina | 6 (1.4%) | 1/6 | 0.08 | 0/6 | 0.75 |
| Doxazosina | 3 (0.7%) | 1/3 | 0.006 | 2/3 | <0.001 |
ECA: enzima convertidora de angiotensina; EA: efectos adversos; BRA: antagonistas de los receptores de la angiotensina II; MODB: minoxidil oral en dosis bajas; El valor de p se considera estadísticamente significativo si <0,05 (negrita).
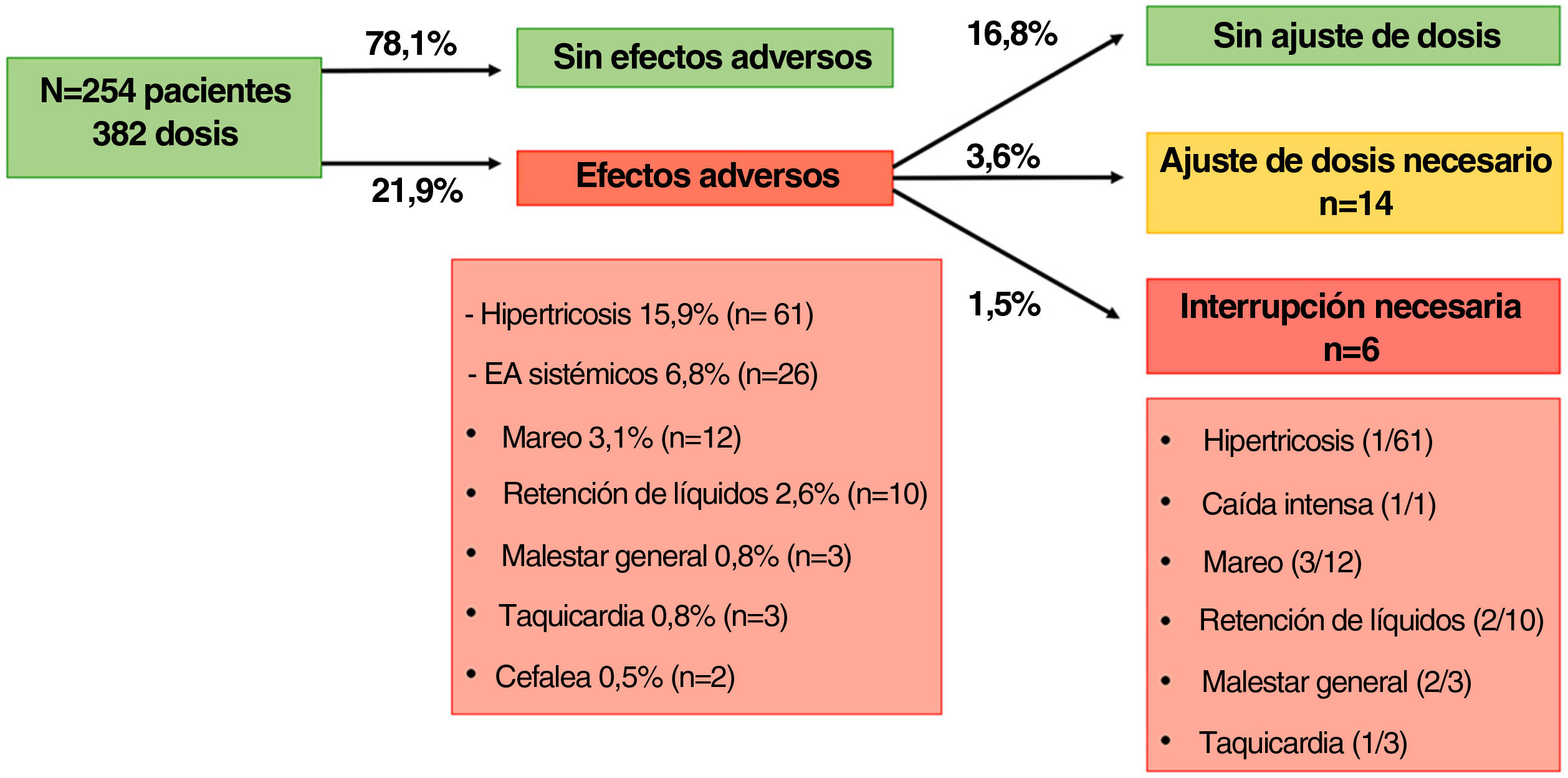
Se detectaron EA en 71 pacientes (27,9%) con 84 dosis (21,9%). El EA más frecuente fue la hipertricosis en 49 pacientes (19,2%) con 61 dosis (15,9%), dado que 7 pacientes (2,7%) desarrollaron hipertricosis con varias dosis. Se identificaron EA sistémicos en 23 pacientes (9%) con 26 dosis (6,8%) y entre estos se incluyeron los mareos (n=12; 3. 1%), la retención de líquidos (n=10; 2,6%), el malestar general (n=3; 0,8%), taquicardia (n=3; 0,8%) y cefalea (n=2; 0,5%). Cinco pacientes (1,9%) desarrollaron más de un EA: hipertricosis más mareo (n=2), hipertricosis más taquicardia (n=1), mareo más malestar general (n=1), y mareo más malestar general más retención de líquidos (n=1, que requirió la interrupción del MODB).
Todos los EA mejoraron con el ajuste de la dosis o la interrupción del fármaco, y no se observaron EA potencialmente mortales. La dosis de MODB se redujo en 14 casos (3,6%), de los cuales 8 se debieron a EA sistémicos y 6 a hipertricosis. Fue necesario interrumpir el tratamiento con MODB en 6 casos (1. 5%) debido a una intensa caída del cabello (n=1), retención de líquidos (n=1), mareos (n=1), mareos más malestar general (n=1), mareo, malestar general más retención de líquidos (n=1), y taquicardia más hipertricosis (n=1; este paciente interrumpió el MODB por taquicardia, luego reinició el tratamiento sin EA sistémicos, y volvió a interrumpirlo al cabo de 1 año por hipertricosis).
El EA más frecuente que condujo al ajuste o la retirada de la MODB fue el mareo (n=7; P<0,001). La hipertricosis se asoció con un mayor riesgo de ajuste de la dosis (P=0,003), pero no con la interrupción (P=0,65). La edad, el sexo y la dosis de MODB no se asociaron con el riesgo de EA sistémicos ni con el ajuste de MODB. Otros factores asociados con el ajuste y la retirada de MODB se muestran en la tabla 1.
Los pacientes que recibían 3 o más fármacos antihipertensivos tenían mayor riesgo de desarrollar más de 1 EA (P<0,001), mareo (P<0,001), malestar general (P<0,001) y de requerir la interrupción del MODB (P=0,012). Asimismo, el tratamiento previo con doxazosina se asoció a un mayor riesgo de mareo (P<0,001), malestar general (P<0,001), retención de líquidos (P=0,01) y necesidad tanto de ajustar la dosis (P=0,006) como de retirar el MODB (P<0,001).
En cuanto al tratamiento antihipertensivo, sólo dos pacientes (0,7%) requirieron un ajuste o la interrupción de su tratamiento previo. Una mujer de 67 años tratada con minoxidil 0,5mg y espironolactona 50mg diarios, desarrolló hipotensión sintomática cuatro días después de cambiar de ramipril a olmesartán (por su médico de cabecera). Se suspendió el olmesartán y se controló la HTA con minoxidil y espironolactona. La otra paciente era una mujer de 71 años cuyo tratamiento previo con losartán se suspendió debido al buen control de su HTA con minoxidil 2,5mg diarios. El resto de pacientes no refirieron cambios o alteraciones de su HTA durante el tratamiento con MODB.
ArritmiaSe incluyeron un total de 10 pacientes (8 mujeres y 2 hombres) con una mediana de edad de 61 años (rango 37-74). De ellos, se tituló la dosis de MODB en tres pacientes, lo que permitió analizar 15 dosis. La mediana de la dosis de MODB fue de 0,75mg (rango 0,25-5) y la mediana de la duración fue de 5 meses (rango 1-11). La indicación más frecuente para el tratamiento con MODB fue la alopecia androgenética (n=6), seguida del efluvio telógeno crónico (n=2), y la alopecia frontal fibrosante (n=2). Nueve pacientes tenían antecedentes personales de arritmia, entre ellas, extrasístole supraventricular (n=3), fibrilación auricular (n=1), taquicardia sinusal (n=1), síncope cardiaco (n=1) y arritmia desconocida (n=3, faltaban datos). De ellos, cuatro pacientes estaban bajo tratamiento médico con betabloqueantes (n=3) o amiodarona (n=1), dos pacientes se habían sometido a una ablación cardíaca, un paciente tenía un marcapasos y dos pacientes no recibían ningún tratamiento. El paciente restante tenía una válvula aórtica mecánica debido a un aneurisma aórtico reparado por el procedimiento de Bentall. De estos 10 pacientes, en cinco de ellos se realizó una consulta con el cardiólogo antes de iniciar el tratamiento con MODB.
Sólo se notificaron EA sistémicos en un paciente con extrasístole supraventricular en tratamiento con carvedilol que desarrolló edema periorbitario y de pies con MODB 1mg, que se resolvió tras ajustar la dosis a 0,25mg. Ningún paciente notificó palpitaciones, empeoramiento de su arritmia previa ni ningún otro EA cardiológico, y ninguno de ellos requirió una modificación de su tratamiento médico previo.
DiscusiónHasta donde sabemos, éste representa el primer estudio sobre la seguridad del MODB en pacientes con HTA o arritmia. Numerosos estudios han demostrado su perfil de seguridad favorable en población general2–4,6 y estudios recientes han investigado el uso de MODB en situaciones especiales como en la población pediátrica9, adolescente10 y anciana11, pero hay escasos datos de su uso en pacientes con HTA o arritmia. La prevalencia global de HTA en adultos es del 34%12, por lo que parece importante ampliar el conocimiento sobre el manejo y los aspectos de seguridad del tratamiento con el MODB en estos pacientes.
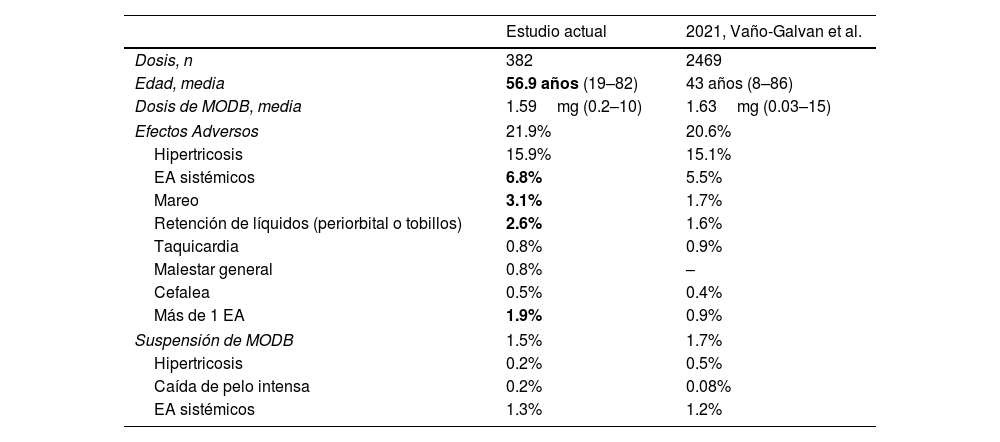
En nuestra cohorte de pacientes hipertensos tratados con el MODB, la frecuencia global y el tipo de EA fueron consistentes con los encontrados en estudios recientes2–4. Se detectaron EA en el 21,9% de los casos, y la hipertricosis fue el más frecuente (15,9%), de forma similar a los datos encontrados por Vaño-Galván et al4. Sin embargo, encontramos una mayor frecuencia de EA cardiovasculares (mareo y retención de líquidos), y más pacientes que presentaron más de 1 EA (tabla 2).
Descripción de la frecuencia de los efectos adversos y de la interrupción de las dosis bajas de minoxidil oral (MODB) encontrados en pacientes hipertensos (estudio actual) y en población general (estudio de Vaño-Galván)
| Estudio actual | 2021, Vaño-Galvan et al. | |
|---|---|---|
| Dosis, n | 382 | 2469 |
| Edad, media | 56.9 años (19–82) | 43 años (8–86) |
| Dosis de MODB, media | 1.59mg (0.2–10) | 1.63mg (0.03–15) |
| Efectos Adversos | 21.9% | 20.6% |
| Hipertricosis | 15.9% | 15.1% |
| EA sistémicos | 6.8% | 5.5% |
| Mareo | 3.1% | 1.7% |
| Retención de líquidos (periorbital o tobillos) | 2.6% | 1.6% |
| Taquicardia | 0.8% | 0.9% |
| Malestar general | 0.8% | – |
| Cefalea | 0.5% | 0.4% |
| Más de 1 EA | 1.9% | 0.9% |
| Suspensión de MODB | 1.5% | 1.7% |
| Hipertricosis | 0.2% | 0.5% |
| Caída de pelo intensa | 0.2% | 0.08% |
| EA sistémicos | 1.3% | 1.2% |
El mareo y la taquicardia se asociaron significativamente con un mayor riesgo tanto de ajuste como de suspensión del MODB (tabla 1). La hipertricosis se asoció al ajuste de dosis pero no a la suspensión, lo que apoya que este EA suele ser bien tolerado. Los pacientes tratados con tres o más fármacos antihipertensivos presentaron un mayor riesgo de mareo y de suspensión del MODB. Entre todos los fármacos antihipertensivos, la doxazosina provocó un mayor riesgo de mareo, retención de líquidos y suspensión del MODB. Esto podría explicarse por el hecho de que la doxazosina es un bloqueante alfaadrenérgico que también provoca vasodilatación arteriolar13, lo que podría producir un efecto sinérgico con el minoxidil. Aunque podría ser plausible que otros vasodilatadores, como la hidralazina o los antagonistas del calcio, aumentaran este efecto sinérgico con el minoxidil, no encontramos una asociación estadísticamente significativa.
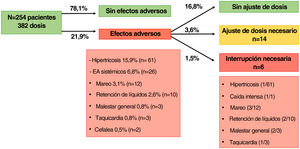
El mareo (también denominado vértigo o hipotensión postural) fue el EA sistémico más frecuente y la causa más común tanto de ajuste como de interrupción del MODB (fig. 1). En general fue leve y se notificó con mayor frecuencia en verano y por la mañana. No hubo casos de hipotensión grave ni de alteración del control de la presión arterial (PA). A este respecto, dos estudios recientes investigaron la variación de la PA en pacientes varones tratados con 5mg de MODB mediante monitorización ambulatoria de la PA durante 24h. Encontraron una ligera reducción de la PA en las 2h posteriores a la toma de MODB 14 y en la semana 247. Pocos estudios adicionales han evaluado la PA durante el tratamiento con MODB a dosis entre 0,45 y 5mg, obteniendo resultados similares15–17. Esto concuerda con estudios de los años setenta con minoxidil de 2,5mg, 5mg y 10mg que encontraron un efecto hipotensor mínimo o nulo en pacientes normotensos18.
Diagrama de flujo que describe el tipo y la frecuencia de los efectos adversos, el ajuste de la dosis y la interrupción del tratamiento con MODB en pacientes hipertensos.* La suma de las frecuencias individuales puede diferir de la frecuencia total porque algunos pacientes desarrollaron más de un efecto adverso.
La retención de líquidos (principalmente edema de pies; sólo 2 casos de edema facial) se detectó en nuestro estudio en el 2,6% de los pacientes, lo que supone una frecuencia ligeramente superior a la de estudios previos en población general3,4, pero muy inferior al tratamiento con dosis estándar (7%)1. No encontramos una frecuencia inferior en los pacientes que tomaban diuréticos como antihipertensivos (tiazidas o espironolactona).
La taquicardia solo se detectó en el 0,8% de los pacientes con hipertensión arterial, requiriendo todos ellos ajuste o suspensión del MODB. La taquicardia es el resultado de una activación simpática refleja inducida por el efecto vasodilatador del minoxidil oral, y tradicionalmente se describe como un EA frecuente con la dosis estándar1. Sin embargo, los estudios con el MODB han demostrado que las palpitaciones son bastante infrecuentes y transitorias, apareciendo generalmente dentro de las primeras tomas del MODB4,7,15,17.
Los cambios en el electrocardiograma son otro EA común con la dosis estándar de minoxidil, presentando cambios en la dirección y en la magnitud de las ondas T hasta en el 60% de los pacientes, debido principalmente a un mecanismo de robo coronario asociado a la reducción de la presión arterial en las arterias coronarias. Son asintomáticas y suelen desaparecer a pesar de la continuación del tratamiento1. Solo en pocos estudios se han realizado electrocardiogramas en pacientes con MODB. Un estudio realizado en Tailandia encontró cambios asintomáticos en la onda T en el 10-20% de los pacientes (inversión de la onda T no isquémica en una derivación)15. Sanabria et al. encontraron un aumento no significativo en la aparición de extrasístole supraventricular y ventricular después de 24 semanas de tratamiento con 5mg del MODB, sin alteraciones notables en la repolarización ventricular en la monitorización Holter de 24h7.
De manera interesante, en esta cohorte de pacientes con arritmia, ningún paciente informó palpitaciones o empeoramiento de su enfermedad previa. A estos pacientes no se les realizó un electrocardiograma de rutina, pero cinco de ellos fueron remitidos a su cardiólogo, quien aprobó el tratamiento con MODB. Sin embargo, se debe extremar la precaución en pacientes con enfermedad coronaria o insuficiencia cardíaca crónica, ya que la taquicardia puede limitar la oxigenación del miocardio (fig. 2).
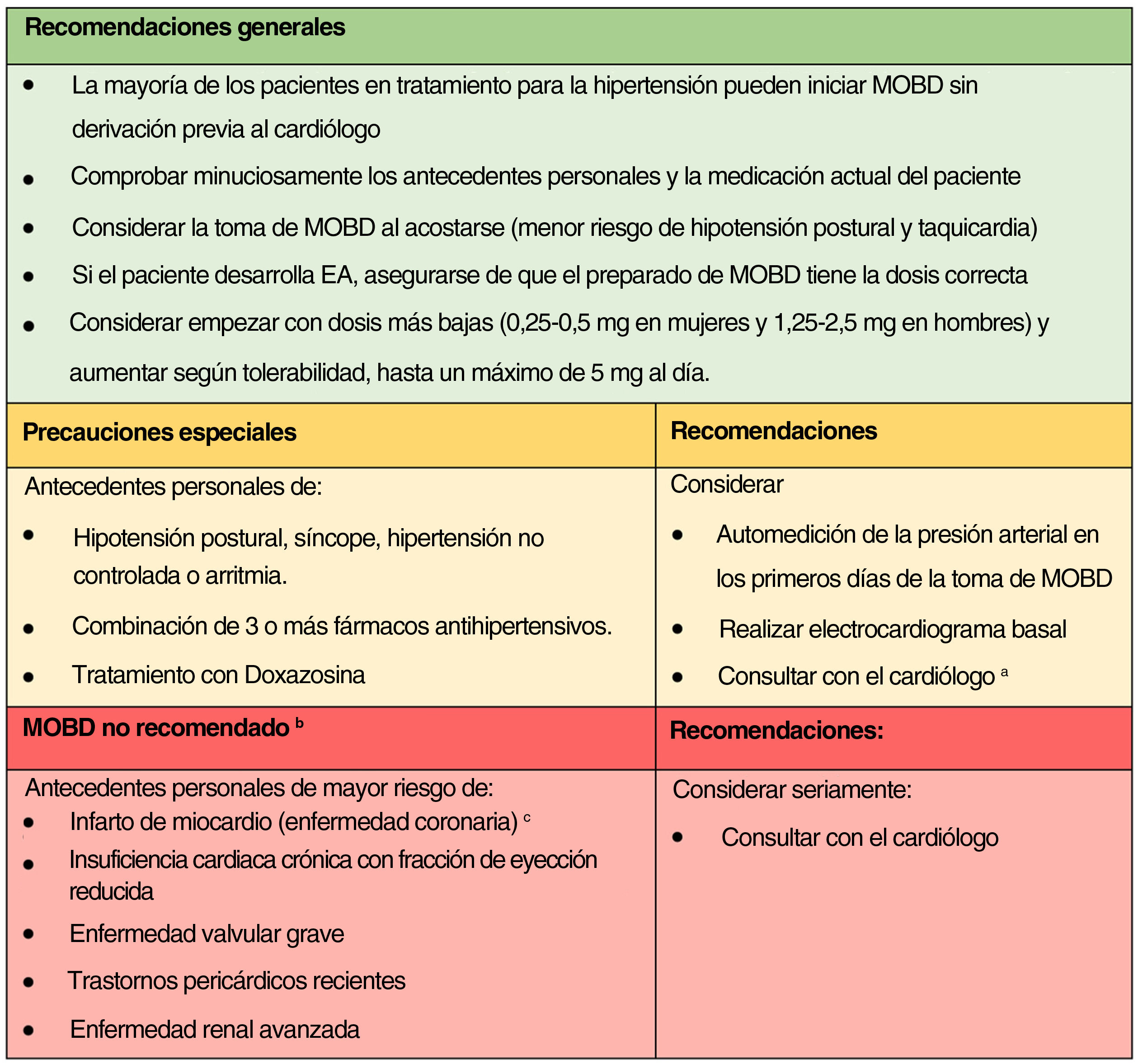
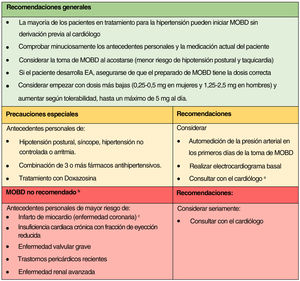
Recomendaciones para el manejo de la terapia con MODB en pacientes con hipertensión o arritmia (basadas en la experiencia clínica de los autores y los resultados de este estudio). a Comentario del cardiólogo: el dermatólogo puede considerar disminuir la dosis o cambiar la hora de ingesta del medicamento antihipertensivo anterior si el paciente desarrolla mareos. b Contraindicaciones según la monografía del producto minoxidil. c Comentario del cardiólogo: El MODB podría utilizarse después de un infarto de miocardio sólo una vez que se haya alcanzado un estado estable después del infarto (12 meses después). No usar si se trata de angina no revascularizada/evento isquémico.
De manera consistente con aquellos estudios previos de MODB, no se detectó ningún EA cardiovascular grave, como la presencia de síncopes, cardiopatía isquémica, pericarditis o derrame pericárdico. Estos EA se describieron con dosis estándar de minoxidil, pero ocurrieron principalmente en pacientes con enfermedades de base como el lupus eritematoso sistémico, la enfermedad renal avanzada o insuficiencia cardíaca congestiva, y son extremadamente raros con el MODB19,20.
Basándonos en nuestros resultados, la experiencia clínica de los autores en el tratamiento del MODB y la colaboración de un cardiólogo en este estudio (MR), la mayoría de los pacientes sometidos a tratamiento para la HTA pueden iniciar MODB sin necesidad de derivación previa al cardiólogo. Sin embargo, sugerimos algunas recomendaciones para el manejo de la terapia MODB en pacientes con HTA o arritmia (fig. 2).
Las limitaciones de este estudio fueron el diseño retrospectivo, la ausencia de un grupo control y la ausencia de la medición objetiva de la presión arterial y la realización de ECG.
En conclusión, el tratamiento con el MODB demostró un perfil de seguridad favorable en pacientes con HTA o arritmia, similar al de la población general. Los EA sistémicos más frecuentes fueron el mareo y la retención de líquidos, que mejoraron tras el ajuste o la retirada del MODB. La combinación de MODB con 3 o más fármacos antihipertensivos o con doxazosina se asoció con un mayor riesgo de estos EA sistémicos.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.