Introducción
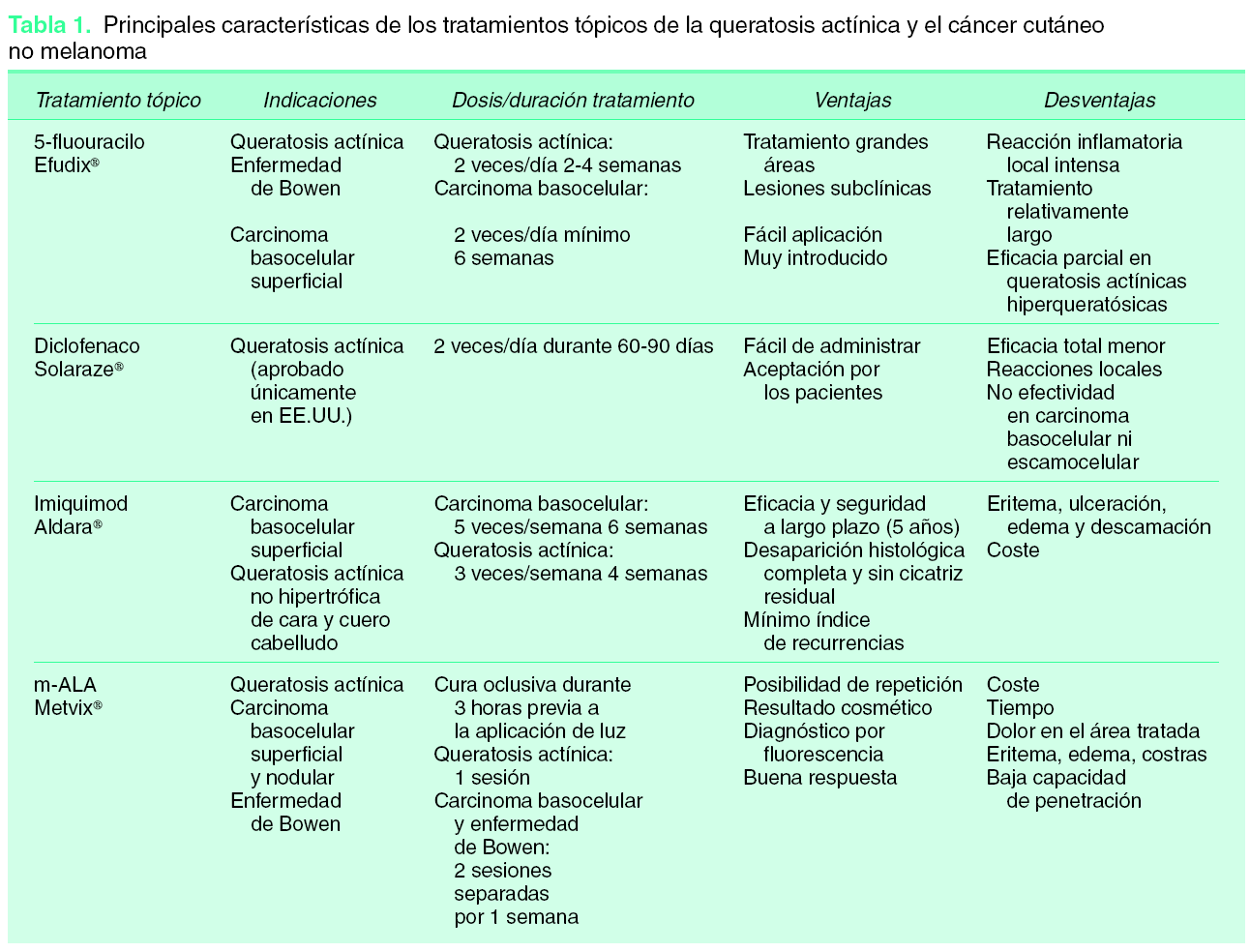
La incidencia tanto del cáncer cutáneo no melanoma como de las lesiones precursoras está en continuo aumento, por lo que es importante tener una adecuada formación oncológica, no solo para su correcto diagnóstico, sino también para que su manejo terapéutico sea el adecuado. Aunque es un tema controvertido, actualmente la mayoría de autores consideran que la queratosis actínica no es un precursor del carcinoma de células escamosas, sino un estadio inicial del mismo, y que por tanto debe ser tratada. Por otro lado, a pesar de que gran parte del cáncer cutáneo no melanoma es ya invasivo en el momento de su presentación clínica, requiriendo tratamientos quirúrgicos para su completa y segura erradicación, hay situaciones en las que la cirugía presenta ciertas limitaciones: cuando es mal tolerada por los pacientes, existe un número elevado de tumores y/o un área extensa a tratar, o es estéticamente inaceptable. Pues bien, hoy día es posible tratar de forma precoz y segura ciertas lesiones precancerosas y/o cancerosas superficiales sin tener que recurrir a tratamientos agresivos. Así, se han desarrollado distintas terapias para el tratamiento de la queratosis actínica y de algunas formas de cáncer cutáneo superficial no melanoma. Entre las diversas alternativas farmacológicas tópicas de que disponemos se encuentran los retinoides, el 5-fluoracilo, el diclofenaco, el imiquimod y la terapia fotodinámica (tabla 1).
Retinoides tópicos
Los retinoides son análogos de la vitamina A, hoy día ingredientes comunes de muchos productos cosméticos, ya que por su mecanismo de acción se les considera agentes con un cierto efecto de quimioprevención. Han demostrado en algunos estudios tener cierta efectividad en el tratamiento de las queratosis actínicas1. En un estudio en el que se aplicó tretinoína al 0,05 % una vez al día durante 3 meses se demostró una reducción del 45 % de las queratosis actínicas frente al 23 % en los pacientes tratados con placebo2. En otro estudio, sin embargo, no se consiguió disminuir el número de queratosis actínicas tras el uso de retinoides tópicos3. Sobre su eficacia en el tratamiento del carcinoma basocelular han aparecido escasos estudios y estos no han demostrado una eficacia suficiente4. Por ello, actualmente parecen tener interés únicamente en la prevención de lesiones precancerosas y como coadyuvantes de otros tratamientos5, y no se recomienda su uso en monoterapia.
Fluoracilo tópico
El 5-fluoracilo ha sido considerado durante años el tratamiento tópico de elección de las queratosis actínicas desde que fue aprobado por la Food and Drug Administration (FDA) en 19706.
Actúa bloqueando la síntesis del ADN por inhibición de la enzima timidilato sintetasa. Existen varias formulaciones de 5-fluoracilo, y está disponible tanto en crema (Efudix® 5 %, Fluoroplex® 1 % y Carac® 0,5 %) como en solución formulado al 5, 2 y 1 %. Está aprobado para el tratamiento de la queratosis actínica, la enfermedad de Bowen y el carcinoma basocelular superficial.
El régimen de tratamiento establecido para la queratosis actínica es de una aplicación dos veces al día durante 2-4 semanas, alcanzando una tasa de curación clínica completa del 82 %7. No se han encontrado diferencias de eficacia entre el fluoracilo al 1 % o al 5 %8.
Esta terapia permite el tratamiento de grandes áreas, así como de las lesiones subclínicas, sin embargo, tiene un inconveniente principal que aparece en todos los estudios revisados, que es la intensa reacción inflamatoria local que genera, con erosiones indeseables y dolorosas, que en muchos casos puede favorecer el incumplimiento terapéutico del paciente y obligar a detener el tratamiento de forma precoz. Se han publicado varios casos de dermatitis de contacto y un caso de colitis inflamatoria9. Para intentar disminuir estos efectos se han propuesto protocolos terapéuticos alternativos, como el empleo concomitante de corticoides tópicos y/o antibióticos (ATB), o el uso de la terapia pulsátil10, en la que el tratamiento se aplica con menor frecuencia y durante un periodo de tiempo mayor (con lo que se disminuye la inflamación pero al mismo tiempo decae la eficacia del tratamiento). La más reciente aprobación del producto a una menor concentración (0,5 %) para las queratosis actínicas de cara y cuero cabelludo, a pesar de no haber mostrado diferencias en cuanto a eficacia y tolerabilidad en comparación con la concentración al 5 %, es preferida por los pacientes al disminuirse el número de aplicaciones a una diaria.
Otras desventajas de la terapia son el periodo de tratamiento relativamente largo y la eficacia parcial en las queratosis actínicas profundas o hiperqueratósicas.
El 5-fluoracilo tópico ha sido también utilizado, aunque de forma más limitada, en el tratamiento de carcinomas basocelulares, recomendándose sólo para el tratamiento del carcinoma basocelular superficial, a la concentración del 5 % y aplicado dos veces al día un mínimo de 6 semanas, con una tasa aproximada de curación del 93 %7. También ha sido documentada la efectividad del 5-fluoracilo al 5 % en casos seleccionados de carcinoma escamocelular in situ7. En estos casos de cáncer cutáneo la respuesta al tratamiento debe ser cuidadosamente monitorizada.
Debido a su acción irritativa local se ha considerado también al 5-fluoracilo útil como marcador preoperatorio de márgenes tumorales en tumores superficiales, aplicándolo dos veces al día durante los 7-10 días previos a la cirugía.
Diclofenaco tópico
El diclofenaco al 3 % en ácido hialurónico al 2,5 % (Solaraze®) es un antiinflamatorio no esteroideo que ha sido formulado en gel tópico para el tratamiento de la queratosis actínica y que actualmente sólo está aprobado su uso en EE.UU. Su mecanismo de acción no es bien conocido, pero ha mostrado tener efecto antitumoral por inhibición del metabolismo del ácido araquidónico. Se aplica dos veces al día durante un periodo de 60 a 90 días. Varios estudios han demostrado su eficacia en el tratamiento de la queratosis actínica10,11 alcanzando una resolución completa de las lesiones en un 47 % de los pacientes, mientras que un 77 % mostraron mejoría significativa12,13. La eficacia total parece ser menor que la alcanzada con 5-fluoracilo7.
Aunque generalmente es un fármaco bien tolerado, genera reacciones locales en hasta un 70 % de los casos13, dando lugar a una inflamación media-moderada, aunque significativamente menor que la que se produce tras la aplicación de 5-fluoracilo. Se han descrito también casos de dermatitis de contacto alérgica. Hasta el momento no hay evidencias de su efectividad en el tratamiento del carcinoma basocelular ni del carcinoma espinocelular.
Se considera una buena opción terapéutica, fácil de administrar y con mayor probabilidad de aceptación por los pacientes que el 5-fluoracilo a pesar de necesitar un periodo de tratamiento largo.
Imiquimod
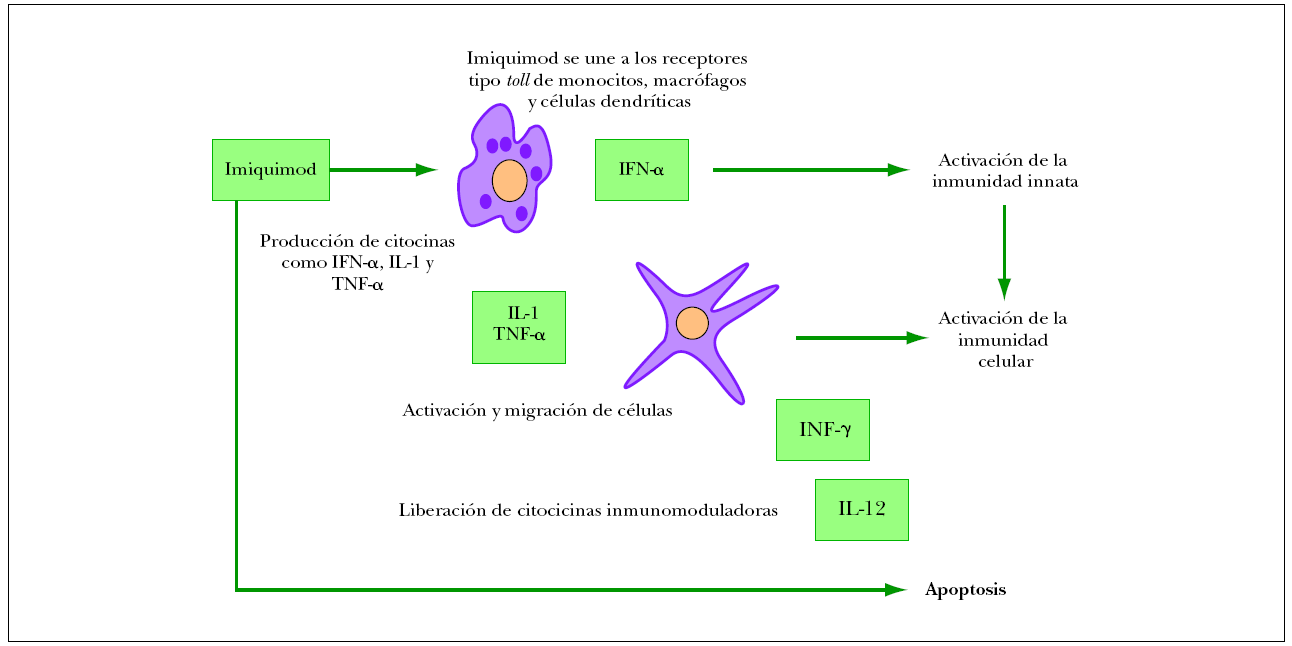
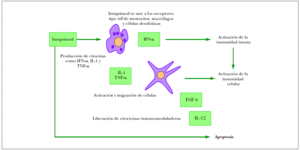
El imiquimod en crema al 5 % (Aldara®) es un modulador de la respuesta inmune con actividad antivírica y antitumoral. Actúa induciendo la liberación local del interferón-a, del factor de necrosis tumoral alfa (TNF-α) y de otras citocinas que estimulan la respuesta inmunitaria tanto innata como celular. Además, tiene la capacidad de inducir la apoptosis de las células tumorales (fig. 1). Está aprobado en Europa para el tratamiento del carcinoma basocelular superficial y recientemente se ha aprobado también su uso para el tratamiento de la queratosis actínica no hiperqueratósica ni hipertrófica de la cara y el cuero cabelludo.
Figura 1. Mecanismo de acción del imiquimod. IFN-α: interferón α; IFN-γ: interferón γ; TNF-α: factor de necrosis tumoral α.
Varios estudios han tratado de determinar la pauta ideal de tratamiento14,15 y han demostrado que cuanto mayor es la dosis mejor es la respuesta, aunque también aumentan los efectos secundarios. Hasta el momento se considera como pauta más efectiva la aplicación una vez al día 5 veces a la semana durante 6 semanas para el carcinoma basocelular, evaluando la respuesta clínicamente a los 3 meses del tratamiento; y 3 veces a la semana durante 4 semanas para la queratosis actínica, pudiéndose repetir otro ciclo de tratamiento si a las 4 semanas sin tratamiento no ha habido respuesta suficiente. En cualquier caso, es conveniente individualizar el tratamiento para conseguir la mayor eficacia con la mejor tolerancia y el mayor cumplimiento terapéutico.
Su eficacia y su seguridad en el tratamiento del carcinoma basocelular han quedado demostradas en numerosos ensayos y estudios clínicos, de forma que se han obtenido tasas de respuesta clínica entre un 69 y un 100 % en los carcinomas basocelulares superficiales16,17. Un 82 % de los pacientes experimentó una resolución histológica completa de la lesión18.
En el tratamiento de la queratosis actínica la tasa de curación oscila entre el 45 y el 84 %19. Un metaanálisis reciente realizado por Gupta et al20 demuestra que la eficacia del imiquimod en el tratamiento de la queratosis actínica es mayor que la del 5-fluoracilo, con tasas de curación media total del 70 y 52 %, respectivamente.
Para evaluar la eficacia del tratamiento a largo plazo se realizó un estudio21 multicéntrico y abierto en fase III que incluyó un total de 182 pacientes que presentaban tumores menores de 2 cm de diámetro y que fueron tratados con imiquimod 5 veces/semana durante 6 semanas, logrando tasas elevadas de curación sostenida y muy similares entre el primer y el segundo año (97,5 y 88,7 %, respectivamente). Recientemente se ha publicado otro estudio en el que se obtienen datos de mantenimiento de la eficacia sobre carcinomas basocelulares de hasta 5 años22.
Se considera, por tanto, una buena alternativa terapéutica que ha demostrado obtener buena eficacia y seguridad a largo plazo, al menos hasta 5 años, y que ofrece excelentes resultados estéticos.
Los efectos secundarios más frecuentes se restringen a la zona de aplicación y pueden ser eritema, ulceración, edema y descamación. En caso de que aparezcan se puede hacer un descanso de varios días, sin que ello parezca interferir en la eficacia del tratamiento.
Aunque no está aprobado aún su uso en otras formas clínicas de carcinoma basocelular, existe suficiente evidencia en la literatura sobre su eficacia, con remisiones completas entre el 71 y el 100 % de los casos en el tipo nodular23 y con varios casos de remisión en los tipos esclerodermiforme e infiltrativo24.
Imiquimod ha demostrado también ser eficaz en la remisión completa o parcial de carcinomas basocelulares múltiples en pacientes con síndrome de Gorlin y xeroderma pigmentoso25,26, así como en pacientes inmunodeprimidos27 y en pacientes con carcinoma escamocelular in situ28.
Algunas de las futuras aplicaciones de este inmunomodulador serán el tratamiento preoperatorio, con el fin de reducir el tamaño tumoral, el marcaje de márgenes tumorales mal definidos o la profilaxis de recidivas tras el tratamiento quirúrgico.
Terapia fotodinámica
La terapia fotodinámica es una modalidad de tratamiento relativamente reciente que se basa en la aplicación de una sustancia fotosensibilizante y la iluminación posterior de la lesión con luz visible para producir moléculas de oxígeno activado que destruyan de forma selectiva las células diana. Ha sido aprobada en Europa para el tratamiento de la queratosis actínica y el carcinoma basocelular superficial y nodular, y recientemente también ha sido aprobado su uso en 22 países europeos para el tratamiento de la enfermedad de Bowen29. Los fotosensibilizantes utilizados son el 5-aminilevulinato tópico (ALA) y su derivado metilaminolevulinato (MAL). Este último es el comercializado en Europa (Metvix®), que posee la ventaja de ser más selectivo y necesitar menor tiempo de absorción.
El régimen de tratamiento óptimo es la aplicación de MAL en cura oclusiva a una concentración de 160 mg/g durante 3 horas, previamente a la aplicación de luz. Se recomienda el curetaje previo de la lesión para eliminar la hiperqueratosis o bien reducir el tumor en el caso del carcinoma basocelular nodular.
Múltiples estudios30-32 han constatado la eficacia de dicha terapia mostrando respuestas de hasta el 90 % en queratosis actínicas y el 93 % para la enfermedad de Bowen con una recurrencia a 64 meses del 17 %. Para el carcinoma basocelular la respuesta oscila entre el 80 y el 97 % en el tipo superficial, con una recurrencia a 4 años del 22 %, y entre el 73 y el 94 % para el tipo nodular, con una recurrencia a 5 años del 14 %. Los índices de respuesta más altos se obtuvieron tras realizar un raspado previo de la lesión.
En general, es un tratamiento bien tolerado, aunque como efecto adverso más común causa dolor en forma de quemazón en el área tratada. También se ha descrito eritema, edema y formación de costras. Estos efectos se consideran menores que los producidos por el 5-fluoracilo. Aunque de forma excepcional, se han descrito casos de reacciones alérgicas.
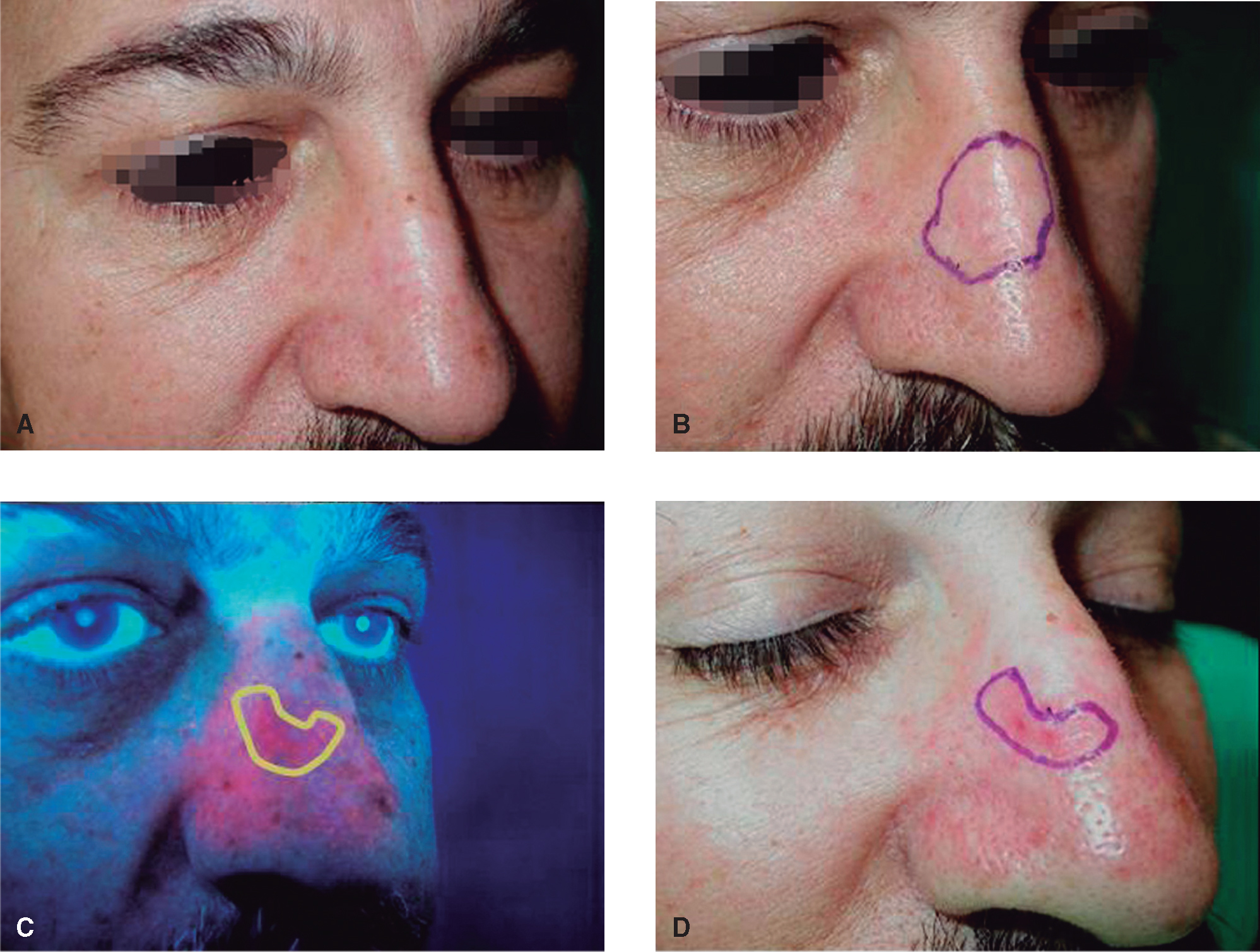
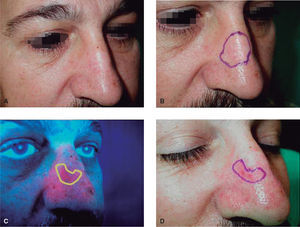
Otras ventajas que ofrece la terapia fotodinámica son la posibilidad de repetirse tantas veces como sea necesario no complicando una futura cirugía, o el excelente resultado cosmético con disminución evidente de los signos de envejecimiento, lo que la hace ser bastante bien aceptada por los pacientes. Además, el diagnóstico por fluorescencia permite la delimitación de la lesión cuando ésta presenta márgenes mal definidos (fig. 2), así como la detección de recidiva tras tratamientos previos.
Figura 2. A. Carcinoma basocelular en dorso nasal. B. Márgenes clínicos. C. Márgenes por fluorescencia. D. Reducción de la zona de extirpación.
Recientemente se han establecido unas guías de aplicación de la terapia fotodinámica29 en las cuales se recomienda su uso y se considera como primera línea de tratamiento para la queratosis actínica y la enfermedad de Bowen, como tratamiento eficaz y seguro para el carcinoma basocelular superficial y nodular, y como tratamiento preventivo de queratosis actínicas y cáncer cutáneo en pacientes trasplantados inmunodeprimidos33. Aunque varios estudios con ALA han demostrado eficacia en el tratamiento del carcinoma espinocelular superficial29, el alto riesgo de recurrencia y el potencial metastatizante de este tumor han restringido su uso. No existen artículos publicados del uso de MAL para este tumor. Por lo tanto, no se puede recomendar hasta el momento la terapia fotodinámica como tratamiento seguro y eficaz para el carcinoma espinocelular.
La principal limitación de esta terapia es su baja capacidad de penetración en la piel, lo que dificulta su eficacia en lesiones profundas. La aparición en un futuro próximo de nuevos fotosensibilizantes y vehículos que permitan una mayor penetración aumentará la efectividad de esta terapia.
Conflicto de intereses
Declaramos no tener ningún conflicto de intereses.
Correspondencia:
María Victoria Barrera Vigo.
Servicio de Dermatología.
Hospital Clínico Universitario Virgen de la Victoria.
Campus Universitario Teatinos. 29010 Málaga. España.
mvbvigo@yahoo.es
Aceptado el 6 de junio de 2007.