Introducción
El sarcoma de Kaposi (SK) se considera inducido por el virus herpes humano tipo 8 (VHH8) en todas sus variantes clínicas. El desarrollo de la enfermedad está modulado por el estado inmunitario del paciente, entre otros factores aún no bien conocidos. En la actualidad no existe un tratamiento de elección y éste depende de la extensión y la localización de las lesiones, así como del tipo clínico de la enfermedad. Se han utilizado diversas pautas de tratamiento, entre las que figuran la quimioterapia (QT), la radioterapia (RT) o el interferón (IFN). En 1999 la Food and Drug Administration (FDA) aprobó la aplicación tópica de alitretinoína (ácido 9-cis-retinoico) al 0,1 % en gel para el tratamiento de las lesiones cutáneas de SK relacionado con el sida. Se trata de una hormona endógena que se une a todos los receptores intracelulares de retinoides conocidos, regulando el proceso de diferenciación celular y la apoptosis 1-5. Presentamos un caso de SK tratado con alitretinoína tópica que evolucionó favorablemente.
Caso clínico
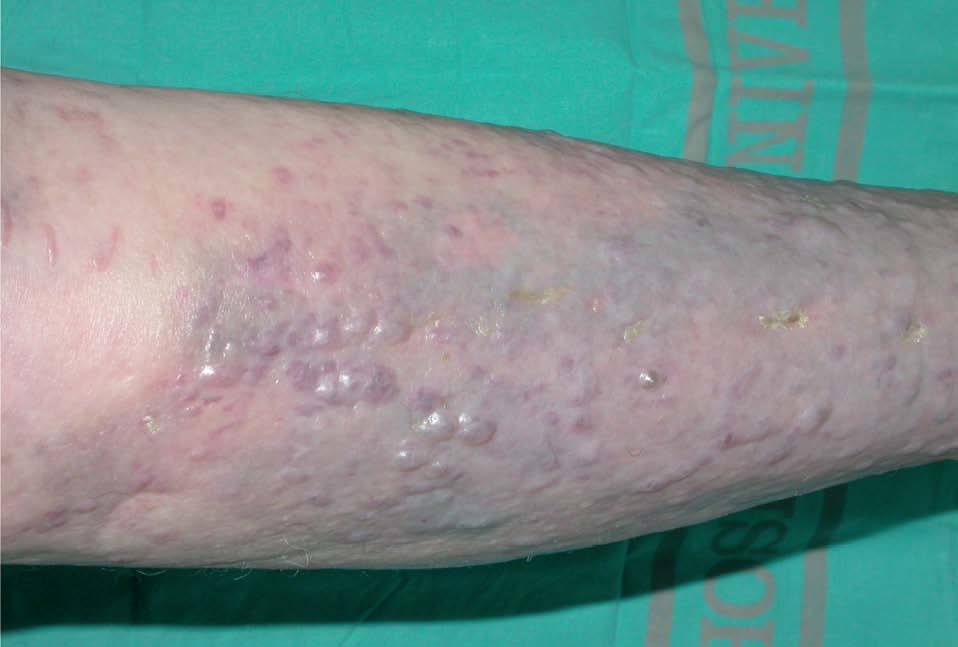
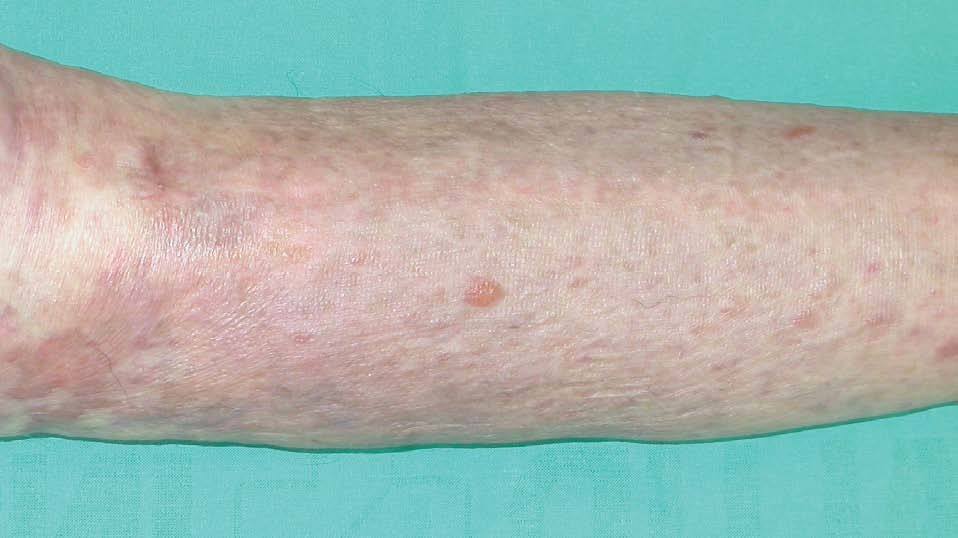
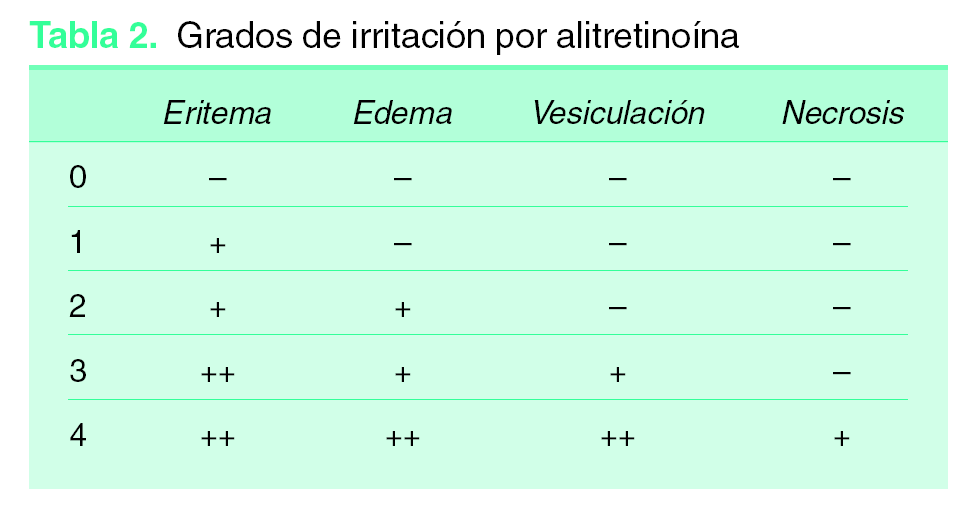
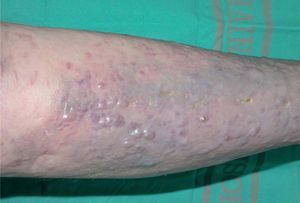
Presentamos el caso de una mujer de 83 años diagnosticada de síndrome de Sjögren en tratamiento con metotrexato y prednisona. Un mes después de iniciado el tratamiento, consultó por la aparición de varias placas eritemato-purpúricas en extremidades, nalgas y tronco. Se realiza el diagnóstico de SK, que se confirmó mediante estudio histopatológico. Entre las pruebas complementarias realizadas destaca: serología para el virus de la inmunodeficiencia humana (VIH) negativa, serología de VHH8 positiva (con valores de IgG > 640) y niveles de linfocitos CD4 de 1088/mm 3 (N: 500-900/mm 3) y CD8 de 174 (N: 200-400/mm 3). La reacción en cadena de la polimerasa (PCR)-VHH8 en biopsia de piel resultó positiva. Las lesiones cutáneas continuaron aumentando en número y tamaño, a pesar de suprimir el metotrexate, coincidiendo con la elevación de la dosis de esteroides. Se inició tratamiento con IFNalfa-2b (5 a 15 MUI subcutáneo 3 veces en semana) durante 5 meses y medio, que suspendió por intensa astenia y toxicidad hematológica grado II de la Organización Mundial de la Salud (OMS). Posteriormente inició RT con baño de electrones, que la paciente no toleró. Se decidió, entonces, comenzar tratamiento, por uso compasivo, con alitretinoína tópica al 0,1 % en gel, que la paciente aplicó sobre las lesiones distales a las rodillas, por ser éstas las más visibles. Dicho tratamiento le produjo intensa reacción local (fig. 1) con eritema, edema y vesiculación (grado 3), únicamente con dos aplicaciones diarias, lo que obligó a disminuir la dosis a tan sólo una aplicación cada 48-72 horas. La evolución fue lenta pero favorable, dejando una pigmentación residual a los 5 meses del tratamiento (fig. 2).
Figura 1. Intensa reacción local (eritema, edema y vesiculación) en la zona de aplicación de alitretinoína al 0,1 % en gel.
Figura 2. Hiperpigmentación residual tras 5 meses de tratamiento con alitretinoína al 0,1 % en gel.
Discusión
El esquema terapéutico para el tratamiento del SK obedece, principalmente, a las necesidades individuales de cada paciente. Los factores implicados en elección del tratamiento son habitualmente:
1.Extensión y tasa de crecimiento del tumor, especialmente la afectación visceral.
2.Sintomatología asociada.
3.Estado inmunológico.
4.Historia de enfermedades oportunistas. Así distinguimos diferentes abordajes: local (reservado para tumores pequeños y/o delgados) y sistémico (para tumores grandes/sintomáticos o extensión visceral). Los diferentes tratamientos para el SK se resumen en la tabla 1.
Los retinoides son análogos estructurales o funcionales de la vitamina A, que regulan la transcripción genética a través de sus receptores intracelulares que se comportan como factores de transcripción dependientes de ligando. Dichos receptores pertenecen a la familia esteroide-tiroidea y se distinguen actualmente dos grupos: RAR (receptores de ácido retinoico) y RXR (receptores del retinoide X). Cada grupo, a su vez, se divide en tres subgrupos (alfa, beta y gamma). En la piel humana encontramos RAR-gamma y RXR-alfa.
Existen tres generaciones de retinoides, que se diferencian en su espectro clínico, toxicidad y farmacocinética, de manera que la ausencia de respuesta de una enfermedad a un retinoide no implica que ocurra lo mismo con otros retinoides.
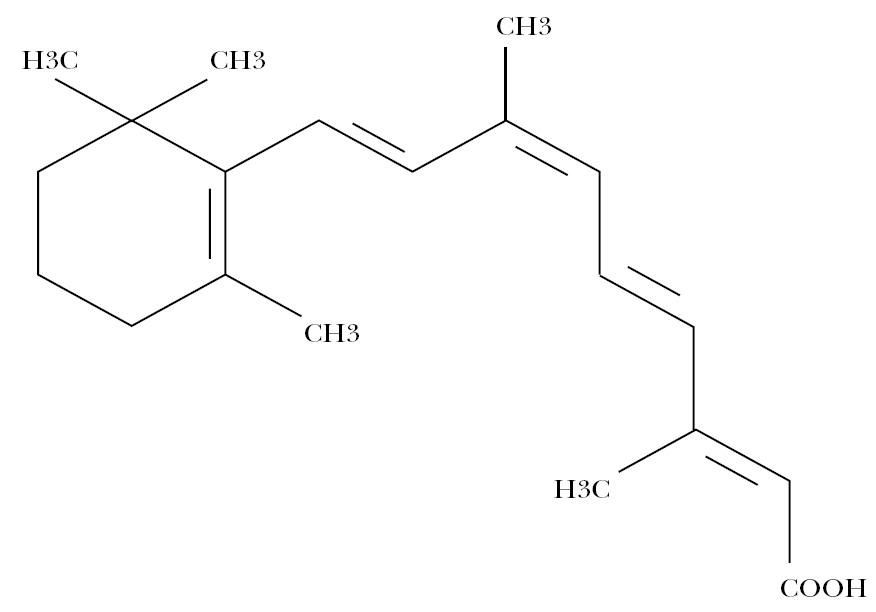
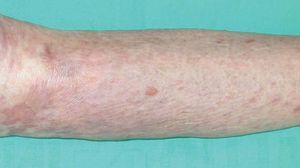
La alitretinoína, o ácido 9-cis-retinoico, es un retinoide monoaromático de primera generación, cuya estructura molecular aparece en la figura 3.
Figura 3. Estructura molecular de la alitretinoína.
La acción retinoidea está mediada por múltiples vías y se traduce en una activación o inhibición compleja de una gran cantidad de genes regulados de manera coordinada. Por un mecanismo directo estimula elementos de respuesta hormonal, provocando la diferenciación celular, mientras que indirectamente actúa sobre genes que no poseen dichos elementos de respuesta hormonal, provocando una disminución de la actividad proliferativa e inflamatoria. Estos efectos biológicos probablemente dependan de su actuación selectiva sobre los diferentes receptores 3.
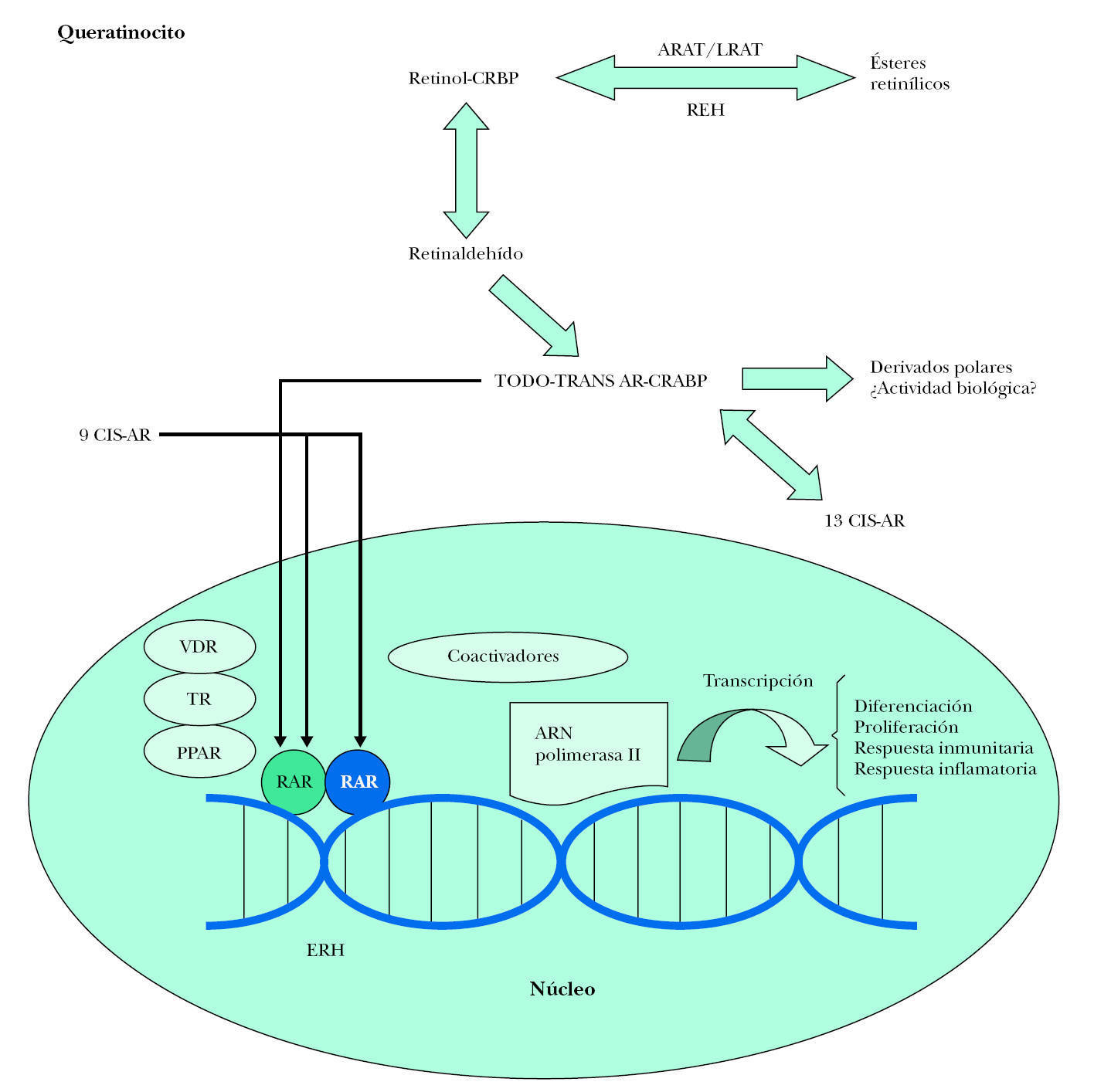
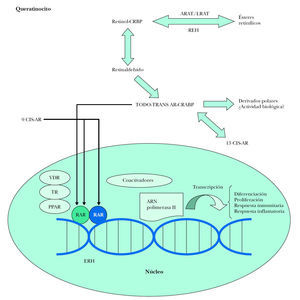
La alitretinoína es capaz de unirse a todos los receptores de retinoides hasta ahora conocidos (RAR y RXR) promoviendo la apoptosis (actuando sobre RXR) y la diferenciación celular (actuando sobre RAR), a la vez que disminuye la proliferación celular (actuando sobre RAR) 3 (fig. 4).
Figura 4. Esquema de actuación de los retinoides sobre sus receptores intracelulares. CRBP: proteína fijadora del retinol celular; LRAT: lecitina retinol acil transferasa; ARAT: acetil CoA retinol acil transferasa; REH: retinil éster hidrolasa; AR: ácido retinoico; CRABP: proteína fijadora del ácido retinoico citosólico; RAR: receptor del ácido retinoico; RXR: receptor del retinoide X; VDR: receptor vitamina D3; TR: receptor tiroideo; PPAR: receptor activado de proliferación del peroxisoma; ERH: elementos de respuesta hormonal. Modificada de Bolognia J, et al. Dermatología. 1.ª ed. Elsevier Mosby; 2004: Vol. II.
La formulación en gel de la alitretinoína está aprobada por la FDA desde 1999 para el tratamiento local de lesiones cutáneas en pacientes con SK relacionado con el sida cuando no están ulceradas, ni son linfedematosas, no se requiere tratamiento visceral, no hay respuesta a terapia antirretroviral de gran actividad (TARGA) y/o no son adecuadas la RT ni la QT. Sin embargo, en la revisión realizada de la literatura hemos encontrado un caso de SK-clásico tratado durante 7 meses con alitretinoína tópica al 0,1 % en gel, con buenos resultados 4.
En nuestra paciente se desestimó el tratamiento quirúrgico por la extensión de las lesiones. La QT no fue considerada por la morbilidad sustancial asociada y la avanzada edad de la paciente. Debido a la toxicidad producida por los diferentes tratamientos recibidos (IFNalfa2b y baño de electrones), comenzó con alitretinoína al 0,1 % en gel como tratamiento tópico, lo que provocó intensa reacción local, que obligó a disminuir la frecuencia de aplicación a una cada 48-72 horas, con la formación de vesículas y ampollas, que finalmente se resolvieron dejando una hiperpigmentación residual.
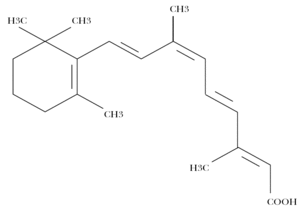
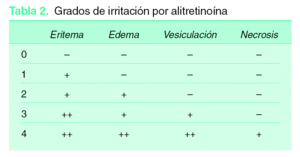
La alitretinoína se debe aplicar generosamente sobre las lesiones a tratar, respetando la piel sana circundante. Inicialmente son dos aplicaciones diarias, pero se debe aumentar la frecuencia de aplicación paulatinamente (cada 2-3 semanas) hasta alcanzar 3-4 aplicaciones al día, salvo que se produzca irritación, en cuyo caso hay que reducir, o incluso suspender, el tratamiento hasta su resolución y reanudarlo siempre y cuando no se haya producido necrosis del tejido. Los grados de irritación se resumen en la tabla 2.
La eficacia de la alitretinoína al 0,1 % en gel ha sido evaluada en pacientes adultos positivos para el VIH con biopsia probada de SK en varios ensayos clínicos, atendiendo a los criterios para el tratamiento tópico del SK cutáneo propuestos por el Grupo de Ensayos Clínicos en sida, observando una tasa de respuesta de 35-37 %; de ellas, un 1-2 % eran completas y un 34-35 % eran parciales 1-3. Se comprobó, además, que dicha respuesta no dependía de la etnia, puntuación en la escala de Karnofsky, número/área de las lesiones, cifras de linfocitos CD4, número de infecciones oportunistas, enfermedad diagnóstica de sida o terapia previa con QT o TARGA 1-3.
En general es bien tolerada y los efectos adversos son reversibles, apareciendo únicamente en el sitio de aplicación: rash (77 %), dolor (34 %), prurito (11 %), descamación (9 %) y edema/otros (8 %), que habitualmente se relacionan con la duración del tratamiento y la frecuencia de aplicaciones 1-3.
Conflicto de intereses. Declaramos no tener ningún conflicto de intereses
Correspondencia:
Ana González de Arriba.
Servicio de Dermatología. Hospital Universitario de La Princesa.
Diego de León, 62. 28007 Madrid.
Aceptado el 18 de octubre de 2006.