INTRODUCCIÓN
El acné vulgar es una enfermedad multifactorial del folículo pilosebáceo, en cuya patogenia se piensa que desempeña un papel importante el Propionibacterium acnes1. La mayoría de los expertos aceptan actualmente que el Propionibacterium acnes no inicia dicha patología, pero contribuye a desencadenar el proceso inflamatorio que en ella se produce2.
Los tratamientos usados en el acné que interfieren en el crecimiento y/o en el metabolismo del Propionibacterium acnes se pueden dividir en antibióticos y antimicrobianos no antibióticos3. El mecanismo de acción de los antibióticos tópicos no está aclarado suficientemente; posiblemente actúen inhibiendo el crecimiento del Propionibacterium acnes y mediante un efecto antiinflamatorio directo4.
Los pacientes con acné son un reservorio considerable de cepas resistentes que pueden ser transferidas a contactos cercanos no afectados de acné5. La rápida inducción de resistencia a antibióticos del Propionibacterium acnes, acompañada de brotes de acné, ha sido descrita tras la aplicación de eritromicina y clindamicina tópicas, así como después de utilizar tetra-ciclina, eritromicina y doxiciclina sistémicas6, 7.
Los Propionibacterium acnes resistentes a la eritromicina y clindamicina fueron detectados por primera vez al final de los años setenta en Estados Unidos8. Desde entonces se han detectado en el Reino Unido, Francia, Alemania, Japón y Nueva Zelanda, así como en otro centros de Estados Unidos9-13. No obstante, dos tipos de preparados con eritromicina son clínicamente efectivos en pacientes con Propionibacterium acnes resistentes, e incluso reducen el número de organismos resistentes en la superficie cutánea14, 15. Ambos preparados contienen dentro de la fórmula un segundo principio activo, el acetato de zinc o el peróxido de benzoilo que inhibiríanin vitro los Propionibacterium acnes resistentes a la eritromicina16.
Los retinoides tópicos son igualmente activos frente a cepas resistentes y sensibles de Propionibacterium acnes2. La isotretinoína también reduce considerablemente el número de Propionibacterium acnes resistentes en la piel de todos los pacientes3.
El objetivo de nuestro estudio es: a) comprobar el grado de utilización de antibióticos tópicos y sistémicos por una población malagueña con acné; b) cuantificar la tasa de resistencia del Propionibacterium acnes a cada antibiótico usado, y c) establecer comparación entre las tasas de resistencia de los distintos antibióticos usados.
PACIENTES, MATERIAL Y MÉTODOS
Se seleccionaron los 100 primeros pacientes consecutivos vistos en una consulta privada de un médico especialista en Dermatología. Todos ellos habían sido diagnosticados en los últimos 5 años de acné vulgar. Se citaron en dicha consulta en el mes de septiembre de 1999 explicándoles el motivo. De los 100 pacientes seleccionados, 7 no acudieron a la cita. Efectuamos una recogida de muestra en esos 93 pacientes con acné vulgar leve o moderado durante 1999. La toma fue realizada en pacientes de la provincia de Málaga y procesada en el laboratorio de la Universidad de Leeds (Reino Unido), con posterior cultivo en medios seleccionados para el Propionibacterium acnes. La toma de muestra y cultivo de nuestro trabajo fue realizada con el sistema utilizado rutinariamente en la clínica de acné del Skin Research Centre de Leeds17. Puesto que se quiso contar con la experiencia del Departamento de Microbiología de la Universidad de Leeds, se seleccionó un medio de transporte contrastado para el envío de muestras desde Málaga.
Se utilizó la clasificación clínica habitualmente usada en España, que divide el acné vulgar en cuatro grados o estadios18. Posteriormente se descartaron del estudio 5 pacientes con acné cuyo cultivo apareció contaminado por bacterias gramnegativas y/o levaduras, con lo que para el estudio se continuó con 88 pacientes.
Se realizó además una toma de muestra a 18 familiares de los pacientes con acné (padres, hermanos o hijos).
Se recogieron los siguientes datos de los pacientes: edad, sexo, tiempo de evolución desde el inicio del acné, grado de acné en el momento de la toma de la muestra, terapéutica tópica o sistémica usada en el momento del estudio o previamente, incluidos los diferentes antibióticos locales o sistémicos utilizados en el momento del estudio o con anterioridad a la toma de muestra.
Toma de muestra, cultivo e identificación del Propionibacterium acnes
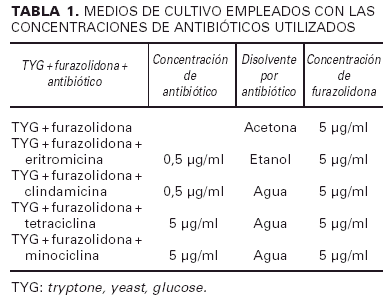
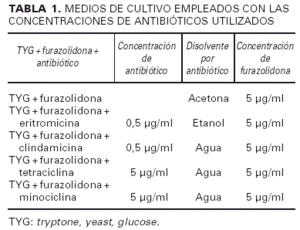
La toma de muestra se realizó en la consulta con un escobillón estéril, previamente sumergido en un líquido preparado («solución de lavado»), consistente en la mezcla de 0,075 M de sodio fosfato monobásico dihidrato y sodio fosfato dibásico, obteniendo una solución de pH 7,9 y a la que añadimos 0,1% Triton X-100 como conservante5. Dicha mezcla da una solución tampón que respeta el equilibrio hídrico de la bacteria sin el cual no sería posible su cultivo adecuado. La torunda del escobillón se pasó con firmeza, de forma que se arqueara el hisopo del escobillón, y con movimientos desde arriba hacia abajo por las mejillas, la frente y la nariz y de izquierda a derecha en la barbilla y el bigote. Mientras se tomaba la muestra se iba dando vueltas a la torunda de algodón, de forma que se le adhirieran las bacterias de forma homogénea. A continuación se introdujo el escobillón en un medio de transporte apto para anaerobios (medio AMIES) hasta que se realizó la siembra en un plazo inferior a 24 horas en el laboratorio. Una vez en el laboratorio se procedió a la inoculación en placas de Agar preparadas con el medio TYG, medio muy específico para el crecimiento del Propionibacterium acnes compuesto por 20 g de peptona trípsica de caseína, 10 g de extracto de levadura, 10 g de Agar y 5 g de glucosa disueltos en 1 litro de agua destilada. A estas placas se les añadieron por separado los antibióticos adecuados (eritromicina, clindamicina, tetraciclina y minociclina); en todas las placas se agregó furazolidona para inhibir el crecimiento de estafilococos (tabla 1). Después de 7 días de incubar en condiciones anaerobias a 37º C, las placas se inspeccionaron para ver el crecimiento, que se graduó en una escala de 0 a 3 + (0: ningún crecimiento; 1: crecimiento bajo [1 a 50 colonias]; 2: crecimiento intermedio [51 a 200 colonias]; 3: crecimiento alto [a partir de 200 colonias]. La equivalencia en términos de resistencia fue interpretada como: 0: no hay resistencia; 1: bajo grado de resistencia; 2: resistencia intermedia; 3: alta resistencia. La identificación del Propionibacterium acnes se basó en la presencia de colonias con el característico color crema/rosa y un olor como a «huevos podridos», apoyándose el diagnóstico en el microscopio óptico que mostró la típica presencia de bacilos curvados grampositivos17.
RESULTADOS
Fueron estudiados 88 pacientes de los que 66 (75%) eran mujeres y 22 (25%) hombres. La edad media fue de 22,25 años, con edades comprendidas entre los 13 y los 35 años, siendo la edad más frecuente los 19 años. En más de la mitad de los casos (57%) el acné se había iniciado al menos 5 años antes. El grado de acné predominante fue el II (pápulo-pustuloso) en 57 pacientes (64,8%); 17 pacientes (19,3%) tuvieron un grado I, 5 pacientes (5,7%) un grado III y 9 pacientes (10,2%) estaban libres de acné en el momento de la toma de la muestra. No se estudió ningún paciente con un acné grado IV.
En el momento del estudio, 44 pacientes (50%) estaban siendo tratados con terapia combinada tópica y sistémica, 37 (42%) sólo con tratamientos tópicos y 7 (8%) no tenían ningún tratamiento en el momento de la toma. Ningún paciente se encontraba exclusivamente con tratamiento sistémico.
Dentro de los tratamientos tópicos usados tanto previamente como en el momento del estudio, el grupo hallado con mayor frecuencia (20%) fue el de los que utilizaron eritromicina tópica, exfoliantes (ácido retinoico, ácido glicólico y/o ácido salicílico) y un gel asociando eritromicina (3%) más peróxido de benzoilo (5%). La eritromicina sola o asociada la habían usado 85 pacientes (97,5%). La clindamicina fue usada por 18 pacientes (20,4%) en combinación con otros tratamientos tópicos. Ningún paciente la había usado sola.
Dentro de los tratamientos antibióticos sistémicos, 46 pacientes (52%) usaron la minociclina sola o asociada en algún momento. De ellos, 18 pacientes usaron exclusivamente la minociclina como tratamiento oral y 28 asociada a otros tratamientos. La doxicilina fue utilizada por 27 pacientes (10 de manera exclusiva y 17 asociada a otros tratamientos). Ningún paciente había utilizado eritromicina oral. La tetraciclina fue usada por 24 pacientes (2 de una manera exclusiva y 22 asociada a otros tratamientos).
En cuanto a los antibióticos usados, y con independencia de si lo eran de forma tópica o sistémica, con carácter previo o en el momento de la consulta el antibiótico más usado fue la eritromicina (85 pacientes; 70 en combinación con otros antibióticos y 15 sola). La minociclina la usaron 46 pacientes (45 de forma combinada y 1 sola); combinaban eritromicina y minociclina, 19 pacientes (22%).
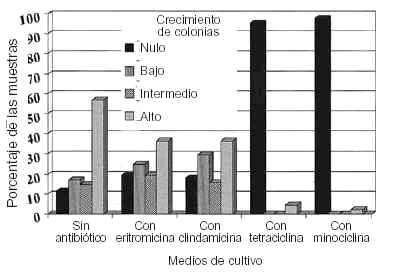
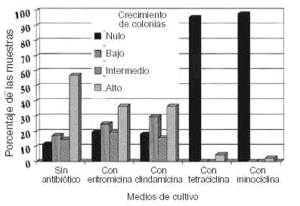
Los resultados de los cultivos de las tomas de los 88 pacientes queda reflejado en la figura 1. El crecimiento de Propionibacterium acne (sin añadirle ningún antibiótico específico al medio de cultivo a excepción de la furazolidona) fue alto (3+) en el 56,8% de los casos. En un 17% el crecimiento fue bajo (1 +) y el 14,8% tuvo crecimiento intermedio (2+); en el 11,4% no creció nada (0+). En las placas en que añadimos eritromicina, el grupo más numeroso fue el de alta resistencia (3+) del Propionibacterium acnes al antibiótico (36,4%), el 25% tuvo un crecimiento bajo (1+), el 19,3% un crecimiento intermedio (2+) y el 19,3% no tuvo ningún crecimiento (0+). En aquellas placas en las cuales se añadió clindamicina, el grupo más numeroso (36,4%) tuvo un crecimiento alto del germen (3+), el 29,5% un crecimiento bajo (1+), el 15,4% un crecimiento intermedio (2+) y el 18,2% no tuvieron ningún crecimiento (0+). En las placas con tetraciclina como antibiótico, en la mayoría (95,5%) no creció Propionibacterium acnes (0+) y sólo en 4 pacientes (4,5%) hubo un crecimiento alto (3+). En el cultivo en el que utilizamos la minociclina llamó la atención que en 86 pacientes (97,7%) no creció nada (0+), mientras que en sólo 2 pacientes (2,3%) hubo un crecimiento alto (3+).
FIG. 1.--Resultados del cultivo (%) del Propionibacterium acnes en los distintos medios de cultivo.
En las muestras de los 18 contactos familiares de nuestros pacientes de acné (padres, hermanos o hijos) hubo un crecimiento alto de Propionibacterium acnes, sin añadir antibióticos específicos en 12 (66,7%); en 5 (27,8%) los cultivos con eritromicina dieron un crecimiento alto del germen y en 7 (38,9%) la clindamicina. Por el contrario, la tetraciclina nos dio un 94,4% de sensibilidad y la minociclina un 100%. Aunque evidentemente este grupo de contactos control es una muestra pequeña, los datos obtenidos pueden ser orientativos.
DISCUSIÓN
Propionibacterium acnes es un factor más a tener en cuenta dentro de la etiopatogenia del acné y el hecho de encontrar este microorganismo resistente o sensible a los distintos antibióticos, como hemos presentado en nuestro trabajo, no implica necesariamente el éxito o fracaso en el tratamiento , ya que este microorganismo también se encuentra en la piel de sujetos sanos1.
En un estudio realizado en Leeds se observó que uno de cada dos contactos más cercanos presentaba cepas resistentes5. Esto nos deja una puerta abierta para investigar los contactos más íntimos en pacientes con acné, con una muestra más amplia y poder corroborar la transferencia de cepas resistentes a antibióticos de personas afectadas con acné a aquellas que no lo tienen.
Los datos presentados en el estudio confirman, tal y como recoge la literatura, un predominio de acné en el sexo femenino y una edad media en torno a los 22 años, observándose el incremento del acné en mujeres mayores de 20 años19, 20. El hecho de que en más de la mitad de los casos (57%) el acné se iniciara 5 años antes de comenzar el estudio, nos puede indicar que los tratamientos utilizados, y en nuestro caso los antibióticos tópicos y/o sistémicos, han sido usados durante largos períodos y por ende pueden haber contribuido a la formación de cepas resistentes de Propionibacterium acnes.
Es interesante subrayar que la mayor parte de los pacientes estudiados fueron del grado II, no pudiendo haber sido afectada la muestra por valores extremos (en la muestra no se recogió ningún caso de acné grado IV ni de acné noduloquístico). El hecho de que el antibiótico más usado en nuestro estudio, con un 97,5%, fuera la eritromicina puede hacernos pensar que realmente es el antibiótico más ampliamente utilizado en el acné por la población general, y esto se puede constatar por la historia clínica de nuestros pacientes, donde no solamente el médico de cabecera lo utiliza habitualmente, sino que el farmacéutico e incluso el propio paciente se lo automedica. Este uso continuado de la eritromicina podría ser un factor predisponente para el desarrollo de cepas resistentes de Propionibacterium acnes5. En nuestro estudio se observó una resistencia alta del Propionibacterium acnes5 frente a la eritromicina en el 36,5% de los cultivos y una resistencia intermedia en el 19,3%; es decir, que en un 55,8% de los casos crecieron más de 51 colonias de Propionibacterium acnes en los cultivos con eritromicina. Esto coincide con la literatura, donde la eritromicina fue el antibiótico que creó más resistencia3, 5. La clindamicina tópica es otro antibiótico ampliamente utilizado en el acné desde hace años. Nuestro trabajo muestra que en un 51,8% de los cultivos con ese antibiótico crecieron más de 51 colonias, lo que significa que, si bien globalmente la eritromicina fue el antibiótico más resistente , la diferencia respecto a la clindamicina fue pequeña.
El grado de resistencia del Propionibacterium acnes obtenido en nuestro trabajo es mayor con las tetraciclinas clásicas que con la minociclina2. El hecho de que en el 95,5% de los casos no hubiera ningún tipo de crecimiento bacteriano en los cultivos con tetraciclina puede hacernos pensar que la resistencia a las tetraciclinas es bastante baja, a pesar de ser uno de los primeros antibióticos usados para el tratamiento del acné y que es considerada aún como un tratamiento de primera elección21. Sin embargo, en el Reino Unido y en Estados Unidos se están detectando cada vez más cepas de Propionibacterium acnes resistentes a diferentes tipos de tetraciclinas, además de a la eritromicina y a la clindamicina, reduciéndose de este modo el número de opciones terapéuticas2.
Diferentes artículos son unánimes a la hora de catalogar la resistencia a la minociclina como extremadamente rara, lo que concuerda con nuestros resultados, donde un 97,7% de los cultivos con ese antibiótico fueron sensibles al mismo, siendo, por tanto, el antibiótico de elección dentro de las diferentes modalidades de tratamiento antibióticas22-25. Sin embargo, conviene recordar que la resistencia a la minociclina a veces no es fiable, ya que es un antibiótico muy inestable en Agar a 34º C5. Esto nos orientará en el futuro hacia la utilización de nuevos antibióticos26-28 para evitar la creación de futuras resistencias.
AGRADECIMIENTOS
Nuestro agradecimiento al Departamento de Microbiología del laboratorio de la Universidad de Leeds, en especial a Trish Coates y Anne Eady por su colaboración en la realización de este trabajo.