INTRODUCCION
El liquen escleroso es una dermatosis crónica de piel y semimucosas, caracterizada por la presencia de pápulas o placas blancas atróficas bien definidas, que aparecen de manera fundamental en la piel de la región anogenital de ambos sexos, y en menor frecuencia en la piel del tronco, afectando sobre todo a mujeres posmenopáusicas.
Fue descrito en el siglo xix por Hallopeau1. En las últimas décadas se ha producido un mayor interés por su conocimiento como demuestra la abundante bibliografía científica en torno al tema2, probablemente por la repercusión que produce sobre la salud cutánea, urinaria y sexual del individuo afectado, así como por el riesgo potencial de desarrollar carcinoma espinocelular sobre las lesiones3. La Sociedad Internacional para los Estudios de la Enfermedad Vulvovaginal recomienda que se denomine simplemente «liquen escleroso», aunque entre sus sinonimias también se encuentran los términos «liquen escleroso y atrófico», «distrofia hipoplásica», y «craurosis vulvar» en la mujer y «balanitis xerótica obliterante» en el varón.
ETIOPATOGENIA
La causa del liquen escleroso es desconocida. No obstante, se ha teorizado sobre la implicación de una serie de factores, como son los siguientes (tabla 1):
Mecanismos autoinmunes
Son varios los argumentos que pueden apoyar esta hipótesis.
1. Presencia histológica de un infiltrado linfoide. El inicio y persistencia de liquen escleroso está unido a la presencia en la dermis de un infiltrado inflamatorio formado por linfocitos. En un trabajo reciente se ha investigado acerca de la relevancia que este infiltrado de células mononucleares pueda tener en la patogénesis del liquen escleroso4, y encuentran que una elevada proporción de las células T del infiltrado tienen una potencial función citotóxica. En el estudio se valoró el infiltrado de células T de 20 pacientes con liquen escleroso activo, que se caracterizaron inmunohistoquímicamente mediante anticuerpos anti-CD3, anti-CD8, antígeno intracelular restringido a células T (TIA-1) y granzima B (GrB). El antígeno TIA-1 marca los gránulos citotóxicos de las células T, tanto las activadas como en reposo, mientras que GrB marca los linfocitos T citotóxicos. En todos los casos se encontró que numerosas células T expresaban gránulos citotóxicos, y que existían un número importante de células T citotóxicas, muchas de las cuales se encontraban relacionadas de proximidad con el área de degeneración hidrópica de la capa basal. Este dato permite suponer que la degeneración hidrópica de los queratinocitos basales, uno de los hechos histológicos de la enfermedad, puede, al menos parcialmente, ser mediada por mecanismos dependientes de los linfocitos T citotóxicos. Este hecho indica que la respuesta inmunitaria celular (linfocitos T) puede desempeñar un papel importante en la patogenia de la enfermedad.
2. Asociación con otras entidades clínicas de estirpe inmunológica. Se ha descrito simultaneidad de liquen escleroso con enfermedades de carácter autoinmune como vitíligo, lupus eritematoso, anemia perniciosa, alopecia areata o tiroiditis de Hashimoto y otras5-7.
3. Aumento de la presencia de anticuerpos órgano-específicos. Se ha encontrado una mayor frecuencia en los pacientes de liquen escleroso de anticuerpos antitiroideos, antimicrosomales, anticélulas parietales y antinucleares, entre otros6,8,9.
4. Hipopigmentación. La hipopigmentación presente en el liquen escleroso se ha interpretado como una reacción autoinmune en contra de los melanocitos, común a la existente en el vitíligo10.
Infecciones previas
La existencia de una infección crónica vaginal por estreptococo o la afectación de la zona genital por el virus del papiloma humano (VPH), puede actuar como un antígeno capaz de desencadenar diversos mecanismos inmunológicos en la piel afectada. Algunos autores11 han demostrado la presencia del virus en las lesiones de liquen escleroso. Un trabajo reciente apoya esta teoría, basándose en la rápida mejoría conseguida en una serie de casos, cuando a los tratamientos clásicos con corticoides se añadió el imiquimod como tratamiento frente al VPH12.
Otros defienden el papel etiológico de la Borrelia burgdorferi basándose en los datos serológicos, en la demostración histológica de espiroquetas en tejidos13 y en el antecedente de picadura de garrapata y subsiguiente infección por Borrelia un mes antes de la aparición del liquen escleroso14.
Sin embargo, otros autores no han podido demostrar esta relación patogénica.
Inflamación crónica
Es uno de los factores más consistentemente invocados en la etiopatogenia del liquen escleroso. A este respecto, se ha publicado recientemente un estudio prospectivo realizado sobre 115 niños con inflamación crónica del glande y el prepucio, para identificar en ellos posibles casos de la enfermedad. De los 115 niños, 55 tenían fimosis congénita, 45 fimosis adquirida, 13 hipospadias y dos balanopostitis crónica. En los estudios anatomopatológicos de la piel afectada se encontraron signos de liquen escleroso en el 30 % de los casos de fimosis congénita, en el 60 % de los casos de fimosis adquirida, en el 15 % de los pacientes con hipospadias, y en el 100 % de las balanopostitis crónicas. El resto de los casos tenía intensa inflamación crónica sin signos de liquen escleroso. Los autores suponen que esta inflamación puede colaborar firmemente en la aparición del liquen15.
Traumatismos repetidos
Se ha descrito el fenómeno de isomorfismo en pacientes de liquen escleroso, que han desarrollado nuevas lesiones en cicatrices y después de traumatismos físicos en las zonas de fricción o tras quemaduras solares16,17.
Alteraciones hormonales
Los picos de máxima incidencia de la enfermedad (prepuberal y posmenopausia), así como la resolución de muchos casos infantiles al producirse el desarrollo hormonal, parecen indicar un papel etiopatogénico hormonal. Por otra parte, se han detectado defectos en la función de los receptores de andrógenos y estrógenos en algunos casos18.
Factores genéticos de predisposición hereditaria
Se han descrito casos de liquen escleroso familiar a lo largo de varias generaciones19, de hermanos afectados e, incluso, parejas de gemelos idénticos que hacen pensar en este factor como agente etiopatogénico20. Además el liquen escleroso se ha relacionado con varios subtipos de HLA (A29, B21, B40, B44 y Aw31). La presencia de HLA-DQ7 parece estar asociada con el comienzo precoz de la enfermedad18.
Diabetes
Aunque no de forma generalizada, algunos autores han encontrado en los pacientes con liquen escleroso una presencia estadísticamente significativa de diabetes21.
EPIDEMIOLOGIA
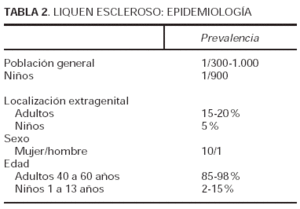
La prevalencia del liquen escleroso en la población general se estima en 1 de cada 300-1.000 individuos. Es más frecuente en mujeres que en varones en una proporción 10/1 (tabla 2). Aparece de forma preferente entre los 40 y los 60 años de edad, y en menor proporción (del 2 al 15 %) en niñas y niños de entre 1 y 13 años de vida22,23. No obstante, puede estar presente en todos los grupos de edad, y aparecer en cualquier momento, como el caso de una joven que empezó con un liquen escleroso a la edad de 18 años24.
En un reciente estudio epidemiológico realizado en una clínica de patología vulvar infantil, sobre 70 casos en tratamiento en el momento del trabajo, se halló una prevalencia del liquen escleroso premenarquial de 1 de cada 900 niñas. De todos los casos, el 17 % tenía historia familiar de liquen, el 14 % sufría alguna enfermedad autoinmune concomitante y el 59 % presentaba atopia22.
La localización extragenital del liquen escleroso se presenta en un 15-20 % de los pacientes, pero es rara en niños, alrededor del 5-9 % de los casos9,25.
MANIFESTACIONES CLINICAS
Se pueden considerar diferentes patrones en función de la localización, el sexo y el momento evolutivo. Aunque las lesiones tienden a localizarse en las áreas genitales y perianales, pueden aparecer en cualquier zona cutánea.
Lesiones mucocutáneas genitales femeninas (tabla 3)
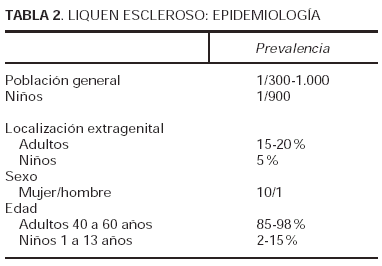
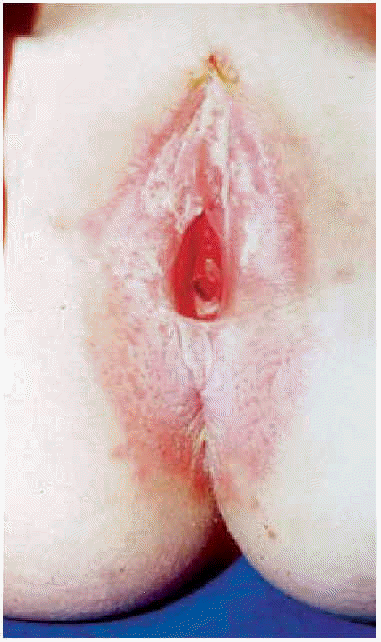
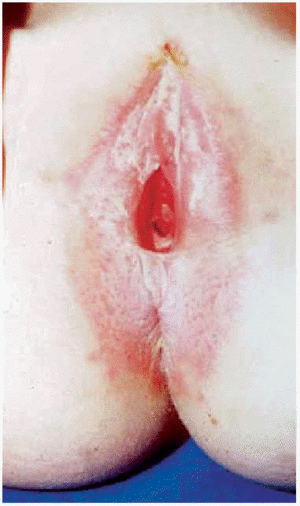
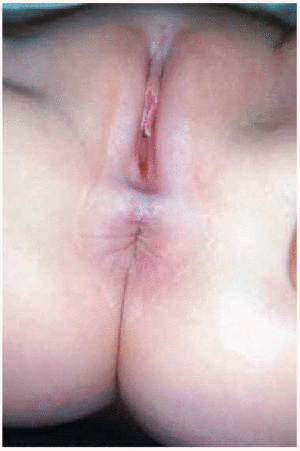
En la mujer las lesiones suelen ser simétricas, afectando principalmente la parte interna de la vulva (fig. 1) (labios menores, introito, clítoris y parte interna de labios mayores) así como periné y área perianal adquiriendo una forma típica en ocho, o en ojo de cerradura (fig. 2). El liquen escleroso nunca afecta a la vagina o al himen, que permanece intacto.
Fig. 1.--Afectación vulvar.
Fig. 2.--Afectación de periné y región perianal.
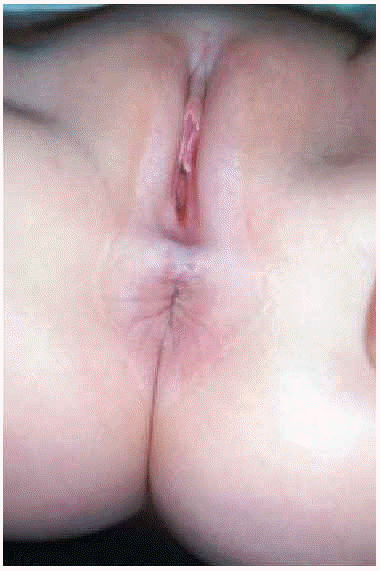
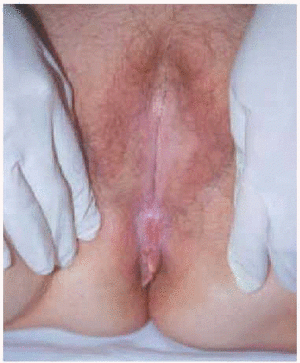
El liquen escleroso comienza en la región vulvar con un eritema, que pronto se transforma en máculas y pápulas de color blanco marfil, brillantes, induradas, bien delimitadas que pueden confluir hasta formar grandes placas. Con el tiempo, la piel lesional de las placas se atrofia, y queda deprimida con respecto a la piel normal. Bajo las placas se pueden producir hemorragias que producen equimosis intralesionales, púrpura o incluso ulceraciones. El aspecto del liquen escleroso vulvar bien instituido es el de una zona hipopigmentada en forma de ocho alrededor de la vulva y el ano, con atrofia y ocasionales zonas purpúricas. La periferia de las lesiones suele estar hiperpigmentada (fig. 3).
Fig. 3.--Afectación vulvar y perianal con la típica imagen en ocho o en ojo de cerradura.
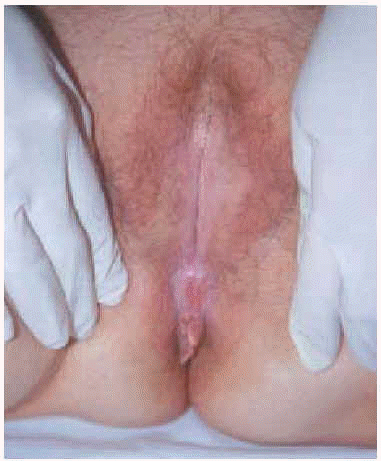
Cuando el cuadro es muy intenso y prolongado, pueden aparecer atrofia y retracción de la vulva (fig. 4). Los labios menores se fusionan y desaparecen, el clítoris se desdibuja, se borra y se entierra por la fimosis del capuchón, y el orificio de entrada a la vagina puede llegar a estenosarse e incluso ocluirse. Sin embargo, la mucosa vaginal nunca está afectada26. En esta situación es cuando al liquen escleroso femenino también se le denomina craurosis vulvar.
Fig. 4.--Craurosis vulvar. La evolución prolongada puede provocar atrofia y retracción de la vulva, con fusión de labios y reducción del introito vaginal.
Lesiones mucocutáneas genitales masculinas (tabla 4)
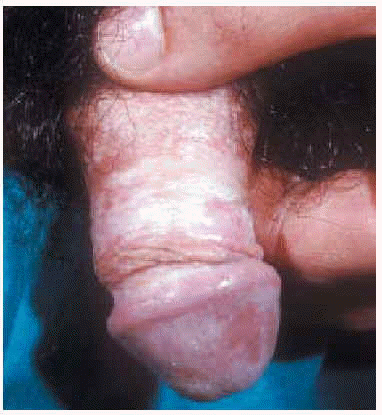
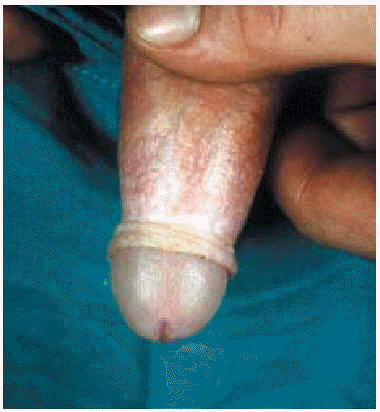
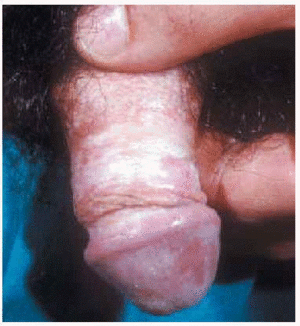
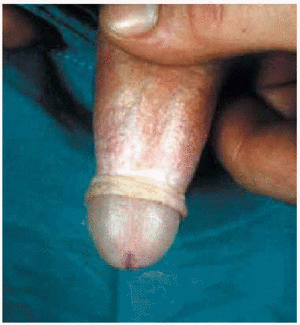
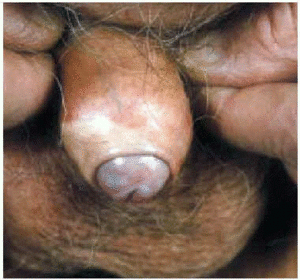
En el varón la afectación común sucede en el glande y la superficie interna del prepucio (fig. 5), aunque se han descrito casos de afectación escrotal única27. El comienzo es similar a las lesiones femeninas, con eritema pasajero, y la instauración posterior de máculas y pápulas de color blanco marfil, brillantes, induradas y bien delimitadas en varias regiones peneanas. Con el tiempo, la piel lesional de las placas se atrofia, formándose una banda esclerótica blanquecina, compresiva, de 1 a 2 cm de tamaño, localizada en el extremo distal del prepucio (fig. 6).
Fig. 5.--Afectación del pene.
Fig. 6.--Banda esclerosa en prepucio.
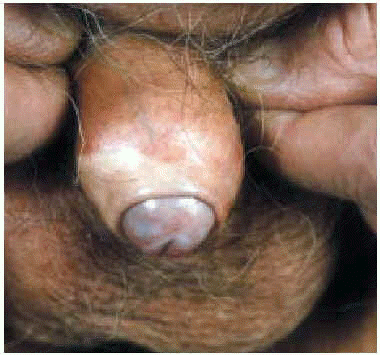
Cuando el proceso esclerótico progresa, el prepucio engrosado queda fijo y no puede ser retraído (fimosis), o puede retraerse con dificultad, y una vez retraído se fija imposibilitando el deslizamiento del prepucio sobre el glande (parafimosis). En esta fase, al liquen escleroso también se le denomina balanitis xerótica obliterante7. En el curso de la enfermedad, se puede llegar a alterar el tamaño del orificio uretral, comprometiendo el flujo urinario. Incluso puede impedir la expulsión de un cálculo uretral como se describió en un caso28 (fig. 7).
Fig. 7.--Evolución de la afectación del pene hacia la balanitis xerótica obliterante.
Lesiones cutáneas extragenitales
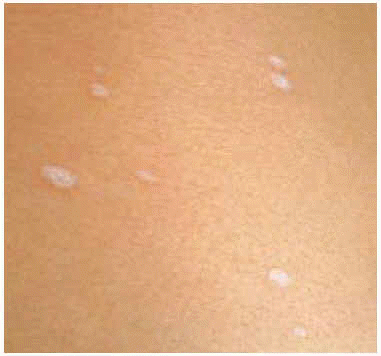
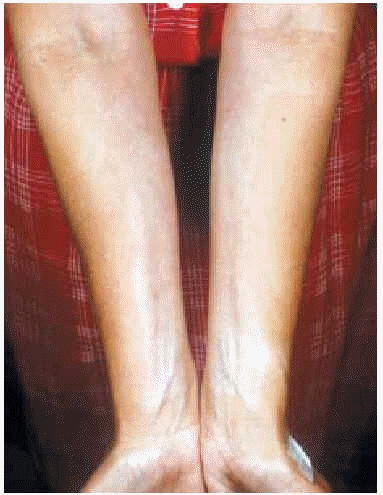
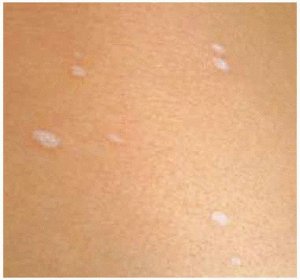
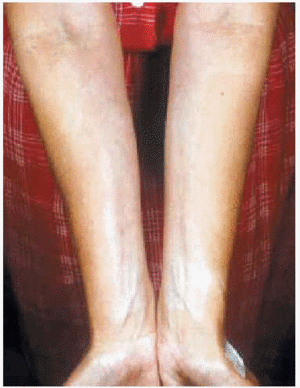
El 20 % de los pacientes adultos presentan también lesiones extragenitales, generalmente localizadas en la zona superior de la espalda (fig. 8), el cuello, la región periumbilical, las axilas y la zona flexora de las muñecas (fig. 9). Se han descrito casos de presentación siguiendo las líneas de Blaschko29,30.
Fig. 8.--Lesiones en tronco.
Fig. 9.--Lesiones en cara flexora de muñecas.
Las lesiones cutáneas están constituidas pápulas o máculas blanquecinas atróficas, que se agrupan en placas redondeadas, bien delimitadas, con aspecto arrugado como el de un papel de cigarrillo, y con formación de tapones foliculares de queratina sobre los orificios de los conductos pilosebáceos o sudoríparos dilatados. La superficie es lisa, aunque en algunos casos puede ser hiperqueratósica y sobreelevada31. Excepcionalmente se pueden ver lesiones ampollosas y hemorrágicas32.
Síntomas
Las lesiones cutáneas suelen ser asintomáticas. La afectación genital en los niños provoca la aparición de síntomas asociados como el prurito, el dolor, el sangrado, la disuria o el estreñimiento. En los adultos se acompaña de prurito, escozor, disminución de la sensibilidad, molestias al orinar y discapacidad para las relaciones sexuales con dispareunia.
ANATOMIA PATOLOGICA
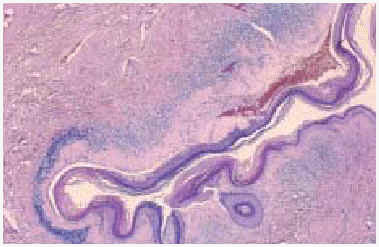
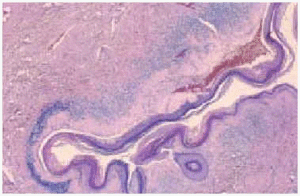
La histología convencional (fig. 10)33 muestra hiperqueratosis ortoqueratósica en la epidermis, atrofia, degeneración hidrópica de las células basales, hendiduras dermoepidérmicas y ocasionales tapones córneos ortoqueratósicos de los orificios foliculares y ecrinos en las lesiones cutáneas. En dermis papilar aparece edema y homogenización del colágeno, adoptando un aspecto en vidrio esmerilado. Se aprecia un infiltrado focal perivascular o en banda de células mononucleares y células plasmáticas, que separa la dermis papilar edematosa de la dermis reticular, junto a capilares dilatados. En casos avanzados la piel adquiere el aspecto de un proceso cicatrizal inespecífico. Estas lesiones histológicas del liquen escleroso pueden asociarse a cambios de liquen plano o morfea34,35.
Fig. 10.--Imagen histopatológica (HE).
El estudio inmunohistoquímico con anticuerpos policlonales para colágeno I y III, y un anticuerpo monoclonal para elastina demuestra una anómala distribución de éstos, que contribuye a la fragilidad y atrofia clínicamente evidentes36.
EVOLUCION
Dos tercios de los casos infantiles experimentan mejoría o curación al llegar la menarquia7 mientras que las formas del adulto tienden a la cronicidad, con fases de exacerbación y remisión. Los cambios histológicos epidérmicos prominentes como la atrofia, la hiperplasia y el taponamiento folicular se asocian a un peor pronóstico17.
En el 5 % de los casos, sobre todo en los de larga evolución, se desarrolla un carcinoma espinocelular37. Aunque clásicamente se ha referido una mayor frecuencia de esta complicación evolutiva en mujeres21, recientes trabajos han demostrado una incidencia similar de carcinoma espinocelular sobre liquen escleroso en hombres y en mujeres38. También se ha debatido el papel que puede desempeñar como cofactor oncogénico el VPH39.
ASOCIACIONES
Se han descrito repetidamente casos de coexistencia de liquen escleroso con lesiones de liquen plano40 y morfea41, con ambos a la vez42 e incluso con esclerodermia sistémica34. La posible relación entre el liquen escleroso y la morfea ha sido, y es todavía, objeto de debate43. Algunos autores consideran ambos procesos como manifestaciones de una misma enfermedad con un distinto grado de afectación de la piel44, mientras que otros opinan que se trata de dos entidades independientes45,46. Aunque en general el diagnóstico diferencial permite distinguir una de otra, las lesiones muy evolucionadas pueden resultar confusas e, incluso, a veces, en una misma lesión se pueden observar rasgos de los dos procesos43.
En un trabajo reciente47 se ha comunicado la asociación del liquen escleroso con proliferaciones melanocíticas. En un estudio de cohorte sobre 11 pacientes de edad media de 40 años con lesiones pigmentadas (nevos) en vulva, periné o pecho, sobre lesiones de liquen escleroso o en la periferia de éstas, se llevó a cabo un estudio anatomopatológico comparando los hallazgos con lesiones pigmentadas de pacientes controles. Los datos histológicos mostraron unas características similares a las de los nevos melanocíticos persistentes tras extirpación quirúrgica incompleta, y recordaban a un melanoma.
DIAGNOSTICO Y DIAGNOSTICO DIFERENCIAL
El diagnóstico se sospecha por la sintomatología y se confirma con el estudio anatomopatológico. Algunas veces el liquen escleroso leve simula otras enfermedades como el liquen plano erosivo, que puede producir placas blancas y cicatrices de forma similar; vitíligo e hipopigmentación postinflamatoria, por ejemplo, tras herpes genital recidivante; formas atróficas de liquen plano, en el que a diferencia del liquen escleroso suele haber afectación de vagina y boca; cicatrices en las que la esclerosis histológica se distribuye irregularmente; morfea o toxicodermias esclerodermiformes en las que la esclerosis es más profunda, liquenificación, atrofia posmenopáusica, penfigoide cicatrizal, vulvitis candidósica atrófica y leucoplasia, con la que a menudo coexiste26.
TRATAMIENTO
No existe un tratamiento absolutamente eficaz. Sólo los corticoides tópicos potentes controlan los síntomas y mejoran la evolución, aunque su uso prolongado puede aumentar la atrofia cutánea48. En las lesiones vulvares intensas está indicado el propionato de clobetasol al 0,05 % dos veces al día durante 4 o 6 semanas, pasando después a un corticoide tópico de menor potencia durante 3 o 4 meses más, a días alternos o dos veces por semana. Con frecuencia existen recidivas si se suspende el tratamiento por completo49, pero responden bien a la restauración del tratamiento50. Según recientes trabajos el tratamiento con corticoides tópicos de larga duración, puede asociarse con la reactivación oportunista de infecciones latentes por VPH mucoso-trópico de alto y bajo riesgo, por lo que el seguimiento a largo plazo es imprescindible51.
Las cremas de estrógenos al 0,01 %, la progesterona tópica al 2 % o la terapia hormonal sustitutiva en posmenopáusicas, ayudan a mejorar el estado del epitelio, pero son insuficientes como tratamiento por sí solos. El ungüento de propionato de testosterona al 2,5 % parece ser beneficioso, pero no se ha demostrado su eficacia en estudios clínicos, en los que, por el contrario, se ha mostrado tan eficaz como el placebo. Además puede provocar hipertrofia de clítoris, aumento de vellosidad, incremento de la libido y cambios en la voz.
En un estudio aleatorizado sobre 79 pacientes adultos, la remisión de los síntomas se produjo en el 75 % de los pacientes tratados con clobetasol, en el 20 % de los tratados con testosterona, en el 10 % de los tratados con progesterona y en el 10 % de los tratados con placebo52.
Recientemente se han publicado casos extragenitales tratados con fototerapia con rayos ultravioleta A (UVA)53; los pacientes recibieron aproximadamente 40 sesiones de tratamiento en 10 semanas con una dosis acumulada de 800 J/cm2. Otros casos se han tratado con calcipotriol54, aunque otros autores no han encontrado éxito con este último9. En 2 casos en los que se demostró la existencia del VPH por inmunohistoquímica y por técnicas de hibridación in situ, se consiguió una rápida mejoría con el tratamiento con imiquimod respecto al tratamiento previo con corticoides, mucho más lento12. La terapia fotodinámica del liquen escleroso vulvar mejoró el prurito en 10 de 12 mujeres tratadas55.
La cirugía y el láser56,57 llegan a mejorar el estado de las lesiones, pero la recidiva alcanza al 85 % de los casos. Sin embargo, son útiles para las cicatrices y disfunciones, como la fimosis inducida por el liquen escleroso, en la que es necesaria la circuncisión. De hecho, la postectomía es el tratamiento de elección en los adolescentes58.
Es preciso el seguimiento continuado para control de infecciones bacterianas o micóticas concomitantes. El hecho de que el liquen escleroso puede sufrir un proceso de malignización aconseja revisiones al menos dos veces al año59,60.