INTRODUCCION
El feto arlequín es la forma más grave y agresiva de las ictiosis congénitas. El primer caso fue descrito por el reverendo Oliver Hart en 17501. Esta entidad ha recibido varias denominaciones a lo largo de la historia como ictiosis congénita maligna, queratoma difuso maligno, ictiosis fetal intrauterina o queratoma maligno. Se presenta con un patrón de herencia autosómica recesiva. Tiene un pronóstico fatal en la mayoría de los casos durante el primer año de vida, aunque se han descrito casos de supervivencia superior2, sobre todo aquellos que han sido tratados precozmente con etretinato3, utilizado en esta entidad por primera vez en 19854. Estos últimos siguen una evolución muy similar a la que presenta la eritrodermia ictiosiforme congénita no ampollosa5,6.
DESCRIPCION DEL CASO
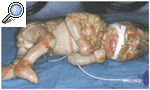
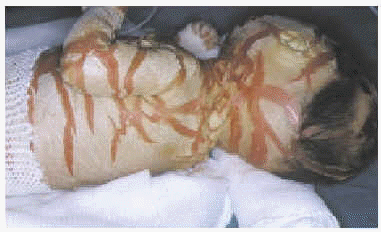
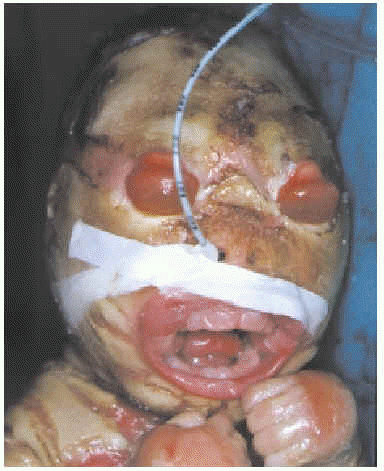
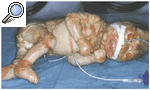
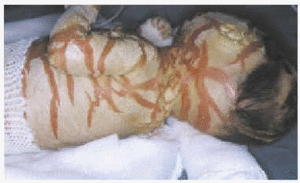
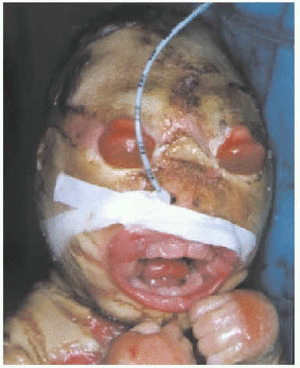
Presentamos a una recién nacida primogénita de 34 semanas de gestación y 2.050 g de peso, de padres consanguíneos (primos hermanos). El parto fue cefálico y espontáneo, y la niña presentó una puntuación de Apgar de 9/10, con líquido amniótico de coloración amarillenta. No había antecedentes familiares de ictiosis ni de enfermedades cutáneas. La niña presentaba grandes placas queratósicas, duras, gruesas y de coloración marrón-amarillenta, separadas por fisuras profundas de fondo eritematoso, que recubrían toda la superficie corporal (figs. 1 y 2). También presentaba ectropión severo, con hiperemia conjuntival que ocultaba los globos oculares, eclabium y alteraciones de la pirámide nasal y los pabellones auriculares (fig. 3).
Fig. 1.--Aspecto general de la paciente.
Fig. 2.--Fisuraciones profundas en la espalda y cuello.
Fig. 3.--Ectropión y eclabium severos.
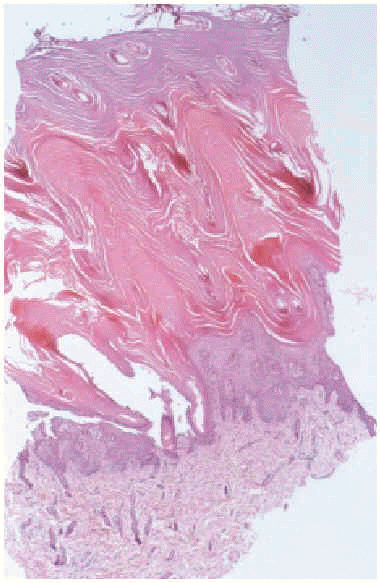
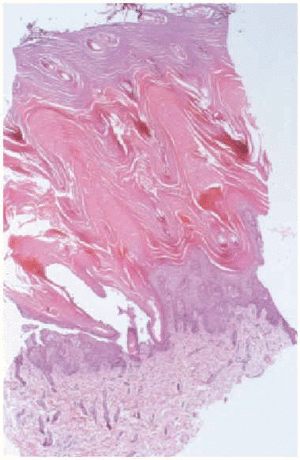
Se realizó una biopsia cutánea de la pierna izquierda, donde se apreciaba una hiperqueratosis compacta lamelar con focos aislados de paraqueratosis y persistencia de la capa granulosa (fig. 4). De acuerdo con los padres, se desestimó el tratamiento con etretinato. Se mantuvo a la paciente con nutrición enteral, sueroterapia, pomadas oculares epitelizantes, analgésicos, emolientes y fomentos con sulfato de cinc (1:1.000). Al final de la primera semana, las grandes escamas empezaron a desprenderse, y apareció debajo un fondo eritematoso. Posteriomente se observaron lesiones cianóticas en las puntas de los dedos de los pies. A los 18 días se produjo el fallecimiento precedido de un empeoramiento de su estado general con intensos episodios de vómitos y pausas de apnea. No se realizó autopsia.
Fig. 4.--Hiperqueratosis compacta lamelar con focos aislados de paraqueratosis y persistencia de la capa granulosa (hematoxilina-eosina).
DISCUSION
Las referencias del feto arlequín en la literatura española son muy escasas. El primer caso en España fue publicado por Azúa en 19097 y, posteriormente, se han descrito 8 casos más8-12. Se presenta con un patrón de herencia autosómico recesivo. Hay casos recogidos en gemelos11 y en varias ocasiones se ha podido demostrar consanguinidad, como en nuestro paciente12,13. Aunque no se ha detectado el gen anómalo en seres humanos, sí se ha determinado en ratones la mutación homóloga en el gen ichq, en el cromosoma 19 múrido12,14.
Se desconoce la fisiopatología del feto arlequín. Los estudios ultraestucturales y bioquímicos realizados en estos casos han revelado, mediante difracción con rayos X, un patrón de queratina anormal, tipo beta, en lugar del patrón normal tipo alfa, si bien se han descrito casos con queratina normal15. El feto arlequín, junto con la eritrodermia ictiosiforme ampollosa, la forma Curth-Macklin de la ictiosis hystrix y la ictiosis hystrix grave, forman un grupo de entidades con trastornos genéticos de la queratinización caracterizados por presentar defectos estructurales de las tonofibrillas16, con persistencia anormal de los desmosomas en la capa córnea10,12. El calcio interviene como factor crítico para la diferenciación epidérmica. Estudios recientes plantean una alteración en la calpaína I (proteasa activada por el calcio) en el feto arlequín, ya que se presentan en menor cantidad en la piel de estos pacientes en comparación con la piel de pacientes sanos o con la de otras entidades en la que haya una alteración de la diferenciación epidérmica17. Además, también se ha demostrado una disminución de la actividad de las proteínas fosfatasas en cultivos de queratinocitos de feto arlequín18. Aunque el feto arlequín ha aparecido asociado con otras anomalías congénitas, principalmente renales9,19, nuestra paciente no presentaba ninguna de ellas. Sí se había observado previamente, en cambio, el desarrollo de necrosis digitales que presentó nuestro caso14,20.
El manejo de los pacientes con ictiosis21 se basa en el tratamiento tópico, principalmente con queratolíticos (alfahidroxiácidos, urea, ácido salicílico y retinoides), emolientes (propilenglicol al 40-60 % en cura oclusiva, parafina, vaselina, aceites vegetales, etc.) y los derivados de la vitamina D que incrementan las concentraciones de calcio intracelular e inducen la diferenciación terminal22. El ácido salicílico en estos pacientes debe administrarse con precaución, ya que no son raras las intoxicaciones. Es sabido que el ácido salicílico puede producir salicilismo en neonatos y lactantes.
El tratamiento sistémico se basa en retinoides orales, etretinato o acitretino, en dosis de 0,5-1 mg/kg/día, o isotretinoína en dosis de 0,5 mg/kg/día. Actualmente, hay estudios sobre un nuevo derivado imidazólico, el liarozol, que inhibe la hidroxilación del ácido retinoico dependiente del citocromo P-45023.
Además de tomarse estas medidas, los pacientes afectados (feto arlequín) también deben ser ingresados en una unidad de cuidados intensivos, para control del balance hidroelectrolítico, la temperatura y las posibles infecciones21.
El diagnóstico prenatal del feto arlequín puede establecerse con biopsia cutánea por fetoscopia en la 22 semana de gestación24 o en células del líquido amniótico25,26. La ecografía en tres dimensiones puede ser útil también para el diagnóstico prenatal de esta enfermedad27.