INTRODUCCION
Existen cuatro variantes bien caracterizadas de neoplasias malignas de células plasmáticas, que son: mieloma múltiple clásico, plasmocitoma extramedular sin mieloma, plasmocitoma solitario de hueso y leucemia de células plasmáticas. La afectación cutánea específica puede presentarse en pacientes con cualquiera de estos cuatro procesos, pero se trata de un hecho clínico muy poco frecuente. El plasmocitoma cutáneo primario es una neoplasia extremadamente rara y los pocos casos en los que aparece una afectación cutánea específica por una neoplasia de células plasmáticas se trata habitualmente de una extensión directa a la piel desde una lesión osteolítica subyacente de un mieloma múltiple que afecta al hueso o desde un plasmocitoma solitario de hueso.
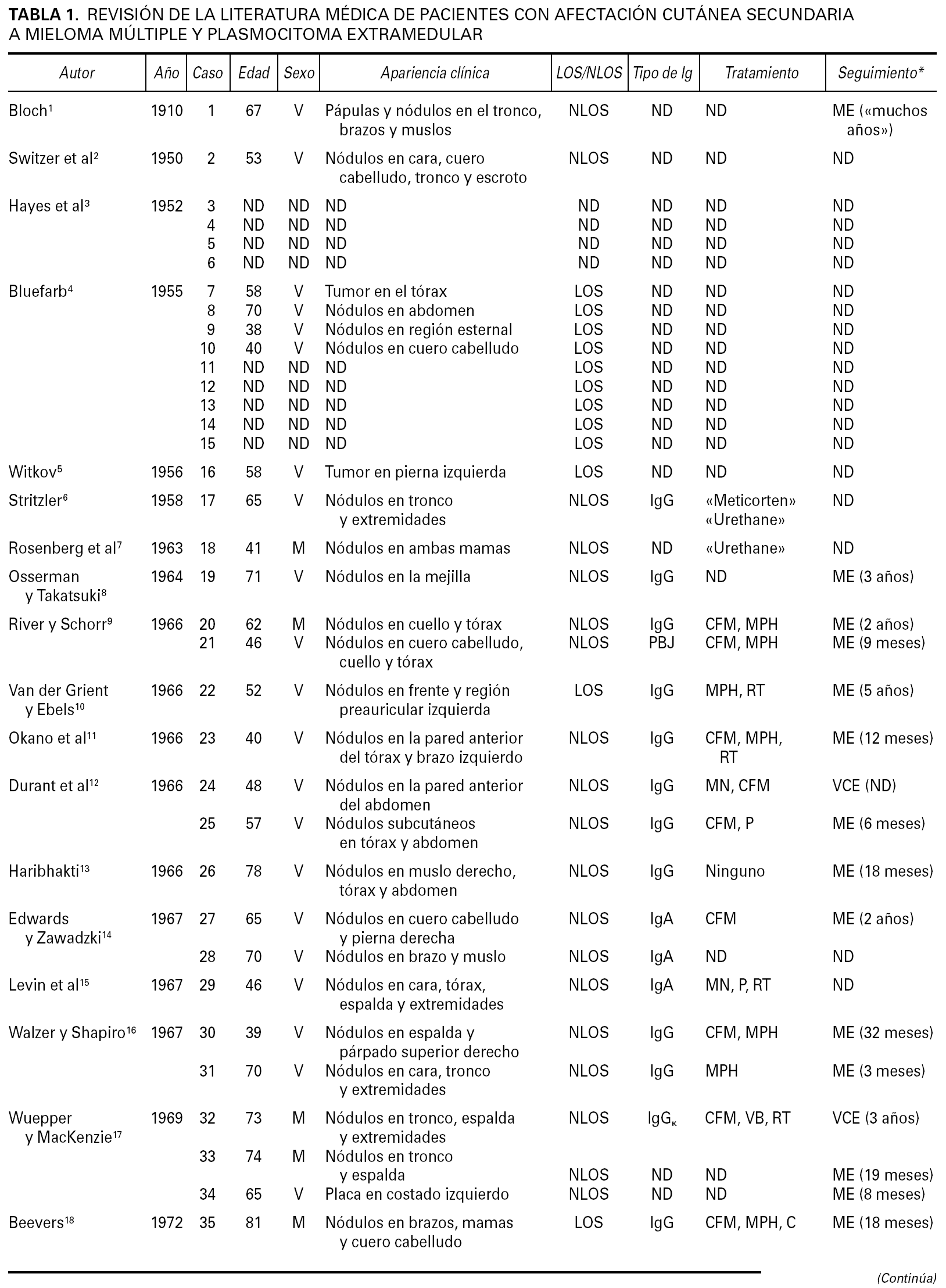
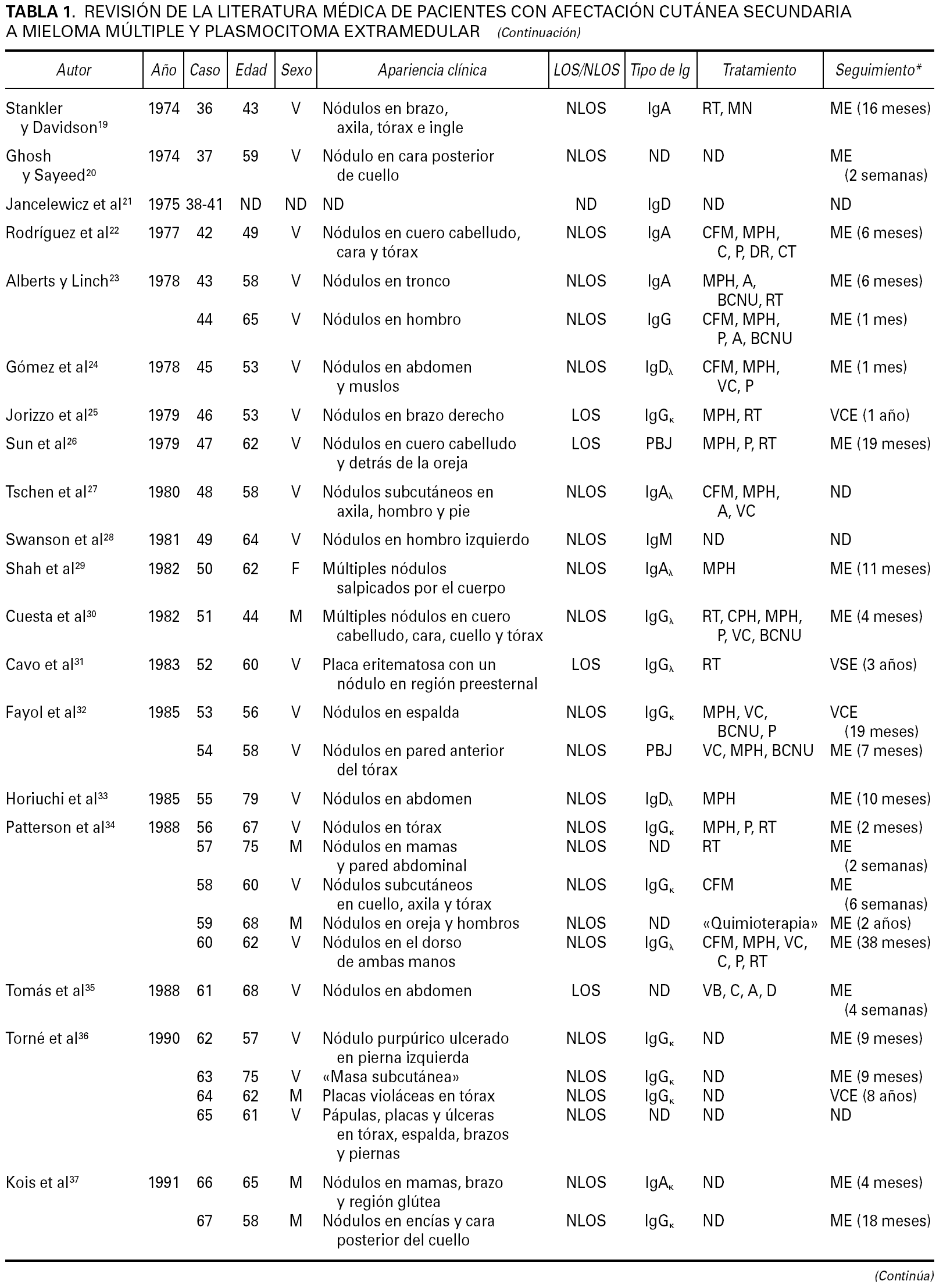
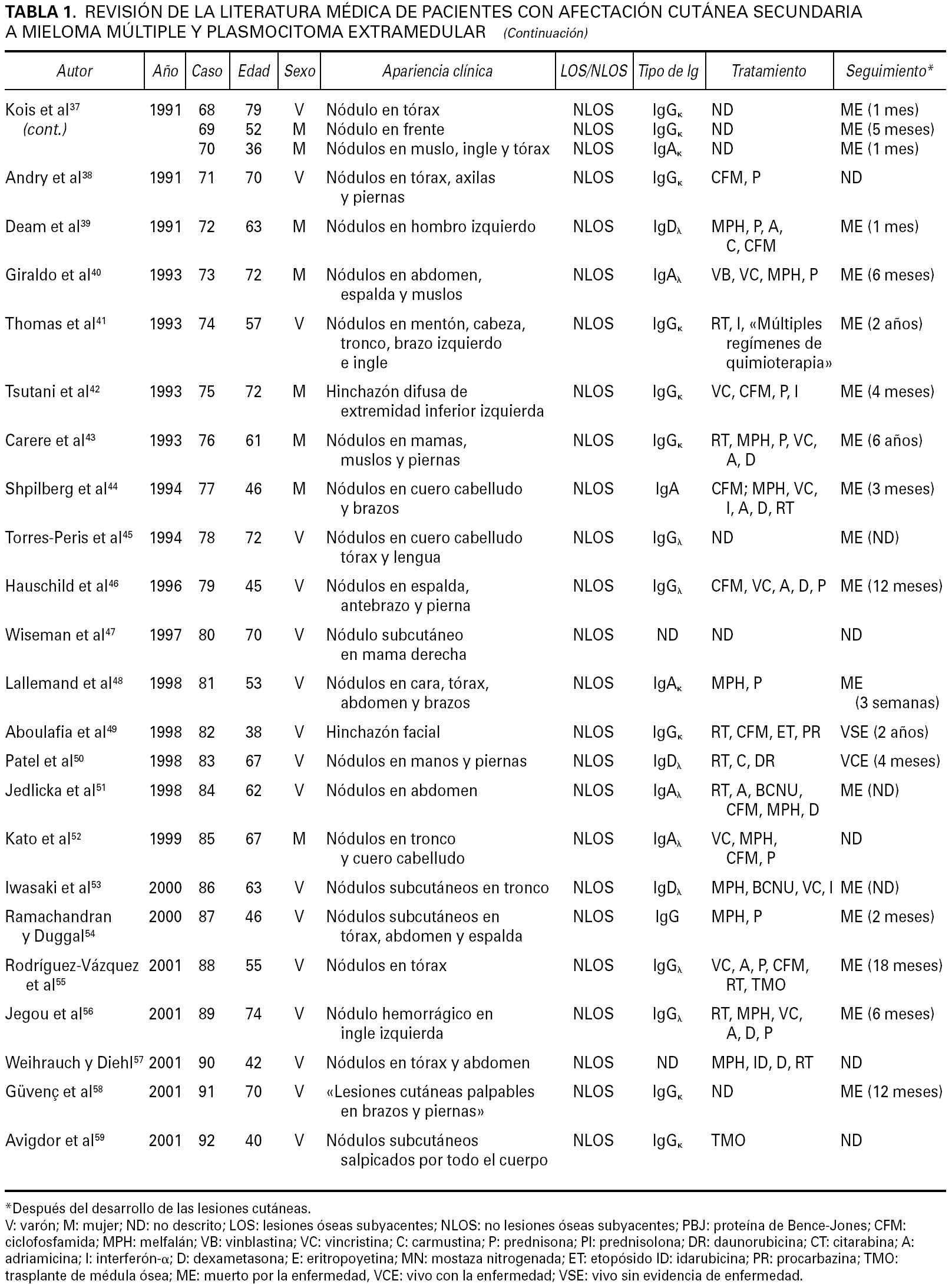
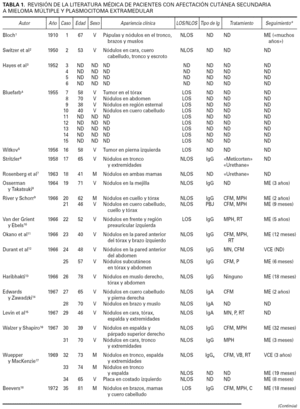
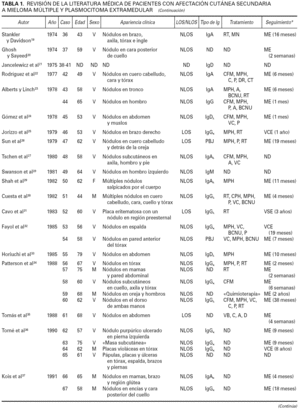
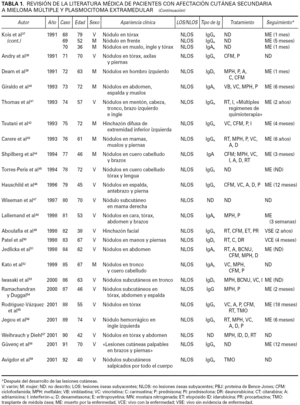
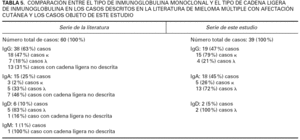
Aunque la afectación de los tejidos blandos de la vía aérea superior y de la mucosa de la cavidad oral es relativamente frecuente en pacientes con mieloma múltiple clásico y plasmocitoma extramedular, la afectación cutánea metastásica en un paciente con mieloma múltiple sin lesiones óseas subyacentes es extraordinariamente rara. En la tabla 1 se enumeran los casos descritos en la literatura médica de afectación cutánea específica metastásica en pacientes con mieloma múltiple y plasmocitoma extramedular, incluyendo tanto los casos en los que la afectación cutánea apareció como consecuencia de una extensión por contigüidad desde una lesión ósea subyacente, como los casos en los que la lesión cutánea se desarrolló sin que los estudios radiológicos y/o gammagráficos pudieran detectar lesiones óseas subyacentes 1-59.
En este estudio, se describen las características clinicopatológicas, así como los hallazgos inmunohistoquímicos, los estudios de reordenamiento genético y las anomalías citogenéticas encontradas en las lesiones cutáneas de 40 pacientes con mieloma múltiple clásico en los que el proceso neoplásico se extendió a la piel. Esta serie constituye, con mucha diferencia, la serie más amplia descrita en la literatura médica, de esta rara enfermedad. Además, los 40 pacientes descritos en este estudio representan ejemplos de infiltración cutánea específica sin que los estudios de imagen practicados (radiografías, gammagrafías óseas o estudios de resonancia magnética [RM], según los casos) pudieran demostrar lesiones óseas subyacentes a las lesiones cutáneas, por lo que en principio se puede descartar que se trate de casos de extensión a la piel por contigüidad. Este estudio está particularmente dirigido a la posible identificación de un inmunofenotipo característico de las lesiones cutáneas específicas en pacientes con mieloma múltiple, así como a la correlación de los estudios de restricción de las cadenas ligeras de inmunoglobulinas y del reordenamiento del gen JH de las cadenas pesadas de inmunoglobulinas, comparando en cada caso los resultados de médula ósea con los de las lesiones cutáneas. Además se realizaron estudios citogenéticos mediante técnicas de hibridación in situ mediante fluorescencia (FISH) para investigar de deleción del gen de retinoblastoma, así como la posible influencia de las distintas opciones de quimioterapia en la supervivencia de los pacientes una vez que las lesiones cutáneas se habían desarrollado.
MATERIAL Y MÉTODOS
En este estudio se han incluido 40 pacientes con diversos tipos de mieloma múltiple que además presentaban lesiones cutáneas de infiltración específica por células plasmáticas neoplásicas. En cada paciente se recogieron los siguientes datos de la historia clínica: edad, sexo, morfología clínica y localización de las lesiones cutáneas específicas, tipo de mieloma múltiple con respecto a la naturaleza de la inmunoglobulina monoclonal y de la cadena ligera de inmunoglobulina producida, tratamiento administrado y supervivencia una vez que las lesiones cutáneas se habían desarrollado.
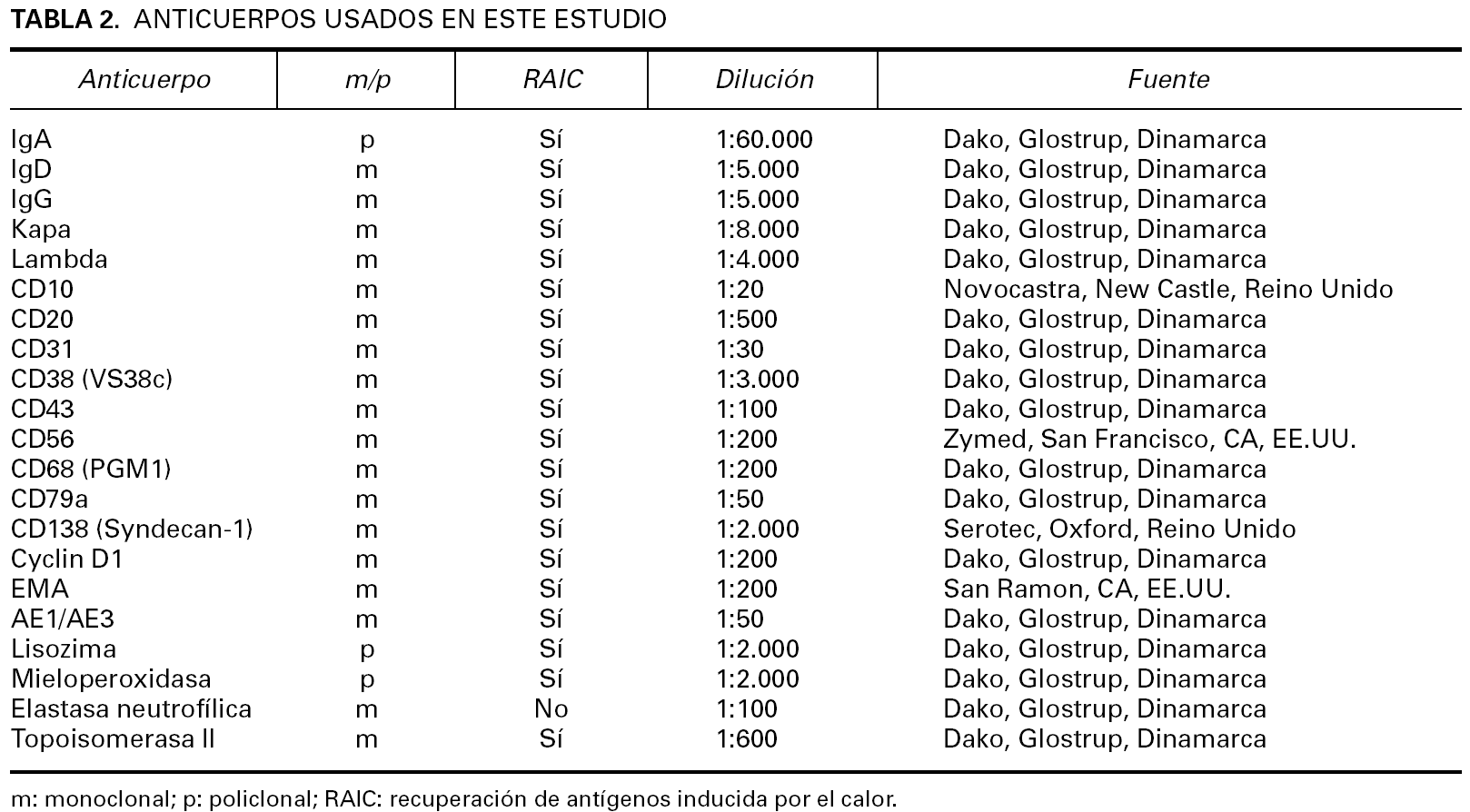
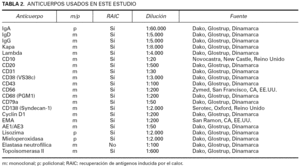
En cada paciente se disponía al menos de una biopsia cutánea demostrativa de la afectación cutánea por el proceso neoplásico de células plasmáticas. A partir de esta biopsia se realizaron también estudios inmunohistoquímicos mediante la técnica estándar de avidina-biotina 60. Los anticuerpos utilizados en el estudio inmunohistoquímico, su carácter monoclonal o policlonal, su fuente y las diluciones empleadas aparecen enumerados en la tabla 2.
En 22 casos en los que después de realizar los estudios histopatológicos e inmunohistoquímicos aún disponíamos de tejido adicional, se realizaron investigaciones de reordenamiento del gen JH de las cadenas pesadas de inmunoglobulinas mediante técnicas de reacción en cadena de la polimerasa (PCR). Por esta misma técnica también se investigó en estos 22 casos la presencia de material genético del virus del herpes humano tipo 8 (HHV-8) y del virus de Epstein-Barr (VEB).
Para la extracción del ADN, entre 4 y 10 cortes de 10 μM del material incluido en parafina de cada bloque de biopsia cutánea se desparafinó con pases sucesivos por xilol y etanol y se digirió el tejido con 0,6 mg proteinasa K durante la noche previa a cada estudio. El ADN obtenido se purificó mediante el kit QIAamp DNA Mini Kit (Qiagen, Hilden, Alemania) y se extrajo con 150 μl de búfer tamponado. La presencia de ADN sujeto a amplificación se confirmó utilizando un gen específico para PCR del factor V. Las investigaciones de reordenamiento del gen JH se llevaron a cabo con 50 μM de la siguiente estructura de primers específicos: FR3: 59 -ACACGGCYGTRTATTACTGT-39 y fluorescente (Cy-5-marcado) JH: 59 -ACCTGAGGAGACGGTGACC-39. Muestras de tejido de un linfoma B de células grandes de las extremidades inferiores se procesaron con idéntica técnica y se utilizaron como control positivo. Los estudios de PCR se llevaron a cabo con 1,5 mM de Cl2Mg, 50 mM de ClK, 10 mM de Tris-ClH a pH 9,0, 200 mM de dNTPs en cada muestra y 1,5 U de taq-polimerasa para un volumen final de 25 μl bajo las siguientes condiciones: 20 s a 94 °C, 20 s a 62 °C y 20 s más a 72 °C durante 33 ciclos. Después de la desnaturalización durante 2,5 min a 85 °C, todas las muestras se aplicaron en un gel de electroforesis desnaturalizado de alta resolución (ReproGel, Amersham Pharmacia Biotech, Freiburg, Alemania) y se procedió a la electroforesis a 55 °C y 30 W durante 200 min. La visualización de los productos fluorescentes de PCR se llevó a cabo mediante un sistema informático de análisis fragmentado (Fragment Analyzer, Amersham Pharmacia Biotech, Freiburg, Alemania) conectado a un secuenciador de láser automático (AlfExpress II, Amersham Pharmacia Biotech, Freiburg, Alemania). Para la investigación de HHV-8, los estudios de PCR se llevaron a cabo en las siguientes condiciones: 20 s a 94 °C, 20 s a 58 °C y 20 s más a 72 °C durante 40 ciclos utilizando 80 μM de KSHV-1: 59 -AGCCGAAAGGATTCCACCAT-39 como primer de avance y 80 μM de KSHV-2: 59 -TCCGTGTTGTCTACGTCCAG-59 como primer reverso. Para las investigaciones del VEB, la PCR se llevó a cabo con 50 μM de los primers EBV-1: 59 - CGCAGGGATGCCTGGACACA-39 y EBV-2: 59 -CTG TTTGTGGGCCTTGTGGC-39. Después de una desnaturalización inicial durante 3 min a 94 °C, las muestras migraron en el gel de electroforesis durante 30 s a 94 °C, 30 s a 69 °C y 20 s más a 72 °C durante 40 ciclos. Ambas investigaciones de PCR viral fueron llevadas a cabo con 1,5 mM Cl2Mg, 50 mM ClK, 10 mM de Tris-ClH a pH 9,0, 200 mM de dNTP en cada muestra y 1,5 U de taq-polimerasa para un volumen final de 25 μl. Todas las muestras migraron en un gel de agarosa al 2 % fueron teñidas con bromuro etídico y visualizadas bajo luz ultravioleta (302 nm).
En estos mismos 22 casos se realizaron estudios de FISH para investigar la deleción del gen del retinoblastoma (rb1). Estos estudios se llevaron a cabo siguiendo la técnica previamente descrita por Kuchinka et al 61. Brevemente, esta técnica consiste en desparafinar una muestra de tejido de 50 μM de espesor e incubarla con 1 mg de colagenasa XI durante 2 h. Posteriormente esta muestra se incuba con una solución de tripsina/EDTA al 0,05 % durante 1-2 h. Los núcleos celulares desprendidos son recuperados sobre portas y calentados a 50 °C. Después de deshidratar las muestras, estas se incuban con una solución pretratamiento (Oncor Appligene, Heidelberg, Alemania) siguiendo las instrucciones del fabricante con proteinasa K (150 μg/ml). Después de deshidratar las muestras se realiza la hibridación durante toda la noche con una sonda rb1 marcada con espectro naranja (Vysis, Bergisch Gladbach, Alemania), lavada con 60 % formamida y un búfer de citrato sódico-cloruro sódico durante 15 min a 45 °C y se contrasta con DAPI (49,6-diamidino-2-fenilindol). Las señales se visualizaron con un microscopio Axioplan 2 (Zeiss, Göttingen, Alemania) usando un filtro de banda única DAPI para la identificación de los núcleos y un filtro de banda estrecha para la visualización del espectro naranja (Vysis, Bergisch Gladbach, Alemania). Como controles positivos se utilizaron muestras de biopsias conteniendo piel normal.
RESULTADOS
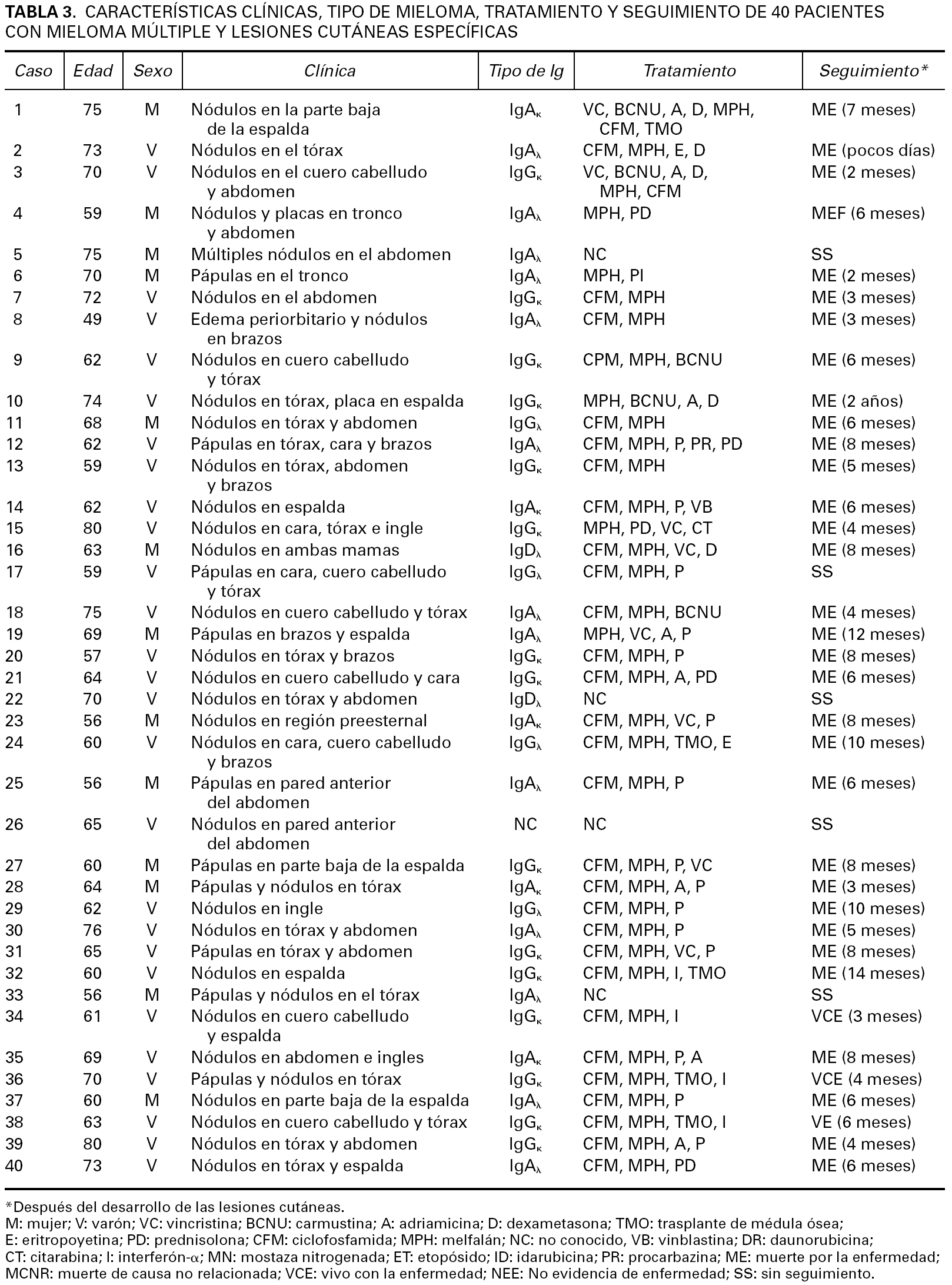
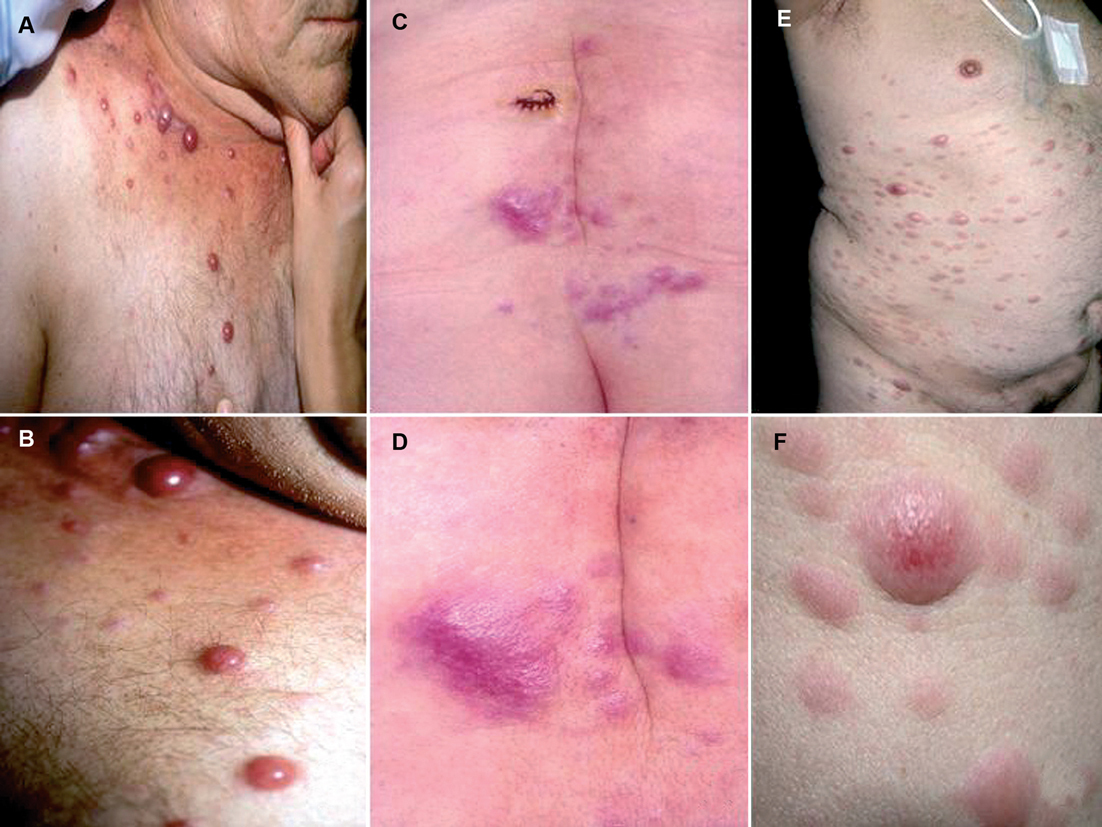
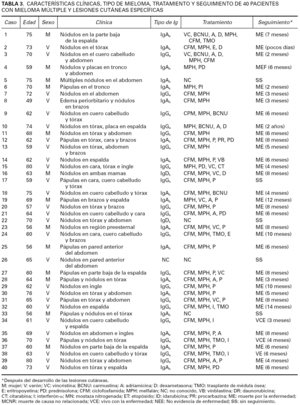
Las características clínicas de nuestros 40 pacientes se enumeran en la tabla 3. Brevemente, 27 pacientes eran varones y 13 mujeres, con unas edades que oscilaban entre los 56 y los 80 años, con una edad media de 65,57 años. Desde el punto de vista clínico, la morfología más frecuente de las lesiones era la de múltiples pápulas o nódulos de consistencia firme, salpicados por distintas áreas corporales, pero preferentemente localizados en la pared anterior del tórax, pared anterior del abdomen y espalda (fig. 1). En algún caso raro la lesión consistía en una placa que era el resultado de la confluencia de los nódulos. La coloración de las lesiones era eritematosa o violácea y estaban cubiertas por una epidermis tersa y brillante, pero no se observaron lesiones ulceradas.
Fig. 1.--Morfología clínica de las lesiones. A) y B) Nódulos en la pared anterior del tórax. C) y D) Placas eritematosas en región lumbosacra. E) y F) Nódulos y placas salpicados por tórax y abdomen.
En 39 de los 40 pacientes se conocía el tipo de inmunoglobulina monoclonal producida por las células plasmáticas neoplásicas del mieloma múltiple: 18 pacientes tenían un mieloma IgA (5 IgAκ y 13 IgAλ), 19 pacientes tenían un mieloma IgG (15 IgGκ y 4 IgGλ) y 2 pacientes tenían un mieloma IgDλ.
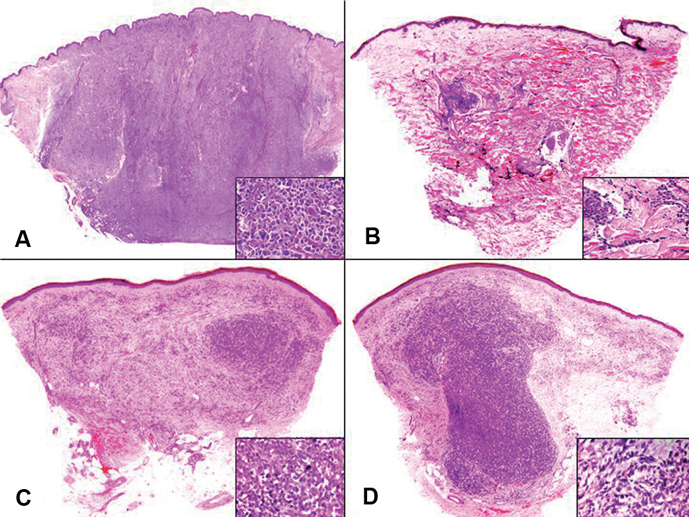
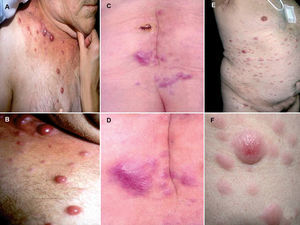
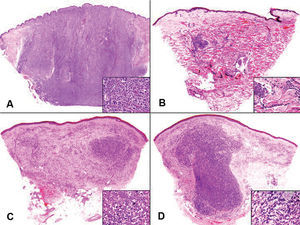
Desde el punto de vista histopatológico (fig. 2), las lesiones cutáneas podían clasificarse en dos grandes patrones morfológicos: a) nodular, y b) difuso intersticial. El patrón nodular era el más frecuente, ya que se observaba en 24 casos, mientras que el patrón intersticial sólo estaba presente en 13 de los casos. En aquellos pacientes que tenían más de una biopsia cutánea, el patrón nodular o intersticial de la biopsia inicial, persistía en las biopsias sucesivas. En 3 casos (casos, 1, 17 y 19) se observaba una combinación de ambos patrones, nodular e intersticial en la misma biopsia. Excepto en 5 casos (casos 7, 14, 15, 29 y 33), en los que se observaba sólo una afectación focal de la dermis, en el resto de los casos la infiltración por células plasmáticas neoplásicas afectaba a todo el espesor de la dermis, incluyendo la dermis papilar y reticular. La epidermis estaba preservada en todos los casos y en la mayoría de los casos se observaba una estrecha banda de dermis papilar respetada. El infiltrado de células plasmáticas neoplásicas se extendía a la hipodermis en 5 casos (casos 1, 6, 8, 19 y 27), con una afectación predominantemente lobulillar, aunque también se observaban hileras de células plasmáticas neoplásicas dispuestas intersticialmente entre los haces de colágeno de los septos hipodérmicos. El patrón nodular estaba constituido por uno o varios agregados de células plasmáticas neoplásicas dispuestos en forma de masas tumorales cohesivas. En contraste, el patrón intersticial difuso estaba constituido por cordones o hileras de células plasmáticas neoplásicas dispuestas entre los haces de colágeno de la dermis. En algunos casos, estas células plasmáticas neoplásicas eran fácilmente identificables como tales, ya que mostraban las características citomorfológicas habituales (núcleo excéntrico con cromatina en rueda de carro, halo claro paranuclear y amplio citoplasma ligeramente basófilo) y a veces eran binucleadas o multinucleadas. Sin embargo, en otros casos estas células neoplásicas infiltrando la dermis mostraban un núcleo vesiculoso y pleomórfico, con nucléolo prominente y un citoplasma granular y eosinófilo. En estos casos resultaba difícil identificar la verdadera naturaleza de estas células debido a sus características citológicas, ya que correspondían a plasmoblastos inmaduros. En 3 casos (casos 6, 14 y 28), las células plasmáticas neoplásicas que infiltraban la dermis mostraban una morfología fusiforme, lo que determinaba que, desde el punto de vista histopatológico, la lesión pareciera más un sarcoma que una infiltración cutánea por un mieloma múltiple. En los casos en que la infiltración dérmica estaba predominantemente constituida por plasmoblastos inmaduros, se observaban frecuentes figuras de mitosis, muchas de ellas atípicas. No se observaron cuerpos de Russel citoplasmáticos ni cuerpos de Dutcher intranucleares.
Fig. 2.--Patrones histopatológicos. A) Patrón nodular; B) patrón intersticial; C) patrón mixto, combinando infiltración nodular e intersticial; D) en este caso el patrón era nodular, pero lo llamativo era la morfología fusiforme de las células plasmáticas neoplásicas. Con cada patrón se muestra un detalle a gran aumento con las características citológicas de las células neoplásicas.
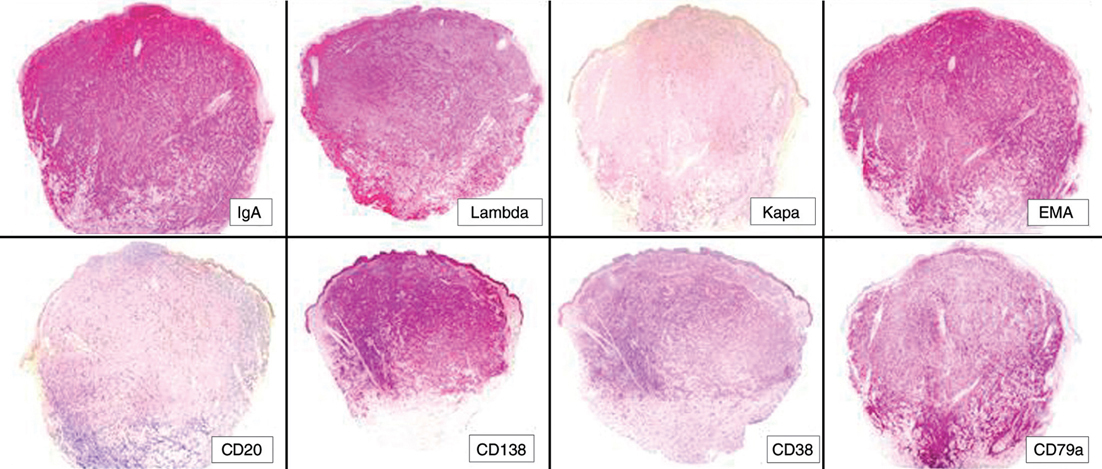
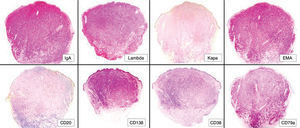
Desde el punto de vista inmunohistoquímico (fig. 3), las células plasmáticas neoplásicas de la dermis mostraban una intensa inmunorreactividad para CD79a, CD138 y antígeno de membrana epitelial (EMA), así como una expresión variable de CD38 y CD43. En 3 casos (casos 3, 17 y 25) las células neoplásicas expresaban CD56, pero este marcador resultó negativo en el resto de los casos. La topoisomerasa II marcó los núcleos de numerosas células plasmáticas infiltrando la dermis, con una proporción variable del 30 al 60 % de las células, según los casos. El resto de los marcadores estudiados resultaron negativos en todos los casos (tabla 4).
Fig. 3.--Características inmunohistoquímicas de uno de los casos. Intensa expresión de IgA en las células neoplásicas. La mayoría de las células expresan las cadenas ligeras l, pero son negativas para las cadenas ligeras k. La mayoría de las células neoplasias también expresan positividad para el antígeno de membrana epitelial (EMA). Otras características inmunohistoquímicas de las células plasmáticas neoplásicas son la escasa positividad del CD20 y CD38 y la intensa inmunorreactividad para el CD138 y CD79a.
En todos los casos, las células plasmáticas neoplásicas de la dermis segregaban inmunoglobulinas, y en cada caso el tipo de inmunoglobulina producida, así como la restricción de cadena ligera detectada, se correspondía con los obtenidos en los estudios inmunoelectroforéticos del suero de cada paciente, lo que también apoyaba la naturaleza neoplásica y monoclonal de las células plasmáticas que infiltraban la dermis.
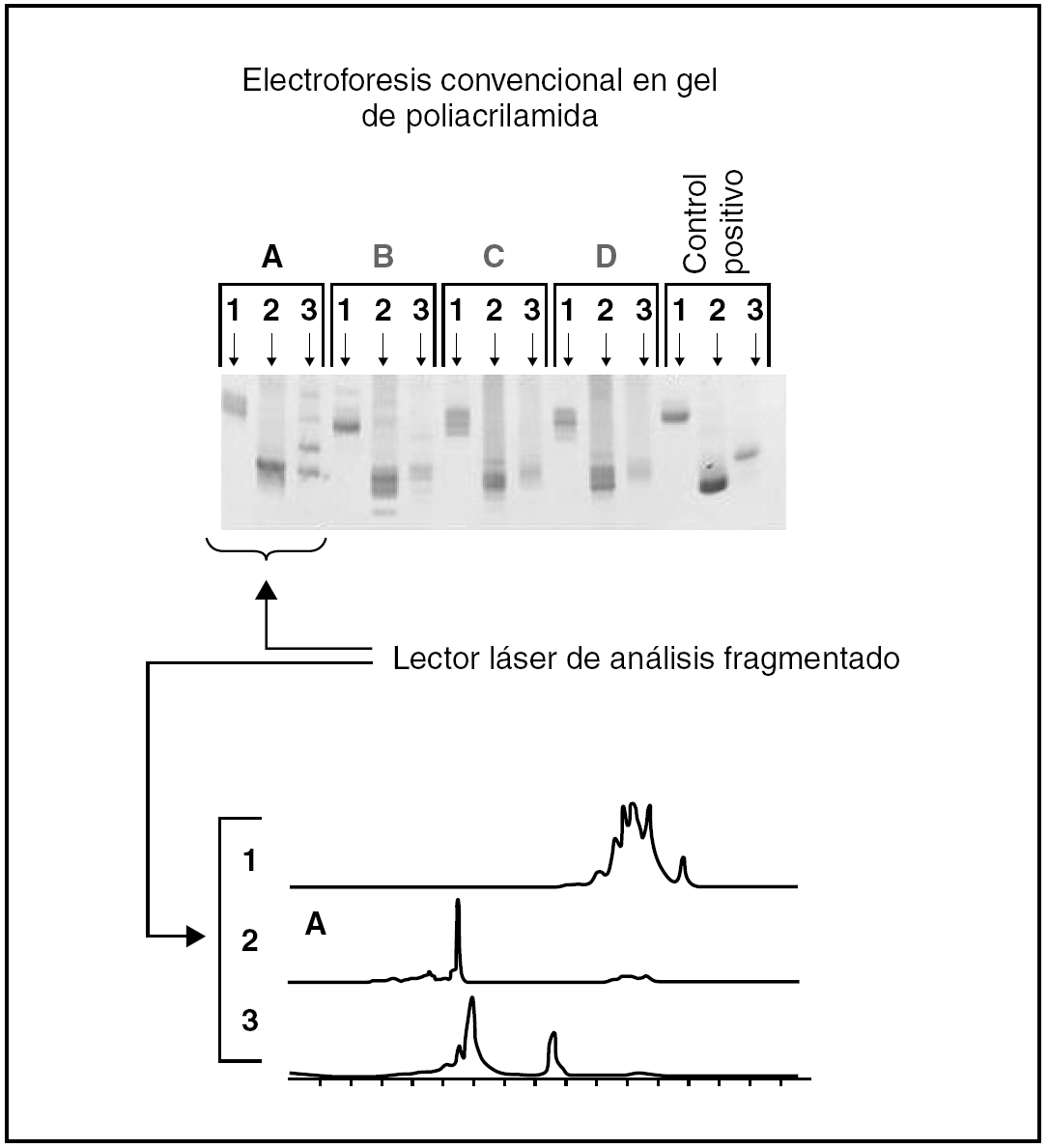
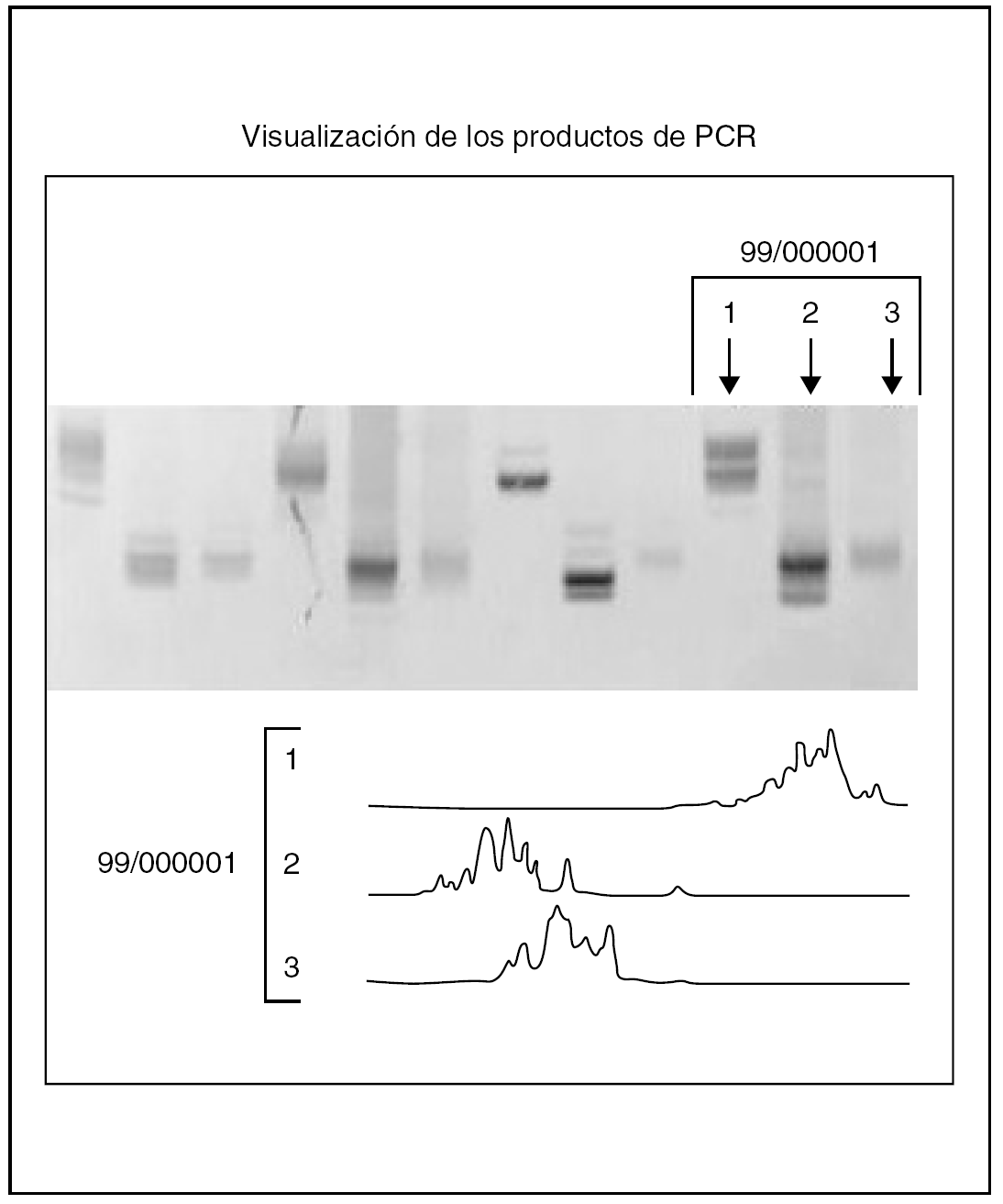
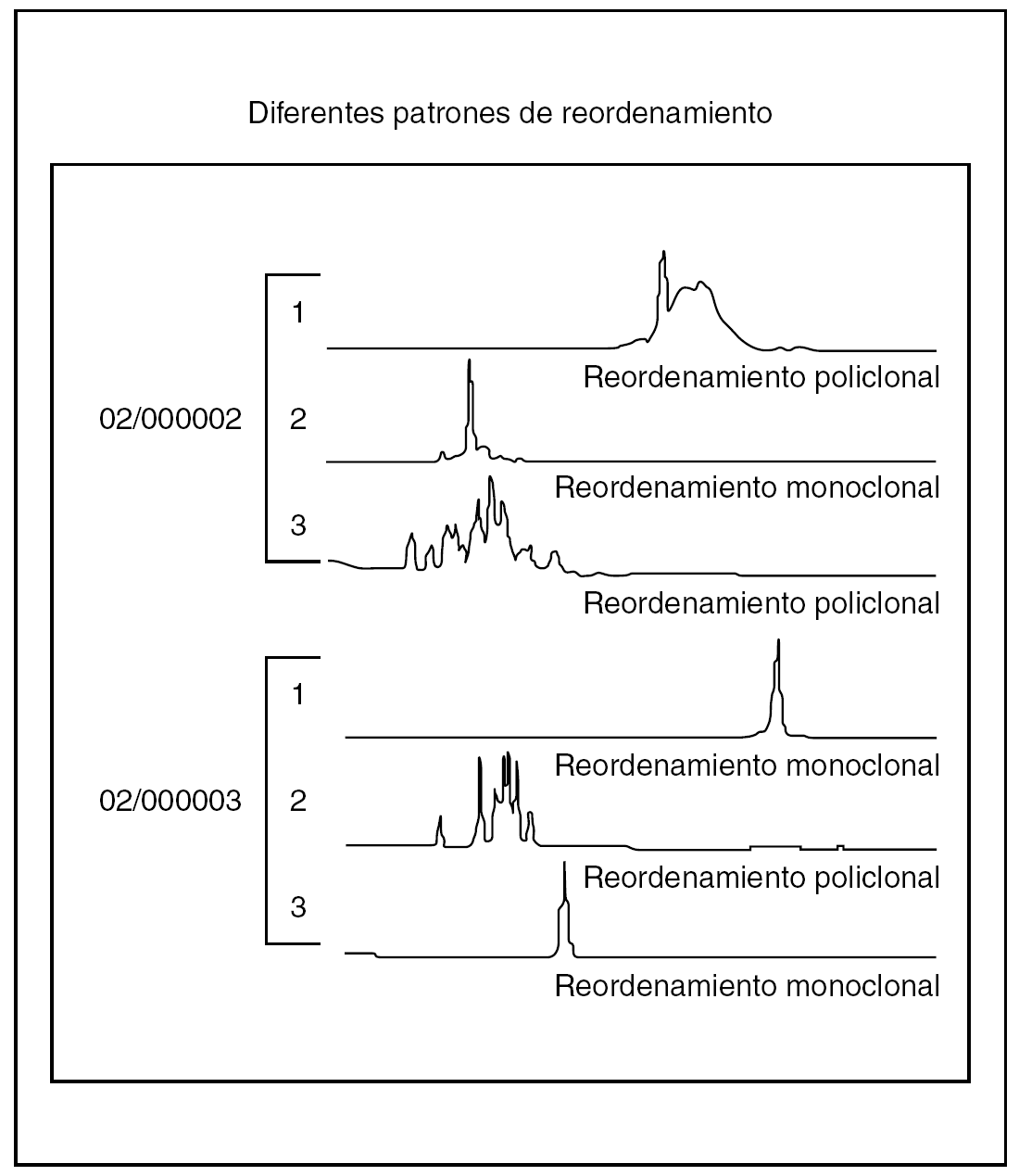
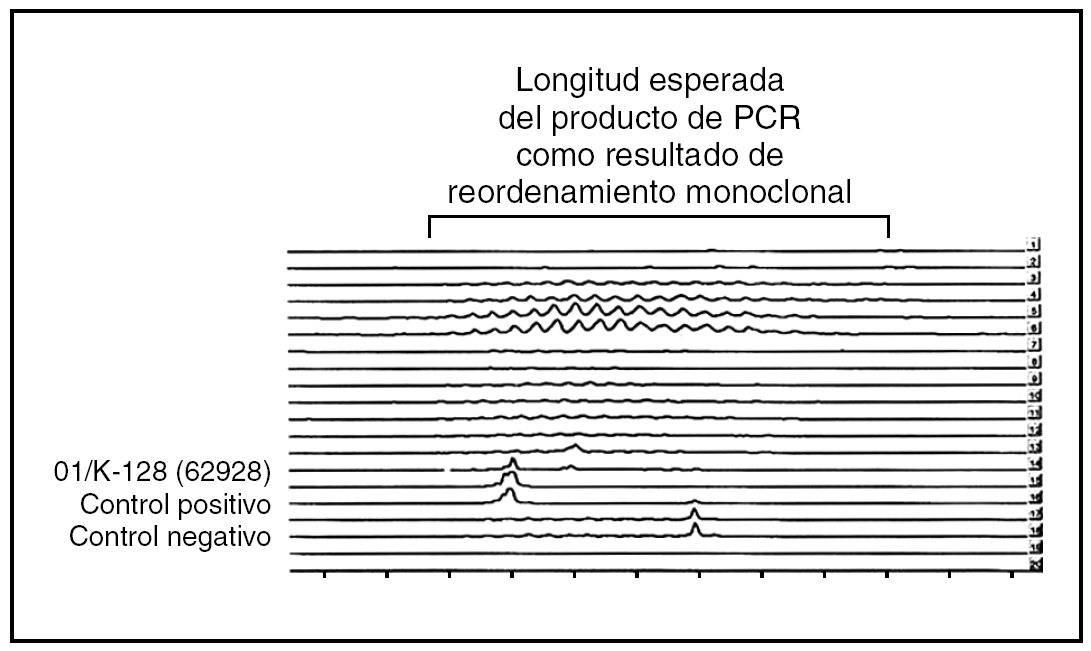
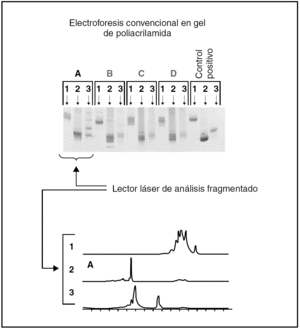
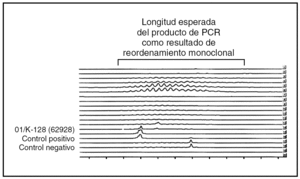
En los 22 casos en los que se llevaron a cabo estudios de reordenamiento del gen JH de las cadenas pesadas de inmunoglobulinas mediante PCR (figs. 4-7) se demostró reordenamiento monoclonal, mientras que las investigaciones virales para tratar de identificar material genético del virus HHV-8 y del VEB dieron resultados negativos en todos los casos.
Fig. 4.--Comparación entre los resultados de los estudios de reordenamiento genético del gen JH por PCR en electroforesis convencional en gel de poliacrilamida y lectura mediante un lector de láser de análisis fragmentado.
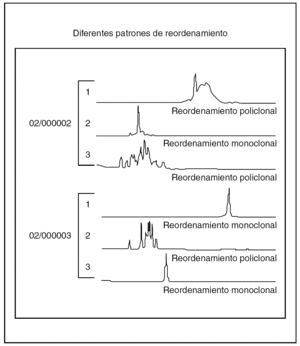
Fig. 5.--Comparación entre electroforesis convencional y el lector de láser de análisis fragmentado en 3 casos de infiltrados reactivos de células plasmáticas en los que no se observa reordenamiento monoclonal: la gráfica muestra varios picos (reordenamiento policlonal o imagen «en cordillera»).
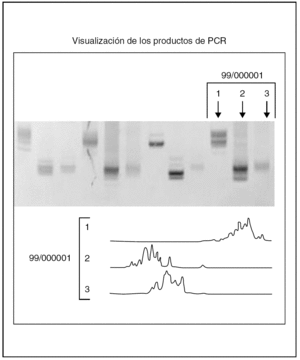
Fig. 6.--Gráficas con el lector de láser de análisis fragmentado de 6 casos. En unos se observa reordenamiento monoclonal (un solo pico), mientras que en los casos de reordenamiento policlonal se observan varios picos (imagen «en cordillera»).
Fig. 7.--Gráfica con el lector de láser fragmento mostrando reordenamiento monoclonal positivo de uno de los casos de esta serie de mieloma múltiple con infiltración cutánea específica.
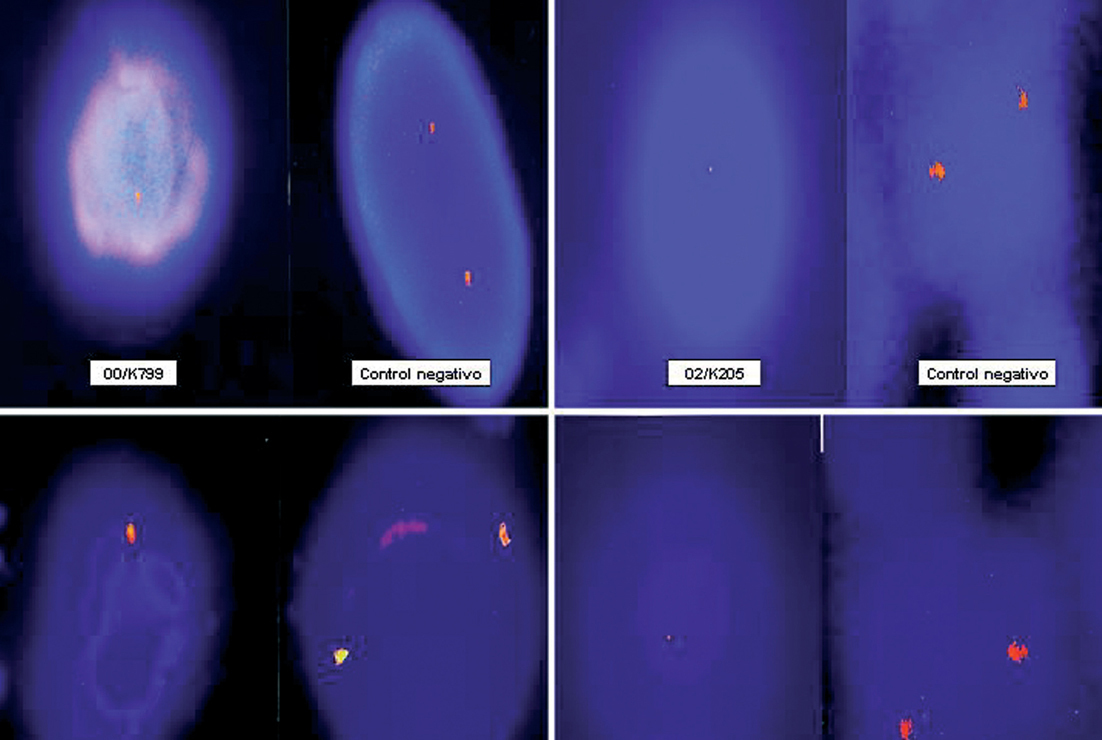
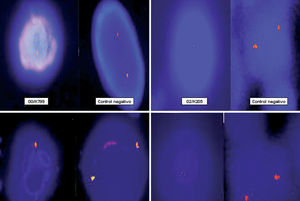
En los 22 casos estudiados mediante FISH se pudo demostrar la deleción del gen rb1 del retinoblastoma en las células plasmáticas neoplásicas que infiltraban la dermis (fig. 8).
Fig. 8.--Imágenes de hibridación in situ fluorescente (FISH) de cuatro de los casos de este estudio en los que se observa deleción del gen del retinoblastoma (rb1). Las células con la deleción del gen rb1 muestran un único punto fluorescente, mientras que en los controles negativos se observan dos.
DISCUSION
Resulta difícil llevar a cabo una revisión de la literatura médica de los casos descritos con afectación cutánea metastásica en pacientes con mieloma múltiple. Esta dificultad se debe, en primer lugar, a que muchos de estos casos fueron simplemente listados como casos formando parte de una serie general de pacientes con mieloma múltiple, sin que los autores prestaran atención especial a la descripción de las características clinicopatológicas o inmunopatológicas de las lesiones cutáneas. Otra dificultad de esta revisión viene determinada porque algunos de los pacientes aparecen descritos en artículos muy antiguos, donde es difícil, por no decir imposible, conocer con exactitud las características particulares de estos pacientes. Por ejemplo, la mayoría de los autores citan a Bruno Bloch como el primer autor que describió en 1910 1 un paciente con mieloma múltiple y afectación cutánea específica. Sin embargo, una lectura detallada de largo y denso artículo de Bruno Bloch demuestra que el paciente en cuestión se trataba de «un hombre que tenía pequeñas máculas eritematosas que evolucionaban hacia pápulas amarillentas o marrón-rojizas o a pequeños nódulos cubiertos de escamocostra. Estas lesiones cutáneas aparecían en forma de erupciones recidivantes, con lesiones diseminadas por toda la superficie corporal, incluyendo el tronco, los brazos y los muslos. Las lesiones desaparecían espontáneamente dejando pequeñas cicatrices atróficas hipopigmentadas. El paciente presentó múltiples episodios recurrentes de este tipo de lesiones durante muchos años. Histopatológicamente, las lesiones mostraban necrosis de la epidermis, con un infiltrado denso de células redondas y alguna célula plasmática aislada. Cuando el paciente tenía 67 años, y muchos años después de haber sufrido estos brotes recidivantes de lesiones cutáneas, se detectó proteína de Bence-Jones en la orina, así como múltiples lesiones osteolíticas que afectan al húmero derecho, varias costillas y numerosas vértebras. El paciente falleció 2 años después con un mieloma múltiple y afectación de pleura, estómago y corazón». Pues bien, la lectura crítica de este trabajo, unánimemente considerado como la descripción original de un paciente con mieloma múltiple y afectación cutánea metastásica, lleva a la conclusión de que el diagnóstico era seguramente incorrecto, porque es muy improbable que un mieloma múltiple de lugar a brotes recidivantes de lesiones cutáneas específicas que regresen de forma espontánea. Obviamente el paciente falleció como consecuencia de un mieloma múltiple, pero es más probable que las lesiones cutáneas correspondieran a brotes recidivantes de pitiriasis liquenoide crónica o de papulosis linfomatoide, y no a una infiltración cutánea específica por el mieloma múltiple.
En cualquier caso, si se aceptan como válidos todos los casos descritos en la literatura médica de afectación cutánea metastásica por un mieloma múltiple, incluyendo tanto los que tenían lesiones osteolíticas subyacentes a las lesiones cutáneas como los que no, encontramos que el número total de casos es de 92, lo que habla de la extraordinaria rareza de este proceso (tabla 1). Si se analizan en conjunto las características clínicas de esta serie de 92 pacientes, recopilando todos los casos descritos en la literatura médica, los datos que obtenemos son los siguientes: se conocen datos clínicos de edad y sexo en 79 pacientes, de los cuales 59 eran hombres y 20 mujeres, con unas edades que oscilaban entre los 36 y 81 años y una edad media de 60,43 años. Las lesiones cutáneas en estos pacientes se describen como pápulas de 1 a 5 cm de diámetro, de consistencia firme, superficie lisa y color eritematoso o violáceo. También se han descrito algunos casos con lesiones en forma de placa y lesiones tumorales de gran tamaño, pero estos casos constituyen las excepciones. Unos cuantos pacientes desarrollaron ulceración superficial e infección bacteriana de las lesiones cutáneas, pero ambos hallazgos son también poco frecuentes 34. Unos pocos pacientes presentaron una única lesión cutánea, y lo más frecuente era que cada paciente tuviera múltiples lesiones salpicadas por la superficie cutánea. Estas lesiones cutáneas metastásicas de mieloma múltiple pueden aparecer en cualquier área de la superficie corporal, pero se desarrollaron con más frecuencia en el tronco y pared abdominal (58 pacientes), seguido en orden de frecuencia por el cuero cabelludo, la cara y el cuello (23 pacientes), las extremidades inferiores (18 pacientes) y las extremidades superiores (15 pacientes). Estas características clínicas de los 79 casos descritos en la literatura médica son superponibles a las de nuestra serie de 40 pacientes.
Algunos autores han postulado que la afectación cutánea específica en pacientes con mieloma múltiple no tiene lugar hasta que la masa tumoral total alcanza un peso de alto riesgo, que se considera de 2 a 3 kg 19. Aunque las lesiones cutáneas pueden desarrollarse precozmente en el curso de la enfermedad o incluso ser la primera manifestación del proceso neoplásico de células plasmáticas 3,29,48,55, lo más habitual es que las lesiones cutáneas específicas en pacientes con mieloma múltiple o plasmocitoma extramedular aparezcan en estadios avanzados de la enfermedad. Es más, en la mayoría de los pacientes con lesiones cutáneas existe una gran diseminación del proceso neoplásico, por lo que la aparición de lesiones cutáneas se considera un signo de mal pronóstico que suele ir seguido de una corta supervivencia del paciente. Aunque existen algunos casos descritos de supervivencias prolongadas en pacientes con mieloma múltiple y lesiones de infiltración cutánea específica 8,10,31,34,36,43, en general la mayoría de los pacientes fallecen durante los 12 meses siguientes al desarrollo de las lesiones cutáneas. En la autopsia de estos pacientes se demuestra la infiltración por células plasmáticas neoplásicas en múltiples órganos, lo cual confirma la diseminación del proceso.
Una revisión de la literatura médica de los casos descritos de mieloma múltiple con infiltración cutánea específica demuestra que el tipo de inmunoglobulina monoclonal producida por las células plasmáticas neoplásicas fue determinada en 60 (100 %) casos: en 38 (63 %) casos era IgG (19 [47 %] casos κ, 7 [18 %] casos λ y en 12 [31 %] casos no se describe el tipo de cadena ligera producida por la IgG monoclonal), en 15 (25 %) casos era IgA (3 casos [20 %] κ, 5 casos [33 %] λ, y en 7 casos [46 %] no se describe el tipo de cadena ligera producida por la IgA monoclonal), en 6 casos (10 %) era IgD (5 casos [83 %] λ y 1 caso [16 %] en el que no se describe el tipo de cadena ligera producido por la IgD monoclonal), en 1 (1 %) caso se trataba de un mieloma IgM (sin descripción del tipo de cadena ligera producida por la IgM monoclonal). En 3 casos se trataba un mieloma normoproteico con proteinuira de de Bence-Jones en la orina. Estos datos difieren ligeramente de los obtenidos en nuestros 40 casos, en los que en 39 (100 %) de ellos se determinó el tipo de inmunoglobulina monoclonal producida por las células plasmáticas neoplásicas, con los siguientes resultados: 19 (47 %) casos era IgG (15 casos [79 %] κ y 4 casos [21 %] λ), en 18 (45 %) era IgA (5 casos [26 %] κ y 13 [72 %] λ), y en 2 casos (5 %) era IgD (2 casos [100 %] λ). En la tabla 5 se comparan los resultados de los casos descritos en la literatura médica con los obtenidos en este estudio respecto al tipo de inmunoglobulina monoclonal producida por las células plasmáticas del mieloma, así como al tipo de cadena ligera de esta inmunoglobulina. Del análisis en su conjunto de estos datos se deduce que no existe un tipo especial de mieloma múltiple con capacidad exclusiva de extenderse la piel, pero en nuestra serie si se observa que los mielomas múltiples IgA poseen un mayor cutaneotropismo, ya que siendo la frecuencia general de mielomas múltiples IgA del 25 %, en los mielomas con infiltración cutánea los de tipo IgA representan el 45 % de los casos. Este hecho, de un mayor tropismo cutáneo por parte de los mielomas múltiples de tipo IgA, ya había sido postulado por algunos autores 34, aunque se trataba de una serie de sólo 4 casos. Nuestra serie de 40 casos parece confirmar con mayor fuerza que los mielomas múltiples de tipo IgA muestran una mayor tendencia a desarrollar infiltración cutánea específica. También se ha postulado un comportamiento biológico más agresivo en los pacientes con lesiones cutáneas de un mieloma múltiple de tipo IgD y en la enfermedad de las cadenas ligeras 17,34, pero el número de casos descritos es tan escaso que hace imposible extraer conclusiones válidas.
Desde el punto de vista histopatológico, las lesiones de afectación cutánea por un mieloma múltiple se pueden encuadrar dentro de dos patrones histopatológicos generales: nodular o difuso intersticial 34. En nuestra experiencia, el patrón nodular es, con mucha diferencia, el más frecuente y en las biopsias se observa que todas las estructuras anexiales, vasculares y neurales preexistentes de la dermis resultan obliteradas y destruidas por la infiltración de células plasmáticas neoplásicas. En una pequeña proporción de los casos, estas células neoplásicas muestran las características citomorfológicas típicas de las células plasmáticas (núcleo redondo y excéntrico, con cromatina en rueda de carro, halo claro paranuclear y citoplasma amplio y basófilo), pero lo más frecuente es que las características citológicas de estas células plasmáticas neoplásicas sean atípicas, apareciendo formas inmaduras con cromatina dispersa, una relación núcleo/citoplasma elevada y un nucléolo prominente. Estos plasmoblastos inmaduros pueden observarse en las lesiones de infiltración cutánea, incluso en los casos en los que la médula ósea muestra los hallazgos típicos de un mieloma múltiple, con abundancia de células plasmáticas maduras 17. En casos raros, como en nuestros casos 6, 14 y 28, las células plasmáticas neoplásicas pueden mostrar una morfología fusiforme, lo cual dificulta enormemente realizar un diagnóstico histopatológico correcto. En este sentido, se han descrito algunos ejemplos de linfoma B cutáneo con linfocitos neoplásicos fusiformes 62,63, pero en estos casos estas células neoplásicas expresaban CD20, que es el principal marcador pan-B, mientras que este marcador resultó negativo en todos nuestros casos de mieloma múltiple con afectación cutánea por células plasmáticas neoplásicas de morfología fusiforme. En aquellos casos en los que las lesiones mostraban un patrón histopatológico intersticial y difuso se observaban finos cordones de células plasmáticas neoplásicas entre los haces de colágeno de la dermis, lo cual obligaba a plantear el diagnóstico diferencial histopatológico con una leucemia cutánea. Sin embargo, en nuestros casos este diagnóstico diferencial histopatológico resultó sencillo, ya que en todos los casos se observó que las células neoplásicas que infiltraban la dermis no expresaban mieloperoxidasa.
Desde el punto de vista inmunohistoquímico, nuestros resultados demuestran que las células plasmáticas neoplásicas de un mieloma múltiple que infiltra la piel tienen un inmunofenotipo bastante constante, con una intensa inmunorreactividad para CD79a, CD138 y EMA; una inmunorreactividad variable para CD38 y CD43; y negatividad para el resto de los marcadores investigados. Habitualmente las células plasmáticas neoplásicas de un mieloma múltiple no expresan los marcadores pan-B, como son el CD19 y el CD20. En contraste con las células plasmáticas normales, que habitualmente no expresan CD43 ni CD56, las células plasmáticas neoplásicas de un mieloma múltiple pueden mostrar inmunoexpresión aberrante de estos dos marcadores. También observamos que algunos de nuestros casos mostraban una débil inmunorreactividad para el CD43. El marcador del proteoglucano fijador del colágeno 1, denominado syndecan-1 o CD138, se ha mostrado como un marcador específico de las células neoplásicas del mieloma múltiple dentro de la médula ósea y parece ser que es importante para fijar estas células en la médula ósea. Este marcador no se expresa por otras células hematopoyéticas ni por las células endoteliales y se ha sugerido que la pérdida de expresión de syndecan-1 (CD138) en la superficie de las células plasmáticas neoplásicas puede contribuir a la proliferación y diseminación del mieloma múltiple 64. Sin embargo, en nuestros casos las células plasmáticas neoplásicas que infiltraban la dermis mostraban una intensa inmunorreactividad para el syndecan-1(CD38), lo que no parece confirmar que la inmunoexpresión de este marcador en las células neoplásicas de un mieloma múltiple sea indicativa de un mejor pronóstico.
Respecto al tipo de inmunoglobulina monoclonal producida por las células plasmáticas neoplásicas del mieloma múltiple, así como respecto a la restricción de la cadena ligera de inmunoglobulina producida, se encontró una perfecta correlación entre los hallazgos obtenidos por electroforesis en el suero de cada paciente y los hallazgos inmunohistoquímicos en las lesiones cutáneas.
Algunos estudios de PCR han descrito la identificación de material genético del virus HHV-8 65 o del VEB 66 en las células plasmáticas neoplásicas del mieloma múltiple. En estos casos se trataba fundamentalmente de pacientes con sida, lo que ha planteado la posibilidad de que el virus HHV-8 o el VEB tuvieran la capacidad de inmortalizar linfocitos B y tuvieran un papel patogénico en el desarrollo de neoplasias de células plasmáticas en estos pacientes. Los 22 casos de nuestra serie en los que investigamos por PCR la presencia de material genético de estos virus en la células plasmáticas neoplásicas infiltrando la dermis eran negativos para el virus de la inmunodeficiencia humana (VIH) y en todos ellos obtuvimos resultados de PCR negativos respecto a la presencia de material genético de estos dos virus, lo que parece indicar que el virus HHV-8 y el VEB no tienen ningún papel patógeno en el desarrollo de un mieloma múltiple en pacientes que no están infectados por el VIH.
En los últimos años se han descrito algunas anomalías citogenéticas que pueden tener importancia pronóstica en pacientes con mieloma múltiple. En este sentido, se han detectado deleciones en el cromosoma 13q y anomalías en el cromosoma 11q de las células plasmáticas neoplásicas de pacientes con mieloma múltiple tratados mediante autotrasplante que parecen conllevar un mal pronóstico 67,68. Además, en un estudio reciente 69 que investigó mediante técnicas de FISH las células plasmáticas en la médula ósea de 89 pacientes con mieloma múltiple, antes de que se llevase a cabo ningún tipo de tratamiento, se observó que la deleción del gen del retinoblastoma (rb1) se asociaba con una peor respuesta a la quimioterapia, un comportamiento biológico más agresivo y, en definitiva, un mal pronóstico. Nuestros resultados también confirman estos hallazgos, porque la infiltración cutánea por un mieloma múltiple es, por sí sola, un signo de muy mal pronóstico, ya que este hallazgo sólo se observa en pacientes con estadios muy avanzados de la enfermedad y en todos los casos en que lo investigamos encontramos que la deleción del gen rb1 estaba presente en las células plasmáticas neoplásicas de las lesiones cutáneas. Por lo tanto, la investigación de la deleción de este gen rb1 puede ser una técnica muy útil para identificar un subgrupo de pacientes con mieloma múltiple que muestran un comportamiento biológico más agresivo, van a responder peor a la quimioterapia y tienen un pronóstico especialmente malo.
CONCLUSIONES
1. La afectación cutánea por un mieloma múltiple es un proceso extraordinariamente raro.
2. La histopatología, la inmunohistoquímica y los estudios de reordenamiento genético constituyen herramientas muy útiles para diferenciar una infiltración de la dermis por células plasmáticas reactivas de una auténtica infiltración neoplásica, mediante la demostración en este último caso de la restricción de cadenas ligeras de inmunoglobulinas o el reordenamiento del gen JH de las cadenas pesadas en las células plasmáticas neoplásicas.
3. El mieloma múltiple de tipo IgA muestra una mayor tendencia a desarrollar infiltración cutánea específica que otros tipos de mieloma.
4. La infiltración cutánea en un paciente con mieloma múltiple es un signo de muy mal pronóstico y la supervivencia es muy corta, con independencia de la pauta de quimioterapia administrada.
5. El syndecan-1 (CD38) es un buen marcador inmunohistoquímico de las células plasmáticas neoplásicas del mieloma múltiple, pero su expresión no debe ser utilizada como marcador pronóstico.
6. La demostración de la deleción del gen rb1 en las células plasmáticas neoplásicas de un mieloma múltiple puede ser una técnica útil para detectar un subgrupo de pacientes con una forma especialmente agresiva de la enfermedad y con un peor pronóstico.
Este trabajo ha sido galardonado con el Premio Juan Azúa de la Academia Española de Dermatología del año 2005.